Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Acta Biológica Colombiana
Print version ISSN 0120-548X
Acta biol.Colomb. vol.19 no.3 Bogotá Sept./Dec. 2014
https://doi.org/10.15446/abc.v19n3.42776
Nota Breve
http://dx.doi.org/10.15446/abc.v19n3.42776
DIVERSIDAD GENÉTICA EN UNA POBLACION DE Rhinoclemmys nasuta (TESTUDINES:GEOEMYDIDAE) ASOCIADA AUN AMBIENTE INSULAR DEL CHOCÓ BIOGEOGRÁFICO
Genetic Diversity in a Population of Rhinoclemmys nasuta (Testudines:Geoemydidae) Associatted with an Insular Locality in the Chocó Biogeographic Region
LESLIE ANAIS CASTILLO-CUTIVA1, Bióloga.; ALAN GIRALDO1, Ph. D.; GUILLERMO BARRETO2, Ph. D
1 Universidad del Valle, Facultad de Ciencias Naturales y Exactas, Departamento de Biología, Grupo de Investigación en Ecología Animal. Calle 13 # 100-00. Cali, Colombia. ecologia@univalle.edu.co; alan.giraldo@correounivalle.edu.co
2 Universidad del Valle, Facultad de Ciencias Naturales y Exactas, Departamento de Biología, Grupo de Investigación en Genética Molecular Humana. Calle 13 n.° 100-00. Cali, Colombia. guillermo.barreto@correounivalle.edu.co
Autor de correspondencia: Alan Giraldo, alan.giraldo@correounivalle.edu.co
Recibido 26 de marzo de 2014, aceptado con modificaciones 7 de mayo de 2014, fecha de reenvío 16 julio de 2014.
Citation / Citar este artículo como: CASTILLO-CUTIVA LA, GIRALDO A, BARRETO G. Diversidad genética en una población de Rhinoclemmys nasuta (Testudines:Geoemydidae) asociada a un ambiente insular del Chocó Biogeográfico. Acta biol. Colomb. 2014;19(3):513-519.
RESUMEN
Se realizó la caracterización de la diversidad genética de la población de Rhinoclemmys nasuta, que habita en la localidad insular de Isla Palma, Bahía Málaga (Valle del Cauca), utilizando tres sistemas de microsatélites (Cm72, Cm58 y Cm3). En esta localidad, R. nasuta se encuentra ampliamente distribuida en los sistemas de riachuelos y quebradas presentes. Se tomaron entre 100 a 200 µL de sangre periférica de diez tortugas en cinco riachuelos, preservando las muestras en una solución 0,5 M de EDTA y el ADN fue extraído mediante las técnicas de Salting-out y Chelex. Los productos amplificados por PCR fueron visualizados y medidos en geles de poliacrilamida teñidos con nitrato de plata. Se obtuvieron productos amplificados exitosos para todos los sistemas analizados, dos de los cuales (Cm72 y Cm3) resultaron ser monomórficos, mientras que el sistema Cm58 presentó un PIC alto (0,698) permitiendo estimar la diversidad genética de esta población. La heterocigosidad observada fue baja (Ho = 0,26) y los índices de endogamia FIS y FIT fueron altos (0,67857 y 0,67881), indicando un exceso de homocigotos en cada uno de los ríos y para la población total. El Análisis Molecular de Varianza sugirió que no existe estructura genética diferencial en esta población (FST = 0,00075; p = 0,95112). En conclusión los resultados sugieren que la diversidad genética de la población de R. nasuta en Isla Palma es baja, siendo una población altamente endogámica
Palabras clave: Chocó Biogeográfico, Colombia, conservación, Neotrópico, tortugas, tortuga río Chocoana.
ABSTRACT
Characterization of the genetic diversity of Rhinoclemmys nasuta population inhabits Isla Palma (Malaga Bay, Valle del Cauca) was carried out using three microsatellite systems (Cm72 , Cm58 and Cm3). In this locality, individuals of R. nasuta are widely distributed in the inland streams and creeks system. 100 to 200 mL of peripheral blood was taken off from ten turtles in five streams of the island, preserving samples in a 0.5 M EDTA. DNA was extracted using Salting-out and Chelex solution techniques. PCR amplified products were visualized and measured in polyacrylamide gels stained with silver nitrate. Successful amplification products were obtained for all systems analyzed, two of which (Cm72 and Cm3) were found to be monomorphic, while the system Cm58 had a high PIC (0.698) allowing to estimate the genetic diversity of this population. The observed heterozygosity was low (Ho = 0.26) and inbreeding indices FIS and FIT were high (0.67857 and 0.67881), indicating an excess of homozygotes in each of the rivers and for the all population. The molecular analysis of variance suggested that there is no difference in genetic structure of the population (FST = 0.00075, p= 0.95112). Therefore, the results suggest that the genetic diversity of R. nasuta population in Isla Palma was low and exhibited a highly inbred index.
Keywords Chocó, Colombia, conservation, large-nosed wood turtle, Neotropical turtles, turtles.
Un elemento clave para la viabilidad temporal de las poblaciones es la cantidad de individuos que las componen. Cuando el tamaño de la población es relativamente bajo se produce una homogenización que conduce a niveles altos de endogamia (Gilpin y Soulé, 1986; Hunter y Gibss, 2006; Pierce, 2010). Bajo estas condiciones, se tiende a reducir drásticamente la diversidad genética y se incrementa notablemente la probabilidad de que algunos factores genéticos conlleven a una extinción local (Alledorf et al., 2012). Esta variabilidad genética es el resultado de una evolución particular, única e irrepetible, y al ser baja, favorece la aparición de nuevas enfermedades, afectando incluso el éxito reproductivo o la capacidad de la población para adaptarse a otras condiciones ambientales (Toledo, 1994; Schneider et al., 1998; Fagan y Holmes, 2006).
En el 2002 la UICN (Unión Internacional para la Conservación de la Naturaleza) evaluó 32 taxa de tortugas continentales en Colombia, encontrando que 19 están en alto riesgo de desaparecer (Rueda et al., 2002). Sin embargo, el conocimiento necesario para establecer estrategias adecuadas de protección aún es escaso, debido a la carencia de información básica relevante de cada especie (Páez et al., 2012). Esta deficiencia es aún más relevante cuando se trata de especies endémicas o de distribución reducida, como es el caso de Rhinoclemmys nasuta, ya que requieren estrategias de conservación aún más sólidas (Mittermeier et al., 1992). En los últimos años el conocimiento generado sobre los aspectos biológicos y ecológicos de R. nasuta se ha incrementado significativamente (Carr y Giraldo, 2009; Carr et al., 2010; Carr et al., 2012; Giraldo et al., 2012; Garcés et al., 2013a; Garcés et al., 2013b; Giraldo et al., 2013), aunque aún no es suficiente para realizar una valoración adecuada de su vulnerabilidad, siendo catalogada como una especie con Datos Deficiente (DD) a nivel local (Castaño-Mora y Medem, 2002) y como Casi Amenazada (NT) a nivel global (IUCN, 2013) debido a su distribución geográfica restringida (Ippi y Flores, 2001; Carr et al., 2012).
De acuerdo con Carr et al., (2012), Giraldo et al., (2012) y Garcés-Restrepo et al., (2013a), la población más grande de R. nasuta que ha sido registrada hasta el momento se encuentra en Isla Palma (Bahía Málaga,Valle de Cauca), y por su carácter insular, es una población que tiene un mayor nivel de endemismo, condición que reduce sustancialmente componentes de valor adaptativo e incrementa el riesgo de extinción local (Frankham, 1995; Eldridge et al., 1999; Castaño-Mora y Medem, 2002; Rueda et al., 2002; Sax y Gaines, 2008). En este contexto, realizar la caracterización de la diversidad genética de esta especie endémica de Colombia se podría convertir, en el corto plazo, en una herramienta muy efectiva para la detección, priorización y solución de problemas de conservación, e incluso podría servir como elemento para definirla como una unidad de manejo priorizado para el recientemente declarado PNN Uramba en Bahía Málaga - Valle del Cauca (MAVDT, 2010). Con el propósito de generar una herramienta práctica que permita fortalecer acciones futuras de manejo, en el presente trabajo se establecen las frecuencias alélicas de tres sistemas de microsátelites en la población de R. nasuta de Isla Palma y se analiza el grado de variación genética intrapoblacional considerando como unidad de muestreo los riachuelos de esta localidad. Para este fin, se recolectaron entre el año 2007 y 2008, diez muestras de sangre periférica (entre 100 μl y 200 μl) de especímenes de R. nasuta provenientes de cinco riachuelos de Isla Palma (Fig. 1). Las muestras fueron almacenadas inmediatamente en tubos de 1,5 mL con una solución de EDTA 0,5 M, rotuladas con el número de identidad asignado a la tortuga, el sexo y el sitio de origen, y preservadas en frio hasta su procesamiento en el laboratorio de Genética Molecular Humana de la Universidad del Valle. Los especímenes utilizados fueron obtenidos durante el desarrollo del programa de monitoreo de la población de R. nasuta de Isla Palma que adelantó el grupo de investigación en Ecología Animal de la Universidad del Valle con la autorización de la Dirección General Marítima de Colombia - DIMAR, autoridad nacional que administró exclusivamente esta localidad hasta el año 2010.
Para extraer el ADN se utilizó el método de salting out (Hillis et al., 1996), modificado, cuando el volumen de muestra disponible fue mayor 100 µL (y no presentaba coagulación), y el método de Chelex 100 (Walsh et al., 1991) cuando el volumen de muestra disponible fue menor a 100 µL y la muestra estaba coagulada. Para el método de salting out, se tomaron entre 20 a 50 µl de muestra en tubos vacutainer de 1.5 ml y se realizó la lisis de los elementos figurados. Posteriormente se degradaron las proteínas con proteinasa K y se precipitó el ADN saturado con sales mediante la adición de etanol frío (Hillis et al., 1996, Thomson et al., 2006). El ADN obtenido fue diluido en bruffer TE y almacenado a 4°C listo para ser usado. Para la extracción de ADN por el método de Chelex, se adicionaron 3 µl de muestra a 1 ml de agua destilada resuspendiendo el botón en una solución de Chelex 100 al 5 % hasta lograr un volumen de 200 µl. La solución se incubó (56 °C por 3 min) y se centrifugó (10.000 rpm) hasta obtener el botón de Chelex.
Se estandarizaron las condiciones de amplificación de los tres sistemas de STR's (Cm3, Cm58 y Cm72) previamente descritos por Fitzsimmons et al., (1995) para Chelonia mydas, y probados por Mühlmann-Diaz et al., (2001) en la tortuga dulceacuícola Trachemys scripta. Para la selección de estos STR's se tuvo en cuenta los índices de heterocigosidad más altos reportados en la literatura, utilizando como cebadores para Cm3 F: 5-AATACTACCATGAGATGGGATGTG-3´ y R: 5´-ATTCTTTTCTCCATAAACAAGGCC-3´; para Cm58 F: 5´-GCCTGCAGTACACTCGGTATTTAT-3´y R: 5´-TCAATGAAAGTGACAGGATGTACC-3´ y para Cm72 F: 5-CTATAAGGAGAAAGCGTTAAGACA-3´ y R: 5´-CCAAATTAGGATTACACAGCCAAC-3. Los diferentes fragmentos generados durante la amplificación de la PCR fueron detectados en geles de poliacrilamida de alta resolución (Ferreira y Grattapaglia, 1998). La visualización de las bandas se realizó directamente usando la técnica de coloración con nitrato de plata (Santos et al., 1993), definiéndose la asignación alélica de los amplificados por comparación con los pesos moleculares conocidos del marcador de peso molecular, toda vez que los marcadores utilizados en esta investigación no están diseñados específicamente para R. nasuta.
Se estimó el número de alelos y las frecuencias alélicas por locus considerando las muestras de cada uno de los riachuelos como una muestra independiente. Se realizó el cálculo de las heterocigosidades observadas y esperadas por locus para cada uno de los ríos muestreados, estableciendo las diferencias estadísticas contra las frecuencias esperadas según el modelo del equilibrio de Hardy-Weinberg (H-W) mediante la prueba de cadena aleatoria de Markov (Guo y Thompson, 1992) utilizando el programa ARLEQUIN versión 3.0 (Excoffier et al., 2005). Se calculó la heterocigosidad insesgada (He) de Mayr (1978), como  , donde n es el tamaño de la muestra y el pi es la frecuencia del alelo i. Adicionalmente se estimó el número efectivo de alelos (Ae) en cada uno de los loci como:
, donde n es el tamaño de la muestra y el pi es la frecuencia del alelo i. Adicionalmente se estimó el número efectivo de alelos (Ae) en cada uno de los loci como: 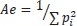
Se utilizaron los estimadores F de Wright (1950) para calcular el coeficiente de endogamia (Fst) y se realizó un análisis de varianza molecular (AMOVA) con el propósito de evaluar la presencia de una estructura genética diferencial entre ríos utilizando el programa ARLEQUIN v3.0 (Excoffier et al., 2005). Para saber la relevancia de la información de los sistemas de microsatélites evaluados, se estimó el contenido de información polimórfica (PIC) como:
donde n representa el número de alelos presentes en el locus, Pi y Pj son las frecuencias alélicas (Xin-Sheng et al., 2008).
Con los métodos de extracción utilizados se logró obtener ADN en una concentración suficiente para amplificar los tres sistemas microsatélites, incluso a partir de muestras coaguladas. El sistema Cm72 fue monomórfico, conteniendo un solo alelo de 234 pb, mientras que los sistemas Cm3 y Cm58 fueron polimórficos, conteniendo dos y seis alelos respectivamente (Tabla 1). El índice de polimorfismo (PIC) sólo se estimó para los sistemas Cm58 y Cm3, encontrando que el sistema Cm58 fue altamente polimórfico (PIC = 0,765), mientras que el sistema Cm3 (PIC = 0,201) fue poco polimórfico (Tabla 2). Al evaluar el número efectivo de alelos para cada uno de los sistemas, se encontró que el sistema Cm58 presentó el mayor número efectivo de alelos que pasará a las siguientes generaciones, con cerca de cinco (Tabla 2), siendo el sistema que tendrá más posibilidades de conservar su diversidad genética en futuras generaciones, mientras que el sistema Cm72 permanecerá efectivamente en todas las nuevas generaciones. Es importante destacar que la heterocigosidad observada en los dos sistemas de STR's polimórficos fue de solo el 26 % y que aunque el sistema Cm3 estuvo en equilibrio H-W, el sistema Cm58, que fue el más polimórfico, no estuvo en equilibrio H-W (p < 0,00485, nivel de confiabilidad > 95 %)(Tabla 2).
No se establecieron los índices de endogamia para el sistema Cm72 debido a su carácter monomórfico. En este mismo sentido, el bajo nivel de polimorfismo detectado en el sistema Cm3 indica que este sistema no sería informativo para el análisis genético poblacional de R. nasuta. Por otro lado, el sistema Cm58 permitió realizar el análisis de endogamia para la población de R. nasuta indicando que solamente el 0,08 % de la varianza genética observada se debe a diferencias entre los ríos, lo que sugiere que los individuos de R. nasuta que habitan en Isla Palma conforman una sola población (Tabla 3). Finalmente, los índices de fijación sugieren la presencia de un exceso de homocigotos tanto para toda la población como en cada uno de los ríos (Tabla 3), lo que sugiere que la población de R. nasuta en Isla Palma exhibe un alto grado de endogamia.
La utilidad de los microsatélites en el estudio de la variación genética de las poblaciones deriva de su herencia biparental (exceptuando los cromosomas sexuales), codominancia, multialelismo, distribución al azar, alta frecuencia en el genoma y su elevado nivel de diversidad alélica debido a las altas tasas mutacionales (Chase et al., 1996; Engstrom et al., 2007). Particularmente para la biología de la conservación, el uso de microsatélites como herramienta de análisis ofrece la ventaja de ser relativamente fáciles de obtener de manera directa a partir del aislamiento de marcadores específicos de la especie, con base en una librería de ADN genómico (Goldstein y Schlötterer, 1999). Lamentablemente, la necesidad de ser aislados de novo se convierte en un inconveniente para las especies que son examinadas por primera vez, como es el caso de R. nasuta, ya que los microsatélites son usualmente encontrados en regiones no codificantes, en donde la tasa de sustitución nucleotídica es mayor que en las regiones codificantes (Zane et al., 2002). Sin embargo, en genomas animales se han detectado algunas regiones flanqueantes altamente conservadas, lo cual permite en algunos casos la transferencia de marcadores entre especies o entre géneros a partir del uso de cebadores heterólogos (Moore et al., 1991; Menotti-Raymond y Obrien, 1995; Pepin et al., 1995). Incluso, se han reportado algunas de estas regiones en cetáceos (Schlötterer et al., 1991), tortugas (Avise et al., 1992; FitzSimmons et al., 1995; King y Julian, 2004) y peces (Rico et al., 1996), permitiendo realizar la amplificación cruzada entre especies que divergen en hasta 470 millones de años.
El alto valor de polimorfismo registrado para el sistema Cm58 en R. nasuta, lo destaca como un marcador de gran utilidad para los estudios de genética de sus poblaciones. Por otro lado, la ausencia de polimorfismo en el sistema Cm72 y el bajo polimorfismo en el sistema Cm3 indican que no se han presentado variaciones o mutaciones que generen nuevos alelos en estos loci, por lo tanto, aunque estos sistemas hayan sido reportados con un alto polimorfismo en otras especies relacionadas filogenéticamente, no siempre se puede esperar que se encuentre el mismo nivel de polimorfismo. En poblaciones aisladas, como la población de R. nasuta de Isla Palma, los niveles de varianza genética tienden a ser determinados por la interacción de tres factores: la selección natural, la deriva genética y la mutación, factores que pueden generar un cambio aleatorio en las frecuencias alélicas, provocando la pérdida de la heterocigosidad y la eventual fijación de alelos (Ellstrand y Elam, 1993). Sin embargo, el riesgo de extinción para estas poblaciones se incrementa debido a los efectos combinados de los cambios genéticos, medioambientales y demográficos (Lande, 1993). En este sentido, si la población mantiene un tamaño poblacional constante, y las presiones de selección son también constantes, se alcanzará un nivel particular de varianza genética bajo un escenario de pseudoequilibrio, en donde la pérdida de varianza genética por selección y deriva se contrarresta con la incorporación de nueva variación por mutación (Lynch, 1996).
De acuerdo con Phillip et al., (2004), la familia Geoemydidae, es una de las familias de tortugas continentales más grande, diversa y menos estudiada. Estos autores utilizando métodos de análisis filogenético establecieron que el género Rhinoclemmys conforma uno de los tres principales clados de esta familia, e incluso sugieren con base en sus resultados una alta posibilidad de hibridación intraespecífica por lo que recomiendan fortalecer la revisión taxonómica con base en la evidencia disponible, como la generada en la presente investigación.
En conclusión la población de R. nasuta en Isla Palma es altamente endogámica, probablemente como consecuencia de un aumento de consanguinidad y la ausencia de flujo génico que podría generar el ingreso de inmigrantes a la población (Ellstrand y Elam, 1993). Bajo esta condición, el apareamiento entre individuos emparentados o con genotipos similares, podría ocasionar a largo plazo una disminución en la variabilidad genética y la eventual fijación de alelos. Por otra parte, el valor alto del FIS estimado para esta población, podría ser un reflejo de un posible efecto fundador, que habría provocado la aparición de cruces entre una pequeña cantidad de individuos con genotipos similares que llegaron a la isla para colonizarla o quedaron aislados durante su formación, razón por la cual estos genotipos se mantienen en las generaciones actuales incrementando la homocigosidad de la población. Adicionalmente, no se detectó una estructura poblacional definida para esta especie en Isla Palma, conformando los grupos de individuos que habitan los diferentes ríos una sola población.
AGRADECIMIENTOS
Los autores agradecen a Mario F. Garcés-Restrepo, Johnatan Loaiza, Viviana Perez, Andrés Quintero y John L. Carr, por el apoyo durante las jornadas de campo. A Brigitte Tosse, Yherson F. Molina y Fanny L. González por su valioso apoyo durante el trabajo de laboratorio. El ingreso a Isla Palma fue otorgado por la Dirección General Marítima de Colombia - DIMAR al grupo de Investigación en Ecología Animal de la Universidad del Valle con el propósito de realizar el monitoreo de la población de Rhinoclemmys nasuta presente en esta localidad. Este trabajo fue parcialmente financiado por el grupo de Investigación en Ecología Animal y el Laboratorio de Biología Molecular Humana de la Universidad del Valle, e hizo parte de la actividad académica desarrollada por uno de los autores (LCC) como trabajo de grado en el programa académico de Biología de la Universidad del Valle. Ninguno de los resultados expresados en este documento tiene valor comercial o se puede derivar su uso para el aprovechamiento económico de recursos genéticos.
REFERENCIAS
Alledorf FW, Luikart GH, Aitken SN. Conservation and the Genetics of Populations. 2ed. Hoboken, NJ, USA: Wiley-Blackwell; 2012. 624 p. [ Links ]
Avise CJ, Bowen WB, Lamb T, Meylan BA, Bermingham E. Mitochondrial evolution at a turtle's pace: evidence for low genetic variability and reduced microevolutionary rate in Testudines. Mol Biol Evol. 1992;9(3):457-473. [ Links ]
Carr JL, Giraldo A. Rhinoclemmys nasuta (Boulenger 1902), Large-Nosed Wood Turtle, Chocoan River Turtle. In: Rhodin AGJ, Pritchard PCH, Van Dyke PP, Saumure RA, Buhlmann KA, Iverson JB, Mittermeier RA, editors. Conservation Biology of Freshwater Turtles and Tortoises: A Compilation Project of the IUCN/SSC Tortoise and Freshwater Turtle Specialist Group. Chel Res Monogr. 2009;5:034.1-034.6. [ Links ]
Carr JL, Garcés-Restrepo MF, Quintero-Ángel A, Giraldo A. Rhinoclemmys nasuta (Chocoan River Turtle). Diet and feeding behavior. Herpetol Rev. 2010;41(3):347-348. [ Links ]
Carr JL, Giraldo A, Garcés-Restrepo MF. Rhinoclemmys nasuta (Boulenger 1902). In: Páez V, Morales-Betancourt MA, Lasso CA, Castaño-Mora OV, Bock B, editores. Biología y Conservación de las Tortugas Continentales de Colombia. Instituto de Investigación de los Recursos Biológicos Alexander von Humboldt (IAvH). Bogotá, Colombia; 2012. p. 315-322. [ Links ]
Castaño-Mora OV, Medem F. Rhinoclemmys nasuta. In: Castaño-Mora OV, editor. Libro Rojo de Reptiles de Colombia. Serie de Libros Rojos de Especie Amenazadas de Colombia. Instituto de Ciencias Naturales- Universidad Nacional de Colombia, Ministerio de Medio Ambiente, Conservación Internacional- Colombia. Bogotá, Colombia; 2002. p. 125. [ Links ]
Chase M, Kesseli R, Bawa K. Microsatellite markers for population and conservation genetics of tropical trees. Am J Bot. 1996;83(1):51-57. [ Links ]
Eldridge MDB, King JM, Loupis AK, Spencer PBS, Taylor AC, POPE LC, et al. Unprecedented low levels of genetic variation and inbreeding depression in an island population of a Black-Footed Rock-Wallaby. Conserv Biol. 1999;13(3):531-541. DOI: 10.1046/j.1523-1739.1999.98115.x [ Links ]
Excoffier L, Laval G, Schneider S. Arlequin version 3.0: An integrated software package for population genetics data analysis. Evol Bioinform Online. 2005;1:47-50. [ Links ]
Ellstrand NC, Elam DR. Population genetic consequences of small population size: implications for plant conservation. Annu Rev Ecol Evol Syst. 1993;24:217-242. DOI: 10.1146/annurev.es.24.110193.001245 [ Links ]
Engstrom TN, Edwards T, Osentoski MF, Myers EM. A compendium of PCR primers for mtDNA, microsatellite, and other nuclear loci for freshwater turtles and tortoises. In: Shaffer HB, Georges A, FitzSimmons N, Rhodin AGJ, editors. Defining turtle diversity: proceedings of a workshop on genetics, ethics, and taxonomy of freshwater turtles and tortoises. Chelonian Research Foundation, Cambridge, Massachusetts. 2007. p. 9-26 [ Links ]
Fagan WF, Holmes EE. Quantifying the extinction vortex. Ecol Lett. 2006;9(1):51-60. DOI: 10.1111/j.1461-0248.2005.00845.x [ Links ]
Ferreira ME, Grattapaglia D. Introducción al uso de marcadores moleculares en el análisis genético. Embrapa. Brasilia D. F. Brasil. 1998. p. 220. [ Links ]
FitzSimmons NN, Moritz C, Moor SS. Conservation and dynamics of microsatellite loci over 300 million years of marine turtle evolution. Mol Biol Evol. 1995;12(3):432-440. [ Links ]
Frankham R. Inbreeding and extinction: a threshold effect. Conserv Biol. 1995;9(4):792-799. DOI: 10.1046/j.1523-1739.1995.09040792.x [ Links ]
Garcés-Restrepo MF, Giraldo A, Carr JL.Population ecology and morphometric variation of the chocoan river turtle (Rhinoclemmys nasuta) from two localities on the Colombian Pacific coast. Bol Cient Mus Hist Nat. 2013a;17(2):160-171. [ Links ]
Garcés-Restrepo MF, Giraldo A, Carr JL, Brown LD. Turtle ectoparasites from the Pacific coastal region of Colombia. Biota Neotrop. 2013b;13(3):74-79. [ Links ]
Gilpin ME, Soulé ME. Minimum viable populations: processes of species extinction. Conservation biology: the science of scarcity and diversity. Sinauer Associates, Sunderland, Massachusetts. 1986. p.19-34. [ Links ]
Giraldo A, Garcés-Restrepo MF, Carr JL, Loaiza J. Tamaño y estructura poblacional de la tortuga sabaletera (Rhinoclemmys nasuta, Testudines: Geoemydidae) en un ambiente insular del Pacífico colombiano. Caldasia. 2012;34(1):109-125. [ Links ]
Giraldo A, Garcés-Restrepo MF, Bolívar-García W, Carr, JL. First report of hatching of the large-nosed wood turtle (Rhinoclemmys nasuta Boulenger 1902, Testudines: Geoemydidae). Bol Cient Mus Hist Nat. 2013;17(2):154-159. [ Links ]
Goldstein BD, Schlötterer C. Microsatellites evolution and applications. Oxford University Press. New York. 1999. p. 352. [ Links ]
Guo S, Thompson E. Performing the exact test of Hardy-Weinberg proportion for multiple alleles. Biometrics. 1992;48(2):361-372. [ Links ]
Hillis DM, Mable BK, Moritz C. Applications of molecular systematics. In: Hillis DM, Moritz C, Mable BK. editors. Molecular systematics. Sinauer Associates Inc., Sunderland.1996. p. 515-543. [ Links ]
Hunter Jr ML, Gibss JP. Fundamentals of conservation biology. 3ed. Wiley-Blackwell, Hoboken, NJ, USA. 2006. p. 516. [ Links ]
Ippi S, Flores, V. Las tortugas neotropicales y sus áreas de endemismo. Acta Zool Mex. 2001;84:49-63. [ Links ]
IUCN. Red list of threatened species. Version 2013.2. 2013. [Cited 15th January 2014]. Available at: http://www.iucnredlist.org. [ Links ]
King TL, Julian SE. Conservation of microsatellite DNA flanking sequence across 13 emydid genera assayed with novel bog turtle (Glyptemys muhlenbergii) loci. Conserv Genet. 2004;5(5):719-725. [ Links ]
Lande R. Risks of population extinction from demographic and environmental stochasticity and random catastrophes. Am Nat. 1993;142(6):911-927. [ Links ]
Lynch M. A quantitative-genetic perspective on conservation issues. In: Avise JC, Hamrick JL, editors. Conservation genetics: case histories from nature. Chapman & Hall, New York;1996. p. 471-501. [ Links ]
MAVDT. Resolución Número 1501 de Agosto 04 de 2010. Ministerio de Ambiente, Vivienda y Desarrollo Territorial. Bogotá; 2010. p. 17. [ Links ]
Menotti-Raymond MA, Obrien SJ. Evolutionary conservation of ten microsatellite loci in four species of Felidae. J Heredity. 1995;86(4):319-322. [ Links ]
Mittermeier RA, Carr JL, Swingland IR, Werner TB, Mast RB. Conservation of amphibians and reptiles. In: Adler K. editor. Herpetology: current research on the biology of amphibians and reptiles. Society for the Study of Amphibian and Reptiles. Missouri. USA; 1992. p. 59-80. [ Links ]
Moore SS, Sargeant LL, King TJ, Mattick JS, Georges M, Hetzel JS. The conservation of dinucleotide microsatellites among mammalian genomes allows the use of heterologous PCR primer pairs in closely related species. Genomics. 1991;10(3):654-660. DOI: 10.1016/0888-7543(91)90448-N [ Links ]
Mühlmann-Diaz MC, Ulsh BA, Whicker FW, Hinton TG, Congdon JD, Robinson JF, Bedford JS. Conservation of chromosome 1 in turtles over 66 million years. Cytogenet Genome Res. 2001;92(1-2):139-143. [ Links ]
Páez V, Morales-Betancourt MA, Lasso CA, Castaño-Mora OV, Bock B. editors. Biología y Conservación de las Tortugas Continentales de Colombia. Instituto de Investigación de los Recursos Biológicos Alexander von Humboldt (IAvH), Bogotá, Colombia. 2012. p. 528. [ Links ]
Pepin L, Amigues Y, Lepingle A, Berthier JL, Bensaid A, Vaiman D. Sequence conservation of microsatellites between Bos taurus (cattle), Capra hircus (goat) and related species: examples of use in parentage testing and phylogeny analysis. Heredity. 1995;74(1):53-61. DOI:10.1038/hdy.1995.7 [ Links ]
Pierce BA. Genetics: a conceptual approach. 4ed. W. H. Freeman Publisher. USA. 2010. p. 400. [ Links ]
Rico C, Rico I, Hewitt G. 470 million years of conservation of microsatellite loci among fish species. Proc Roy Soc London Series B, Biol Sci. 1996;263(1370):549-557. DOI: 10.1098/rspb.1996.0080 [ Links ]
Rueda JV, Rodríguez C, Vaca D, Caicedo D. Tortugas marinas y continentales en Colombia: programa nacional para la conservación. Ministerio del Medio Ambiente. Bogotá, Colombia. 2002. p. 63. [ Links ]
Santos FR, Pena SDJ, Epplen JT. Genetic and population study of an Y-linked tetranucleotide repeat DNA polymorphism with a simple non-isotopic technique. Hum Genet. 1993;90(6):655-656. DOI: 10.1007/BF00202486 [ Links ]
Sax DF, Gaines SD. Species invasions and extinction: the future of native biodiversity on islands. Proc Natl Acad Sci USA. 2008;105(Suppl. 1):11490-11497. [ Links ]
Schneider CJ, Cunningham M, Moritz C. Comparative phylogeography and the history of endemic vertebrates in the Wet Tropics rainforests of Australia. Mol Ecol. 1998;7(4):487-498. DOI: 10.1046/j.1365-294x.1998.00334.x [ Links ]
Schlötterer C, Amos B, Tautz D. Conservation polymorphic simple sequence loci in cetacean species. Nature. 1991;354(6348):63-65. DOI:10.1038/354063a0 [ Links ]
Spinks PQ, Shaffer HB, Iverson JB, Mccord WP. Phylogenetic hypotheses for the turtle family Geoemydidae. Mol Phylogenet Evol. 2004;32(1):164-182. DOI: 10.1016/j.ympev.2003.12.015. [ Links ]
Thomson S, Georges A, Limpus CJ. A new species of freshwater turtle in the genus Elseya (Testudines: Chelidae) from central coastal Queensland, Australia. Chelonian Conserv Biol. 2006;5(1):74-86. DOI: http://dx.doi.org/10.2744/1071-8443(2006)5[74:ANSOFT]2.0.CO;2 [ Links ]
Toledo V. La diversidad biológica de México. Ciencias. 1994;34(1):43-59. [ Links ]
Xin-Sheng W, Tian-Wen W, Hui-Ling Z, Guang-Long C, Qi X, et al. Correlation analysis of wool yield in wan line angora rabbits using microsatellite DNA markers. J Biol Scien. 2008;8(3):679-682. DOI: 10.3923/jbs.2008.679.682 [ Links ]
Walsh PS, Metzger DA, Higuchi R. Chelex 100 as a medium for simple extraction of DNA for PCR-based typing from forensic material. Biotechniques. 1991;10:506-513. [ Links ]
Wright S. Genetical structure of populations. Nature. 1950;166(4215):247-249. DOI: 10.1038/166247a0. [ Links ]
Zane L, Bargelloni L, Patarnello T. Strategies for microsatellite isolation: a review. Mol Ecol. 2002;11(1):1-16. [ Links ]


















