Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Facultad de Ingeniería Universidad de Antioquia
Print version ISSN 0120-6230On-line version ISSN 2422-2844
Rev.fac.ing.univ. Antioquia no.39 Medellín Jan./Mar. 2007
Revista Facultad de Ingeniería N. o 39. pp. 33-41. Marzo, 2007
bLIEC. Universidad Estadual Paulista. Instituto de Química. Araraquara, Brasil.
Resumen
En este trabajo se utilizaron los métodos de coprecipitación y precursor polimérico para obtener nanopartículas de SnO2 dopado con TiO2, CoO, Nb2O3 y Al2O3. Los polvos cerámicos obtenidos fueron caracterizados utilizando difracción de rayos X (DRX), y microscopía electrónica de barrido (MEB). Posteriormente se determinó su sinterabilidad a través de estudios de dilatometría. Muestras sinterizadas del sistema de interés fueron caracterizadas eléctrica y microestructuralmente para determinar su uso como varistores.
--------- Palabras clave: nanopartículas, SnO2, polvos cerámicos, varistores.
Abstract
SnO2 nanoparticles doped with TiO2, CoO, Nb2O3 and Al2O3 were obtained in this work using the methods of coprecipitation and polymeric precursor. X Ray Diffraction (XRD), and Scanning Electron Microscopy (SEM) were used to characterize the ceramic powders obtained. Their synterization capacity was determined by dilatometric studies. Sinterized samples of the system on study were also characterized electrically and microstructurally to determine their suitability as varistors.
--------- Key words: nanoparticles, SnO2, ceramic powders, varistors.
Introducción
El desarrollo en el campo de las nanopartículas cerámicas ha tenido gran efecto en varias áreas de investigación entre las que se destacan la fisicoquímica de las superficies, la adsorción destructiva, catálisis, entre otras. Los cambios de las propiedades de un sistema con el tamaño del mismo, es un tema de interés actual ya que es bien conocido que en la región intermedia, entre 2 y 10 nm, ni la mecánica cuántica ni las leyes clásicas permiten justificar completamente el comportamiento de los mismos [1]. Así, por ejemplo, en las nanopartículas de un tamaño de 3 nm el 50% de los átomos o iones están en la superficie lo que permite manipular las propiedades del interior, “bulk”, del material a través de efectos superficiales y, además, favorecer la química de las reacciones cerca de las condiciones estequiométricas [2]. Por otro lado, cuando existen fuertes enlaces químicos, la deslocalización de los electrones puede variar con el tamaño de la partícula lo que conduce a propiedades físicas y químicas especiales [3]. Las ventajas específicas de los materiales nanocristalinos están relacionadas con la alta uniformidad de las fases que presentan y la posibilidad de sinterizar los dispositivos a baja temperatura [4].
La síntesis de nanopartículas ha recibido considerable atención en vista de la potencialidad de obtener nuevos materiales con propiedades mecánicas, eléctricas, térmicas, catalíticas, ópticas, etc., novedosas y únicas [1, 5, 6]. Lo anterior, ha motivado a muchos investigadores a desarrollar e innovar métodos de síntesis tanto físicos como químicos. Los nuevos métodos de síntesis, o los existentes optimizados, deben permitir la obtención de nanopartículas con cierta morfología, homogeneidad química y características superficiales garantizando la reproducibilidad del método de producción.
El dióxido de estaño, SnO2, cristaliza en una estructura tipo rutilo tetragonal, con valores parámetros de red a = 474 pm y c = 319 pm. Es un semiconductor con una banda prohibida, “gap” de energía, bastante ancha con la banda de valencia, derivada del orbital 2p del oxígeno, completamente llena y la banda de conducción, derivada del orbital 5s del estaño, vacía; el valor del “gap” a 0 K es de aproximadamente 3,7 eV por lo que el SnO2 estequiométrico, a temperatura ambiente, sería un buen aislador (con una resistividad de 106 .m) [7, 8].
En la práctica, tanto los cristales sintéticos como los naturales son deficientes en oxígeno lo que genera niveles donores ubicados a 0,1 eV por debajo de la banda de conducción ocasionando que el SnO2 presente un comportamiento de semiconductor tipo n; dopando el cristal con elementos del grupo V, como el antimonio que favorece el comportamiento tipo n [7, 8].
El SnO2 no sinteriza como cerámica densa debido a su alta covalencia y es necesario adicionar otros óxidos como ZnO, CuO, MgO y CoO para lograr una adecuada densificación; la densidad teórica del óxido de estaño es de 6,95 g.cm-3 y bajo ciertas condiciones de sinterización se han obtenido densidades del 98% de la densidad teórica con composiciones que contienen alrededor del 98% en peso de SnO2 [7].
Por sus propiedades físicas (transferencia, conductividad, etc.), el SnO2 es un óxido de gran interés tecnológico destacándose sus aplicaciones como conductor a alta temperatura (electrodo en los hornos de fundido de vidrio), electrodo transparente para películas delgadas [7], sensor de gas [7, 9, 10], varistor [11] y catalizador [12, 13], aunque no haya recibido la suficiente atención en este último campo [14]. Las nanopartículas de óxido de estaño se han sintetizado por precipitación [15], método hidrotérmico [16], sol-gel [17], proceso hidrolítico [18] reducción carbotérmica [19] y precursor polimérico [20].
En este trabajo se sintetizó SnO2 dopado con TiO2, CoO, Nb2O5 y Al2O3 usando los métodos de coprecipitación y precursor polimérico, garantizando la eliminación de los iones cloruro provenientes del precursor de estaño a través del lavado de la fase sólida del sistema con una solución acuosa de dietilamina. El polvo cerámico obtenido se caracterizó utilizando difracción de rayos X (DRX) y microscopía electrónica de barrido (MEB). Con esta materia prima se conformaron piezas en verde para estudiar su sinterabilidad y con base en estos resultados se obtuvieron muestras densificadas que se caracte¬rizaron microestructural y eléctricamente.
Procedimiento experimental
Los polvos cerámicos utilizados en este trabajo fueron obtenidos por coprecipitación y por el método de precursor polimérico; metodologías que ya fueron descritas y analizadas en artículos previos [21, 22]. Estos polvos contenían 1% en moles de TiO2, 1% en moles de CoO, 0,05% en moles de Nb2O5 y se varió la concentración de Al2O3 utilizando 0,05 y 0,2% en moles de este óxido; los polvos se carcterizaron por DRX, utilizando un difractómetro Siemens D-5000, y microscopía electrónica de barrido, MEB, con el microscopio SM-300 TOPCON.
Se conformaron muestras en verde, con espesor mayor a 1 mm, prensando los polvos inicialmente con una presión de 20 Mpa, de manera uniaxial, y luego con 200 Mpa isostáticamente. Se conformaron algunas muestras para realizar los estudios de contracción y velocidad de contracción de las mismas, utilizando para un dilatómetro NETZSCH 402E, y algunos de los discos iniciales se sinterizaron bajo condiciones definidas partiendo de los resultados de dilatometría con el fin de obtener muestras densificadas.
Las muestras sinterizadas se pulieron y se analizaron a través del microscopio de barrido para conocer su microestructura. A otras muestras pulidas se les depositaron, electrodos de oro sobre su superficie para obtener las curvas de campo eléctrico, E (V/cm) en función de la densidad de corriente, J (mA/cm); para ello se utilizó una fuente Keithey 237 high voltaje source measurement.
Resultados y discusión
En la figura 1 se muestran los difractogramas de los polvos obtenidos por coprecipitación que contenían 0,05% (SCNT05ACS) y 0,2% en moles (SCNT2ACS) de Al2O3. La fase cristalina más importante que presentan las muestras es el SnO (romarchite PDF 6-0395) y aparecen, además, otros picos pequeños y anchos correspondientes al SnO2 (casiterita PDF 41-1445). Por otro lado, los difractogramas correspondientes a las muestras obtenidas por Pechini indican que son amorfas, tal como se puede observar en la figura 2 para una muestra con 0,2% de alúmina.
Si las anteriores se tratan térmicamente a 450 ºC se obtienen los difractogramas de la figura 3. La muestra obtenida por el método de precursor polimérico, y tratada a 600 ºC figura 3 (b), presenta como única fase cristalina la casiterita (PDF 41-1445), mientras que el sólido obtenido por coprecipitación, figura 3 (a), además de los picos de casiterita presenta otros muy pequeños correspondientes al oxihidróxido de estaño Sn3O3(OH)2 (PDF 14-0140).
En la figura 4 se observan las fotografías obtenidas con MEB de los polvos cerámicos sintetizados por coprecipitación, figura 4 (a), y por el método de precursor polimérico, figura 4 (b) muestra que los polvos obtenidos por coprecipitación forman aglomerados con un tamaño mayor a 2 m y que las partículas individuales son nanométricas ( a 200 nm). La muestra sintetizada utilizando el método de precursor polimérico presenta aglomerados más pequeños, menores a 2 m, y partículas primarias nanométricas, más pequeñas que las de coprecipitación.
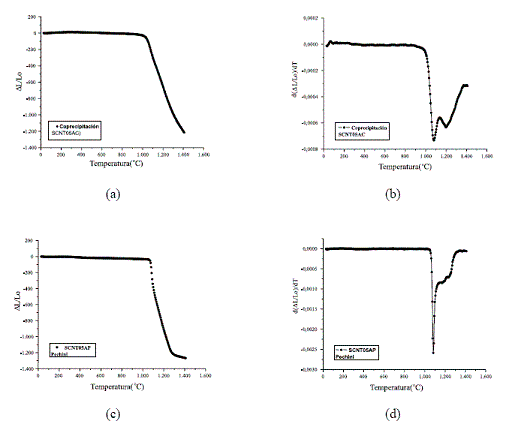
En la figura 5 se indican las curvas de contracción y velocidad de contracción de muestras compactadas utilizando los polvos cerámicos sintetizados por los dos métodos empleados en el trabajo. Como se observa en la curva de contracción de la figura 5 (a), la muestra conformada con los polvos por coprecipitación no alcanza la completa contracción lo que sí sucede con la muestra que contiene los polvos obtenidos por el método de precursor polimérico, figura 5 (c); a partir de 1.290 ºC esta última muestra prácticamente no se contrae.
Figura 1 Difractogramas de rayos X de polvos obtenidos por coprecipitación que contenían 0,05% (SCNT05ACS) y 0,2% en moles (SCNT2ACS) de Al2O3
Figura 2 Difractograma de rayos X de polvo obtenido por Pechini (0,2% de Al2O3—SCNT2APS)
Figura 3 Difractogramas de rayos X de muestras obtenidas por coprecipitación, tratada térmicamente a 450 oC (a) y por Pechini tratada a 600 oC (b)
Figura 4 Fotografías tomadas con MEB de muestras del sistema Sn-Ti-Co-Nb con 0,5% de Al2O3 obtenidas por: (a) coprecipitación y (b) precursor polimérico
Figura 5 Curvas de contracción y velocidad de contracción obtenidas para muestras compactadas de polvos cerámicos, tratados térmicamente a 600 oC, y sintetizados por coprecipitación, (a) y (b), y por el método de precursor polimérico, (c) y (d)
Las curvas de velocidad de contracción muestran que los principales mecanismos de sinterización ocurren a 1.080 y a 1.200 ºC, aproximadamente, con algunos cambios dependiendo del método de síntesis. De acuerdo a la literatura [22], el mecanismo de sinterización que se presenta a 1.080 ºC se podría atribuir tanto a las vacancias generadas por el CoO, a los defectos intersticiales del Ti, así como al efecto relacionado con la naturaleza del enlace ionicovalente; el que ocurre a mayor temperatura se debe principalmente a la presencia de vacancias de oxígeno generadas por el cobalto.
Con base en estos resultados, se sinterizaron las muestras prensadas de polvos obtenidos por coprecipitación a 1.450 ºC en aire, durante 2 horas y a una velocidad de calentamiento de 5 ºC/min, y a 1.350 ºC las que contenían los polvos obtenidos por Pechini, bajo las mismas condiciones de tratamiento térmico. En la tabla 1 se indican los valores de densidad obtenidos para las muestras sinterizadas.
Tabla 1 Valores de densidad de las muestras sinterizadas y de algunos de sus parámetros eléctricos característicos
En la figura 6 se muestran las curvas de campo eléctrico (E) en función de densidad de corriente (J) para las muestras sinterizadas y electrodadas. En la tabla 1 se indican los valores de los principales parámetros eléctricos de los dispositivos. El mejor comportamiento varistor lo presentan las muestras obtenidas por el método de precursor polimérico, SCNT05AP y SCNT2AP con valores de coeficiente no lineal de 15 y 22 respectivamente. Una diferencia importante entre estas dos muestras es el voltaje de ruptura, mayor para la que tiene más contenido de alúmina (SCNT2AP); esto indica que es mayor el número de bordes de grano activos en esta muestra situación que pudo ser ocasionada por un menor tamaño de grano.
Figura 6 Curvas de E(V/cm) en función de J(mA/cm2) para muestras sinterizadas conformadas con polvos sintetizados por coprecipitación (a) y Pechini (b)
En la figura 7 se indican las microestructuras de las muestras sinterizadas. La microestructura de las muestras conformadas con polvos cerámicos obtenidos por coprecipitación, figura 7 (a), presenta poca porosidad, un tamaño de grano de aproximadamente 10 m y una distribución de tamaño no muy uniforme. Algo similar ocurre con las muestras sinterizadas de polvos sintetizados por el método Pechini, figura 7 (b); en este caso el tamaño de grano es ligeramente menor.
Los resultados anteriores ponen en evidencia el efecto de los aglomerados de partículas que inicialmente conformaban el material compactado. Entre otras palabras, durante la densificación de estas muestras se presentaron dos etapas de sinterización: intra aglomerados, sinterización de las nanopartículas al interior de los aglomerados, e inter aglomerados, sinterización de los “agregados” de nanopartículas. Es necesario realizar un estudio más cuidadoso de estas etapas de sinterización para lograr un mayor control sobre la microestructura de la muestra densificada.
Figura 7 Microestructura de muestras conformadas con polvos obtenidos por Pechini (a) y Coprecipitación (b) sinterizadas a 1.350 y 1.450 oC respectivamente.
Conclusiones
Se sintetizaron nanopartículas de SnO2 dopadas con TiO2-CoO-Nb2O5 y Al2O3. Los polvos cerámicos obtenidos estaban constituidos por SnO, fase cristalina mayoritaria, y SnO2 cuando se utilizó coprecipitación y amorfos por el método de precursor polimérico; mientras los primeros presentaron gran aglomeración los segundos resultaron más dispersos. La casiterita es la principal fase cristalina después de tratar térmicamente los polvos a 450 (coprecipitación) y 650 ºC (sintetizados por el método de precursor polimérico).
Las muestras en verde que presentaron mejor sinterabilidad fueron las conformadas utilizando polvos cerámicos sintetizados por el método de precursor polimérico; la máxima contracción se obtuvo a 1.320 ºC y los principales mecanismos de sinterización ocurrieron a 1.080 y 1.200 ºC.
El mejor efecto varistor lo presentaron las muestras conformadas con polvos sintetizados por el método de precursor polimérico y sinterizadas a 1.350 ºC durante 2 horas. Los valores de obtenidos fueron altos, 15 y 22, y la mayor diferencia entre las dos muestras estudiadas fue el voltaje de ruptura, ma yor para el de mayor contenido de Al2O3 y además, presentó mayor valor de [22].
Las muestras sinterizadas no presentaron muy alta porosidad, salvo la muestra SCNT05AC, y las que mejor densificaron fueron las conformadas con los polvos obtenidos por el método de precursor polimérico (98% de la densidad teórica). El desarrollo de dos etapas de sinterización fue evidente: uno intra y otro interaglomerado. Para lograr un mejor control de la microestructura de estos dispositivos, y por lo tanto de sus propiedades, es necesario estudiar más cuidadosamente estas etapas que ocurren durante la sinterización.
Agradecimientos
Los autores desean agradecer al proyecto CIAM-COLCIENCIAS que brindó ayuda económica para que Jorge E. Rodríguez Páez pudiera realizar actividades de investigación en el Laboratorio Interdisciplinar de Cerámicos LIEC-Araraquara/Brasil e INTEMA-Mar de Plata/Argentina, así como al proyecto PROSUR-CNPq/Brasil por el aporte en suministros y reactivos y al proyecto PROALERTA-VIII.13 por la ayuda económica brindada al Sr. Adolfo A. Mosquera Lozano.
Referencias
1. J. Klabunde. Nanoscale materials in chemistry. New York. John Wiley & Sons Ind. 2001. pp. 85-120. [ Links ]
2. K. J. Klabunde, J. V. Stark, O Koper, C Mohs, D. G. Park, S. Decker, Y. Jiang, I. Lagadic, D. Zhang, “Study of nanoscale powder preparation”. J. Phys. Chem., Vol 100. 1996. pp. 12142-12153. [ Links ]
3. K. J. Klabuncfe, C. Mohs. Chemistry of advanced materials. NewYork. L. V.Interrante, M. J. Hampden-Smith (editors). 1998. Chap. 7. pp. 317-358. [ Links ]
4. J. Herring. “Effect of change of scale on sintering phenomena”. J. Appl. Phys. Vol. 21. 1950. pp. 301-330. [ Links ]
5. F. F. Lange. “Powder processing science and technology for increased reliability”. J. Am. Ceram. Soc. Vol 72. 1989. pp. 3-15. [ Links ]
6. W. Luán, L. Gao, J. Guo. “Study on drying stage of nanoscale powder preparation”. Nanostruct. Mater. Vol. 10. 1998. pp. 1119-1125. [ Links ]
7. J. Moulson, J. M. Herbert. Electroceramics. John Wiley & Sons. Inc. second edition. 2003. pp. 135 - 240. [ Links ]
8. J. M. Jorzebsk, J. P. Marton. “Physical properties of SnO2 materials. II Electrical properties”. J. Electrochem. Soc. Vol. 129. 1976. pp. 299C-310C. [ Links ]
9. M. A. Ponce. Comportamiento eléctrico de sensores de gases de SnO2, Tesis doctoral Universidad Nacional de Mar del Plata-INTEMA. 2005. [ Links ]
10. L. Hozer. “Semiconductor ceramics: grain boundary effects”. Ellis Horwood series in Physics and its applications. 1994. pp. 44-98. [ Links ]
11. S. A. Pianaro, P. R. Bueno, E. Longo, J. A. Varela. “A new SnO2 based varistor system”. J. Mater. Sci. Lett. Vol. 14. 1995. pp. 692-694. [ Links ]
12. J. Shen, R. D. Cortright, Y. Chen, J. A. Dumisec. “Microcalorimetric and infrared spectroscopic studies of Al2O3 modified by tin oxides”. Catal. Lett. Vol. 26. 1984. pp. 247-257. [ Links ]
13. T. Tagawa, S. Kataoka, T. Hattori, Y. Murakami. “Supported tin dioxide catalysts for the oxidative dehydro¬genation of ethylbenzene”. Appl. Catal. Vol. 4. 1982. pp.1-4. [ Links ]
14. N. Sergent, P. Gélin, L. Périer-Cambry, H. Praliaud, G. Thomas. “Preparation and characterization of high surface area stannic oxides: structural, textural and semiconducting properties”. Sens. Actuators B. Vol. 84. 2002. pp. 176-1888. [ Links ]
15. A. C. Bose, D. Kalpana, P. Thangadurar, S, Ramasamy. “Synthesis and characterization of nanocrystalline SnO2 and fabrication of lithium cell using nano-SnCY”. J. Pow. Source. Vol. 107. 2002. pp. 138-141. [ Links ]
16. N. S. Baik, G. Sakai, N Miura, N. Yamazoe. “Preparation of stabilized nanosized tin oxide particles by hydrothermal treatment”. J. Am. Ceram. Soc. Vol. 83. 2000. pp. 2983-2987. [ Links ]
17. Z. Zhang, L Gao. “Synthesis and characterization of nanocrystalline tin oxide by sol-gel method”. J. Solid State Chem. Vol. 177. 2004. pp.1425-1430. [ Links ]
18. Z. Deng, C. Wang, Y. U. “New hydrolytic process for producing zirconium dioxide, tin dioxide and titanium dioxide nanoparticles”. J. Am. Ceram. Soc. Vol. 85. 2002. pp. 2837-2839. [ Links ]
19. E. R. Leite, J. W. Gomes, M. M. Oliveira, E. J, H. Lee, E. Longo, J. A. Varela, C. A. Paskocimas, T. M. Boschi, F. Lanciotti, P. S. Pisan, P. C. Soares. “Synthesis of SnO2 nanoribbons by a carbothermal reduction process”. J. Nanosci. Nanotechn. Vol. 2. 2002. pp. 125-128. [ Links ]
20. E. R. Leite, A. P. Maciel, I. T. Weber, P. N. L. Filho, E. Longo, C, O. P. Santos, A. V. C. Andrade, C. A. Pakos¬cimas, Y. Manietle, W. H. Schreiner. “Development of metal oxide nanoparticles with high stability against particle growth using a metastable solid solution”. Adv. Mater. Vol. 14. 2002. pp. 905-908. [ Links ]
21. C. Ararat, J. A. Varela, J. E. Rodríguez Páez. “Uso de métodos químicos para obtener polvos cerámicos del sistema (Sn, Ti)O2”. Bol, Soc. Esp. Ceram. Vol. 44. 2005. pp. 215-222. [ Links ]
22. C. Ararat, J. A. Várela, J. E. Rodríguez-Páez. “Efecto del método de síntesis sobre la sinterabilidad de los polvos cerámicos de (Sn, Ti)O2”. Revista de la Academia Colombiana de Ciencias Exactas, Físicas y Naturales, Vol. 29. 2005. pp. 271-281. [ Links ]
* Autor de correspondencia. Teléfono + 57+7 – 820 98 00 ext 2410, fax 57+7+ 820 98 60, correo electrónico: aamosquera@unicauca.edu.co