Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
CES Medicina
Print version ISSN 0120-8705
CES Med. vol.24 no.2 Medellín July/Dec. 2010
ARTÍCULOS DE INVESTIGACIÓN CIENTÍFICA O TECNOLÓGICA
Costo efectividad del dasatinib en el tratamiento de la leucemia mieloide crónica en pacientes resistentes al imatinibs
Cost-effectiveness of dasatinib in the treatment of chronic myeloid leukemia patients resistant to imatinib
JOHN JAIRO OROZCO1, JUAN ESTEBAN VALENCIA2, ELEONORA AIELLO3; GABRIEL RIBÓ,N4;FERNANDO GUERRERO5, RAFAEL GARCÍA6, JOSE L. MUJICA7
1 Investigador Grupo Evaluación de Tecnologías en Salud - Universidad CES Medellín Colombia
2 Gerente Médico Científico Oncología - Bristol Myers Squibb (BMS) Colombia
3 Gerente Economía de la Salud - BMS Sudamérica 4 Gerente Médico Científico Cardio-Metabólicos - BMS Colombia
5 Director Médico - BMS North Hub
6 Gerente Médico Científico Oncología - BMS Venezuela
7 Médico Hematólogo, Centro Clínico La Urbina - Caracas, Venezuela
RESUMEN
Objetivo: con base en una evaluación económica realizada previamente, se realizó una adaptación de ésta a Venezuela y Colombia, previo análisis de transferibilidad de datos. Mediante esta adaptación se compararon los costos y la relación de costo-efectividad del uso de la dosis de 100 mg/día y 140 mg/día de dasatinib, el uso de 800 mg/día de nilotinib y el uso de una dosis mayor de imatinib (800mg/día), para cada fase de la enfermedad, en pacientes que desarrollaron resistencia a la dosis habitual de imatinib.
Métodos: para realizar la adaptación de la evaluación económica, se asumieron las probabilidades de cambio de acuerdo al modelo de Markov, donde se consideró una cohorte de 10 000 pacientes con LMC en sus tres fases (crónica, acelerada y blástica) a lo largo de toda la vida y con una tasa de descuento del 3,5 % para los costos y beneficios. Los resultados del modelo incluyeron los costos de cada alternativa de tratamiento con dasatinib, nilotinib o imatinib y los años de vida ajustados a calidad ganados. Los costos se expresan en pesos colombianos y bolívares fuertes del año 2009.
Resultados: en la fase crónica de la enfermedad, dasatinib 100 mg/día produjo la mayor cantidad de años de vida ajustados a calidad, tanto para Colombia como para Venezuela (6,88 y 6,54, respectivamente) y la menor relación de costo-efectividad. En la fase acelerada, dasatinib 140 mg/día también mostró la menor relación de costo-efectividad en comparación con imatinib y nilotinib. En la fase blástica, dasatinib mostró menor relación de costo-efectividad que imatinib.
Conclusiones: el dasatinib a dosis de 100 mg/día y 140 mg/día mostraron los índices más bajos de costo-efectividad que en las dosis de 800 mg/día de nilotinib para el tratamiento de pacientes con resistencia a la dosis habitual de imatinib en la fase crónica de la LMC, así como en la acelerada y la blástica. Aunque hubo un aumento de los costos en general, especialmente debido al costo de dasatinib en 140 mg/dosis al día, este hecho se explica por el aumento en años de vida ganados y, en consecuencia, el uso de recursos médicos y medicamentos.
PALABRAS CLAVES
Leucemia, Resistencia, Imatinib,Dasatinib, Nilotinib, Costo Efectividad, Transferibilidad
ABSTRACT
Objective: Based on a previously performed economic evaluation, we adapted a Cost-effectiveness model for Venezuela and Colombia, after a data transferability analysis. We compared the costs and cost-effectiveness ratio of using 100mg/day and 140 mg/day doses of Dasatinib versus 800 mg/day doses of Nilotinib or an increased dose of Imatinib (800mg/day), for each phase of the disease, in patients who developed resistance to habitual doses of Imatinib.
Methods: To adapt the economic evaluation, we assumed the transition probabilities based on the Markov model used for this economic evaluation, which considered a cohort of 10.000 CML patients in its three phases (chronic, accelerated or blast phase), a lifetime horizon and a 3.5 % discount rate for costs and benefits. Model results included the costs of each treatment alternative with Dasatinib, Nilotinib or Imatinib, and the Quality Adjusted Life Years (QALYs) gained. Costs were measured in Colombian pesos and Bolivares Fuertes (BsF) of year 2009.
Results: In the chronic phase of the disease, dasatinib 100 mg/day yielded the highest amount of QALYs both for Colombia and Venezuela (6,88 and 6,54 respectively) and the lowest cost-effectiveness ratio. In the accelerated phase, Dasatinib 140 mg/day also showed the lowest cost-effectiveness compared to Nilotinib and Imatinib. In the blast phase, dasatinib showed lower cost-effectiveness ratio than imatinib.Conclusions: Dasatinib 100 mg/day and 140 mg/ day showed the lowest cost-effectiveness ratios than doses of 800 mg/day of Nilotinib for the treatment of patients with CML resistant to usual imatinib doses in the chronic phase, as well as in the accelerated and blast phases. Although there was an overall cost increase, especially due to the cost of Dasatinib in 140 mg/day doses, this fact was explained by the increase in years of life gained and, consequently, the use of medical resources and drugs in the timeline of treatment.
KEY WORDS
Leukemia, Imatinib, Dasatinib, Nilotinib, Cost Effectiveness, Resistence, Transferability
INTRODUCCIÓN
La leucemia mieloide crónica (LMC) es una condición maligna de las células hematopoyéticas primordiales y representa cerca del 15 % de los pacientes con leucemia (1). Es una enfermedad más común en adultos que en niños, aunque la leucemia es el cáncer más común éstos, siendo la leucemia linfocítica aguda la más común en ellos. El tipo más frecuente de leucemia en adultos es la leucemia mieloide aguda, seguida por la leucemia linfocítica crónica, la leucemia mieloide crónica y la leucemia linfocítica aguda (2-4).
En la LMC se produce un excesivo número de células leucémicas de la línea blanca, de manera que suprimen la producción de células blancas normales. En un 95 % de los casos, los pacientes con LMC tiene una anormalidad cromosómica conocida como cromosoma Filadelfia que consiste en una traslocación recíproca entre el brazo largo del cromosoma 22 y el cromosoma 9 (5). La consecuente anormalidad molecular es la proteína quimérica BCR-ABL, una tirosin quinasa (6). Esta alteración en la proteína ABL favorece la proliferación, la resistencia a la apoptosis y altera la adhesión (7-9). La incidencia de LMC es de 1,5 por 100 000 personas por año, y la incidencia ajustada para la edad es más alta en hombres que en mujeres (2,0:1,2).
La incidencia de este tipo de leucemia aumenta lentamente con la edad hasta mediados de la década de los cuarenta, cuando empieza a aumentar rápidamente (2-4).
Generalmente, la enfermedad comienza con una fase crónica que progresa durante varios años, alrededor de cuatro a seis si se deja sin tratamiento, para pasar a una fase acelerada de 18 meses aproximadamente y finalmente entrar en una fase blástica, de unos cuatro a seis meses. El 90 % de los pacientes son diagnosticados en la fase crónica (10-12). Los pacientes diagnosticados en esta fase tienen un promedio de vida de tres a cinco años.
A la fecha, no existe un tratamiento de inmunoterapia o quimioterapia que ofrezca una curación definitiva. Solo el trasplante de medula ósea ofrece una cura, con un alto riesgo y está disponible sólo para una minoría de pacientes con condiciones muy específicas y dependiendo de la disponibilidad de un donante. Los tratamientos con medicamentos para el control de la enfermedad incluyen interferon alfa e hidroxiurea. El primero, con una marcada toxicidad y una disminución de su eficacia directamente proporcional al tiempo de duración de la fase crónica (12) y el segundo no ha mostrado evitar la progresión de la enfermedad hacia la fase blástica y acelerada (13).
Adicionalmente, existen los medicamentos inhibidores de la tirosin quinasa BCR-ABL, cuyo primer exponente fue imatinib, una molécula pequeña que se convirtió desde el año 2001 en el tratamiento estándar de primera línea para la LMC recién diagnosticada (14-16).Sin embargo, se ha encontrado que hasta el 30 % de los pacientes recién diagnosticados en la fase crónica, y tratados con imatinib, habían descontinuado la terapia después de cinco años de seguimiento debido a falla terapéutica o a toxicidad (17-18). De otro lado, la resistencia a imatinib a dosis de 400 a 600 mg está bien documentada en los pacientes con LMC y sus alternativas terapéuticas son limitadas.
Más recientemente, fue aprobado en Estados Unidos y en la Unión Europea, el medicamento dasatinib, un inhibidor multi objetivo de la tirosin quinasa BCR-ABL, SRC, c-Kit, ephrin y PDGFR, que ha demostrado ser seguro y efectivo en las tres fases de la LMC cromosoma Filadelfia positivo (19-21).
In vitro, dasatinib posee 325 veces más potencia que imatinib en la inhibición de la tirosin quinasa BCR-ABL y a diferencia de éste y de su derivado, nilotinib, puede unirse tanto a la forma activa como inactiva de la enzima (22-25).
En modelos de línea celular, dasatinib inhibió, con excepción de una, todas las mutaciones BCR-ABL referidas a la resistencia al imatinib, lo que puede explicar en parte, la mayor eficacia reportada con dasatinib in vitro (26-29). Una respuesta durable, tanto hematológica como citogenética ha sido demostrada con dasatinib en un número de estudios clínicos fase II, en pacientes con LMC (30-32).
Es así como para el tratamiento de los pacientes resistentes a las dosis convencionales de imatinib o que han presentado eventos adversos severos, se ha propuesto aumentar a 600 u 800 mg o cambiar a dasatinib a dosis de 100 mg o de 140 mg en la fase crónica y a 140 mg en la fase acelerada y en la fase blástica. También se ha propuesto la utilización de otro medicamento inhibidor de la SRC-ABL kinasa, como es nilotinib a dosis de 800 mg en la fase crónica y en la fase acelerada. Este último no es recomendado para uso en la fase blástica (33).
En febrero de 2009 se presentó el reporte final de la investigación "An economic evaluation of dasatinib for the treatment of chronic myelogenous leukaemia in imatinib - resistant patients", el cual mostró que dasatinib se asocia con un incremento en la expectativa de vida y en los años de vida ajustados por calidad (QALY´s por sus siglas en ingles Quality Adjusted Life Year) con un costo efectivo incrementado de 36, 435 libras por QALY, y en la gran mayoría, los costos aumentados eran debidos a un incremento en la expectativa de vida asociada con el tratamiento con dasatinib (34).
Teniendo en cuenta que existe concordancia entre los protocolos latinoamericanos e ingleses en el manejo de la LMC y que se requiere explorar alternativas de acción para el manejo de aquellos pacientes que presentan resistencia al imatinib tanto en la fase crónica como en las fases acelerada y blástica, es importante hacer un análisis de costos y de costo efectividad de los medicamentos dasatinib, nilotinib y dosis incrementales de imatinib.
El presente trabajo pretende hacer una evaluación económica de dasatinib en el tratamiento de la LMC en pacientes resistentes a imatinib a partir de la probabilidad de cambio entre estados de salud, reportada en el estudio realizado por el Consorcio de Economía de la Salud de York. Y aunque las probabilidades del trabajo original, previo análisis de transferibilidad, pueden ser asumidas para Colombia y Venezuela, los costos y las tasas de mortalidad diferentes en cada jurisdicción, obligan a hacer las adaptaciones del modelo con el objetivo de encontrar las relaciones de costo efectividad en cada entorno particular.
MÉTODOS
Este trabajo hace una evaluación económica de los costos y de la relación de costo-efectividad del medicamento dasatinib en relación con dosis mayores del imatinib y con el nilotinib, en pacientes con resistencia a las dosis habituales de imatinib o que han presentado eventos adversos severos a éste. Para ello se basó en el trabajo original realizado por el Consorcio de Economía de la Salud de York, haciendo una transferibilidad de datos de acuerdo a las recomendaciones de expertos.
Teniendo en cuenta que la evaluación económica de intervenciones en salud es utilizada cada vez más en diferentes países y que los decisores económicos las están demandando para una mejor utilización de los recursos sociales, se requiere que las evaluaciones económicas realizadas en un contexto puedan ser transferidas a otros. Sin embargo, estas evaluaciones presentan limitación a la hora de transferir resultados entre distintos países o regiones, ya que aunque muchos resultados pueden ser comunes, existen variables que necesariamente deben ser ajustadas. Este es el caso por ejemplo de la incidencia, prevalencia y severidad de una determinada enfermedad, disponibilidad de recursos para la salud, disposición a pagar, precios de los recursos, así como diferentes prácticas médicas. De acuerdo a la Task force on good research practices on transferability of economic data in health technology (35), los datos pueden ser transferibles si ellos pueden ser adaptados para aplicar en otros países o regiones.
Dependiendo de si el estudio de costo efectividad es relevante en la nueva jurisdicción y si las prácticas clínicas son comparables para la intervención que se evalúa, la transferibilidad se puede asumir a través de una parametrización de un modelo de decisión analítico (35), aunque también se podrían hacer algunas inferencias de los resultados del estudio de costo efectividad original. Este modelo analítico debe evaluar si hay evidencias de heterogeneidad en los patrones de uso, costos, sobrevivencia, riesgos de mortalidad y utilidades, y adicionalmente debe obtener datos sobre disposición a pagar y restricciones presupuestarias.
En el trabajo original que nos ocupa, la revisión de las guías y protocolos de manejo de la LMC en Colombia y Venezuela (36) nos permite asumir unos patrones de uso similares a los contemplados en el modelo original. Igualmente, en el trabajo de York, no encontramos variables que permitan inferir diferencias en la efectividad de los tratamientos en razón de características poblacionales particulares. Es decir, las probabilidades de pasar de un estado de salud a otro, en el modelo de Markov planteado para la LMC, se asumen según el modelo original.
Sin embargo, y siguiendo las recomendaciones de expertos en temas de transferibilidad de datos, consideramos que sí es muy alta la probabilidad de que se presenten diferencias en los costos de tratamiento médico adicionales a los del tratamiento farmacológico y, adicionalmente es evidente que existen diferencias en la mortalidad por causas diferentes a la LMC entre Inglaterra, Colombia y Venezuela.
Estos últimos parámetros debieron ser ajustados en el modelo y por supuesto afectan tanto las utilidades en términos de QALY como los costos de los tratamientos. Los datos de mortalidad en Colombia fueron tomados de la información oficial del DANE para el año 2008 (37) y en el caso de Venezuela del Instituto Nacional de Estadística que reportó datos para el año 2007 (38).
Métodos para la evaluación económica
Con el objetivo de poder hacer una evaluación de la eficiencia de dos o más alternativas de acción, con unos recursos determinados, en relación con un mismo objetivo médico o en relación con el mejoramiento de la calidad de vida, se utiliza el análisis de costo-efectividad de cada una de estas alternativas de acción que permite evaluar los resultados en salud por cada unidad de recurso invertido. Adicionalmente, podemos evaluar los costos adicionales en que se incurriría por cada unidad adicional de resultados si eligiéramos una intervención más efectiva que otra, pero con una relación de costo-efectividad menos favorable. Esto último se denomina análisis incremental, y es conocido por sus siglas en inglés como ICER (Incremental cost-effectiveness ratio) (39).
Para la evaluación económica de dasatinib en pacientes con LMC resistentes a dosis habituales de imatinib, se tuvieron en cuenta las efectividades reportadas en el estudio original, y con los costos para Colombia y Venezuela, y para los ajustes en la mortalidad se procedió a adaptar el modelo para así obtener los resultados de costos de los tratamientos, las relaciones de costo-efectividad y los análisis incrementales entre los diferentes tratamientos con los inhibidores de la SRC-ABL kinasa.
El desarrollo del modelo contempló los supuestos iniciales del trabajo de York de una población de diez mil pacientes con una edad de inicio de 56 años y un horizonte de tiempo de toda la vida, la tasa de descuento para los costos y para los beneficios se conservó en 3,5 % para ambos. La Organización Mundial de la Salud recomienda tasas de descuento para los resultados en salud que van entre 3 % y 5 %, dependiendo del nivel de ingreso de cada país (40).
Para el caso de los eventos adversos, solo se incluyeron aquellos que impactaran el costo y la calidad de vida, es decir, eventos adversos serios (EAS). Su ocurrencia afecta la utilización de recursos en el paciente, así como su calidad de vida.
Los EAS no constituyen un estado en sí mismos, sino que se incorporan dentro del estado existente para el paciente. El modelo original de York, solo los consideró en el periodo inicial de tratamiento, en parte debido a la falta de datos con el dasatinib en el largo plazo. Estos EAS fueron tenidos en cuenta, tanto en los costos como en la perdida de utilidad. El cálculo de los costos se hizo a partir de la probabilidad de ocurrencia del evento y de la frecuencia de uso de los recursos para cada evento, según lo reportado en el trabajo de York, con los valores monetarios en Colombia y Venezuela, de cada uno de estos recursos individuales.
Modelo de Markov
Como en el trabajo original, se usó un modelo de Markov que permitiera evaluar el costo-efectividad de los tratamientos, teniendo en cuenta la probabilidad de cambiar entre un estado y otro, al tiempo que pudiera hacerse una predicción de los costos y de los beneficios en salud a lo largo de toda la vida para cada uno de las opciones de tratamiento. Lo anterior permite ajustar el hecho de que la evidencia actual sólo permite medir los resultados y los costos en el corto plazo, y en realidad estos se prolongarán a lo largo de la vida del paciente (41).
Cálculo de los costos
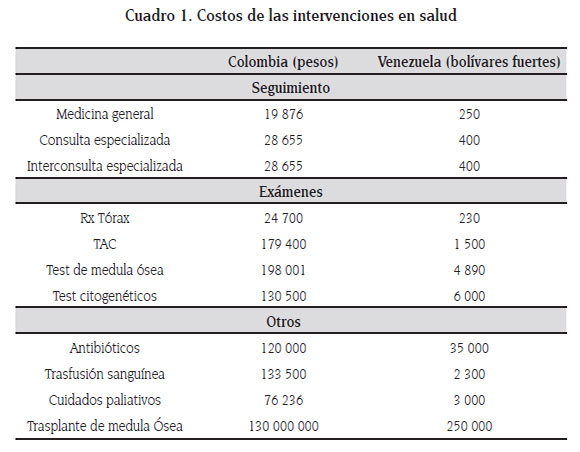
Los costos de los medicamentos fueron tomados de los reportes de las tarifas máximas vigentes para la comercialización, tanto para Colombia como para Venezuela y en monedas nacionales, es decir, pesos colombianos y bolívares fuertes del año 2009. Para el cálculo de los costos de las intervenciones médicas en Colombia se empleó el Decreto 2423 de 1996 del entonces Ministerio de Salud, actualizado al año 2009 y que sirve de referente para las negociaciones entre prestadores y aseguradores de salud (42). En el caso de los tratamientos médicos en Venezuela se consultó a un experto que utilizó como referencia los costos en instituciones privadas clase A y C, de acuerdo a la denominación de las normas Covenin. Estos costos son ajustados cada tres meses de acuerdo al índice inflacionario. En el cuadro 1 se pueden observar los costos de las intervenciones médicas tanto en pesos colombianos como en bolívares fuertes.
El horizonte de tiempo para el cálculo de estos costos fue desde el diagnóstico inicial de la LMC, durante la vida del paciente y hasta su muerte.
Para el cálculo de los QALY´s se asumieron las utilidades contempladas en el estudio original, siendo afectadas en su valor total por la mortalidad particular de cada país.
Análisis Incremental
El análisis incremental permite saber cuál es el costo marginal (incremental) por cada unidad adicional de efectividad de la opción más efectiva, por encima de la alternativa menos efectiva y menos costosa (44). Cuando una alternativa de acción más efectiva es más costosa que la otra y al mismo tiempo tiene mejor relación de costo efectividad, se considera que tiene dominancia extendida sobre la alternativa a comparar. Cuando tiene no solamente una mejor relación de costo efectividad que sus alternativas, sino que además es más efectiva y menos costosa, se puede afirmar que es costo ahorrador y se considera que tiene dominancia fuerte. Cuando hay dominancia fuerte no aplica el análisis de costo incremental.
RESULTADOS
Costos
Cuando dasatinib es usado en la fase crónica a una dosis de 100 mg, el costo del tratamiento total para el resto de la vida de cada paciente se calculó en $987 893 242 pesos colombianos y $1 256 253 bolívares fuertes. Cuando es usado a una dosis de 140 mg, el costo del tratamiento total para el resto de la vida de cada paciente se calculó en $963 976 565 pesos colombianos y de $1 264 644 bolívares fuertes para Venezuela. El costo para los pacientes del grupo nilotinib se calculó en $945 459 343 pesos colombianos y de $1 402 205 bolívares fuertes para Venezuela.
Estos costos incluyen medicamentos, consultas por medicina general y especializada, exámenes de laboratorio, imagenología y las visitas médicas intrahospitalarias. Son el resultado del manejo durante toda la enfermedad y no solamente como resultado de dasatinib o nilotinib. A mayor efectividad, mayores costos, en la medida en que los pacientes incrementan su expectativa de vida.
En Colombia, para el grupo dasatinib a 100 mg y a 140 mg, el 76,2 % y 76,4 % de los costos respectivamente, fueron debidos al medicamento directamente; mientras que para el grupo de nilotinib esta participación fue de 77,5 %. En el caso de Venezuela, la participación porcentual del costo del medicamento para el grupo dasatinib a 100 mg y a 140 mg fue del 59,4 % y 60,9 % respectivamente, mientras que esta participación para el grupo de nilotinib fue del 67 %.
Para pacientes en la fase acelerada tratados con dasatinib a 140 mg, los costos totales durante su vida alcanzarían $595 171 509 pesos colombianos y de $957 770 bolívares fuertes para Venezuela. En el caso de Colombia, el 60 % y el 56 % de estos costos fueron debidos directamente al costo de dasatinib y del nilotinib, respectivamente. Para Venezuela, el 40 % de estos costos fueron debidos directamente al medicamento, tanto para dasatinib y nilotinib.
En la fase blástica, el costo del tratamiento para los pacientes tratados con dasatinib a 140 mg fue de $123 667 085 pesos colombianos y de 202 423 bolívares fuertes para el caso de Venezuela. En el caso de Colombia, el 87 % de este costo corresponde al costo del medicamento, mientras que para Venezuela fue del 58 %.
Efectividad
Los resultados de efectividades en términos de QALY's, se pueden observar en los cuadros 2-4 para las fases crónica, acelerada y blástica, para Colombia y Venezuela, respectivamente
Fase crónica
Los pacientes tratados con dasatinib experimentaron una mayor expectativa de vida ajustada por calidad tanto para Colombia como para Venezuela, comparados con los pacientes 38 Revista CES MEDICINA Volumen 24 No.2 Julio - Diciembre / 2010 tratados con imatinib o nilotinib. En esta fase se utilizaron dos esquemas de tratamiento con dasatinib: 100 y 140 mg, en las demás fases sólo se utilizó dasatinib de 140 mg.
Para la rama de dasatinib de 100 mg, los pacientes experimentaron 6,88 QALY para Colombia y 6,54 QALY para Venezuela. En el grupo de dasatinib de 140 mg los pacientes experimentaron un total de 6,33 QALY para Colombia y 6,03 QALY para Venezuela. Para pacientes del grupo de nilotinib la ganancia fue de 6,03 QALY para Colombia y de 5,73 QALY para Venezuela; y en el grupo de pacientes tratados con imatinib fue de 4,23 QALY para Colombia y 4,10 QALY para Venezuela.
En el cuadro anterior se puede observar cómo dasatinib de 100 mg, presenta la mejor relación de costo efectividad media y la mayor ganancia de QALY's, seguido por dasatinib de 140 mg, y luego por nilotinib, dejando en el último lugar, con la menor producción de QALYs (4,23 para Colombia y 4,1 para Venezuela) y la menos favorable relación de costo efectividad, al imatinib de 800 mg.
Al realizar el análisis incremental, se encuentra que en Venezuela, tanto dasatinib de 100 mg como de 140 mg tuvieron dominancia fuerte sobre el nilotinib. En Colombia, el análisis incremental muestra que el costo adicional por cada QALY ganado sobre la efectividad de nilotinib de 800 mg, fue de $49 922 234 para dasatinib de 100 mg y de $61 724 073 para dasatininb de 140 mg.
Cuando se realizó el análisis de dasatinib en sus dos presentaciones, en relación a imatinib de 800 mg, en ambos casos para Colombia, el costo incremental por QALY, fue de $30 693 725 para dasatinib de 100 mg y de $27 343 664 para dasatinib de 140 mg. Estos valores son inferiores, incluso que el costo efectividad medio para todas las alternativas. Igual sucede en Venezuela, en donde el costo incremental sobre el imatinib de 800 mg, fue de $2 238 y $7 177 bolívares fuertes, para dasatinib de 100 mg y 140 mg, respectivamente.
Fase acelerada
Los pacientes tratados con dasatinib a dosis de 140 mg presentaron una mayor expectativa de vida y más QALY´s, en comparación con aquellos tratados con imatinib o nilotinib. Los pacientes con LMC durante esta fase y que fueron tratados con dasatinib tuvieron un total de 2,89 QALY´s para Colombia y de 2,78 QALY´s para Venezuela. En contraste, aquellos tratados con imatinib experimentaron 0,83 QALY´s, tanto para Colombia como para Venezuela, al tiempo que aquellos tratados con nilotinib experimentaron 2,03 QALY´s para Colombia y 1,97 QALY´s para Venezuela. Los pacientes que recibieron dasatinib ganaron más años que los pacientes de los otros dos medicamentos. La expectativa de vida de los pacientes tratados con dasatinib fue de cinco años para Colombia y de 4,82 para Venezuela, comparadas con 2,02 y 2,01 años de los grupos de imatinib y de 3,82 y 3,70 años para el nilotinib.
Se puede observar como dasatinib de 140 mg presenta la mejor relación de costo efectividad media y la mayor producción de QALY´s, seguido por nilotinib de 800 mg, dejando en el último lugar con la menor producción de QALY´s (0,83 para Colombia y Venezuela) y la menos favorable relación de costo efectividad, a imatinib de 800 mg.
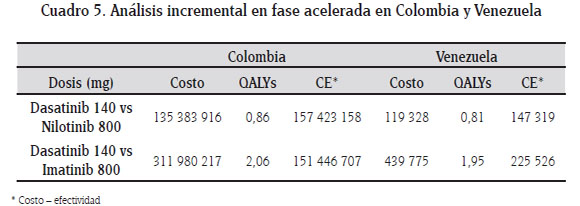
Al realizar el análisis incremental, se encuentra que tanto en Colombia como en Venezuela, dasatinib de 140 mg tuvo dominancia extendida sobre nilotinib e imatininb. En Colombia, el análisis incremental muestra que el costo adicional por cada QALY ganado sobre la efectividad de imatinib de 800 mg y nilotinib de 800 mg, fue de $157 423 158 y de $151 446 707 respectivamente. En Venezuela fue de $147 319 Bs.F. y 225 526 bolívares fuertes, respectivamente.
Fase blástica
Aquellos pacientes que recibieron dasatinib a 140 mg experimentaron una expectativa de vida significativamente mayor que los pacientes que recibieron imatinib. Igual ocurrió con los QALY´s: para dasatinib e imatinib fueron de 0,47 y 0,14, para Colombia y Venezuela, respectivamente. La expectativa de vida para los pacientes con dasatinib fue alrededor de 2,3 veces más que la de los pacientes con imatinib, tanto en Colombia como en Venezuela. Los años de vida para el grupo de imatinib fueron de 0,41 tanto para Colombia como para Venezuela, lo que muestra 0,5 años adicionales de vida para aquellos tratados con dasatinib en relación con aquellos pacientes tratados con imatinib.
Estos resultados evidencian que dasatinib de 140 mg presenta una mejor relación de costo efectividad media y mayor producción de QALY´s, que imatinib de 800 mg. El análisis incremental mostró que el costo adicional por cada QALY ganado sobre la efectividad del nilotinib de 800 mg, fue de $145 642 894 y de $212 388 para Colombia y Venezuela, respectivamente.
Análisis de sensibilidad
Se decidió realizar un análisis de sensibilidad del modelo frente a un potencial aumento del precio del dasatinib de un 5 %, tanto en Colombia como para Venezuela.
En la fase crónica con dasatinib de 100 mg, éste continuó teniendo una mejor relación de costo efectividad, tanto en términos de años de vida, como de QALY´s, cuando se comparó tanto con imatinib como con nilotinib, en ambos países. Sin embargo, cuando se aumentó el costo de dasatinib de 140 mg en un 5 %, en dicha fase, nilotinib mostró una mejor relación costo efectividad en el modelo para Colombia, a pesar de producir menos años de vida y menos QALY´s. Para el modelo en Venezuela, dasatinib continuó teniendo una mejor relación costo efectividad.
En la fase acelerada, dasatinib de 140 mg mostró una mejor relación costo efectividad en términos de años de vida y QALY´s en Venezuela y en términos de QALY´s en Colombia.
En la fase blástica, dasatinib de 140 mg continuó teniendo una mejor relación de costo efectividad, a pesar de un aumento de 5 % del costo del medicamento, en comparación al imatinib y al nilotinib, tanto para los dos países.
Así que, en una situación hipotética de aumento del costo del dasatinib en un 5%, éste continuaría teniendo una mejor relación de costo efectividad en relación con el imatinib y el nilotinib, con excepción de la fase crónica en Colombia con el dasatinib de 140 mg, en relación con el nilotinib.
DISCUSIÓN
El presente trabajo comparó los costos y los beneficios en salud relacionados con el tratamiento de LMC en pacientes mayores, utilizando para ello una adaptación del modelo desarrollado por el Consorcio de Economía de la Salud de York. Los resultados para Colombia y Venezuela mostraron una mejor relación de costo efectividad de dasatinib en comparación con nilotinib y con dosis aumentadas de imatinib, así como una mayor cantidad de QALY´s. Igualmente tuvo una mejor relación de costo efectividad que sus comparadores. Aunque el costo por QALY´s sigue siendo alto, el análisis incremental muestra que el valor por cada QALY´s ganado adicional a los dos medicamentos con que se comparó es relativamente bajo.
Los resultados fueron coherentes con otros trabajos. Es así como en la presente evaluación el tratamiento con dasatainib de 100 mg y de 140 mg, obtuvo una ganancia en QALY´s sobre el resultado con el imatinib, de 2,65 y 2,10 para Colombia, y de 2,44 y 1,93 para Venezuela. Por su parte, Hialte y Ghatnekar (45), reportaron una ganancia de 0,62 QALY´s en esta fase cuando se comparó dasatinib de 140 mg con imatinib de 600 mg, con un costo incremental de 6 880 euros por QALY. Este último valor es coherente con el costo incremental para Colombia y Venezuela. Aunque en los dos trabajos el resultado fue favorable a dasatinib, la diferencia en los QALY´s ganados puede obedecer a que, en el trabajo citado, se consideró una menor dosis de imatinib como nivel de resistencia.
Esta mayor ganancia en QALY´s por parte del tratamiento con dasatinib cuando se compara con el imatinib, fue corroborada por Taylor y Scuffham (43) en 2009, en un trabajo realizado en el York Health Economics Consortium, de la Universidad de York en el Reino Unido.
Aunque dasatinib tiene unos mayores costos en términos de medicamentos, así como de costos médicos directos, estos están relacionados con una mayor sobrevida y por ende unos mayores consumos de recursos.
La nueva evidencia clínica está proporcionando datos de efectividades de los medicamentos inhibidores de la tirosin quinasa, que permite hacer nuevos análisis económicos, los cuales, hasta el momento, han mostrado que estas terapias son aceptables en términos de costos y de efectividad dándoles a los pacientes cada vez, mayores años de vida ajustados por calidad (46). Es importante monitorear estos estudios en función de mantener esta creciente tendencia en los logros en términos de QALY´s y de costo efectividad, es decir, de uso eficiente de los recursos en cada sociedad.
CONCLUSIONES
El dasatinib a dosis de 100 mg y de 140 mg por día mostró una mejor relación de costo efectividad media frente a las dosis de 800 mg de imatinib y 800 mg de nilotinib para el tratamiento de los pacientes con LMC resistentes a las dosis habituales de imatinib. Lo cual se verificó para las tres fases de la enfermedad, tanto en el modelo para Colombia como para Venezuela.
En la fase crónica, el tratamiento con dasatinib 100 mg, presentó una mejor relación de costo efectividad media y produjo más QALY´s, cuando se comparó con dasatinib de 140 mg, nilotinib de 800 mg e imatinib de 800 mg, teniendo este último la menor producción de QALY´s y la más desfavorable relación de costo efectividad de los cuatro tratamiento comparados. Esto fue cierto tanto para el modelo en Colombia como en Venezuela.
En la fase acelerada, es claro que, tanto para Colombia como para Venezuela, el tratamiento con dasatinib de 140 mg, cuando se comparó con el nilotinib de 800 mg y el imatinib de 800 mg, mostró más QALY´s ganados y una mejor relación de costo efectividad media, siendo la rama de imatinib de 800 mg, la que menos QALY´s obtiene y el que tuvo la relación costo efectividad media menos favorable.
En la fase blástica, cuando se comparó con el imatinib de 800 mg, dasatinib de 140 mg. obtuvo más de tres veces los QALY´s obtenidos con el imatinib y mejor relación de costo efectividad media. Esto fue válido tanto para Colombia como para Venezuela.
El mayor valor en el costo de dasatinib de 140 mg se explica principalmente por la mayor cantidad de años ganados en cada una de las fases en comparación con los otros dos grupos y por ende mayor consumo de recursos médicos y de medicamentos.
CONFLICTO DE INTERESES
Este trabajo de investigación fue realizado por la Universidad CES en Medellín - Colombia y financiado por Bristol-Myers Squibb. Durante el proceso de revisión por parte de colegas, los cambios derivados de los comentarios recibidos se hicieron con base en mérito científico y editorial. Parte de este trabajo fue presentado como póster y presentación oral en ISPOR 2010 en Atlanta y en HTAi 2010 en Dublin.
ASPECTOS ÉTICOS
Al tratarse de una adaptación de un modelo de evaluación económica previamente realizado, durante el análisis de transferibilidad solo se utilizaron del trabajo original, las probabilidades de cambio entre estados de salud tomadas de estudios clínicos previamente publicados. Para recalcular los resultados para Venezuela y Colombia, se tomaron datos generales relacionados con costos de los medicamentos y de los tratamientos médicos directos, así como las probabilidades de muertes publicadas por la Organización Mundial de la Salud. Teniendo en cuenta esto, esta adaptación no tiene implicaciones éticas.
REFERENCIAS
1. National Comprehensive Cancer Network (NCCN). Clinical practice guidelines in oncology: chronic myelogenous leukemia v.2.2010 [online]. [ Links ]
2. National Comprehensive Cancer Network Available URL:http://www.nccn.org/professionals/ physician_gls/PDF/cml.pdf [Accessed 2010 Nov 30]. [ Links ]
3. Staudt LM. Molecular diagnosis of the hematologic cancers. N.Engl.J.Med. 2003 May 1;348(18):1777-85. [ Links ]
4. Anthony S. Fauci, Eugene Braunwald, Dennis L. Kasper, Stephen L. Hauser, Dan L. Longo, J. Larry Jameson, and Joseph Loscalzo, Eds. editor. Harrison's Principles of Internal Medicine. 17ª ed.: McGraw-Hill; 2008. [ Links ]
5. Baccarani M, Saglio G, Goldman J, Hochhaus A, Simonsson B, Appelbaum et al. Evolving concepts in the management of chronic myeloid leukemia: recommendations from an expert panel on behalf of the European LeukemiaNet. Blood 2006 Sep 15; 108 (6): 1809-20 [ Links ]
6. Dalziel K, Round A, Stein K, Garside R Price A. Effectiveness and cost-effectiveness of imatinib for first-line treatment of chronic myeloid leukaemia in chronic phase: a systematic review and economic analysis. Health Technology Assessment 2004; Vol. 8: No. 28. [ Links ]
7. Goldman JM, Melo JV. Chronic myeloid leukemia-- advances in biology and new approaches to treatment. N.Engl.J.Med. 2003 Oct 9;349(15):1451-64. [ Links ]
8. Aguilera DG, Tsimberidou AM. Dasatinib in chronic myeloid leukemia: a review. Ther. Clin.Risk Manag. 2009 Apr;5(2):281-9. [ Links ]
9. Apperley JF. Part I: mechanisms of resistance to imatinib in chronic myeloid leukaemia. Lancet Oncol 2007 Nov;8(11):1018-29. [ Links ]
10. Jabbour E, Cortes JE, Giles FJ, O'Brien S, Kantarjian HM. Current and emerging treatment options in overchronic myeloid leukemia. Cancer 2007 Jun; 109 (11): 2171-81 [ Links ]
11. Hochhaus A. Dasatinib for the treatment of Philadelphia chromosome-positive chronic myelogenous leukaemia after imatinib failure. Expert Opin Pharma cother 2007 Dec; 8 (18): 3257-64 [ Links ]
12. Kantarjian H, O'Brien S, Talpaz M, Ravandi F, Faderl S, Verstovsek S, et al. Outcome of patients with Philadelphia chromosome-positive chronic myelogenous leukemia postimatinib mesylate failure. Cancer 2007 Apr; 109 (8): 1556-60 [ Links ]
13. Reksodiputro AH, Syafei S, Prayogo N, Karsono B, Rinaldi I, Rajabto W, Mulansari NA. Clinical characteristics and hematologic responses to Imatinib in patients with chronic phase myeloid leukemia (CML) at Cipto Mangunkusumo Hospital. Acta Med Indones 2010 Jan;42(1):2-5. [ Links ]
14. Wong SF. New dosing schedules of dasatinib for CML and adverse event management. J HematolOncol 2009 Feb 23;2:10. [ Links ]
15. Schiffer CA. BCR-ABL tyrosine kinase inhibitors for chronic myelogenous leukemia. N Engl J Med 2007 Jul 19;357(3):258-65. [ Links ]
16. Kantarjian HM, Talpaz M, Giles F, O'Brien S, Cortes J. New insights into the pathophysiology of chronic myeloid leukemia and imatinib resistance. Ann Intern Med 2006 Dec 19;145(12):913-23. [ Links ]
17. Joske DJ. Chronic myeloid leukaemia: the evolution of gene-targeted therapy. Med J Aust 2008 Sep 1;189(5):277-82 [ Links ]
18. Druker BJ, Guilhot F, O'Brien S, Gathmann I, Kantarjian H, Gattermann N, et al. Five year follow-up of patients receiving imatinib for chronic myeloid leukemia. New Engl J Med. 2006;355: 2408-2417. [ Links ]
19. Talpaz M, Kantarjian M, Paquette R, et al. A phase I study of BMS-354825 in patients with imatinib-resistant and intolerant chronic phase chronic myeloid leukemia (CML): results from CA180002. J Clin Oncol. 2005;23(Suppl):6519 [ Links ]
20. Sawyers CL, Shah NP, Kantarjian H, et al. A phase I study of BMS-354825 in patients with imatinib-resistant and intolerant accelerated and blast phase chronic myeloid leukemia (CML): results from CA180002. J Clin Oncol. 2005; 23(Suppl):6520. [ Links ]
21. Guilhot F, Apperley J, Kim D-W, Bullorsky EO, Baccarani M, Roboz GJ. Dasatinib induces significant hematologic and cytogenetic responses in patients with imatinib-resistant or -intolerant chronic myeloid leukemia in accelerated phase. Blood. 2007 Jan 30; [ [ Links ]E-pub ahead of print].
22. Cortes J, Rousselot P, Kim DW, Ritchie E, Hamerschlak N, Coutre S et al. Dasatinib induces complete hematologic and cytogenetic responses in patients with imatinib-resistant or -intolerant chronic myeloid leukemia in blast crisis. Blood. 2007;109:2303-2309. [ Links ]
23. Hochhaus A, Kantarjian HM, Baccarani M, Lipton JH, Apperley JF, Druker BJ, et al. Dasatinib induces notable hematologic and cytogenetic responses in chronic phase chronic myeloid leukemia after failure of imatinib therapy. Blood. 2007;109:3207-3213. [ Links ]
24. Coutre S, Martinelli G, Dombret H, et al. Dasatinib in patients with chronic myelogenous leukemia in lymphoid blast crisis or Philadelphia- chromosome positive acute lymphoblastic leukemia who are imatinib -resistant or intolerant: the CA180015 'START-L' study. J Clin Oncol 2006;24(Suppl):6528. [ Links ]
25. Quinta´s-Cardama A, Kantarjian H, Jones D, et al. Dynamics of molecular response to dasatinib (BMS-354825) in patients (pts) with chronic myelogenous leukemia (CML) resistant or intolerant to imatinib. J Clin Onco 2006;24(Suppl):6525. [ Links ]
26. Talpaz M, Shah NP, Kantarjian H, Donato N, Nicoll J, Paquette R, et al. Dasatinib in imatinib- resistant Philadelphia chromosomepositive leukemias. N Engl J Med 2006; 34:2531- 2541. [ Links ]
27. O'Hare T, Walters DK, Stoffregen EP, Sherbenou DW, Heinrich MC, Deininger MW, Druker BJ. Combined Abl inhibitor therapy for minimizing drug resistance in chronic myeloid leukemia: Src/Abl inhibitors are compatible with imatinib. Clin Cancer Res 2005;11:6987- 6993. [ Links ]
28. Shah NP, Tran C, Lee FY, Chen P, Norris D, Sawyers CL. Overriding imatinib resistance with a novel ABL kinase inhibitor. Science 2004;305:399-401. [ Links ]
29. Tokarski J, Newitt J, Lee F, et al. The crystal structure of ABL kinase with BMS-354825, a dual SRC/ABL kinase inhibitor. Blood 004;104:160a. [ Links ]
30. Lombardo LJ, Lee FY, Chen P, Norris D, Barrish JC, Behnia K, et al. Discovery of N-(2-chloro- 6-methyl-phenyl)-2-(6-4(4-(2-hydroxyethyl)- piperazin-1-yl)-2-methyl-pyrimidin-4-ylamino) thiazole-5-carboxamide (BMS-354825), a dual Src/Abl kinase inhibitor with potent antitumor activity in preclinical assays. J Med Chem 2004;47:6658-6661. [ Links ]
31. Tokarski JS, Newitt JA, Chang CY, Cheng JD, Wittekind M, Kiefer SE, et al. The structure of dasatinib (BMS-354825) bound to activated ABL kinase domain elucidates its inhibitory activity against imatinib-resistant ABL mutants. Cancer Res 2006;66:5790-5797. [ Links ]
32. McFarland KL, Wetzstein GA. Chronic myeloid leukemia therapy: focus on second-generation tyrosine kinase inhibitors. Cancer Control 2009 Apr;16(2):132-40. [ Links ]
33. Rosti G, le Coutre P, Bhalla K, Giles F, Ossenkoppele G, Hochhaus A, Gattermann N, et al. A phase II study of nilotinib administered to imatinib resistant and intolerant patients with chronic myelogenous leukemia (CML) in chronic phase (CP). Journal of Clinical Oncology, 2007 ASCO Annual Meeting Proceedings Part I. Vol 25, No. 18S (June 20 Supplement), 2007: 7007. [ Links ]
34. Davis C. An economic evaluation of dasatinib for the treatment of chronic myelogenous leukaemia in imatinib-resistant patients. York Health Economic consortium. Bristol-Myers SQUIBB. February 2009. [ Links ]
35. Drummond M, Barbieri M, Cook J, Glick H, Lis J, Malik F et al, on behalf of the ISPOR Good Research Practices on Economic Data Transferability Task Force. Value in Health (in press) (www.ispor.org). Transferability of Economic Evaluations across Jurisdictions: ISPOR Good Research Practices Task Force Report. [ Links ]
36. Cortes J, De Souza C, Ayala-Sanchez M, Bendit I, Best-Aguilera C, Enrico A, Hamerschlak N, Pagnano K, Pasquini R, Meillon L. Current patient management of chronic myeloid leukemia in Latin America: a study by the Latin American Leukemia Net (LALNET). Cancer. 2010 Nov 1;116(21):4991-5000. [ Links ]
37. Departamento Administrativo Nacional de Estadística DANE. Estadísticas Vitales. Defunciones por grupos de edad y sexo, según departamento, municipio de residencia y grupos de causas de defunción (lista de causas agrupadas 6/67 CIE-10 de OPS). Colombia 2008. [ Links ]
38. Instituto Nacional de Estadística INE. Tasa bruta de mortalidad corregida por sexo, según grupos de edad, 2004-2008. República Bolivariana de Venezuela 2008. [ Links ]
39. M. F. Drummond, Mark J. Sculpher, George W. Torrance, Bernie J. O'Brien, Greg L. Stoddart. Methods for the economic evaluation of health care programmes Oxford University Press, 2005. [ Links ]
40. Edejer TT, Baltussen R, Adam T, R. Making choices in health: WHO Guide to cost-effectiveness analysis. World Health Organization Geneva 2003. [ Links ]
41. Epstein D. Una revisión de métodos empleados en evaluación económica para extrapolación de resultados en el largo plazo. Centre for Health Economics, York. Revista Española de Economía de la Salud. Vol 6. N° 1. [ Links ]
42. República de Colombia - Ministerio de Protección Social. Decreto 2423 de 1996. Por el cual se determina la nomenclatura y clasificación de los procedimientos médicos, quirúrgicos y hospitalarios del Manual Tarifario y se dictan otras disposiciones. Diario Oficial No. 42.961, del 20 de enero de 1997. [ Links ]
43. Taylor MJ, Scuffham PA. Pharmacoeconomic benefits of dasatinib in the treatment of imatinib- resistant patients with chronic myelogenous leukemia. Expert Rev Pharmacoecon Outcomes Res 2009 Apr;9(2):117-21. [ Links ]
44. Costa AM, L'italien G, Nita ME, Araujo ES. Cost-effectiveness of entecavir versus lamivudine for the suppression of viral replication in chronic hepatitis B patients in Brazil. Braz J Infect Dis 2008 Oct;12(5):368-73. [ Links ]
45. Ghatnekar O, Hialte F, Taylor M. Cost-effectiveness of dasatinib versus high-dose imatinib in patients with Chronic Myeloid Leukemia (CML), resistant to standard dose imatinib - a Swedish model application. York Health Economics Consortium, University of York, York, UK. August 2010, Vol. 49, No. 6 , Pages 851- 858 (doi:10.3109/0284186X.2010.495132). [ Links ]
46. Frame D. New strategies in controlling drug resistance. J Manag Care Pharm. 2007 Oct;13(8 Suppl A):13-7. [ Links ]
Recibido: octubre 28 de 2010; revisado: noviembre 30 de 2010; aceptado: diciembre 5 de 2010.
Forma de citar: Orozco JJ, Valencia Z JE, Aiello E, Ribón G, Guerrero F, García R, Mujica L. Costo efectividad del dasatinib en el tratamiento de la leucemia mieloide crónica en pacientes resistentes al imatinib. Rev CES Med 2010;24(2):31-46