Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Medicas UIS
Print version ISSN 0121-0319
Medicas UIS vol.27 no.3 Bicaramanga Sep./Dec. 2014
Histoplasmosis diseminada, reporte de casos
desde el año 2008 al 2012 en el Hospital San Juan
de Dios, San José, Costa Rica
Manuel Antonio Villalobos Zúñiga*
Saúl Mauricio Rodríguez Sánchez**
* Médico Internista e Infectólogo. Jefe de Servicio de Infectología del Hospital San Juan de Dios. Seguro Social. San José. Costa Rica.
** Médico Internista. Residente de Posgrado en Cuidados Intensivos en el Hospital San Juan de Dios. Seguro Social. San José. Costa Rica.
Correspondencia: Dr. Manuel Villalobos. Apartado Postal 2434-1000. San José. Costa Rica. Correo electrónico: manuel701@gmail.com.
Artículo recibido el 17 de febrero de 2014 y aceptado para publicación el 25 de julio de 2014.
RESUMEN
Introducción: la histoplasmosis es una micosis que fue descrita por primera vez en Panamá, producida por la especie Histoplasma capsulatum, un hongo dimórfico endémico de los valles fluviales de América, el cual produce infección sobretodo en personas con deficiencias en la inmunidad celular, particularmente el virus de la inmunodeficiencia humana. Las guías internacionales definen la primera línea de tratamiento contra la histoplasmosis con anfotericina B liposomal hasta que la condición clínica mejore, y entonces traslaparlo a itraconazol oral por al menos 12 meses. Objetivo: determinar las características de la población con histoplasmosis en el Hospital San Juan de Dios, y valorar los resultados del uso combinado de anfotericina B deoxicolato y fluconazol como tratamiento alternativo de anfotericina liposomal e itraconazol. Materiales y métodos: se realizó un estudio retrospectivo con los casos positivos por histoplasmosis entre el año 2008 y el 2012 atendidos en el Hospital San Juan de Dios, obtenidos con datos del laboratorio y de la Clínica de HIV-SIDA del hospital. Se encontraron 36 casos pero debido a problemas técnicos de archivo solo se tuvo acceso a 15 expedientes. Este trabajo contó con el aval del Comité Local de Bioética y su análisis estadístico fue realizado en Excel 2007 con la estimación de las frecuencias absolutas y relativas de las variables de interés. Resultados: se presenta un reporte de 15 casos con el diagnóstico de histoplasmosis hecho por cultivo u observación directa en muestras de médula ósea, y solo uno por biopsia. El 60% eran hombres, el promedio de edad fue cerca de los 35 años, 86,7% tenían virus de la inmunodeficiencia humana con una media de linfocitos CD4 de 60 celulas/mm3. Los 15 pacientes tuvieron histoplasmosis diseminada aguda progresiva como forma de presentación clínica y dos además tuvieron compromiso intestinal. Solo dos pacientes tuvieron una recaída de la histoplasmosis y ambos con abandono del tratamiento antirretroviral asociado. Conclusiones: de acuerdo a los datos obtenidos en el estudio, se encontró que la combinación de anfotericina B deoxicolato, fluconazol y tratamiento antirretroviral en un 86,5% tuvo buena respuesta clínica con un año libre de recaídas. Esta combinación de tratamiento antirretroviral y un tratamiento para la histoplasmosis de segunda línea con fluconazol fue efectivo, evitando limitaciones en cuanto a biodisponibilidad e interacciones medicamentosas con el itraconazol, sobretodo en pacientes con VIH. MÉD.UIS. 2014;27(3):19-26.
Palabras clave: Histoplasmosis. Infecciones por VIH. Fármacos Anti-VIH. Fluconazol. Anfotericina B.
Treatment efficacy of the disseminated histoplasmosis in Costa Rica with the Use of
Amphotericin B deoxycholate and Fluconazole. Report of 15 cases since 2008 to 2012 at
the Hospital San Juan de Dios
ABSTRACT
Background: histoplasmosis is a fungic infectious disease described for the first time in Panama by the specie Histoplasma capsulatum, a dimorphic fungus endemic from the fluvial valleys from America, the disease is developed in very few persons mostly in those with deficience in their celular inmunity particularly with HIV. The International Guidelines define the first line of therapy against histoplasmosis with Liposomal Amphotericin B therapy until the clinical condition improve, and then switched to itraconazole for at least 12 months. Objetive: to know the characteristics of the patients with histoplasmosis at Hospital San Juan de Dios and to state the value of the combined use of amphotericin B deoxycholate and fluconazole as alternative therapy to liposomal amphotericin and itraconazole. Methods: It was made a retrospective study with histoplasmosis positive cases in 2008 to 2012 attended in the Hospital San Juan de Dios, obtained from laboratory and HIV local group files. It was founded 36 cases, and for archive technical reasons we only had access to review 15 clinical records. This study had the local bioethical and research commission approval. The statistical analysis was made in Excell 2007 through the estimation of absolute and relative frecuencies of the variables of interest. Results: this is the case of 15 patients with the diagnosis of histoplasmosis made by culture and direct observation in bone marrow samples, and only one by biopsy. A 60% were male, the average age of the infection onset nearby 35 years old, 86,7% corresponded to HIV patients among which the mean of lymphocites CD4 was 60 cells/mm3. The 15 patients have acute progressive disseminated histoplasmosis as clinical presentation, and two also have intestinal involve. Only two patients had a histoplasmosis relapse and both with HAART desertion associated. Conclusions: it was founded the combination of Amphotericin B deoxycholate, fluconazole and HAART with good clinical outcome in 86,5% with a year relapse free. This combination of HAART and a second line treatment for histoplsmosis with fluconazole was effective, avoiding the bioavailability issues and drug interactions with the itraconazole, particularly in HIV patients. MÉD.UIS. 2014;27(3):19-26.
Keywords: Histoplasmosis. HIV infections.Anti- HIV Agents. Fluconazole. Amphotericin B.
¿Cómo citar este artículo?: Villalobos MA, Rodríguez SM. Histoplasmosis diseminada, reporte de
casos desde el año 2008 al 2012 en el Hospital San Juan de Dios, San José, Costa Rica. MÉD.UIS.
2014;27(3):19-26.
INTRODUCCIÓN
La histoplasmosis es una enfermedad infecciosa de etiología fúngica, descrita hace más de un siglo por el médico estadounidense Samuel Darling durante la autopsia de un trabajador del canal de Panamá proveniente de Martinica1,2. El hongo es endémico de valles fluviales de norte, centro y sur América1-3 y un patógeno dimórfico del suelo, que posee la morfología de conidia durante su estancia en el ambiente pero se transforma en levadura in vivo e in vitro a 37ºC como en el cuerpo humano4. La distribución geográfica del hongo se corresponde con las características del suelo, clima y humedad, siendo favorecido por temperaturas de 22 a 29ºC, precipitaciones de 35 a 50 pulgadas y humedad relativa del 67 a 87%2-5.
Pese a que la infección es muy común en las zonas endémicas, la enfermedad se desarrolla en muy pocas personas y la infección trascurre de forma asintomática o con síntomas mínimos que pasan desapercibidos1. Con el advenimiento de la pandemia del Virus de la Inmunodeficiencia Humana (VIH) y la aparición de nuevas terapias inmunosupresoras para el manejo de enfermedades autoinmunes y trasplante de órganos y tejidos, la enfermedad ha tomado importancia con una prevalencia de 1,5 a 5% en pacientes con serología positiva por VIH1,6,7.
El Histoplasma capsulatum es agente causal de una amplia gama de enfermedades, desde cuadros clínicos muy localizados como fibrosis mediastinal, histoplasmosis pulmonar aguda y crónica hasta su forma diseminada con afección del sistema retículo endotelial y médula ósea. La enfermedad puede evolucionar hacia un estado crítico, con desarrollo de shock séptico, síndrome de estrés respiratorio del adulto, meningitis e insuficiencia suprarrenal con una alta mortalidad1-7. El diagnóstico se realiza mediante un trabajo multidisciplinario a través del análisis histopatológico, el cultivo microbiológico y el análisis de antígenos y anticuerpos8. El cultivo del hongo se convierte en el estándar de oro para el diagnóstico; sin embargo, el microorganismo posee crecimiento lento lo que permite que las colonias sean aisladas en un plazo no menor a dos semanas mientras que el diagnóstico histopatológico es una forma más rápida de confirmar la enfermedad1-9. La detección de antígenos polisacáridos de Histoplasma capsulatum3 en sangre y orina, es un método rápido y no invasivo para realizar el diagnóstico. Dicha prueba a su vez sirve para valorar la efectividad del tratamiento y detectar recaídas. Sin embargo, no estaba disponible en Costa Rica en el momento del estudio5-9.
El tratamiento de la infección depende de la severidad de la enfermedad y sus manifestaciones clínicas10. Hay evidencia de efectividad con el uso de anfotericina B deoxicolato, anfotericina liposomal, anfotericina B en complejos lipídicos y de imidazólicos. Las equinocandinas no han sido probadas en este contexto. Las guías estadounidenses para el tratamiento de la histoplasmosis diseminada moderada a severa establecidas por la Infectious Disease Society of America (IDSA), establecen que se debe iniciar anfotericina liposomal hasta que la condición clínica mejore, después de lo cual se sigue una fase de mantenimiento con itraconazol por al menos 12 meses5. De los problemas que se reportan con el uso de itraconazol cabe citar sus interacciones con diversos antirretrovirales, fundamentalmente con el grupo de los inhibidores de la transcriptasa reversa no nucleósidos ya que comparten el metabolismo por el citocromo P450 3A411-4. El perfil farmacocinético y su biodisponibilidad favorable han hecho del fluconazol el tratamiento de primera línea en el Hospital San Juan de Dios, a pesar de no ser esta la recomendación de elección a nivel mundial para dicha enfermedad. Debido a razones económicas y falta de oferentes a nivel local no se dispone de anfotericina liposomal en Costa Rica.
El objetivo del presente estudio es determinar las características de la población con histoplasmosis y valorar los resultados del uso combinado de anfotericina B deoxicolato y fluconazol como tratamiento alternativo de anfotericina liposomal e itraconazol, medicamentos de primera línea según guías internacionales.
MATERIALES Y MÉTODOS
Se realizó un estudio retrospectivo mediante la revisión de los expedientes clínicos de pacientes que se encontraban bajo el diagnóstico de histoplasmosis en las bases de datos del Laboratorio Clínico del hospital y de la Clínica de VIH/SIDA del mismo centro. Se definió histoplasmosis diseminada como la afección de múltiples órganos y sistemas en pacientes en quienes se documentó la presencia de Histoplasma capsulatum mediante cultivo o visualización histopatológica.
Los criterios de inclusión utilizados fueron que todos los pacientes, independiente del género o etnia, en los cuales se realizó el diagnóstico microbiológico o histopatológico de histoplasmosis y posterior a su egreso siguieran control en el servicio de Infectología. Los criterios de exclusión utilizados fueron los pacientes con diagnóstico presuntivo de histoplasmosis (no confirmado microbiológica o histopatológicamente), pacientes cuyo expediente clínico no se localizó para su revisión, pacientes con el diagnóstico de histoplasmosis que no siguieron control médico posterior en la consulta externa de infectología. Con los criterios de inclusión se encontraron 46 expedientes, de los cuales fue posible revisar 15 de ellos debido a que el resto de expedientes no fueron localizados en el archivo clínico del Hospital San Juan de Dios. Es posible que algunos de los expedientes no disponibles o extraviados correspondieran a pacientes fallecidos por histoplasmosis, lo cual evidentemente conlleva a un sesgo en este sentido, pero no hay forma de corroborarlo.
El diagnóstico microbiológico de histoplasmosis se estableció con el cultivo de Histoplasma capsulatum en el medio de Sabouraud en la sección de micología del laboratorio clínico y el diagnóstico histopatológico se estableció mediante la tinción de Wright de aspirados de médula ósea valorados en el laboratorio de hematología y mediante las tinciones argénticas de otras muestras tisulares en la sección de patología. De los expedientes clínicos se recolectaron las siguientes variables: edad, sexo, inmunosupresión asociada, conteo de linfocitos CD4, hemograma, niveles basales y mínimos de potasio sérico, niveles basales y máximos de creatinina sérica, la presencia de hallazgos clínicos al ingreso, el tratamiento administrado y la presencia o no de Terapia Antiretroviral Altamente Efectiva (HAART, por sus siglas en inglés), previo al diagnóstico y el inicio de éste posterior al inicio de tratamiento de la histoplasmosis.
Se definió lesión renal aguda como la elevación en más de 0,5 mg/dL del nivel basal de creatinina en un periodo no mayor de 48 horas (de acuerdo a lo establecido en la clasificación AKIN para daño renal agudo) una vez iniciado el tratamiento con anfotericina B deoxicolato15.
El seguimiento se hizo inicialmente a un plazo de seis meses concluida la fase de consolidación y luego se postergó el mismo a un año plazo. El estudio contó con la aprobación del comité local de bioética (CLOBIHSJD) previo a su realización. El análisis estadístico se realizó con los datos obtenidos en la revisión de expedientes clínicos y fueron almacenados en una base de datos en formato de Microsoft Excel 2007; para el análisis de éstos se utilizaron herramientas de estadística descriptiva, a saber: las frecuencias absolutas y relativas y el cálculo de desviaciones estándar de las variables de interés.
RESULTADOS
Posterior a la revisión inicial de las bases de datos se obtuvo un total de 46 pacientes en el periodo de enero de 2008 a julio de 2012. De estos 46 pacientes se eliminaron dos pacientes que por error fueron asignados a las bases de datos y no presentaban ni diagnóstico ni sospecha clínica, un paciente de quien se tenía la sospecha clínica de histoplasmosis, pero el diagnóstico definitivo fue linfoma de Hodgkin y tres pacientes a quienes no fue posible comprobar el diagnóstico con estudios microbiológicos o histopatológicos, quedando un total de 40 pacientes.
De estos 40 pacientes, solamente se pudo completar la información de 15, quienes conforman el subgrupo de pacientes vivos con el diagnóstico de histoplasmosis. Los restantes 25 expedientes corresponden en su mayoría a pacientes fallecidos y su expediente clínico no pudo ser valorado por problemas del archivo clínico del hospital ya que no estaban disponibles, existe aquí un sesgo de mortalidad importante en el estudio ya que algunos de esos pacientes pudieron fallecer por la misma histoplasmosis; sin embargo, el principal objetivo de este estudio no es analizar mortalidad sino las características de la población y la efectividad del tratamiento aplicado en el Hospital San Juan de Dios para estos casos.
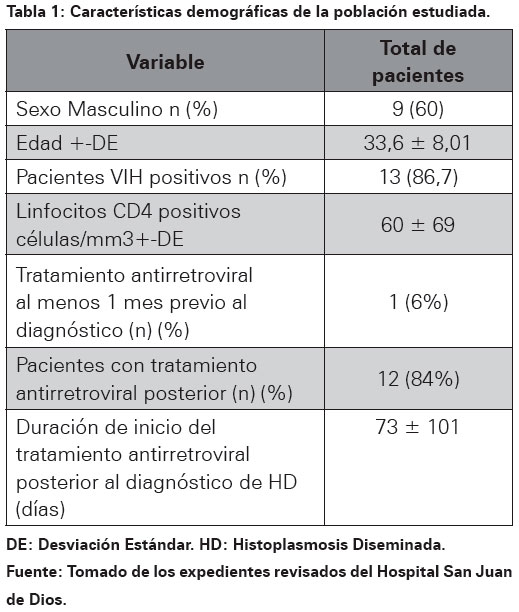
Con respecto al diagnóstico de histoplasmosis, en el 73 % de los pacientes se realizó mediante mielocultivo, el 63,2% con citología de médula ósea y un 20% mediante histología. De los 15 pacientes analizados nueve eran hombres para un 60% y seis eran mujeres para un 40%. La edad promedio de aparición de la enfermedad ronda los 35 años, con una desviación estándar de 9,23: 33,6 para hombres y 35,8 para mujeres (Ver Tabla 1).
De la totalidad de casos un 86,7% correspondían a pacientes con VIH en los cuales el promedio de linfocitos CD4 fue de 60 células/mm3 con un valor mínimo de 3 células/mm3 y un valor máximo de 255 células/mm3. Solo un paciente se encontraba recibiendo HAART durante más de un mes previo al diagnóstico de histoplasmosis, se trataba de un esquema con lopinavir/ritonavir, abacavir y lamivudina; e inclusive el diagnóstico de histoplasmosis se realizó en medio del síndrome de reconstitución inmunológica inflamatoria como consecuencia de la elevación de linfocitos CD4 durante el tratamiento antirretroviral, siendo esto muy infrecuente con este hongo. Al 84% de los pacientes con histoplasmosis se le inició HAART posteriormente, en un periodo promedio de 73 días. Solamente un paciente presentó coinfección con otros gérmenes oportunistas además de la histoplasmosis, en este caso toxoplasmosis cerebral. Dos pacientes recibían medicación inmunosupresora, uno con esteroides para lupus eritematoso sistémico y otro con tacrólimus y micofenolato de mofetilo por un trasplante renal.
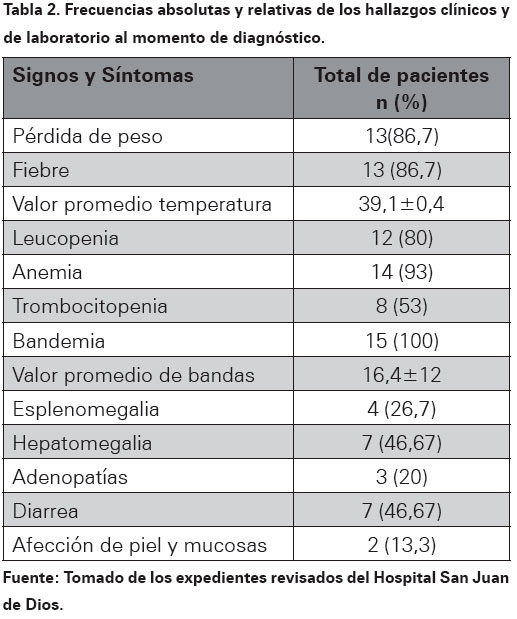
Respecto a la presentación clínica de la histoplasmosis los síntomas principales de fueron la pérdida de peso y la fiebre; las cuales se presentaron en un 86,7% de los pacientes. Un 46,67% de los pacientes consultó por diarrea al momento del diagnóstico, lo cual es llamativo debido a que esta patología fúngica no suele afectar el tracto gastrointestinal de forma directa (Ver Tabla 2).
Como hallazgos a la exploración física se documentó hepatomegalia en un 46,7%, esplenomegalia en un 26,7% y adenopatías generalizadas en un 20%. Se reportó presencia de lesiones en piel y mucosas en dos casos, uno con úlceras orales al momento del diagnóstico y otro con lesiones cutáneas similares a molusco contagioso, cuya biopsia determinó la presencia de granulomas y levaduras compatibles con Histoplasma capsulatum. La afección hematológica se presentó fundamentalmente como anemia y bandemia, estando presentes en un 93 % y 100% respectivamente, le sigue la leucopenia en un 80% y la trombocitopenia en un 50%.
Se presentaron tres cuadros clínicos poco frecuentes como diagnóstico de histoplasmosis diseminada, en un caso se diagnosticó mediante el cultivo de lesiones en piel durante la aparición de síndrome de reconstitución inmunológica en un paciente con un mes de HAART. En los otros dos casos el diagnóstico fue anatomopatológico, al visualizar H capsultum en una pieza de colon transverso, obtenida durante colectomía por obstrucción intestinal y en otro al visualizarla en biopsia de epiplón durante una laparotomía por perforación intestinal.
En relación al tratamiento de inducción, esta se dio en 14 casos con anfotericina B deoxicolato y en un caso se dio con fluconazol intravenoso por 10 días debido a contraindicación renal para el uso de anfotericina B deoxicolato. La dosis acumulada de anfotericina en promedio fue de 520 mg y esta se administró durante un promedio de 16 días. Se presentó hipocalemia en siete pacientes (50%) y daño renal agudo en 43% de los pacientes tratados.
La fase de consolidación se dio en 11 pacientes con fluconazol a una dosis de 400 mg/día, con un promedio de tiempo de 4,6 meses. Un paciente solicitó salida voluntaria y un paciente no recibió fase de consolidación. Los dos restantes pacientes recibieron tratamiento de consolidación con itraconazol por periodos de siete y cinco meses.
Durante la fase de consolidación y en un periodo de 12 meses posterior a la conclusión del tratamiento, no se reportó recaída de la enfermedad. Se sospechó de recaída en dos pacientes en promedio 13 meses después de concluida la fase de consolidación quienes consultaron por cuadros clínicos muy similares al mismo con el cual se hizo diagnóstico de histoplasmosis. En ambos pacientes se documentó abandono de tratamiento HAART por un periodo de tiempo no menor a dos meses. En ninguno de los dos casos fue posible cultivar el hongo ni visualizarlo de los aspirados de médula ósea y ambos casos desarrollaron buena respuesta a la prueba terapéutica con anfotericina B deoxicolato y un nuevo ciclo de fluconazol oral.
DISCUSIÓN
Respecto a la afección por histoplasmosis de acuerdo a género y edad de presentación los resultados son similares a las series publicadas por Gutiérrez et al., Tobon et al. y Hernández et al.; de 104, 40 y 24 pacientes respectivamente, donde hubo mayor existencia de casos en hombres y a una edad promedio de 35 años6,16,17. Las formas de presentación clínica no distan tampoco mucho de lo publicado siendo las principales manifestaciones fiebre y pérdida de peso en más del 85% de los casos. El hallazgo de hepatomegalia y esplenomegalia correspondió a un 46 y 26% respectivamente y la diarrea se presentó en siete pacientes para un 46%, datos dentro de los rangos reportados en otras series y que se contraponen a la baja incidencia de afección gastrointestinal que documenta el Centro de Control de Enfermedades de los Estados Unidos6,16-8. Al igual que la serie panameña y las estadounidenses, la presencia de hallazgos cutáneos y en mucosas es poco frecuente sumando ambas afecciones solamente dos pacientes; este hallazgo difiere de lo presentado en reportes suramericanos donde se cree que las manifestaciones cutáneas rondan el 40- 50%6,16,18.
La histoplasmosis se considera una infección oportunista cuyo riesgo de enfermedad diseminada aumenta en los pacientes VIH positivos con conteos de linfocitos CD4 por debajo de 200 células/mm3; sin embargo, en el presente reporte de casos al igual que en otras series, los pacientes diagnosticados poseían mayor grado de inmunocompromiso siendo el conteo promedio de 60 células/mm3,19. A pesar de tener en promedio menos de 100 linfocitos CD4 por milímetro cúbico ninguno de los pacientes presentó manifestaciones pulmonares, meningitis o histoplasmosis diseminada severa. Estos datos son comparables con otras series publicadas en el continente americano (Ver Figura 1).
El tiempo de retraso en el inicio de la terapia antirretroviral tuvo un promedio de 74 días, periodo en general prolongado; sin embargo, se debe aclarar que esto obedece a las condiciones socioeconómicas de los pacientes que les confieren un perfil de baja adherencia para el inicio del HAART. De acuerdo a las recomendaciones internacionales no existe razón para postergar el inicio del HAART durante el tratamiento de la histoplasmosis, inclusive ante la posibilidad del síndrome de reconstitución inmunológica el cual de presentarse tampoco contraindica la continuidad del HAART9.
La anfotericina B deoxicolato se utilizó como inducción en 14 pacientes, los efectos adversos tuvieron tasas tan altas como las ya previamente descritas para un 50% de hipocalemia y un 43% para lesión renal aguda15,20. En los casos analizados no se documentó fallo terapéutico durante la inducción. Según el estudio de Johnson, Wheat et al. la tasa de nefrotoxicidad presente con anfotericina liposomal es significativamente menor a la de anfotericina deoxicolato, hasta en un 28%20.
La fase de consolidación se dio con fluconazol para 11 pacientes, cabe mencionar que se utilizó una dosis más baja que las recomendadas para el uso de fluconazol, basadas en los datos del estudio de McKinsey et al. donde fue necesario incrementar las dosis debido a falla terapéutica superior 22% y que culminó con una efectividad de 71% en el subgrupo de histoplasmosis diseminada, al igual en el estudio de Wheat et al. donde dosis de 400 mg resultaron ser menos efectivas que dosis de 200 mg al día de itraconazol1,14,18.
Pese a que en contraste con las recomendaciones solo se brindó tratamiento por 4,6 meses en promedio, no se documentó ninguno de los datos que estipula McKinsey como falla al tratamiento (progresión de la enfermedad, recaída, persistencia o muerte) del mismo modo que ocurrió con los dos pacientes que recibieron fase de consolidación con itraconazol. Se debe mencionar que dicho estudio no contó con pacientes VIH positivos y que el estudio de Wheat se llevó a cabo en pacientes VIH sin reportar el uso de terapia HAART14. Tampoco se reportaron efectos adversos con el medicamento y existió incremento paulatino en el conteo de CD4 al iniciar HAART sin la necesidad de medir niveles de itraconazol tal como lo recomiendan las guías de la IDSA5,11,12,21.
En la serie hubo dos casos de recaída de la infección luego de un año, pero cabe señalar que ninguno de ellos recibió más de seis meses de fluconazol y que además habían suspendido el tratamiento antirretroviral. En estos dos pacientes el diagnóstico siempre fue presuntivo, ya que nunca se aisló el hongo pero ambos casos presentaron respuestas positivas a la prueba terapéutica. De acuerdo con Tobon el inicio de HAART durante el tratamiento con antifúngicos mejora la efectividad de los mismos, pudiendo alcanzar el 100% y poniendo en desventaja a la población que no lo recibe, teniendo esta una efectividad del 47%. Se considera que la combinación entre el antifúngico y el HAART con la respectiva elevación del conteo de linfocitos CD4 fue responsable de la efectividad alcanzada en esta serie de casos, cuya duración y dosis de tratamiento de consolidación fue mucho menor a las recomendaciones internacionales1,5,17,21.
De acuerdo con Wheat, Conelli et al. el fluconazol posee menor actividad contra Histoplasma capsulatum y a su vez existe aumento en la concentración inhibitoria mínima para el hongo a lo largo del tratamiento de consolidación, hecho que se relaciona con resistencia fúngica y recaída clínica22. A pesar de recibir tratamiento por un periodo menor y dosis inferiores a las recomendadas como se ha mencionado, no se logró evidenciar recaída durante el tratamiento, documentando en esta serie de casos la utilidad de la inducción con anfotericina B deoxicolato en casos moderados; para obtener una mayor actividad fungicida temprana acompañado de la supresión de la carga fúngica restante por fluconazol y la mejoría de la inmunidad celular lograda con la terapia HAART. Ninguno de los estudios previos empleo fluconazol como fármaco durante la fase de consolidación posterior a un ciclo de anfotericina B.
Lamentablemente, debido a la incapacidad de revisar los restantes expedientes no fue posible determinar la tasa de efectividad de anfotericina B deoxicolato y fluconazol. A nivel nacional se cuenta con una tasa de efectividad de 62,5% en el tratamiento de histoplasmosis con la combinación de anfotericina B deoxicolato e itraconazol17. Se obtuvieron tasas de diagnóstico similares a los reportes de otras series y a diferencia del estudio colombiano, en esta serie de casos no se realizó ningún diagnóstico mediante el cultivo de tejido ganglionar4-17-23. Existe una mayor tasa de diagnóstico mediante frotis de médula ósea que lo reportado en el Hospital Calderón Guardia (Hospital de Costa Rica)17.
Limitaciones
Se presentó dificultad para revisar todos los expedientes que cumplían los criterios de inclusión, debido a problemas en el archivo clínico, lo cual no permitió determinar tasas de efectividad. Asimismo existe la limitante de carecer de la detección de antígenos de Histoplasma capsulatum en el hospital en el momento del estudio, con lo cual no se puede dar seguimiento óptimo a la carga fúngica ni a la aparición de presuntas recaídas.
CONCLUSIONES
La serie de casos de histoplasmosis revisada en este trabajo posee el mismo comportamiento epidemiológico que otras series publicadas; sin embargo, el grado de inmunocompromiso encontrado es mayor que en otras latitudes. El tratamiento de inicio con anfotericina B deoxicolato seguido por el tratamiento de consolidación con fluconazol oral por seis meses fue eficaz en mantener a los pacientes al menos un año libre de recaídas, a pesar de tratamientos menores a los recomendados internacionalmente y de no ser este el fármaco de primera línea en la literatura mundial. La combinación de HAART y el tratamiento de segunda línea como lo es anfotericina B deoxicolato y fluconazol parecen incidir de forma favorable en la respuesta terapéutica obtenida ante la infección por Histoplasma capsulatum en esta serie de casos, lo cual podría ofrecer una alternativa razonable al uso de otros medicamentos con mayores efectos adversos e interacciones farmacológicas.
REFERENCIAS BIBLIOGRÁFICAS
1. Kauffman C. Histoplasmosis a Clinical and Laboratory Up date. Clin Microb Rev. 2007;20:115-32. [ Links ]
2. Mandell G, Benett J y Dolin F. Principles and Practice of Infectious Diseases. 7ma edición. Churchill Livingston Elsevier: Philadelphia; 2010. [ Links ]
3. Kauffman C. Diagnosis of Histoplasmosis in immunosuppressed patients. Curr Opin Infec Dis. 2008;21:421-25. [ Links ]
4. Fernández C, Illnait M, Martinez G, Perurena M y Monroy E. Una actualización acerca de histoplamosis. Rev Cubana Med Trop. 2011;63(3):189-205. [ Links ]
5. Wheat LJ, Freifeld AG, Kleiman MB, Braddley JW, McKinsey DS, Loyd JE et al. Clinical Practice Guidelines for the management of patients with histoplasmosis: 2007 Update by the Infectious Disease Society of America. Clin Infect Dis. 2007;45(7):807-25. [ Links ]
6. Gutierrez ME, Canton A, Sosa N, Puga E y Talavera L. Disseminated Histoplasmosis in Patients with AIDS in Panama: A review of 104 cases. Clin Infect Dis. 2005;40(8):1199-202. [ Links ]
7. Wheat LJ, Chetchotisakd P, Williams B, Connolly P, Shutt K y Hajjeh R. Factors associated with severe manifestations of histoplasmosis in AIDS. Clin Infect Dis. 2000;30(6):877-81. [ Links ]
8. Hage CA, Ribes JA, Wengenack NL, Baddour LM, Assi M, McKinsey DS, et al. A multicenter evaluation of tests for diagnosis of Histoplasmosis. Clin Infect Dis. 2011;53(5):448-54. [ Links ]
9. Kaplan JE, Benson C, Holmes KK, Brooks JT, Pau A, Masur H. Guidelines for prevention and Treatment of Opportunistic Infections in HIV-infected adults and adolescents: recommendations from CDC, the National Institutes of Health, and the HIV Medicine Association of the Infectious Diseases Society of America. MMWR Recomm Rep. 2009;58(RR-4):1-207. [ Links ]
10. Brilhante RS, Fechine MA, Cordeiro RdeA, Rocha MF, Ribeiro JF, Monteiro AJ, et al. In vitro effect of sulfamethoxazoletrimethoprim against histoplasma capsulatum var. capsulatum. Antimicrob Agents Chemother. 2010;54(9):3978-79. [ Links ]
11. Crommentuyn KM, Mulder JW, Sparidans RW, Huitema AD, Schellens JH, Beijnen JH. Drug-Drug interaction between itraconazole and the antiretroviral drug lopinavir/ritonavir in an HIV-1 infected patient with disseminated histoplasmosis. Clin Infect Dis. 2004;15(38):e73-5. [ Links ]
12. Koo H, Hamill R, Andrade R. Drug-Drug interaction between Itraconazole and Efavirenz in a patient with AIDS and disseminated Histoplasmosis. Clin Infect Dis. 2007;45(6):e77-9. [ Links ]
13. Hills-Nieminen C, Hughes CA, Houston S, Shafran SD. Drug drug interaction between itraconazole and the protease inhibidor lopinavir /ritonavir. Ann Pharmacother. 2009;43(12):2117-20. [ Links ]
14. McKinsey DS, Kauffman CA, Pappas PG, Cloud GA, Girard WM, Sharkey PK, et al. Fluconazole Therapy for Histoplasmosis. Clin Infect Dis. 1996;23(5):996-1001. [ Links ]
15. Mehta RL, Kellum JA, Shah SV, Molitoris BA, Ronco C, Warnock DG, et al. Acute Kidney Injury Network: report of an initiative to improve outcomes in acute renal injury. Crit Care. 2007;11(2):R31. [ Links ]
16. Tobon A, Medina A, Orozco L, Restrepo C, Molina D, de Bedout C, et al. Histoplasmosis diseminada progresiva en una cohorte de pacientes coinfectados con el VIH. Acta Med Colomb. 2011;36(2):63-7. [ Links ]
17. Hernández H, Solano A, Carrillo P. Histoplasmosis en pacientes con infección por VIH en un hospital de Costa Rica; estudio comparativo. La Gaceta de Infectología y Microbiología Clínica Latinoamericana. 2012;2(2):16-31. [ Links ]
18. Wheat J, MaWhinney S, Hafner R, McKinsey D, Chen D, Korzun A, et al. Treatment of Histoplasmosis with fluconazole in patients with acquired immunodeficiency syndrome. National Institute of Allergy and Infectious Diseases Acquired Immunodeficiency Syndrome Clinical Trials Group and Mycoses Study Group. Am J Med. 1997;103(3):223-32. [ Links ]
19. Vargas C, Boza R. Condición inmunológica de los pacientes portadores de VIH/SIDA en el momento de su diagnóstico en el Hospital San Juan de Dios. Acta Med Costarric. 2012;154(3):159-64. [ Links ]
20. Johnson PC, Wheat LJ, Cloud GA, Goldman M, Lancaster D, Bamberger DM, et al. Safety and Efficacy of Liposomal Amphotericin B compared with conventional amphotericin B for induction therapy of Histoplasmosis in patients with AIDS. Ann Intern Med. 2002;137(2):105-9. [ Links ]
21. Tobón AM, Agudelo CA, Rosero DS, Ochoa JE, De Bedout C, Zuluaga A, et al. Disseminated Histoplasmosis: A comparative study between patients with Acquired immunodeficiency syndrome and non human immunodeficiency virus infected individuals. Am J Trop Med Hyg. 2005;73(3):575-82. [ Links ]
22. Wheat LJ, Connolly P, Smedema M, Brizendine E, Hafner; AIDS Clinical Trials Group, The Mycoses Study Group. Emergence of resistance to fluconazole as a cause of failure during treatment of histoplasmosis in patients with acquired immunodeficiency disease syndrome. Clin Infect Dis. 2001;33(11):1910-3. [ Links ]
23. Kurowski R, Ostaochuk M. Overview of Histoplasmosis. Am Fam Physician. 2002;66(12):2247-52. [ Links ]