Introducción
El Síndrome de Boerhaave (SB) es una patología caracterizada por un desgarro transmural espontáneo del esófago secundario a un aumento súbito en la presión esofágica intraluminal, generalmente en un esófago normal sin relación causal con cuerpos extraños, cirugía, instrumentación o trauma1-3. A pesar de la rareza de esta patología, suele afectar con mayor frecuencia a hombres con rangos de edad entre los 50 y 70 años. Sin embargo, debido a que es muy inusual, en Colombia no se cuentan con cifras de incidencia de la misma. Adicionalmente, cuenta con una alta mortalidad, la cual oscila entre el 30 y 50 %1-4y está relacionada con las complicaciones propias de la afección como mediastinitis, neumonitis, pericarditis, entre otros. El retraso en el diagnóstico y consiguiente tratamiento por la inespecificidad de su presentación clínica también son razones que influyen en dicha mortalidad1.
Tradicionalmente, se presenta con dolor abdominal, disfagia, disnea, signos clínicos de sepsis relacionados con la progresión de la enfermedad y la tríada de Mackler, caracterizada por dolor torácico, vómito y enfisema subcutáneo, aunque esta tríada se presenta solo en el 14 % de los pacientes1. Asimismo, esta patología se ha visto relacionada con la infección por SARS-CoV-2 debido a la sintomatología gastrointestinal que presentan estos pacientes, siendo la emesis una de las primeras causas por la cual se podría desencadenar este síndrome5. Al examen físico, la presencia de enfisema subcutáneo resulta especialmente útil para confirmar el diagnóstico, no obstante, suele detectarse en etapas avanzadas del padecimiento2.
El abordaje diagnóstico paraclínico inicia con una radiografía de tórax y su hallazgo más común es el derrame pleural de predominio izquierdo. Otros hallazgos usualmente descritos son el neumotórax, neumomediastino e hidroneumotórax. El estudio de líquido pleural con pH <6 y amilasa elevada aumentará la sospecha diagnóstica de SB1. Además, se confirmará el diagnóstico con un estudio tomográfico contrastado, que tiene una sensibilidad del 92 % y especificidad del 100 %1, el cual resulta útil en pacientes gravemente enfermos y/o un esofagograma que evidencia la extravasación del medio de contraste a la cavidad pleural, lo que permite localizar y caracterizar la perforación2. Las opciones de tratamiento actuales del SB incluyen el tratamiento conservador, el endoscópico y el quirúrgico1-6; sin embargo, no existe una modalidad estandarizada, ya que la decisión suele depender de varios factores como el estado clínico del paciente. El tratamiento conservador se prefiere en pacientes estables, sin signos y/o síntomas de sepsis7 y consiste en suspender la vía oral, dar soporte nutricional para favorecer la cicatrización y realizar cubrimiento antibiótico de amplio espectro2.
No obstante, la gran mayoría de pacientes requieren manejo quirúrgico, es decir, la reparación de la fuga esofágica cubriendo el sitio de perforación con tejido apropiadamente vascularizado y con poco compromiso inflamatorio como colgajos de pleura, pericardio, omento o músculo y el desbridamiento y drenaje de la cavidad mediastinal y pleural8. Adicionalmente, se debe continuar con el manejo integral teniendo en cuenta que la nutrición adecuada es un pilar fundamental a pesar de la dificultad para mantener una vía de alimentación lo más fisiológica posible1.
El pronóstico está directamente relacionado con el temprano reconocimiento de la patología, la localización de la lesión y su oportuno tratamiento9,10. Primeramente, se ha establecido que el inicio tardío del abordaje quirúrgico, sobre todo después de las primeras 24 horas posterior al diagnóstico, se ha relacionado con una tasa de falla más alta en la reparación del defecto anatómico9,11. Además, se ha descrito que aquellas perforaciones que ocurren debajo de la porción cervical del esófago incurren con una mortalidad más elevada respecto a las perforaciones más proximales10.
El objetivo de este artículo es presentar el caso de un paciente con SB concomitante con enfermedad por SARS-CoV-2 en quien se realizó manejo quirúrgico combinado y destacar su impacto sobre la evolución y desenlace favorable del paciente, así como la importancia del diagnóstico oportuno en este tipo de casos basados en una sospecha clínica inicial, de una patología que si bien no tiene una alta prevalencia, tiene una tasa alta de morbimortalidad sobre aquellos que la padecen.
Presentación del caso
Se presenta el caso de un paciente masculino de 68 años con antecedente de ataque cerebrovascular isquémico hace 12 años sin secuelas que acude al servicio de urgencias de una institución de segundo nivel con cuadro clínico de inicio súbito de 3 horas de evolución aproximadamente por múltiples episodios eméticos de contenido alimentario sin hematemesis, deposiciones líquidas que luego asoció a diaforesis, sin otros síntomas respiratorios o de otra índole asociados.
Posteriormente, presentó aparición progresiva de disnea en reposo y taquipnea. Al examen físico, se evidenció enfisema subcutáneo a nivel cervical y murmullo vesicular disminuido en ambas bases pulmonares; por lo anterior, se realizó estudio tomográfico de tórax que reportó neumonía basal derecha, derrame pleural bilateral y neumomediastino. Con estos hallazgos, se inició cubrimiento antibiótico con piperacilina tazobactam 3.75 gr IV cada 8 horas, claritromicina 500 mg cada 12 horas y vancomicina 1 g IV cada 12 horas.
Al siguiente día, se remitió a institución de tercer nivel donde ingresó con soporte de oxígeno por máscara de no reinhalación a 10 litros y se realizó reacción en cadena de la polimerasa (PCR) para SARS-COV-2 con resultado positivo. Ante el cuadro clínico y paraclínicos tomados que indicaban alta sospecha de SB secundario a neumonía por COVID-19 y, teniendo en cuenta el compromiso hemodinámico del paciente dado por hipotensión sostenida a pesar de reanimación hídrica adecuada, se decidió realizar una tomografía axial computarizada de tórax de alta resolución (TACAR) que confirmó perforación esofágica en el tercio distal anterolateral izquierdo con engrosamiento de las paredes esofágicas proximal a zona de perforación y derrame pleural bilateral (ver Figura 1).
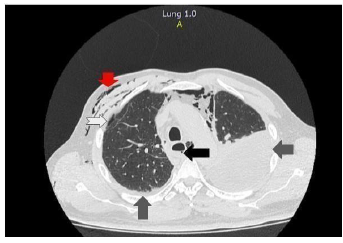
Fuente: autores.
Figura 1 TACAR tórax. Flecha negra: perforación esofágica del lado izquierdo. Flechas grises: derrame pleural bilateral. Flecha blanca: neumomediastino. Flecha roja: enfisema del tejido celular subcutáneo.
Al segundo día de hospitalización, se realizó una toracentesis diagnóstica y terapéutica en la cual se obtuvo 800 CC de líquido pleural hemático con exudado neutrofílico, pH ácido, LDH y amilasa elevadas (Ver Tabla 1); teniendo en cuenta estos hallazgos, se continuó manejo antibiótico con piperacilina tazobactam 3.75 gr cada 8 horas, Claritromicina 500 mg cada 12 horas y se rotó el manejo de vancomicina a linezolid 600 mg cada 12 horas. Con lo anterior, se solicitó endoscopia de vías digestivas altas (EVDA) donde se caracterizó perforación a 35 cm de la arcada dentaria de aproximadamente 5 - 6 cm (Ver Figura 2) por lo que fue llevado de forma emergente un par de horas después a procedimiento quirúrgico vía abierta a través de una toracotomía posterolateral izquierda; en esta cirugía se realizó drenaje de colección mediastinal purulenta, esofagorrafia (puntos separados en un solo plano) con poliglactina 3-0, posterior a desbridamiento de bordes de zona de perforación (Ver Figura 3) y toracotomías cerradas anterior y posterior izquierda. Adicionalmente, se inició nutrición parenteral postquirúrgica para satisfacer los requerimientos nutricionales que favorecieran la cicatrización.
Tabla 1 Examen de líquido pleural.
| Color | Hemático |
| Aspecto | Turbio |
| pH | 7 |
| Recuentos de hematíes | 9.850 mm3 |
| Hematíes normales | 80% |
| Hematíes crenados | 20% |
| Recuento de leucocitos | 10.700 mm3 |
| Diferencial | Neutrófilos 67% Linfocitos 31% Monocitos 2% |
| Examen químico | Glucosa 8 mg/dl Proteínas 4.310 mg/dl LDH 3.635 U/L |
| Amilasa | 1.091 UI/L |
Fuente: autores.
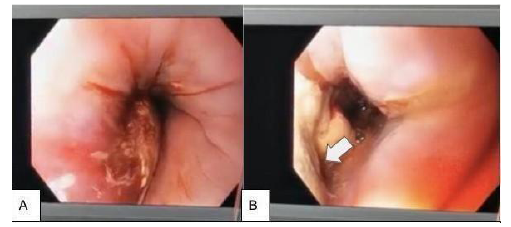
Fuente: autores.
Figura 2 Hematoma con tejido necrofibrinoide. Flecha blanca: área de perforación con burbujeo.
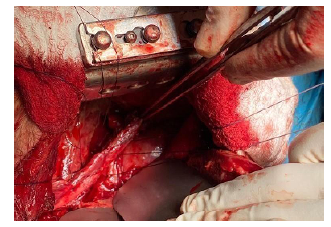
Fuente: autores.
Figura 3 Esofagorrafia con poliglactina 3-0 puntos separados en un solo plano por abordaje de toracotomía posterolateral izquierda
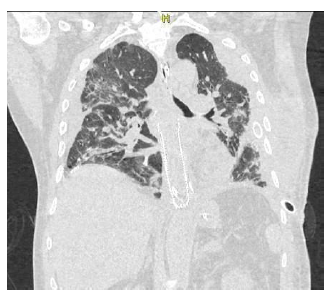
Al día 12 posoperatorio, presentó evolución clínica tórpida, con mala mecánica ventilatoria, requerimiento de intubación orotraqueal, elevación de reactantes de fase aguda y drenaje purulento por tubo a tórax por lo que se realizó nuevo estudio tomográfico que reportó hemotórax izquierdo y hematoma de pared torácica izquierda (Ver Figura 4), con necesidad de escalonamiento antibiótico a meropenem con continuación de linezolid y de reintervención para evaluar dehiscencia de sutura esofágica así como decorticación pulmonar por toracoscopia con pleurectomía parietal y lavado de cavidad.
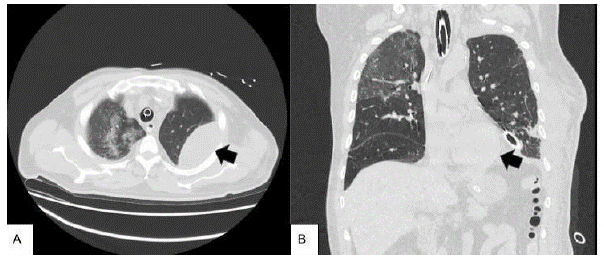
Además se evidencia el compromiso pulmonar bilateral en patrón de vidrio esmerilado sugestivo de infección por COVID 19.
Fuente: autores.
Figura 4 A. Flecha negra. Colección en pared lateral de hemitórax izquierdo 10x 5.4 x12.2 cm para volumen aproximado de 343 cc compatible con hematoma de pared torácica izquierda. B. Flecha negra. Hematoma previamente mencionado en una vista coronal.
Debido a que no hubo posibilidad de descartar dehiscencia de sutura esofágica, se realizó nueva EVDA encontrando pérdida de la continuidad de la mucosa esofágica de 10-12 mm a 30 cm de la arcada dentaria por lo que se decidió colocación de stent esofágico más terapia de vacío endoluminal con dren de Jackson Pratt (ENDOVAC) (Ver Figura 5) y se avanzó una sonda nasogástrica (SNG) para asegurar nutrición enteral.
Fuente: autores.
Figura 5 Stent esofágico metálico autoexpandible de 10x28 mm ubicado en tercio distal del esófago.
Posteriormente a la reintervención, el paciente completó 23 días de manejo con evolución favorable, por lo que se indicó retiro de stent esofágico, previo retiro accidental de sonda de Jackson Pratt al movilizar paciente e inserción de SNG para iniciar nutrición enteral; y se confirmó con nueva EVDA la ausencia de orificios fistulosos y un área de ulceración de 1.5 cm cubierto por fibrina a 30 cm de la arcada dentaria. Sin embargo, dada la alta posibilidad de trastorno deglutorio del paciente crítico y no posibilidad de realización completa de estudio contrastado por retardo de inicio de fase oral y penetración laríngea y aspiración laringotraqueal del medio de contraste, se consideró continuar terapias de deglución y definir reinicio de vía oral de forma ambulatoria según rehabilitación en terapia fonoaudiológica. Se realizó control por cirugía de tórax 4 meses después del egreso hospitalario, en donde se evidenció paciente con adecuada tolerancia de nutrición enteral asociada a dieta blanda por vía oral, sin sintomatología, por lo que se da aval para retiro de SNG, a definir en control por servicio de gastroenterología.
Discusión
Solo se han reportado tres casos en la literatura en los que se relaciona el SB con la infección por SARS-Cov-212,13,14, lo que implica que la información es realmente limitada. Se ha descrito que podría existir relación causal entre pacientes que cursan infección por SARS-COV-2 con la aparición de SB, dado el compromiso del sistema digestivo encontrado hasta en el 20 % de los afectados con esta infección, con síntomas como diarrea, dolor abdominal y emesis, siendo esta última la que puede ocasionar este síndrome, dado el aumento de la presión intraluminal conocida en la fisiopatología del SB como principal condicionante para su aparición5. Adicionalmente, el diagnóstico de esta afección puede ser un desafío porque la presentación puede variar de forma significativa, lo que requiere un mínimo de sospecha basados en el conocimiento de sus síntomas. Además, es importante tener en cuenta que el SB se asocia clásicamente con la tríada de Mackler; sin embargo, los pacientes rara vez presentan todos estos síntomas y a menudo tienen quejas vagas e inespecíficas15.
Meloy et al.12 presentaron el caso de una adulta mayor de 92 años, con antecedentes de hipertensión arterial, insuficiencia cardíaca congestiva, estenosis aórtica, demencia y osteoartritis quien acudió al servicio de urgencias con un cuadro clínico de 3 horas de evolución de náuseas, emesis y dolor abdominal de aparición repentina, sin asociarse a síntomas respiratorios, al igual que en nuestro caso, quien posteriormente dada la aparición de sangrado digestivo alto a través de melenas. Se realizó una EVDA con hallazgo de ruptura esofágica, así como de opacidades difusas en vidrio esmerilado en una tomografía de tórax, con prueba antigénica para COVID-19 positiva. El manejo de soporte inicialmente consistió en administración de líquidos endovenosos, antieméticos y sedantes dada la agitación presentada, pero posteriormente requirió traslado a unidad de cuidado intensivo por la progresión del cuadro clínico y eventual requerimiento de reanimación; sin embargo, dadas sus comorbilidades y en concepto conjunto con su familia se optó por un manejo netamente sintomático, sin implementación de medidas avanzadas de reanimación y, finalmente, falleció. En el caso actual, a diferencia de la paciente descrita anteriormente, el paciente no presentaba comorbilidades que influyeran en su tratamiento, por lo que es fundamental realizar un abordaje individualizado con cada paciente, teniendo en cuenta la gravedad con la que ingresan al servicio de urgencias, edad y las diversas comorbilidades que pueden dificultar su evolución y tratamiento.
Por otro lado, el caso presentado por Ahmed Saad13, se trató de un paciente masculino de 72 años cuya sintomatología inicial era netamente respiratoria, quien posteriormente inicia con dolor abdominal en epigastrio y episodios eméticos, lo que le lleva a consultar a urgencias. Al examen físico, presentó hallazgos similares con los encontrados en nuestro paciente como el enfisema subcutáneo y disminución del murmullo vesicular en ambas bases pulmonares. Posteriormente, le realizaron una tomografía de tórax contrastada con hallazgo de ruptura esofágica distal asociada a neumomediastino y posteriormente a EVDA como abordajes diagnósticos. En la endoscopia, se identificó un defecto de 8 cm en el esófago anterior que comenzaba en el nivel vertebral T4 y se reparó mediante malla permanente tunelizada. El paciente luego de 35 días en UCI presentó una evolución clínica favorable, por lo que fue trasladado a salas generales al comprobar mediante estudios de deglución que el defecto esofágico había sido corregido y egresó al día 110 de hospitalización, pero presentó un reingreso por presentar disfagia secundaria a una estenosis del sitio de reparación con malla, por lo que se realizó nueva EVDA y se insertó un stent autoexpandible. Es importante resaltar que el enfisema subcutáneo es apreciado en la mayoría de casos de SB con algunas variaciones en la localización anatómica en la que es encontrado (tórax, cuello, etc), como es posible observar en el caso anterior y el actual; debido a esto, es necesario tener en cuenta los signos y síntomas que son característicos en este síndrome para realizar un diagnóstico temprano en los pacientes y, de esta forma, proporcionar un manejo oportuno para evitar las complicaciones asociadas.
La literatura ha demostrado que en pacientes críticamente enfermos con un tracto gastrointestinal funcional, la nutrición enteral ha tenido efectos favorables en reducción de la estancia en Unidad de Cuidados Intensivos (UCI), además de estar relacionada con mayor facilidad de acceso, mayor tolerancia por parte del paciente y menor costo. No obstante, en aquellos casos en los que no sea posible iniciar nutrición enteral de forma temprana o el uso de la misma no logre suplir los requerimientos nutricionales del paciente, la nutrición parenteral puede ser beneficiosa en términos de disminución de infecciones nosocomiales y aumento de la ingesta de proteínas; por lo anterior, es de vital importancia individualizar a cada paciente para lograr ofrecer el manejo más adecuado posible según la condición clínica propia de cada paciente16,17.
Al igual que otro caso descrito previamente en un paciente que presentó SB como complicación de neumonía por COVID-19, se utilizó el manejo combinado con reparo primario de la perforación y posterior colocación de stent esofágico con muy buena efectividad18. En este caso, se describe a un paciente de 53 años con antecedentes de enfermedad coronaria, diabetes mellitus y enfermedad renal crónica, quien consultó por dolor toraco-abdominal de inicio súbito, posterior a presentar accesos de tos, sintomatología con la que cursaba días previos al ingreso. A la exploración se encontraba taquicárdico, hipotenso y taquipneico, documentando además en laboratorios de extensión, leucocitosis y fue positivo para SARS-COV-2 en prueba de PCR. En la TAC de tórax con contraste oral se encontró neumomediastino sugestivo de SB. El paciente fue sometido a toracotomía y reparación de la perforación esofágica y finalmente se le realizó una endoscopia y colocación de un stent esofágico. Existen algunas diferencias en cuanto al manejo realizado en comparación al caso que les presentamos, teniendo en cuenta que en nuestro paciente se utilizó el stent en un tercer tiempo quirúrgico como manejo de refistulización, a diferencia del caso anteriormente descrito, en el cual se realizó la colocación del stent inmediatamente posterior al cierre primario; sin embargo, nos podría sugerir que el uso de esta terapia combinada puede ser un manejo seguro y efectivo para estos pacientes de alta complejidad, sea esta utilizada en un mismo momento o en varios tiempos quirúrgicos o como manejo de complicaciones postoperatorias.
Por otro lado, el tratamiento endoscópico representa la opción con menor tasa de mortalidad en series de casos13, con varias opciones como derivación con stents autoexpandibles (SEMS) y cierre con over-the-scope-clips (OTSC) u otros dispositivos19. La terapia de vacío endoluminal (EVAC) asociada al uso de stents esofágicos es una alternativa que ha demostrado reducción en la estancia hospitalaria y morbimortalidad asociada a procedimientos quirúrgicos grandes e invasivos18,19; esto se logra a través de la administración de presión negativa al sitio de fuga del tracto gastrointestinal (TGI), controlando la misma, fomentando la reperfusión tisular, la descontaminación del tejido afectado y eventualmente, la cicatrización para finalmente restablecer la continuidad del TGI20. Este tipo de manejo se ha descrito en paciente con SB posterior al reparo primario19,21y ha sido ampliamente utilizado para el uso en casos de fístulas o fugas esofágicas, incluyendo pacientes con SB17.
Se han desarrollado diferentes métodos como el Score de Pittsburgh para la estratificación de la perforación esofágica, especialmente en pacientes con SB1,22. Este último tiene en variables tanto de tipo clínicas como paraclínicas a las que se les asignan puntos con un rango de 1-3 para una puntuación total posible de 18 (Ver Tabla 2)15. La importancia de este Score pudiera ser de gran utilidad para la predicción en términos de complicaciones post perforación, postoperatorias y días de estancia hospitalaria22, por lo que además de contribuir para guiar el tratamiento, puede ser de utilidad como escala para evaluación de pronóstico. Sin embargo, se requieren estudios adicionales para un mejor conocimiento sobre dichos factores asociados y por tanto, del abordaje de esta enfermedad.
Tabla 2 Variables y cálculo de Score de Pittsburgh.
| Variable | Puntaje |
|---|---|
| Edad >75 años | 1 |
| Taquicardia (>100 lpm) | 1 |
| Leucocitosis (>10.000 glóbulos blancos/ml) | 1 |
| Derrame pleural (en radiografía de tórax, tomografía computarizada o trago de bario) | 1 |
| Fiebre (>38.5grados) | 2 |
| Fuga no contenida (en trago de bario o tomografía computarizada) | 2 |
| Compromiso respiratorio (Frecuencia respiratoria >30 rpm, aumento de requerimiento de oxígeno o necesidad de ventilación mecánica) | 2 |
| Tiempo de diagnóstico >24 hrs | 2 |
| Cáncer | 3 |
| Hipotensión | 3 |
Fuente: autores.
Finalmente, se debe reconocer la importancia en la sospecha diagnóstica de esta patología que es infrecuente pero que representa una alta tasa de morbimortalidad, tal como se presenta en nuestro caso, en el cual se debe resaltar que a pesar de la complejidad del caso y la alta carga de morbimortalidad, dada por lo antecedentes patológicos del paciente, la edad y la tasa de mortalidad del SB, asociado a neumonía por COVID-19, se logró un resultado exitoso que fue la recuperación integral del paciente, todo esto gracias a la terapia quirúrgica combinada utilizando el método de reparo por vía abierta y posteriormente el uso de la vía endoscópica con colocación de Stent y ENDOVAC. Demostrando que esta puede ser una forma de tratamiento adecuada en este tipo de pacientes.
Conclusión
El SB es una patología poco común pero potencialmente mortal, representando un desafío diagnóstico y terapéutico para el personal de la salud. El abordaje e identificación temprana son cruciales para el pronóstico y sobrevida de los pacientes, con un gran impacto en esta última si se logra identificar en las primeras 24 horas de la aparición de síntomas. Por último, hay que resaltar la complejidad de este caso, siendo un paciente adulto mayor con alta carga de comorbilidad, quien presentaba concomitantemente compromiso pulmonar por COVID-19, recibiendo además abordaje de su ruptura esofágica 24 horas posteriores al diagnóstico, con la implementación adicional de stent esofágico más terapia de vacío endoluminal (ENDOVAC), logrando una recuperación exitosa.















