Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Iatreia
Print version ISSN 0121-0793
Iatreia vol.18 no.1 Medellín Jan./Mar. 2005
ARTÍCULO DE INVESTIGACIÓN
El tratamiento amodiaquina–sulfadoxinapirimetamina tiene eficacia del 98% para la malaria falciparum no complicada (Antioquia, Colombia; 2003)
Treatment with amodiaquine–sulfadoxine–pyrimethamine is 98% effective against uncomplicated falciparum malaria
Jaime Carmona Fonseca; Alberto Tobón C.; Gonzalo Álvarez S.; Silvia Blair Trujillo
Grupo Malaria, Universidad de Antioquia, Medellín, Colombia.
Calle 62 No 62–59, laboratorio 610. Medellín (Colombia)
RESUMEN
Antecedentes: la combinación amodiaquina (AQ) con sulfadoxinapirimetamina (SP) es el tratamiento de primera elección para la malaria falciparum no complicada (MFNC) en el departamento de Antioquia desde 1985 y en Colombia desde 2000.
Objetivo: medir la frecuencia de falla terapéutica de AQ–SP en pacientes con MFNC, residentes en Turbo (zona de Urabá) y en El Bagre (zona del Bajo Cauca), Antioquia.
Metodología: este estudio hace parte de uno mayor, que tiene diseño experimental balanceado, con ocho grupos; muestra de tamaño 50 en cada municipio, diseñada con criterios estadísticos y epidemiológicos; tratamiento aplicado en orden de llegada de los pacientes y según los esquemas usuales; seguimiento por 21 días; evaluación no ciega del efecto con el protocolo 1998 de la Organización Mundial de la Salud OMS.
Resultados: se evaluaron 90 pacientes con MFNC; la falla terapéutica fue 2.2%: un caso precoz y otro tardío. El tratamiento fue bien tolerado. La parasitemia asexual se eliminó totalmente en 90% en los tres días de tratamiento (otro 10% tenía 40–80 parásitos/µL, que no es falla) y en 100% antes de 7 días de haber iniciado el tratamiento. AQ–SP mostró total capacidad de eliminar la fiebre: 100% afebriles el día 3. En los pacientes con gametocitos la cantidad de estos creció entre los días 0 y 7 y decreció luego hasta el día 21, cuando 52% los presentaban (promedio: 63 gametocitos/µL), pero no se evaluaron la viabilidad ni la fertilidad de tales gametocitos.
Conclusión: el tratamiento de la MFNC con AQ–SP es altamente eficaz y debe mantenerse como la primera opción terapéutica, reforzada su eficacia antimalárica por el bajo costo, la buena tolerancia y la escasez y levedad de los efectos adversos imputables al tratamiento.
PALABRAS CLAVE: amodiaquina, colombia, falciparum, falla terapéutica, malaria, sulfadoxina–pirimetamina
SUMMARY
Background: The combination of amodiaquine (AQ) and sulfadoxine–pyrimethamine (SP) is the firstchoice treatment for uncomplicated falciparum malaria (UCFM) in Antioquia (northwestern Colombia) since 1985 and in the country at large, since 2000.
Objective: To measure the frequency of therapeutic failure of AQ–SP in patients with UCFM, residents of Turbo (Urabá zone) and El Bagre (Bajo Cauca zone) of Antioquia in northwestern Colombia.
Methodology: This study is part of a larger one which has balanced design, with eight groups; the sample size in each municipality was 50 patients and it was obtained with statistical and epidemiological criteria; treatment was administered in the order of admission of patients according to the usual schedule; follow–up was done during 21 days; not–blind evaluation of the effect with the 1998 WHO protocol.
Results: Ninety patients with UCFM were evaluated; therapeutic failure frequency was 2%; that is 2 cases, one early and one late.
Conclusion: Treatment of UCFM with AQ–SP is highly effective and should be maintained as the first therapeutic choice; its effectiveness is reinforced by its low cost and good tolerance; also by the fact that undesirable effects attributable to the treatment are few and mild.
KEY WORDS: amodiaquine, colombia, falciparum, malaria, sulfadoxine–pyrimethamine, therapeutic failure
INTRODUCCIÓN
Ante el aumento de la falla terapéutica de la cloroquina para la malaria falciparum no complicada, 1–7 en el departamento de Antioquia se adoptó en 1985, como primera opción terapéutica la combinación amodiaquina (AQ) con sulfadoxina–pirimetamina (SP), asociada a primaquina como gametocida; esta misma decisión se tomó en Colombia en 2000, 8 aunque todavía en 2004 son muchos los sitios maláricos del país (no en Antioquia) donde se sigue aplicando cloroquina con primaquina, según nuestro conocimiento directo de la situación.
Los datos para Colombia, en el lapso 1961–2003, sobre la falla terapéutica de la monoterapia con amodiaquina (AQ) están en la tabla Nº 1 2–7,9–19 y se comparan con los de cloroquina (CQ) y sulfadoxina–pirimetamina (SP).
La falla promedio de la AQ es de 22% (mediana 20%). La AQ y SP no se han usado como monoterapias en los programas antimaláricos oficiales de Colombia. La respuesta terapéutica frente a la combinación AQ–SP ha sido evaluada en Colombia solo una vez, con 11% de falla, en Tadó (Chocó) (informado por González IJ en la reunión de Ravreda, Belem, 2003). La opinión de los médicos de las zonas maláricas sobre el tratamiento AQ–SP sugiere que es altamente eficaz y la Dirección Seccional de Salud de Antioquia (DSSA) considera lo mismo, según informe personal del jefe de Epidemiología y control de enfermedades, doctor Armando Galeano M. Entre agosto 2002 y julio 2003 se interrumpió en Antioquia el tratamiento AQ–SP por la escasez de la AQ en el mercado internacional y, en su reemplazo, se aplicó mefloquina–SP; cuando se obtuvo nuevamente AQ, la DSSA no dudó en regresar al esquema AQSP. Sin embargo, hay que reconocer que no se conoce un informe escrito detallado sobre el desempeño de este esquema de tratamiento y, por ello, es altamente conveniente adelantar una investigación sobre el particular.
En 1998, en El Bagre y en Zaragoza se evaluó la respuesta terapéutica antimalárica (RTA) a AQ y SP. El Bagre fue parte integrante de Zaragoza, antes de ser definido como municipio aparte, y comparten similares condiciones demográficas, socioeconómicas, culturales y maláricas; el Índice Parasitario Anual (IPA) 2001–2003 de El Bagre fue de 37.35 por mil y el de Zaragoza fue de 34.36 por mil (datos de la DSSA); la frecuencia de falla en El Bagre, en 1998, con 14 días de seguimiento, fue de 12% para AQ y 15% para SP 4 y en Zaragoza, con un seguimiento de 21 días, usando el mismo protocolo OMS 1996, la falla fue 3% para AQ y 9% para SP. 1–3 En Turbo, también en 1998, se evaluó la RTA para AQ y SP y se obtuvo una incidencia de falla de 7.0% con AQ y 13.0% con SP. 1–3 En 2001–2003, el IPA fue 19.65 en Turbo (datos de la DSSA).
Es muy interesante saber que dos medicamentos que como monoterapia tienen en Antioquia falla moderada (AQ: 7.3%, resultado de 12+3+7= 22/3; SP: 12.3%, resultado de 15+9+13= 37/3), combinados presenten un desempeño excelente. Mejor todavía es saber que este comportamiento no es excepcional, sino que ha sucedido en muchos otros lugares, en particular en África; por ejemplo, en Uganda, AQ–SP falló en 6% (mediana de 3 a 21) 20–25 y la monoterapia AQ en 21% ; 26 en Tanzania AQ–SP falló en 4% 27 y AQ en 25%; 28 en Rwanda la combinación tuvo falla en 3% 29 y la AQ falló en 24% 30 (Tabla Nº 2).31–46

Con estos antecedentes, el presente informe da cuenta de los resultados de la evaluación de la RTA al tratamiento con AQ–SP presentada por 90 pacientes con malaria falciparum no complicada, mayores de 1 año de edad, hombres y mujeres, residentes en los municipios antioqueños de Turbo y El Bagre. La RTA se evaluó con el protocolo OMS de 1998. 47
MATERIALES Y MÉTODOS
Las poblaciones estudiadas
Dos artículos recientes de nuestro grupo forman un marco de referencia integral para interpretar la falla y la resistencia antimaláricas y para orientar las políticas y programas para enfrentarlas. Allí se describió el fracaso del programa de erradicación–control del paludismo en Colombia y se analizaron sus causas; por otra parte, se presentaron las características geográficas, ambientales, sociodemográficas, económicas y de morbimortalidad general y malárica de Antioquia, las regiones de Urabá y Bajo Cauca y los municipios de El Bagre y Turbo. 48–50
Urabá y Bajo Cauca son las dos áreas maláricas más importantes del departamento de Antioquia y generan el 90% del paludismo en este departamento. Urabá está situada sobre el golfo de ese nombre en el mar Caribe colombiano, hacia los límites con Panamá; el 97% de su territorio es de clima cálido. 51–52 El Bajo Cauca antioqueño está al norte del departamento y el 98% de su extensión está en clima cálido húmedo–muy húmedo; se destacan las tierras húmedas de colina y del piedemonte, con relieve plano u ondulado.52,53
Urabá tiene 11.671 km2 de extensión y el Bajo Cauca posee 8.498 km2. En 2002 (junio 30), las poblaciones eran de 463.496 en Urabá y 219.951 habitantes en Bajo Cauca, respectivamente. La densidad poblacional (habitantes/km2) de Urabá era 39.71 en 2002 y la del Bajo Cauca era 25.88 en 2002. 51,53 En estas dos regiones, la totalidad de la población está expuesta al riesgo de malaria. Los habitantes de ambas regiones son mestizos (hijos de padres procedentes de etnias o razas diferentes en su mayoría), negros de origen africano (afroamericanos) que tienen un peso importante en ellas y, en la zona de Urabá, unos pocos indígenas kunas (tule), emberas (katíos) y zenúes. 51 La tasa de analfabetismo entre mayores de 12 años, en 1993, fue de 19% en Urabá y de 19% en Bajo Cauca. 52–53 En 1995–2000, la población desplazada, casi siempre por problemas de violencia y orden público, fue de 25.000 en Urabá y 5.000 en Bajo Cauca. 52
En Turbo (8º 05' 42'' N, 76º 44' 123''), el 60% de la población está en zona rural (aldeas o pequeños poblados y dispersa), mientras que en El Bagre (7º 35'25'' N, 74º 48' 27'') sólo el 38% es rural. La estructura de edad de las dos poblaciones es bastante similar. 52 En 2002, el 8.38% de la población de Antioquia residía en Urabá y el 3.98% en Bajo Cauca. Por otra parte, Turbo poseía el 25.62% de la población de Urabá, mientras que El Bagre reunía el 27.2% de la población del Bajo Cauca.
Durante los últimos 50 años y sobre todo en los últimos veinte, las migraciones por razones económicas (colonización de tierras, explotación de oro y maderas, desarrollos agropecuarios en gran escala, cultivos de marihuana y coca, desempleo y subempleo graves) o sociopolíticas (desplazamientos por carencia de tierra, por violencia, por guerra) han tenido fuerte expresión en Urabá y Bajo Cauca. Estas migraciones no han sido medidas en forma adecuada pero muy probablemente han contribuido de alguna manera a acentuar el problema malárico y han ayudado a diseminar clones de Plasmodium falciparum resistentes a cloroquina y otros medicamentos, tal como se sabe que estas migraciones lo hacen en la frontera de Tailandia con Camboya y Myanmar. 54
La principal actividad económica del Bajo Cauca es la minería de aluvión, seguida por la ganadería y, en menor grado, los cultivos de arroz y sorgo.53 La agroindustria bananera es la principal actividad de Urabá, concentrada en la zona central (Apartadó, Carepa, Chigorodó y Turbo); la ganadería es la segunda actividad económica, destacada sobre todo en la parte norte de la región (Arboletes, Necoclí, San Juan de Urabá, San Pedro de Urabá); la explotación de madera, a partir de la tala de selvas naturales, es la tercera actividad de Urabá y la más importante de su zona sur (Mutatá, Murindó, Vigía del Fuerte). La participación de la población económicamente activa de las dos regiones según los sectores económicos fue muy similar en 1998: primario 49%, secundario 5% y terciario 46%. 52
En cuanto a servicios públicos, en Urabá, en 1998, entre el 60 y el 95% de los habitantes tenían acueducto y Turbo tenía la más baja cobertura, con 60%. También en alcantarillado y aseo, Turbo poseía los valores más bajos (60% y 50%, en su orden). El Bagre tenía coberturas de acueducto de 75%, alcantarillado de 40% y aseo de 65%. A pesar de esa realidad se ha informado que la calidad del agua en todos los municipios listados era excelente, mientras que era mala la disposición final de las basuras. 52
El promedio del índice parasitario anual (IPA) en 1995–2000 fue de 39 por mil en Turbo, de 134 en El Bagre y 33.44 en Zaragoza (1998–2000); en 2001–2003, el IPA fue 19.65 en Turbo, 37.35 en El Bagre y 34.36 por mil en Zaragoza (datos de la DSSA), valores que corresponden a áreas de alto riesgo (IPA >10 por mil).
Clase de estudio
El conjunto de ocho trabajos es un diseño experimental, con grupos iguales, donde el 'factor de exposición' lo constituye cada tratamiento y el 'efecto' corresponde a la RTA. La asignación del paciente a un tratamiento se produjo a medida que se captaba. La RTA se midió, en forma secuencial, en 2003.
Diseño de la muestra
El tamaño de la muestra se obtuvo con el procedimiento clásico que parte de la frecuencia conocida o supuesta de falla terapéutica del tratamiento en evaluación y del tamaño de la respectiva población de pacientes con malaria falciparum, donde n = (N Z2 p (1 – p )) / (N e2) + (Z2 p(1–p)). 55,56 El tamaño de las muestras fue de 42 personas en cada uno de los dos lugares (Turbo y El Bagre) y se elevó a 50 pacientes (20% de aumento) para compensar las casi seguras pérdidas durante el seguimiento. El nivel de confianza aplicado fue de 95% (error alfa = 0.05) y el poder de la prueba estadística fue de 80% (error beta= 0.20). En 1998, el tamaño de la población con malaria falciparum fue de 2.200 pacientes (sumados los tres municipios). 1,57 La proporción esperada de ocurrencia del evento falla terapéutica es variable de un tratamiento a otro y se decidió tomar el valor 50% para todos los tratamientos y obtener así la muestra de mayor tamaño. El error de muestreo fue fijado en 15%.
Población de referencia
La población de referencia está conformada por pacientes con historia de fiebre al menos en los 2–3 días previos, con síntomas compatibles con malaria, con gota gruesa positiva exclusivamente para P. falciparum, que acudieron por su propia iniciativa al puesto de diagnóstico de malaria en el respectivo hospital local, con diagnóstico de malaria falciparum no complicada; se captaron hombres y mujeres (sin embarazo según una prueba de tirilla reactiva), mayores de 1 año de edad, residentes en la zona urbana o rural de su municipio, en el cual debían ser residentes habituales.
Criterios de inclusión
Los criterios de inclusión, además de las características descritas en 'Población de referencia', fueron: a) tener malaria no complicada (según evaluación médica y según la parasitemia asexual); b) poseer entre 500 y 50.000 parásitos asexuados/mL en el momento de ingresar al estudio; c) no tener, cuando se hace el diagnóstico de paludismo, alguna otra enfermedad, según evaluación clínica (entrevista y examen al paciente realizados por los investigadores); d) aceptar participar en el estudio; e) comprometerse a acudir a los controles.
Criterios de exclusión
Los criterios de exclusión del estudio fueron: a) presentar, en cualquier momento, complicación de la malaria o alguna enfermedad intercurrente; b) aparición de efectos adversos graves debidos a las drogas antimaláricas, a otros medicamentos o a otras causas; c) no cumplir con alguno de los tres primeros controles estipulados en el protocolo (días 1, 2, 3).
La aparición de falla terapéutica del tratamiento antimalárico implicó para el paciente abandonar el estudio, habiendo conseguido el objetivo de la investigación, y recibir tratamiento de rescate, formulado según las pautas colombianas de tratamiento del paludismo. 8
Diagnóstico de malaria y evaluación clínica y parasitaria
El diagnóstico de paludismo se hizo con la gota gruesa según el procedimiento indicado por la OMS 58 y usado de rutina por nosotros. La gota gruesa y el extendido se colorearon con Field y Giemsa, respectivamente. La gota gruesa se observó con aumento de 100X y la búsqueda de parásitos se hizo en 200 campos microscópicos consecutivos. La parasitemia se calculó con base en 200 leucocitos y un estándar de 8.000 leucocitos/µL y se expresó en anillos/µL. Una gota gruesa se diagnosticó como negativa cuando no se observó ninguna forma asexual en 200 campos microscópicos.
Al ingresar al estudio y en cada control, a cada paciente se le hicieron: a) evaluación por el médico para conocer la presencia de malaria; b) un estudio parasitario (gota gruesa, extendido, cuantificación de parásitos).
Hubo especial énfasis para detectar, identificar, clasificar y definir el origen de los efectos adversos aparecidos durante los 21 días de seguimiento. Esta búsqueda de efectos adversos estuvo restringida a su manifestación clínica (síntomas, signos), pues no se hizo búsqueda de ellos mediante exámenes de laboratorio.
En cada municipio, el grupo de trabajo de campo estuvo conformado por un médico general y un laboratorista clínico profesional, quienes interactuaron siempre y en forma intensa con el grupo local de trabajo en malaria, conformado por un microscopista (no profesional) y un auxiliar de salud, con quienes se hizo una búsqueda activa de los pacientes cuando no acudieron al control, logrando casi siempre rescatarlos y reintegrarlos al estudio.
TRATAMIENTO
Los medicamentos se administraron acompañados con agua, 8 en las dosis establecidas por el Ministerio de Salud de Colombia.
• Amodiaquina: dosis total de 25 mg/kg peso corporal, que se fracciona en tres días: el 1º se da 40% y los días 2 y 3 se suministra 30% en cada uno; en el adulto promedio la dosis es de 600 mg (4 tabletas) en el día uno y 450 mg (3 tabletas) en cada uno de los otros 2 días. Dosis total máxima: 1.500 mg. Tabletas de 150 mg, Laboratorio Alkem, lote 3001–ET.
• Sulfadoxina: 25 mg/kg peso corporal, en dosis única, dada el día 1. Dosis total máxima: 1.500 mg. Lote RJ0002, Laboratorio Roche.
• Pirimetamina: 1.25mg/kg peso corporal, en dosis única, dada el día 1. Dosis total máxima: 75 mg. Lote RJ0002 Laboratorio Roche.
• Primaquina: 0.75 mg/kg (máximo 45 mg), en dosis única; se aplicó el último día de seguimiento; se usa como gametocitocida. Lote C091200.
Los tratamientos se obtuvieron en la DSSA–Ministerio de Salud; fueron suministrados en forma supervisada por los investigadores y se observó al paciente durante la primera media hora; en caso de vómito, se repitió la dosis completa; entonces, se repetía la observación (30 minutos) y si el paciente vomitaba de nuevo se lo excluía y se remitía al hospital municipal.
CLASIFICACIÓN DE LA RESPUESTA TERAPÉUTICA
El seguimiento fue de 28 días en AQ y de 21 días en SP y AQ–SP. El 'día 0' es el del ingreso, antes de administrar el tratamiento, y los días 1 a 28 son los días posteriores al inicio del tratamiento, o sea que día 1 equivale a completar 24 horas de tratamiento, día 2 corresponde a completar 48 horas de tratamiento y así sucesivamente. La RTA se clasificó según el protocolo OMS 1998: 47
Falla precoz del tratamiento: si aparecen:
a) Signos de peligro o malaria grave los días 1, 2 ó 3; o
b) Parasitemia del día 2 mayor a la del día 0; o
c) Parasitemia del día 3 ≥ 25% del recuento del día 0.
Falla tardía del tratamiento: si aparecen:
a) Signos de peligro o malaria grave después del día 3 con presencia de parasitemia; o
b) Regreso no programado del paciente entre los días 4 a 21 debido a deterioro clínico con parasitemia; o
c) Parásitos (de la misma especie que el día 0) en los días 7, 14, 21 ó 28 (días 7 a 28).
Respuesta clínico–parasitaria adecuada: si el paciente no presenta fallas precoz ni tardía.
Procesamiento y análisis de los datos
Se usó el programa epiinfo 6.04 para construir formularios y bases de datos, así como para analizar la información. También se empleó el SPSS 10.0 para el análisis de datos y la construcción de gráficos.
Se midieron las asociaciones entre grupos o variables independientes (como tratamientos, clases de respuesta terapéutica) con la prueba chi cuadrada (X2), se compararon medianas con la prueba de Wilcoxon o la de Kruskal–Wallis (K–W).
Siempre se aplicó un nivel de significación del 5% (Α = 0.05) para la toma de decisiones.
Se usan estas abreviaturas y expresiones: n es número de pacientes, media o promedio se refiere a la media aritmética, DE es la desviación estándar, EE es el error estándar, P25 es percentil 25, P75 es percentil 75, IC95% es el intervalo de confianza del 95% para una determinada medida, como la media; LI y LS son los límites inferior y superior del IC95%, p es probabilidad.
ASPECTOS ÉTICOS
Cada paciente o un acudiente en caso de un menor de edad, aceptó la participación voluntaria, mediante consentimiento informado y escrito. Cada proyecto fue aprobado por el Comité de Ética del Centro de Investigaciones Médicas (CIM) de la Universidad de Antioquia.
RESULTADOS
Se incluyeron 90 pacientes. Los datos se presentan y analizan sin discriminar por la variable 'lugar de residencia del paciente' porque no se hallaron diferencias importantes en función de ella. Se evaluaron 44 pacientes en Turbo y 46 en El Bagre.
Los enfermos tenían estas características:
a) el 67% residían en la zona rural (fuera de la cabecera del municipio);
b) el 88% eran mestizos, 10% negros y 2% indígenas embera (katíos) o tule (kunas);
c) el 68% eran hombres;
d) el 27% eran menores de 15 años (3% < 5, 15% 5–9 años, 9% 10–14 años), 72% correspondían a pacientes de 15 a 64 años (34% 15–24, 28% 25–44 y 10% 45–64 años) y 1% eran mayores de 64 años. La edad promedio fue de 30 años, con mediana de 24 y desviación estándar de 17.6.
El 38% de los pacientes narró antecedentes de malaria en el último año y entre ellos el número anual de episodios de malaria (según los pacientes) osciló entre 1 y 7: 61% un episodio, 18% dos episodios, 12% 3–4 y 9% 5–7. El último ataque palúdico había sucedido, dijeron los pacientes, hacía menos de 1 mes en el 19% de los casos, entre 1 y 6 meses en 62% y entre 7 y 12 meses en 19%.
El tiempo de evolución de la enfermedad actual era de 4 días como mediana (promedio: 5.8). El 13% tenía 1–2 días de enfermedad, 31% 3 días, el 30% entre 4 y 7 días, 22% entre 8 y 15 días y 3% más de 15 días (20 y 34 días).
Los síntomas narrados por los pacientes, asociados al actual episodio de malaria, fueron: fiebre, cefalea, escalofrío y dolor osteomuscular en 82 a 94% de los enfermos; dolor abdominal, náuseas y vómito en 39 a 61% de los pacientes; diarrea en 16%; tos en 36% y odinofagia y disnea en 13 a 17% de los pacientes. Ninguno narró sangrados ni convulsiones.
En el examen médico al ingresar en el estudio se hallaron palidez conjuntival en 62% de los enfermos, palidez palmar en 28% e ictericia en 2%; no se hallaron cianosis, coluria, fenómenos hemorrágicos, edema, ni cambios cardiopulmonares o neurológicos. La hepatomegalia se halló en 30% de los pacientes y la esplenomegalia, en 11%. El 61% de los pacientes estaban afebriles (hasta 37.5 ºC de temperatura axilar) en el momento de ingresar al estudio, 31% tenían entre 37.6 y 39.0 ºC y el restante 8% mostraban entre 39.1 y 39.4 ºC (Figura Nº 1).
Antes del tratamiento (día 0), la parasitemia asexual osciló entre 520 y 37.800 parásitos/µL, con promedio de 8.766 parásitos/µL y mediana de 5.400/µL. El 7% de los pacientes tenían menos de 1.000 parásitos/µL, 19% tenían hasta 2.000, 49% hasta 5.000, 69% hasta 10.000, 89% hasta 20.000 y 95% hasta 30.000 parásitos/µL. Antes del tratamiento (día 0), los gametocitos se hallaron en el 21% de los pacientes y la gametocitemia (entre quienes la tenían) osciló entre 40 y 7.600 gametocitos/µL, con promedio y mediana de 160; 95% (18 de 19 pacientes) tenían menos de 1.000 gametocitos y sólo uno mostró 7.600.
La evolución de la parasitemia asexual, la gametocitemia y la temperatura corporal (axilar) entre los días 0 y 21 aparece en la tabla Nº 3.
La evolución temporal de la parasitemia asexual es claramente decreciente (Figura Nº 1).

Al completar 24 horas de tratamiento (día 1), la magnitud promedio de la parasitemia se redujo en 76% (en promedio bajó de 8.766 a 2.081 parásitos/µL), el 100% de los pacientes seguían con parásitos, la temperatura promedio bajó de 37.4 ºC a 36.9 ºC y 79% estaban afebriles. El día 2 (completadas 48 horas de terapia antimalárica) había 40 parásitos/μL en promedio, 63% no los presentaban, la temperatura promedio era de 36.3 ºC y 99% estaban sin fiebre. A las 72 horas de tratamiento (día 3) 90% de los pacientes no tenían parásitos, pero 10% aún los presentaban (entre 40 y 80 parásitos/µL) y la temperatura de todos los pacientes (incluso los 9 con parasitemia) estaba por debajo de 37.5 ºC. Estos nueve pacientes no se consideran falla, según el protocolo, porque estaban sin fiebre y porque la parasitemia que presentaban era inferior al 25% de la hallada antes de iniciar el tratamiento. Desde el día 7 hasta el 21, la parasitemia fue nula en los pacientes, excepto en uno que presentó falla tardía (día 21) y mostró 4.720 parásitos/µL, 80 gametocitos/µL y 36.4 ºC.
La gametocitemia presentó tendencia creciente entre los días 0 y 7 y decreciente a partir de este y hasta el final (día 21). El promedio de gametocitos el día cero era de 140 y de 265 el día 7, (aumento de 89%); el día 21 era de 63 (disminución de 76% con respecto al día 7 y de 55% con respecto al día 0) (Figura Nº 1). Además del aumento cuantitativo de la gametocitemia, hubo un aumento del número de pacientes portadores de gametocitos, que el día 0 eran 21% del total, se elevaron a 68% el día 7, a 69% el día 14 y todavía eran 52% el día 21. No se evaluaron la viabilidad ni la fertilidad de tales gametocitos, asuntos críticos para definir la permanencia de la fuente de transmisión de la malaria.
El promedio de temperatura corporal nunca fue elevado (fiebre), pero se redujo de 37.4 ºC el día 0 a 36.9 ºC el 1, a 36.3 el día 2 y a 36.2 el día 3. Los síntomas, signos y efectos adversos desaparecieron en forma rápida y definitiva al avanzar los días de terapia.
Se evaluaron las correlaciones simples entre las variables parasitemia, gametocitemia, temperatura corporal, número de episodios de malaria en el último año y días de evolución de la enfermedad actual. Ninguna de estas variables tuvo distribución normal, excepto la temperatura, por lo que se aplicó la técnica de Spearman (coeficiente rho). Se halló asociación significativa en las correlaciones parasitemia asexual–días de evolución, gametocitemia–parasitemia asexual y gametocitos días evolución (Tabla Nº 4), mientras que la correlación temperatura corporal–parasitemia fue muy próxima a la significación estadística (p = 0.054).
Así, la cantidad de gametocitos depende de la parasitemia asexual y de los días de evolución del paludismo actual y, a la vez, la parasitemia depende de los días de evolución. La fuerte dependencia de la gametocitemia con respecto al tiempo de evolución de la enfermedad se corrobora al conocer que el promedio de días de evolución (considerando todos los pacientes y los 21 días de seguimiento) es de 4.2 cuando no se tienen gametocitos, sube a 5.7 cuando se tienen 1–100 gametocitos/µL, pasa a 7.4 con 101–200/µL, a 10.3 con 201–400/µL y a 8.5 con más de 400/µL (p = 0.000).
Se perdieron 10% de los pacientes (10 personas de las 100 incluidas en el estudio) durante el seguimiento y las causas fueron siempre la inasistencia del paciente al control y la imposibilidad posterior de encontrarlo, a pesar de la búsqueda activa, inmediata e intensa.
La frecuencia de falla terapéutica fue 2.2%: solo hubo dos casos de falla, una precoz y otra tardía. La falla terapéutica no se asoció con municipio, zona de residencia, etnia, sexo, grupo de edad, antecedentes maláricos, antecedentes de hospitalización o transfusión, tiempo de evolución de la enfermedad, parasitemia ni gametocitemia iniciales.
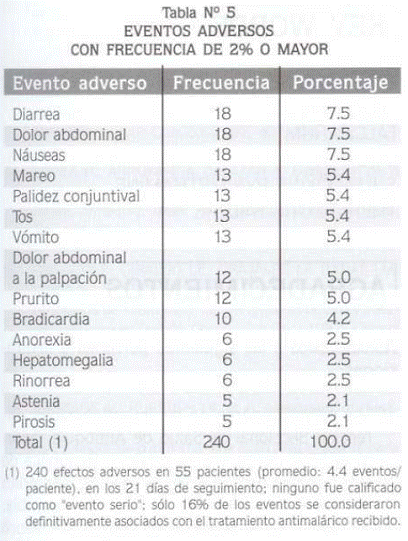
En los seis controles (días 1, 2, 3, 7, 14 y 21) se detectaron 240 eventos adversos en 55 pacientes (promedio: 4.4 eventos/paciente) y ninguno fue calificado como 'evento serio'. Los eventos con frecuencia de 2.0% o más fueron: diarrea, dolor abdominal y náuseas 7.5% cada uno; mareo, palidez conjuntival, tos y vómito 5.4% cada uno; dolor abdominal a la palpación y prurito 5.0% cada uno; bradicardia 4.2%, anorexia, hepatomegalia y rinorrea 2.5% cada una; astenia y pirosis 2.1% cada una (Tabla Nº 5).
Al avanzar el tiempo, los eventos y sus frecuencias se redujeron. Nunca hubo que suspender el tratamiento antimalárico por los efectos adversos y en 86% de los casos no se tomó ninguna medida para tratar el evento, mientras que en 14% se aplicó alguna. Sólo el 16% de los 240 eventos totales, en los 21 días de seguimiento, se consideraron definitivamente asociados con el tratamiento antimalárico recibido, el 23% se consideraron probablemente asociados, el 12% posiblemente asociados, el 13% poco probablemente asociados y el 35% sin ninguna relación. Al terminar la evaluación del paciente, la remisión del evento adverso fue completa en 82% de los casos y estaba aún presente en 18%.
DISCUSIÓN
El protocolo de evaluación de la RTA se aplicó con todo rigor y las modificaciones se especificaron en forma clara y precisa, como la relacionada con la parasitemia (valor mínimo 500 y máximo 50.000 parásitos asexuados/µL). Las dosis, vías de administración y formas de hacerla (tomar los medicamentos con agua, bajo estricta supervisión) se ajustaron al protocolo y a las normas del Ministerio de Salud de Colombia, donde este esquema AQSP se emplea como la primera opción terapéutica para la malaria falciparum no complicada.
Haber logrado medir el efecto (RTA) en el 90% de los pacientes incluidos en el estudio no es un acontecimiento aleatorio, sino que obedece, seguramente, a la estrategia diseñada para evitar las pérdidas, que consistió en el apoyo económico dado al paciente para pagar el transporte (asistencia a los controles) y en la búsqueda activa inmediata de los pacientes que no cumpliesen algún control, búsqueda efectuada por el equipo de investigadores desplazados a cada municipio, quienes organizaron y recibieron el apoyo permanente y generoso de los trabajadores locales encargados del programa antimalárico, todo ello patrocinado en la parte económica por la Dirección Seccional de Salud de Antioquia. Ese porcentaje de pérdidas puede parecer alto, mirado desde el cómodo escritorio de una oficina citadina, pero algo bien distinto es en el terreno.
El cuadro clínico presentado por estos pacientes concuerda con el hallado en diferentes lugares y por nosotros mismos en otros estudios. Fiebre, cefalea, escalofrío y dolor osteomuscular fueron síntomas que ocurrieron en por lo menos 82% de los enfermos. La palidez conjuntival, que sugiere anemia, fue un hallazgo médico presente en 2 de cada 3 pacientes y fue el signo más frecuente en el examen de ingreso, seguida del dolor abdominal al palpar, de la hepatomegalia y la esplenomegalia, todo lo cual es usual en la malaria falciparum no complicada. 60–63
Corresponde a una zona endémica de malaria el que 38% de los pacientes hubiesen narrado antecedentes de malaria en el último año, así como el número de episodios referidos en ese año (61% dijeron haber padecido otro ataque palúdico en el año anterior), dato este último inferior al hallado en niños de 4–11 años de El Bagre, en quienes la frecuencia fue mucho mayor 64–65 pero ello puede explicarse porque en el presente trabajo el 72% de los pacientes eran adultos, lo cual implica desarrollo de inmunidad protectora parcial.
El corto tiempo de evolución de la enfermedad actual (mediana: 4.0 días) está de acuerdo con el hecho de que se trata de malaria no complicada y con la levedad de los síntomas y signos encontrados, así como con el hallazgo de que 79% de los pacientes no tenían gametocitos al ingresar al estudio.
La frecuencia de efectos adversos durante el tiempo de aplicación del tratamiento fue baja, los efectos fueron leves, no requirieron la adopción de medidas especiales de tratamiento y desaparecieron al mejorar el estado general del paciente y al finalizar el tratamiento.
La rápida y potente actividad antipirética del tratamiento (79% afebriles en 24 horas y 99% sin fiebre en 48 horas), derivada de su componente AQ, es ya conocida. 62,63 De acuerdo con otros informes, 66,67 el poder esquizonticida eritrocitario de la combinación AQ–SP fue notorio, como se deduce del hecho de que al completar 48 horas de terapia había, en promedio, 40 parásitos/µL y 63% de los pacientes no tenían parásitos, así como que al completar 72 horas de tratamiento (día 3) solo 10% de los pacientes aún presentaban parásitos (40–80 parásitos/µL), lo cual no es suficiente para decir que se trata de una falla (puesto que la cantidad es muy inferior al 25% de la parasitemia inicial; además, todos los pacientes, inclusive los nueve con parásitos, estaban afebriles); esto podría revelar el comienzo de una reducción de la capacidad antiparasitaria de la combinación, aunque es claro que antes del día 7 esos pacientes estaban todos sin parasitemia y así continuaron hasta el final.
Hay que señalar que el tratamiento AQ–SP no impidió que la gametocitemia aumentara entre los días 0 y 7 (aumentó 89%), cuando empezó a rebajar hasta llegar a un 76% en el día 28 del siguimiento, ni tampoco redujo la cantidad de pacientes portadores de gametocitos, que aumentó hasta el día 14, para luego reducirse. Este hallazgo difiere de lo informado en niños nigerianos, en quienes AQ–SP redujo significativamente el estado de portador de gametocitos en cualquier tiempo entre los días 1 y 14 de seguimiento. 43 Se ha informado que la gametocitemia es afectada por tres factores: 1) la clase de medicamento antimalárico (AQ tiene mayor capacidad de reducirla que la cloroquina y ésta que la SP); 2) la eficacia del tratamiento antimalárico (la prevalencia de portadores y la magnitud de la gametocitemia son mayores en pacientes con 'infecciones sensibles' que en aquellos con 'infecciones resistentes'); 3) la duración de la enfermedad antes de iniciar el tratamiento específico (a mayor tiempo de enfermedad, mayores prevalencia y densidad de gametocitos). 45 Al comparar los tratamientos SP y SPcloroquina, no encontramos efecto de los factores 1) y 2) sobre el estado de portador ni la densidad de gametocitos pero sí hallamos influencia del factor 3). 68 Los gametocitos son la clave para la transmisión del hombre al Anopheles y sus elevadas presencia y cantidad podrían significar que AQSP no sirve para romper la cadena epidemiológica, lo cual debería investigarse a fondo, pues en este trabajo no se evaluaron la viabilidad ni la fertilidad de tales gametocitos, condiciones indispensables para garantizar la transmisión de malaria.
La falla terapéutica con el AQ–SP no se asoció con ninguna de las variables municipio, zona de residencia, etnia, sexo, grupo de edad, antecedentes maláricos, antecedentes de hospitalización o transfusión, tiempo de evolución de la enfermedad, parasitemia ni gametocitemia iniciales. Este hecho coincide con la escasez de informes sobre la asociación de la falla con otra variable que pudiera servir de predictor de la misma ('factor de riesgo para presentar falla terapéutica'). Hay que decir, sin embargo, que existen unos pocos informes que encuentran tal asociación para tratamientos con monoterapia con cloroquina o mefloquina, 34,69–73 pero no conocemos ninguno con amodiaquina sola o combinada.
El hallazgo más importante de este informe es haber comprobado que la eficacia del tratamiento AQ–SP para la malaria falciparum no complicada es excelente (98%), lo cual obliga a conservarlo como la primera opción terapéutica, como sucede desde 2000, cuando se adoptó nacionalmente, aunque en el departamento de Antioquia se usa como tal desde 1985.
Cada vez son más abundantes los estudios, particularmente en África, que muestran igualdad o superioridad de AQ–SP frente a mefloquina–SP y a artesunato–SP 22,23 no solo por su elevada capacidad de eliminar los síntomas y la parasitemia en forma más intensa y acelerada 23,27,31,40,44 sino también por su alto poder para eliminar los gametocitos (bloqueo de transmisión), 26,27,43,45 a lo cual se suman su bajo costo relativo (15 centavos de dólar) y los pocos, leves y pasajeros efectos adversos derivados de su empleo como antimalárico.21,29,33,35,36,37,62,63 En Uganda y en otros países de África se informó recientemente la gran eficacia de esta combinación (falla clínica del tramiento: 9%), mucho mejor que la demostrada por artesunato más sulfadoxina–pirimetamina (falla clínica del tratamiento: 33%); los efectos adversos asociados a uno u otro tratamiento fueron escasos. 25
El poco uso relativo de la AQ se derivó de las reacciones adversas observadas cuando se la emplea para profilaxis 74 situación en la que se la toma por semanas o meses, pero son prácticamente inexistentes los informes sobre efectos adversos graves asociados con su empleo como antimalárico, 62–63 aunque existen. Un reciente editorial de la revista American Journal of Tropical Medicine and Hygiene, suscrito por Peter B. Bloland, señala el entusiasmo excesivo que se tiene ahora por los tratamientos basados en derivados de la artemisinina, de tal manera que sugerir cualquier alternativa 'se aproxima a la herejía'; de igual manera, el autor denuncia las presiones sobre los gobiernos africanos para que adopten esquemas basados en derivados de la artemisinina, presiones que ha ejercido de diversas maneras hasta la OMS; 75 compartimos plenamente estas afirmaciones de Bloland, mucho más cuando el problema del tratamiento se sitúa en América, donde es mucho menos grave que en África, continente este donde AQ–SP mostró excelente desempeño cuando se decidieron a investigar en los años recientes (2000–2004). Una revisión sistemática sobre la AQ vs. CQ y SP para el tratamiento de la malaria, efectuada en 2003, incluyó 56 estudios, la mayoría en África y concluyó que 'hay evidencia para apoyar la continuación del uso de la AQ para tratar la malaria no complicada, debe considerarse la resistencia local al medicamento', 76 precaución que debe tenerse con cualquier otro tratamiento. Otra revisión de 2001 comparó las combinaciones AQ–SP y CQ–SP para tratar la malaria no complicada; encontró 7 estudios (1.277 pacientes en total) y concluyó que 'no hubo evidencia de efectos colaterales serios con las combinaciones' y que ellas, más que la monoterapia con SP, 'pueden hacer que las personas se sientan mejor más rápido' y causaron mejor eliminación sostenida de los parásitos sanguíneos. 77 Sugerimos enfáticamente, que los países de la cuenca amazónica evalúen a fondo la eficacia de la combinación AQ–SP, hasta ahora muy poco usada en ellos: según un informe de la OMS en diciembre de 2004, ningún país de América la emplea actualmente en sus esquemas terapéuticos; 78 ellos deben analizar con criterios científicos la conveniencia de adoptarla, sin dejar que suceda lo que acaba de pasar en Ecuador: allí se evaluaron varios tratamientos, entre ellos AQ–SP y AS–SP, pero antes de conocerse los resultados y sin atender el informe investigativo, el gobierno y la OMS decidieron imponer el esquema AS–SP.
Las principales conclusiones de este estudio son:
1. El desempeño de AQ–SP ha sido excelente en Colombia en los pocos estudios realizados, reducidos a la costa Pacífica del departamento de Nariño y a las zonas de Urabá y Bajo Cauca en el departamento de Antioquia, lo que plantea la necesidad de más estudios en otros lugares (Chocó, Cauca, Orinoquia, Amazonia, Catatumbo), lo cual también debiera hacerse en los demás países americanos, en los que el uso de AQ–SP ha sido prácticamente nulo.
2. La combinación AQ–SP causó rápida eliminación de los síntomas y de los parásitos asexuales circulantes y produjo pocos y leves efectos adversos; todo esto, sumado al bajo costo, a la alta adhesión al tratamiento, a la experiencia en su aplicación (20 años en Antioquia y 5 en Colombia) y a la aceptación de los usuarios, hacen que sea obligatorio mantenerla como la primera opción de tratamiento de la malaria falciparum no complicada.
3. Entre el comienzo y el día 7 del tratamiento, la combinación AQ–SP causó nula reducción del número de portadores de gametocitos y de la cantidad de estos (en realidad, ambas variables crecieron), pero sí ocurrió la reducción de esta masa celular a partir de ese momento, de tal forma que al final del tratamiento la cantidad promedio de gametocitos se había reducido en un 76% respecto al día 7, aunque todavía el 52% de los pacientes eran portadores de tales células, lo que significa que se podrían mantener las fuentes de transmisión; sin embargo, en este estudio no se evaluaron la viabilidad y la fertilidad de los gametocitos, que son fundamentales para que suceda la transmisión.
4. Los estudios recientes realizados en África en número alto y creciente, están de acuerdo con nuestros hallazgos y apuntan a que esta combinación produce mejor respuesta clínica y parasitaria que la de artesunato–sulfadoxinapirimetamina, con las grandes ventajas de su bajísimo costo y la amplia experiencia en su uso.
5. Sin duda alguna, AQ–SP debe mantenerse en Colombia como el tratamiento de primera opción para la malaria falciparum no complicada.
REFERENCIAS BIBLIOGRÁFICAS
1. BLAIR S, LACHARME L, CARMONA J, TOBÓN A. Resistencia del Plasmodium falciparum a los antimaláricos en Urabá y Bajo Cauca Antioqueño, 1998. Rev Epidemiol Antioquia 1999; 24: 207–215. [ Links ]
2. BLAIR S, LACHARME LL, CARMONA–FONSECA J, TOBÓN A. Resistencia de Plasmodium falciparum a 3 antimaláricos en Turbo (Antioquia, Colombia), 1998. Rev Panam Salud Pública 2001; 9: 23–29. [ Links ]
3. BLAIR–TRUJILLO S, LACHARME–LORA L, CARMONAFONSECA J. Resistance of Plamodium falciparum to antimalarial drugs in Zaragoza (Antioquia, Colombia), 1998. Mem Inst Oswaldo Cruz 2002; 97: 401–406. [ Links ]
4. LÓPEZ YL, ARROYAVE A, SALAZAR A. Evaluación de la resistencia in vivo a los medicamentos antimaláricos. El Bagre, Antioquia, 1998. Rev Epidemiol Antioquia 1999; 24: 181–194. [ Links ]
5. OSORIO LE, GIRALDO LE, GRAJALES LF, BARAT LM, CÓRDOBA F, ARRIAGA AL, et al. Evaluación in vivo de la resistencia de Plasmodium falciparum a cloroquina y sulfapirimetamina en Quibdó, Chocó. Biomédica 1997; 17(supl 2): 201–202. [ Links ]
6. OSORIO LE, GIRALDO LE, GRAJALES LF, ARRIAGA AL, ANDRADE AL, RUEBUSH TK, et al. Assessment of therapeutic response of Plasmodium falciparum to chloroquine and sulfadoxine–pyrimethamine in an area of low malaria transmission in Colombia. Am J Trop Med Hyg 1999; 61: 968–972. [ Links ]
7. CASTILLO CM, OSORIO LE, PALMA GI. Assessment of therapeutic response of Plasmodium vivax and Plasmodium falciparum to chloroquine in a malaria transmission free area in Colombia. Mem Inst Oswaldo Cruz 2002; 97: 559–562. [ Links ]
8. COLOMBIA, MINISTERIO DE SALUD. Guía de atención clínica para el diagnóstico y tratamiento de la malaria. Bogotá, Minsalud, 1999. [ Links ]
9. WALKER AJ, LÓPEZ–ANTUÑANO FJ. Response to drugs of South American strains of Plasmodium falciparum. Trans Roy Soc Trop Med Hyg 1968; 62: 654–667. [ Links ]
10. BLAIR S. Resistencia de P. falciparum a drogas en Colombia. Biomédica 1986; 6: 95–100. [ Links ]
11. BOTERO D. Informe de Ravreda (Red Amazónica de Vigilancia de la Resistencia a los Antimaláricos), Belem, Brasil, 2003. [ Links ]
12. ESPINAL CA, CORTES GT, GUERRA P, ARIAS AE. Sensitivity of Plasmodium falciparum to antimalarial drugs in Colombia. Am J Trop Med Hyg 1985; 34: 675–680. [ Links ]
13. RESTREPO M. Informe de Ravreda (Red Amazónica de Vigilancia de la Resistencia a los Antimaláricos), Belem, Brasil, 2003. [ Links ]
14. FLÓREZ D. Comportamiento del P. falciparum a 4–aminoquinolinas, Barrancabermeja y Buenaventura, 1981–1982. Documento Servicio Nacional de Erradicación de la Malaria SEM (Colombia). Informe 1988 del Ministerio de Salud a la OPS. Bogotá: SEM, 1988. [ Links ]
15. COMER RD, YOUNG MD, PORTER JA JR, GAULD JR, MERRITT W. Chloroquine resistance in Plasmodium falciparum malaria on the Pacific coast of Colombia. Am J Trop Med Hyg 1968; 17: 795–799. [ Links ]
16. GONZÁLEZ IJ. Informe presentado en la reunión de Ravreda (Red Amazónica de Vigilancia de la Resistencia a los Antimaláricos), Belem, Brasil, 2003. Dato de 2002. [ Links ]
17. MÉNDEZ F, MUÑOZ A, CARRASQUILLA G, JURADO D, AREVALO–HERRERA M, CORTESE JF, PLOWE CV. Determinants of treatment response to sulfadoxine pyrimethamine and subsequent transmission potential in falciparum malaria. Am J Epidemiol 2002; 156: 230–238. [ Links ]
18. FLÓREZ D. Estudio de susceptibilidad del P. falciparum a drogas en Colombia: Tumaco, Caucasia, Guajira, San José del Guaviare, Barrancabermeja y Buenaventura, 1981–1982. Documento Servicio Nacional de Erradicación de la Malaria SEM (Colombia). Informe 1988 del Ministerio de Salud a la OPS. Bogotá: SEM, 1988. [ Links ]
19. GONZÁLEZ IJ, PADILLA JO, GIRALDO LE, SARAVIA NG. Eficacia de la amodiaquina y la sulfadoxina–pirimetamina en el tratamiento de la malaria por Plasmodium falciparum no complicada en Nariño, Colombia, 1999–2002. Biomédica 2003; 23: 38–46. [ Links ]
20. TALISUNA AO, NALUNKUMA–KAZIBWE A, BAKYAITA N, LANGI P, MUTABINGWA TK, WATKINS WW, et al. Efficacy of sulphadoxine–pyrimethamine alone or combined with amodiaquine or chloroquine for the treatment of uncomplicated falciparum malaria in Ugandan children. Trop Med Int Health 2004; 9: 222–229. [ Links ]
21. GASASIRA AF, DORSEY G, NZARUBARA B, STAEDKE SG, NASSALI A, ROSENTHAL PJ, KAMYA MR. Comparative efficacy of aminoquinoline–antifolate combinations for the treatment of uncomplicated falciparum malaria in Kampala, Uganda. Am J Trop Med Hyg 2003; 68: 127–132. [ Links ]
22. DORSEY G, VLAHOS J, KAMYA MR, STAEDKE SG, ROSENTHAL PJ. Prevention of increasing rates of treatment failure by combining sulfadoxine–pyrimethamine with artesunate or amodiaquine for the sequential treatment of malaria. J Infect Dis 2003; 188: 1.231–1.238. [ Links ]
23. DORSEY G, NJAMA D, KAMYA MR, CATTAMANCHI A, KYABAYINZE D, STAEDKE SG, et al. Sulfadoxine/pyrimethamine alone or with amodiaquine or artesunate for treatment of uncomplicated malaria: a longitudinal randomised trial. Lancet 2002; 360: 2.031–2.038. Comentarios en: Lancet 2002; 360: 1998–1999. Lancet 2003; 361: 1229; réplica del autor 1.229–1.230. [ Links ]
24. STAEDKE SG, KAMYA MR, DORSEY G, GASASIRA A, NDEEZI G, CHARLEBOIS ED, et al. Amodiaquine, sulfadoxine/pyrimethamine, and combination therapy for treatment of uncomplicated falciparum malaria in Kampala, Uganda: a randomised trial. Lancet 2001; 358: 368–374. [ Links ]
25. STAEDKE SG, MPIMBAZA A, KAMYA MR, NZARUBARA BK, DORSEY G, ROSENTHAL PJ. Combination treatments for uncomplicated falciparum malaria in Kampala, Uganda: randomised clinical trial. Lancet 2004; 364: 1.950–1.957. [ Links ]
26. CHECCHI F, PIOLA P, KOSACK C, ARDIZZONI E, KLARKOWSKI D, KWEZI E, et al. Antimalarial efficacy of sulfadoxine–pyrimethamine, amodiaquine and a combination of chloroquine plus sulfadoxine–pyrimethamine in Bundi Bugyo, western Uganda. Trop Med Int Health 2004; 9: 445–450. [ Links ]
27. SCHELLENBER D, KAHIGWA E, DRAKELEY C, MALENDE A, WIGAYI J, MSOKAME C, et al. The safety and efficacy of sulfadoxine–pyrimethamine, amodiaquine, and their combination in the treatment of uncomplicated Plasmodium falciparum malaria. Am J Trop Med Hyg 2002; 67: 17–23. [ Links ]
28. GORISSEN E, ASHRUF G, LAMBOO M, BENNEBROEK J, GIKUNDA S, MBARUKU G, et al. In vivo efficacy study of amodiaquine and sulfadoxine/ pyrimethamine in Kibwezi, Kenya and Kigoma, Tanzania. Trop Med Int Health 2000; 5: 459–463. [ Links ]
29. RWAGACONDO CE, NIYITEGEKA F, SARUSHI J, KAREMA C, MUGISHA V, DUJARDIN JC, et al. Efficacy of amodiaquine alone and combined with sulfadoxine pyrimethamine and of sulfadoxine pyrimethamine combined with artesunate. Am J Trop Med Hyg 2003; 68: 743–747. [ Links ]
30. DELORON P, SEXTON JD, BUGILIMFURA L, SEZIBERA C. Amodiaquine and sulfadoxine–pyrimethamine as treatment for chloroquine–resistant P. falciparum in Rwanda. Am J Trop Med Hyg 1988; 38: 244–248. [ Links ]
31. BASCO LK, SAME–EKOBO A, NGANE VF, NDOUNGA M, METOH T, RINGWALD P, et al. Therapeutic efficacy of sulfadoxine–pyrimethamine, amodiaquine and the sulfadoxine–pyrimethamine–amodiaquine combination against uncomplicated Plasmodium falciparum malaria in young children in Cameroon. Bull World Health Org 2002; 80: 538–545. [ Links ]
32. ABACASSAMO F, ENOSSE S, APONTE JJ, GOMEZ–OLIVE FX, QUINTO L, MABUNDA S, et al. Efficacy of chloroquine, amodiaquine, sulphadoxine–pyrimethamine and combination therapy with artesunate in Mozambican children with non–complicated malaria. Trop Med Int Health 2004; 9: 200–208. [ Links ]
33. DINIS DV, SCHAPIRA A. Estudio comparativo de sulfadoxina–pirimetamina y amodiaquina + sulfadoxinapirimetamina para el tratamiento de malaria causada por Plasmodium falciparum cloroquino–resistente en Maputo, Mozambique. Bull Soc Pathol Exot 1990; 83: 521–527. Consultado: resumen. [ Links ]
34. SOWUNMI A, FATEYE BA, HAPPI TC, GBOTOSHO GO, ODUOLA AM. Plasmodium falciparum gametocytaemia in Nigerian children: Peripheral immature gametocytaemia as an indicator of a poor response to chloroquine treatment, and its relationship to molecular determinants of chloroquine resistance. Ann Trop Med Parasitol 2003; 97: 453–468. [ Links ]
35. NGOUESSE B, BASCO LK, RINGWALD P, KEUNDJIAN A, BLACKETT KN. Cardiac effects of amodiaquine and sulfadoxine–pyrimethamine in malaria–infected African patients. Am J Trop Med Hyg 2001; 65: 711–716. [ Links ]
36. RINGWALD P, KEUNDJIAN A, SAME EKOBO A, BASCO LK. Quimiorresistencia de Plasmodium falciparum en la región urbana de Yaounde, Camerún. Parte 2: Evaluación de la eficacia de amodiaquina y la combinación sulfadoxinapirimetamina en el tratamiento de malaria por Plasmodium falciparum no complicada en Yaounde, Camerún [artículo en francés]. Trop Med Int Health 2000; 5: 620–627. [ Links ]
37. YAVO W, MENAN EI, ADJETEY TA, BARRO–KIKI PC, NIGUE L, KONAN YJ, et al. Sensibilidad in vivo de Plasmodium falciparum a amino–4–quinolinas and sulfadoxina pirimetamine en Agou (Ivory Coast). [artículo en francés]. Pathol Biol (Paris) 2002; 50: 184–188. [ Links ]
38. NDOUNGAA M, BASCO LK. Rapid clearance of P. falciparum hyperparasitaemia after oral amodiaquine treatment in patients with uncomplicated malaria. Acta Tropica 2003; 88: 27–32. [ Links ]
39. AUBOUY A, BAKARY M, KEUNDJIAN A, MBOMAT B, MAKITA JR, MIGOT NABIAS F, et al. Combination of drug level measurement and parasite genotyping data for improved assessment of amodiaquine and sulfadoxine–pyrimethamine efficacies in treating Plasmodium falciparum malaria in Gabonese children. Antimicrob Agents Chemother 2003; 47: 231–237. [ Links ]
40. VAN DILLEN J, CUSTERS M, WENSINK A, WOUTERS B, VAN VOORTHUIZEN T, VOORN W, et al. A comparison of amodiaquine and sulfadoxine–pyrimethamine as first–line treatment of falciparum malaria in Kenya. Trans Roy Soc Trop Med Hyg 1999; 93: 185–188. [ Links ]
41. CHECCHI F, BALKAN S, VONHM BT, MASSAQUOI M, BIBERSON P, ELDIN DE PECOULAS P, et al. Efficacy of amodiaquine for uncomplicated Plasmodium falciparum malaria in Harper, Liberia. Trans Roy Soc Trop Med Hyg 2002; 96: 670–673. [ Links ]
42. CHECCHI F, RODDY P, KAMARA S, WILLIAMS A, MORINEAU G, WURIE AR, et al. Evidence basis for antimalarial policy change in Sierra Leone: five in vivo efficacy studies of chloroquine, sulphadoxine–pyrimethamine and amodiaquine. Trop Med Int Health 2005;10:146–153. [ Links ]
43. SOWUNMI A, FATEYE BA. Plasmodium falciparum gametocytaemia in Nigerian children: before, during and after treatment with antimalarial drugs. Trop Med Int Health 2003; 8: 783–792. [ Links ]
44. MOLTA NB, OGUCHE S, PAM SD, OMALU IC, AFOLABI BM, ODUJOKO JB, et al. Amodiaquine treatment of uncomplicated malaria in children, in an area of chloroquine resistant Plasmodium falciparum in north–central Nigeria. Ann Trop Med Parasitol 2003; 97: 663–669. [ Links ]
45. SOKHNA CS, TRAPE JF, ROBERT V. Gametocytaemia in Senegalese children with uncomplicated falciparum malaria treated with chloroquine, amodiaquine or sulfadoxine + pyrimethamine. Parasite 2001; 8: 243–250. [ Links ]
46. VAN DEN BROEK IV, GATKOI T, LOWOKO B, NZILA A, OCHONG E, KEUS K. Chloroquine, sulfadoxine–pyrimethamine and amodiaquine efficacy for the treatment of uncomplicated Plasmodium falciparum malaria in Upper Nile, south Sudan. Trans Roy Soc Trop Med Hyg 2003; 97: 229–235. [ Links ]
47. ORGANIZACIÓN MUNDIAL DE LA SALUD, ORGANIZACIÓN PANAMERICANA DE LA SALUD. Evaluación de la eficacia terapéutica de los medicamentos para el tratamiento del paludismo por Plasmodium falciparum sin complicaciones en las Américas. Documento OPS/HCP/HCT/113/98. Washington DC: OPS–OMS, 1998. [ Links ]
48. CARMONA–FONSECA J. La malaria en Colombia, Antioquia y las zonas de Urabá y Bajo Cauca: panorama para interpretar la falla terapéutica antimalárica. Parte 1. Iatreia 2003, 16: 299–318. [ Links ]
49. CARMONA–FONSECA J. La malaria en Colombia, Antioquia y las zonas de Urabá y Bajo Cauca: panorama para interpretar la falla terapéutica antimalárica. Parte 2. Iatreia 2004; 17: 34–53. [ Links ]
50. CARMONA–FONSECA J. Malaria, desnutrición y parasitosis intestinal en los niños colombianos: interrelaciones. Iatreia 2004; 17: 354–369. [ Links ]
51. PLANEA Plan Estratégico de Antioquia. De la visión de futuro hacia la identificación de las líneas estratégicas. Subregión del Bajo Cauca. Medellín: Planea, 1999. [ Links ]
52. DIRECCIÓN SECCIONAL DE SALUD DE ANTIOQUIA. Diagnóstico de la situación de salud de Antioquia. Rev Epidemiol Antioquia 2000; 25: 1–239. [ Links ]
52. GONZÁLEZ LM, BLAIR S, CARMONA J. Hepatotoxicidad causada por la amodiaquina. Acta Med Col 2000; 25: 333–336. [ Links ]
53. PLANEA Plan Estratégico de Antioquia. De la visión de futuro hacia la identificación de las líneas estratégicas. Subregión del Urabá. Medellín: Planea, 1999. [ Links ]
54. BLOLAND PB. Drug resistance in malaria. Documento WHO/CDS/CSR/DRS/2001.4. Geneve: WHO; 2001. [ Links ]
55. MARTÍNEZ–BENCARDINO C. Estadística, 4ª ed. Bogotá: Ecoe; 1987: 599–601. [ Links ]
56. MARTÍNEZ–BENCARDINO C. Muestreo. Bogotá: Ecoe; 1984: 45–47. [ Links ]
57. SIERRA ML, VÉLEZ LM, CASTAÑEDA AM, GALEANO LA, MOLINA AL, TABARES Z. Diagnóstico de la situación de salud en Antioquia. Rev Epidemiol Antioquia 2000; 25: 129–132. [ Links ]
58. LÓPEZ–ANTUÑANO FJ. Diagnóstico microscópico de los parásitos de la malaria en la sangre. En: Diagnóstico de malaria. López–Antuñano FJ, Schmunis G, eds. Washington DC: OPS–OMS; 1988. Vol. 512: 39–50. [ Links ]
59. ADOU–BRYN KD, KOUASSI D, OUHON J, ASSOUMOU A, KONE M. Clinical trial of amodiaquine in the community of Attecoube (Abidjan, Cote d'Ivoire)(May–December 1995). Bull Soc Pathol Exot 2000; 93: 115–118. [ Links ]
60. ECHEVERRI M, TOBÓN A, ÁLVAREZ G, CARMONA J, BLAIR S. Clinical and laboratory findings of Plasmodium vivax malaria in Colombia, 2000. Revista Instituto Medicina Tropical São Paulo 2003; 45: 29–34. [ Links ]
61. BLAIR S, TOBÓN A, ECHEVERRI M, ÁLVAREZ G, CARMONA J. Adecuada respuesta clínica y parasitológica de Plasmodium vivax a la cloroquina (Turbo, Antioquia). Infectio (Medellín) 2002; 6: 21–26. [ Links ]
63. PIÑEROS JG, LÓPEZ ML, BLAIR S, CARMONA J. Efectos hepatotóxicos y hematotóxicos de la amodiaquina usada como antimalárico. Comunicación personal. [ Links ]
64. BLAIR S, CARMONA J, CORREA A. Malaria en niños: relaciones entre nutrición e inmunidad. Revista Panam Salud Pública 2002; 11: 5–14. [ Links ]
65. BLAIR S, ÁLVAREZ G, VILLA A, CARMONA J, RÍOS L. Estado nutricional y niveles de inmunoglobulinas y citoquinas en niños con malaria. Anales Pediatría (España) 2003; 58: 418–424. [ Links ]
66. QILIN H, WEICHUAN O, JIEXIAN Z, ZHU W, KUNYAN Z, JIANKANG H, et al. Effectiveness of amodiaquine, sulfadoxine–pyrimethamine, and combinations of these drugs for treating chloroquine–resistant falciparum malaria in Hainan Island, China. Bulletin World Health Org 1988; 66: 353–358 [ Links ]
67. SOWUNMI A. A randomized comparison of chloroquine, amodiaquine and their combination with pyrimethaminesulfadoxine in the treatment of acute, uncomplicated, Plasmodium falciparum malaria in children. Ann Trop Med Parasitol 2002; 96: 227–238. [ Links ]
68. ARANGO E, ÁLVAREZ T, CARMONA J, BLAIR S. Gametocitemia de Plasmodium falciparum en el tratamiento con sulfadoxina–pirimetamina y cloroquina en dos municipios de Antioquia, Colombia. Biomédica 2004; 24: 79–88. [ Links ]
69. HESS FI, IANNUZZI A, LEAFASIA J, COWDREY D, NOTHDURFT HD, VON SONNENBURG F, et al. Risk factors of chloroquine resistance in Plasmodium falciparum malaria. Acta Tropica 1996, 61: 293–306. [ Links ]
70. HESS FI, NUKURO E, JUDSON L, RODGERS J, NOTHDURFT HD, RIECKMANN KH. Anti–malarial drug resistance, malnutrition and socio–economic status. Trop Med Int Health 1997, 2: 721–728. [ Links ]
71. OLANREWAJU WI, JOHNSON AW. Chloroquine–resistant lasmodium falciparum malaria in Ilorin, Nigeria: prevalence and risk factors for treatment failure. Afr J Med Sci 2001, 30: 165–169 [ Links ]
72. FONTANET AL, WALKER AM. Predictors of treatment failure in multiple drug resistant falciparum malaria: results from a 42–day follow–up of 224 patients in eastern Thailand. Am J Trop Med Hyg 1993, 49: 465–472. [ Links ]
73. TER KUILE FO, LUXEMBURGER C, NOSTEN F, THWAI KL, CHONGSUPHAJAISIDDHI T, WHITE NJ. Predictors of mefloquine treatment failure: a prospective study of 1590 patients with uncomplicated falciparum malaria. Trans Roy Soc Trop Med Hyg 1995; 89(6): 660–664. [ Links ]
74. ORGANIZACIÓN MUNDIAL DE LA SALUD. Terapia com associacao de medicamentos antipalúdicos. Ginebra: OMS, 2001: 10–11. WHO/CDS/RBM/2001. 35. [ Links ]
75. BLOLAND PB. A contrarian view of malaria therapy policy in Africa (editorial). Am J Trop Med Hyg 2003; 68: 125–126. [ Links ]
76. OLLIARO P, MUSSANO P. Update of: Cochrane Database Syst Rev 2000; (2): CD000016. Amodiaquine for treating malaria. Cochrane Database Syst Rev 2003; CD000016. [ Links ]
77. MCINTOSH HM. Update of: Cochrane Database Syst Rev. 2000; (2): CD000386. Chloroquine or amodiaquine combined with sulfadoxine–pyrimethamine for treating uncomplicated malaria. Cochrane Database Syst Rev 2001; CD000386. [ Links ]
78. ORGANIZACIÓN MUNDIAL DE LA SALUD. Global AMDP database – AMRO. http://mosquito.who.int/amdp/amdp_amro.htm. Consultada: 13 enero 2005. [ Links ]
79. BOTERO D, RESTREPO M, MONTOYA A. Prospective double–blind trial of two different doses of mefloquine plus pyrimethamine–sulfadoxine compared with pyrimethamine–sulfadoxine alone in the treatment of falciparum malaria. Bull World Health Organ 1985; 63: 731–737. [ Links ]
Recibido: 16 de diciembre de 2004
Aceptado: 01 de febrero de 2005