Introducción
En Colombia, el Bosque seco Tropical (bs-T) se define como aquella formación vegetal que presenta una cobertura boscosa continua y que se distribuye entre los 0-1.000 m de altitud; presenta temperaturas superiores a los 24 °C (piso térmico cálido) y precipitaciones entre los 700 y 2.000 mm anuales, con uno o dos periodos marcados de sequía al año (Espinal 1985; Murphy y Lugo 1986; Instituto de Investigación de Recursos Biológicos Alexander von Humboldt-IAvH 1997). De acuerdo con Hernández (1990), esta formación corresponde a los llamados bosques higrotropofíticos, bosque tropical caducifolio de diversos autores y bosque seco Tropical (bs-T) de Holdridge (1967). Se caracteriza por poseer especies con importantes estrategias adaptativas, como respuesta principalmente a la estacionalidad climática, entre ellas la presencia de especies deciduas (Murphy y Lugo 1986).
Los bs- T son ecosistemas que albergan un gran número de especies en fauna y flora, con una alta riqueza en mariposas diurnas en la región del valle interandino del Cauca (Kattan et al. 2004). El Parque Regional El Vínculo es una de las zonas con mayor riqueza de especies de mariposas del bosque seco en Colombia, y cuenta con el 16,43 % del total de la diversidad de lepidopterofauna del país (Gavíria-Ortíz y Henao-Bañol 2011).
En la región del valle seco del río Patía, en el departamento del Cauca, se registran 12 fragmentos de bosque seco (Instituto de Investigación de Recursos Biológicos Alexander von Humboldt - IAvH 2014), en ellas se presentan amenazas de origen natural, antrópicas y mixtas (socio-naturales) que resultan de condiciones naturales pero aceleradas por las actividades del hombre, se encuentran la desertificación y la sequía que tienen gran relevancia en este municipio y, a nivel regional, colmatada por la actividad ganadera de manera extensiva (Corporación Autónoma Regional del Cauca - CRC 2009).
Debido a la fuerte intervención en el bs-T y a la constante amenaza sobre este ecosistema, es necesaria la identificación de grupos faunísticos que sean indicadores útiles en el monitoreo ambiental (Brown 1991). Las mariposas diurnas son un grupo importante para el estudio y monitoreo de la biodiversidad (Llorente-Bousquets et al. 1993; Andrade 2002; Vargas et al. 2011) y figuran entre los mejores grupos indicadores ya que tienen un ciclo biológico corto, especificidad ecológica y son fáciles de muestrear en cualquier época del año (Brown 1991; Lucci-Freitas et al. 2006). Además, es el tercer orden más numeroso de animales en el mundo y su taxonomía está bien definida. Han mostrado ser altamente sensibles a los cambios de microclima, temperatura, humedad nivel de luminosidad, parámetros que cambian con la perturbación de los hábitats (Brown 1991; Kremen et al. 1993) lo que posibilita el monitoreo a largo plazo de una comunidad de mariposas específica y así detectar cambios en la diversidad biológica en zonas amenazadas y poder establecer estrategias de manejo y conservación (Constantino 1996). La especificidad de algunas mariposas en estado larval por determinadas especies vegetales como hospederas y los requerimientos nectarívoros de los adultos, las convierte en un componente importante dentro de los ecosistemas, que se traduce en la función de remoción de área foliar; en su papel ecológico dentro de las pirámides tróficas como fuente importante de alimento para otros organismos y, la abundancia de sus poblaciones, las hace en importantes polinizadores de diferentes especies vegetales. Estas interacciones han sido interpretadas como el resultado de procesos coevolutivos y uno de los factores responsables de la megadiversidad en los bosques tropicales (Brown 1991). Por lo tanto, la presencia de ciertos grupos puede indicar la continuidad de comunidades y su ausencia una fragmentación o alteración de la integridad del paisaje (Andrade 1998; Bonebrake y Ponisio 2010; Shahabuddin y Ponte 2005).
El presente estudio tuvo como objetivo evaluar el impacto que la ganadería ha tenido sobre remanentes de bosque seco en la cuenca del Patía, a través del estudio de la comunidad de mariposas Rhopalocera como grupo indicador; la riqueza, abundancia y la influencia de los cambios en la composición entre los fragmentos y la matriz, acompañados de la caracterización habitacional de cada fragmento.
Materiales y métodos
Área de estudio
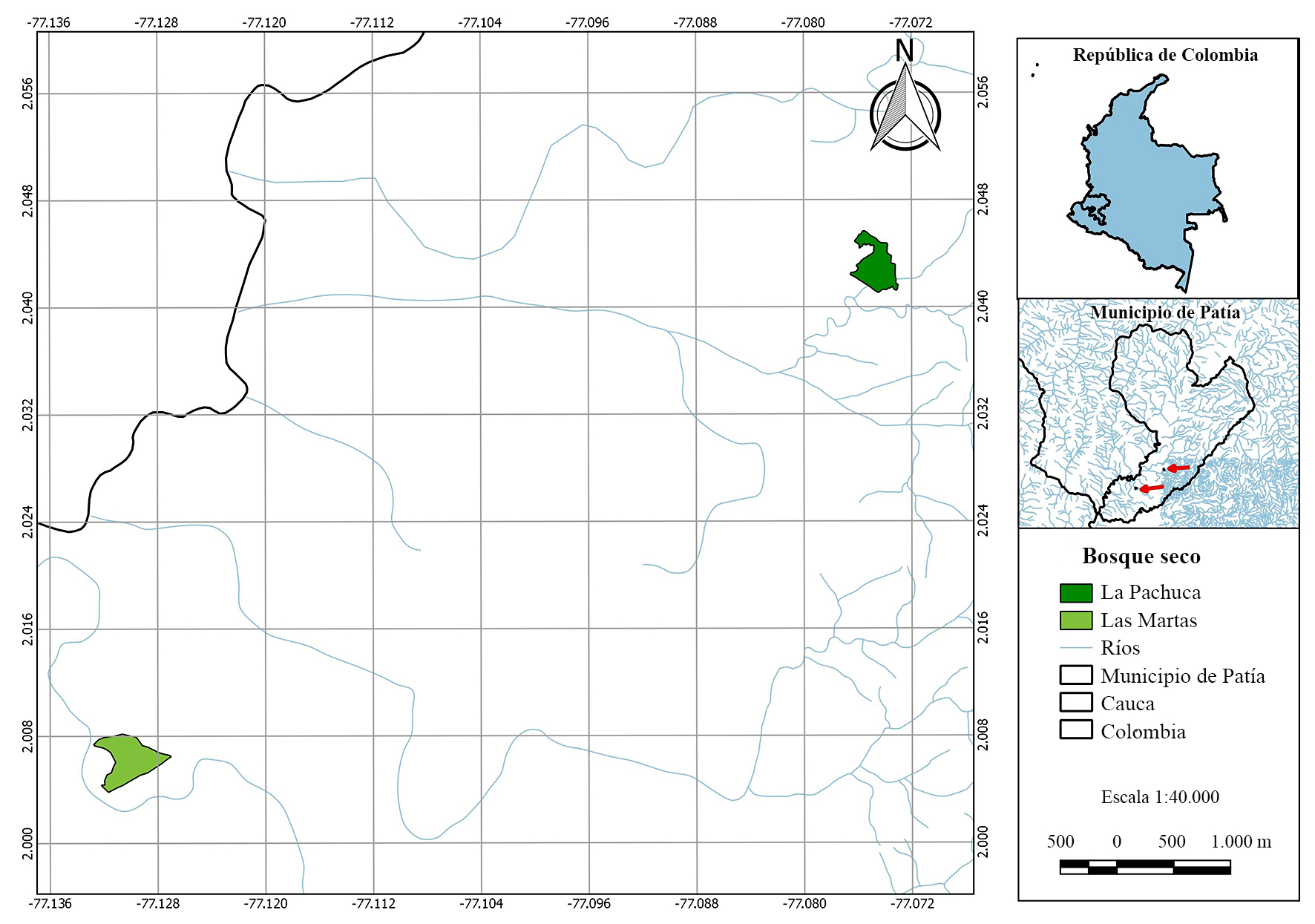
El estudio fue realizado en dos fragmentos de bs-T que hacen parte de las haciendas Las Martas (2º00’22.88”N; 77º08’13.92”O) con 35 ha y La Pachuca (2º02’33.98”N; 77º04’29.78”O) con 18 ha (Fig. 1), ubicadas en los corregimientos de Patía y El Puro, municipio de Patía. En general se presenta un deterioro, producto de la deforestación intensiva, implementación de ganadería extensiva, invasión de cauces, intervenciones antrópicas con impactos sobre la cobertura vegetal y reducción de la producción hídrica (Alcaldía Municipal de Patía Cauca 2013).
Captura de especímenes
En cada uno de los fragmentos y la matriz aledaña, se establecieron dos transectos de 300 m separados 150 m entre sí. Los transectos se ubicaron de tal manera que 150 m del transecto quedará dentro del fragmento de bosque y se continuará 150 m hacia la matriz. En cada transecto se marcó cada 50 m una estación y se instaló a 3 m del suelo, una trampa van Someren Rydon, cebada con fruta y pescado descompuesto, intercaladas entre cada estación. Las trampas se expusieron durante dos días y se revisaron cada tres horas entre las 8 y las 17 horas. El muestreo se complementó capturando ejemplares con jama entomológica en los dos transectos, en los intervalos de tiempo entre la revisión de las trampas durante el día, con el mismo esfuerzo de muestreo de dos horas jameo/día/transecto. Es de aclarar que se hizo una primera recolecta de individuos y con ellos se elaboró una cartilla de campo con los morfotipos de las mariposas que facilitó la identificación en campo y evitó el sacrificio de individuos. Las mariposas colectadas, y registradas, se marcaron en su ala derecha con un marcador Sharpie para no sobreestimar la abundancia relativa (Villarreal et al. 2004; Triplehorn y Jhonson 2005; Prieto et al. 2007). Los cuatro muestreos en total de se realizaron cada dos meses, entre septiembre 2014 y febrero 2015.
Los individuos recolectados se rotularon con la información del muestreo (localidad, hora, fecha, tipo de recolecta, recolector). Las mariposas se almacenaron en sobres de papel milano para su montaje e identificación en el laboratorio de biología de la Universidad del Cauca. Se emplearon las claves de (Le Crom et al. 2002; 2004) y la guía de campo de mariposas diurnas de la zona central cafetera colombiana (Valencia et al. 2005). Las identificaciones fueron, corroboradas por el especialista Jean Francois Le Crom. La colección de especímenes se depositó en el Museo de Historia Natural de la Universidad del Cauca.
Caracterización del hábitat en los fragmentos de bs-T
Se midieron cinco variables (Tabla 1) que describen el hábitat: cobertura de dosel (medido con un densímetro esférico Forestry Suppliers), espesor y volumen de hojarasca, DAP de los árboles, altura estimada y se coleccionaron muestras de los árboles con diámetro a la altura del pecho mayor o igual a 2,5 cm, con el fin de estimar la riqueza y densidad arbórea por unidad de área (Gentry 1996; Mendoza y Ramírez 2000). Para identificar las actividades que tensionan los fragmentos de bs-T, se realizó una evaluación cualitativa mediante la Matriz de Fearo (Federal Environmental Assessment Review Office) Figueroa et al. (1998) o Matriz de Cribado, para evaluar el impacto ambiental generado.
Tabla 1 Variables tomadas para la caracterización de los fragmentos de bosque seco La Pachuca y Las Martas, Patía (Cauca, Colombia).
| Variables | La Pachuca | Las Martas |
|---|---|---|
| Cobertura de dosel | 92,28 % | 91,43 % |
| Volumen de hojarasca | 13,70 litros | 3,40 litros |
| DAP | 7,61 cm | 9,28 cm |
| Altura estimada | 6,12 m | 7,44 m |
| CAP | 23,91 cm | 29,16 cm |
| Espesor de hojarasca | 4,37 cm | 5,13 cm |
Análisis de datos
La riqueza y abundancia de lepidópteros diurnos fueron analizados con el programa Estimates (Colwell 2008) y Past 3.14, determinando el índice de diversidad de Shannon, riqueza verdadera de Jost, estimadores de riqueza Chao1 y Ace, eficiencia de muestreo. En cuanto al cambio en la abundancia y composición entre los fragmentos se empleó el índice de diversidad beta, coeficiente de similitud de Jaccard y coeficiente de similitud de Sorensen (Moreno 2001).
Resultados y discusión
Riqueza, abundancia y composición
Entre los dos fragmentos de bosque seco, se registraron 679 individuos, distribuidos en seis familias, 14 subfamilias y 81 especies (Tablas 2 y 3). Es importante aclarar que durante la temporada seca en Las Martas no se obtuvo registro por cuestiones de orden público.
Tabla 2 Riqueza de lepidópteros diurnos en los fragmentos de bosque seco La Pachuca y Las Martas, Patía (Cauca, Colombia).
| Total | La Pachuca | Las Martas | |||||
|---|---|---|---|---|---|---|---|
| Familia | Subfamilia | Temporada seca | Temporada de lluvia | Temporada de lluvia | |||
| % individuos | No. especies | % individuos | No. especies | % individuos | No. especies | ||
| Nymphalidae (61,12 %) | Biblidinae | 72,12 | 3 | 73,26 | 3 | 44,95 | 4 |
| Charaxinae | 4 | 5 | 7 | ||||
| Danainae | 1 | 4 | 3 | ||||
| Heliconiinae | 1 | 2 | 3 | ||||
| Nymphalinae | 3 | 4 | 3 | ||||
| Satyrinae | 2 | 8 | 2 | ||||
| Pieridae (19,00 %) | Coliadinae | 13,46 | 6 | 10,41 | 8 | 29,62 | 10 |
| Pierinae | 1 | 1 | 1 | ||||
| Hesperiidae (13,99 %) | Hesperiinae | 11,54 | 2 | 9,72 | 3 | 19,16 | 6 |
| Pyrginae | 7 | 8 | 9 | ||||
| Lycaenidae (2,21 %) | Theclinae | 1,92 | 2 | 0,69 | 1 | 3,83 | 2 |
| Polyommatinae | 0 | 1 | 1 | ||||
| Papilionidae (2,65 %) | Papilioninae | 0 | 0 | 3,81 | 2 | 2,44 | 2 |
| Riodinidae (1,03 %) | Riodininae | 0,96 | 1 | 2,08 | 3 | 0 | 0 |
Tabla 3 Distribución de lepidópteros en dos fragmentos de bosque seco La Pachuca y Las Martas, Patía (Cauca, Colombia). discriminados por: borde (Br), bosque (Bs) y matriz (Mt).
| Familia | Especie | La Pachuca | Las Martas | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Mt | Br | Bs | Mt | Br | Bs | ||||||||
| Nymphalidae | Biblis hyperia pacifica (A. Hall, 1928) | X | - | - | - | - | X | ||||||
| Hamadryas feronia (Linnaeus, 1758) | X | X | X | - | - | X | |||||||
| Hamadryas februa ferentina (Godart, [1824]) | X | X | X | - | - | - | |||||||
| Hamadryas amphinome fumosa (Fruhstorfer, 1915) | - | X | - | - | - | X | |||||||
| Eunica tatila (Herrich-Schäffer, [1855]) | - | - | - | - | - | X | |||||||
| Prepona pylene (Hewitson, 1854) | - | - | X | X | - | X | |||||||
| Fountainea eurypyle glanzi (Rotger, Escalante y Coronado, 1965) | X | X | X | X | X | X | |||||||
| Fountainea ryphea (Cramer, 1775) | X | X | X | X | X | X | |||||||
| Archaeoprepona amphimachus (Fabricius, 1775) | - | X | - | - | - | - | |||||||
| Prepona philipponi Le Moult, 1932 | - | - | X | - | - | - | |||||||
| Siderone galanthis (Cramer, 1775) | X | - | X | X | X | X | |||||||
| Fountainea glycerium glycerium (E. Doubleday, [1849]) | X | - | - | X | - | X | |||||||
| Memphis philumena (E. Doubleday, 1849) | - | - | - | X | - | - | |||||||
| Archaeoprepona demophon muson (Fruhstorfer, 1905) | - | - | - | - | - | X | Mechanitis polymnia chimborazona H. Bates, 1864 | X | X | X | - | - | - |
| Mechanitis polymnia caucaensis Haensch, 1909 | - | - | X | - | - | - | |||||||
| Lycorea cleobaea atergatis (Doubleday, 1847) | - | - | X | - | - | - | |||||||
| Mechanitis doryssus Bates, 1864 | - | - | X | X | - | - | |||||||
| Hypoleria ocaela (E. Doubleday, 1847) | - | - | - | - | - | X | |||||||
| Danaus eresimus (Cramer, [1777]) | X | - | - | - | - | - | |||||||
| Danaus gilippus (Cramer, 1776) | - | - | - | X | - | - | |||||||
| Euptoieta hegesia (Cramer, 1779) | X | - | - | X | - | - | |||||||
| Heliconius sara (Fabricius, 1793) | - | - | X | - | - | - | Agraulis vanillae (Linnaeus, 1758) | - | - | - | - | - | X |
| Eueides isabella arcuata Stichel, 1903 | - | - | - | - | - | X | |||||||
| Anartia amathea (Linnaeus, 1758) | X | - | - | - | - | - | |||||||
| Anartia jatrophae (Linnaeus, 1763) | X | - | - | X | X | X | |||||||
| Junonia evarete (Cramer, 1779) | X | X | X | X | X | - | |||||||
| Siproeta stelenes (Linnaeus, 1758) | - | - | X | - | X | - | |||||||
| Siproeta epaphus (Latreille, 1813) | - | X | - | - | - | - | |||||||
| Pareuptychia metaleuca (Boisduval, 1870) | X | - | - | - | - | - | |||||||
| Cissia pseudoconfusa Singer, DeVries y Ehrlich, 1983 | X | X | X | - | X | X | |||||||
| Caligo illioneus oberon Butler, 1870 | - | X | - | - | - | - | |||||||
| Taygetis andromeda (Cramer 1779) | X | - | - | - | - | X | |||||||
| Magneuptychia libye (Linnaeus, 1767) | X | - | X | - | - | - | |||||||
| Hermeuptychia hermes (Fabricius, 1775) | X | - | X | - | - | - | |||||||
| Manataria maculata (Hopffer, 1874) | - | - | X | - | - | - | |||||||
| Caligo telamonius (C. Felder y R. Felder, 1862) | - | - | X | - | - | - | |||||||
| Pieridae | Eurema xantochlora xanthochlora (Kollar, 1850) | X | - | X | X | X | X | ||||||
| Pyrisitia proterpia (Fabricius, 1775) | X | - | - | X | X | - | |||||||
| Eurema daira lydia (C. Felder y R. Felder, 1861) | X | - | X | X | X | X | |||||||
| Eurema albula marginella (C. Felder y R. Felder, 1861) | X | - | X | - | X | - | |||||||
| Phoebis sennae marcellina (Cramer, 1777) | X | - | - | X | X | X | |||||||
| Eurema elathea (Cramer, 1777) | X | - | - | - | - | X | |||||||
| Eurema gratiosa (Doubleday, 1847) | X | - | - | - | X | - | |||||||
| Pyrisitia nise venusta (Boisduval, 1836) | X | - | - | X | - | - | |||||||
| Phoebis philea (Linnaeus, 1763) | X | - | - | - | - | X | |||||||
| Phoebis agarithe agarithe (Boisduval, 1836) | - | - | - | - | X | - | |||||||
| Melete lycimnia reducta Constantino, Le Crom y Torres, 2004 | X | - | - | - | - | - | |||||||
| Ascia monuste (Linnaeus, 1764) | X | - | - | X | - | - | |||||||
| Hesperiidae | Pompeius pompeius (Latreille, 1824) | X | - | - | X | - | - | ||||||
| Eprius velleda (Godman, 1900) | - | - | X | - | X | - | |||||||
| Conga chlydaea (Butler, 1877) | X | - | - | - | - | - | |||||||
| Hylephila phyleus phyleus (Drury, 1773) | - | - | - | X | X | - | |||||||
| Atalopedes campestris huron (W. H. Edwards, 1863) | - | - | - | X | - | - | |||||||
| Papias sp. | - | - | - | - | X | - | |||||||
| Decinea percosius (Godman, 1900) | - | - | - | - | X | - | |||||||
| Pyrgus orcus (Stoll, 1780) | X | - | X | X | X | X | |||||||
| Xenophanes tryxus (Cramer, 1780) | X | - | - | - | - | - | |||||||
| Urbanus teleus (Hübner, 1821) | X | X | - | X | X | X | |||||||
| Antigonus erosus (Hübner, [1812]) | X | - | X | X | X | - | |||||||
| Eantis thraso (Hübner, [1807]) | X | - | X | - | - | - | |||||||
| Chioides catillus (Cramer, 1779) | X | - | - | - | X | X | |||||||
| Urbanus simplicius (Stoll, 1790) | X | - | X | - | - | - | |||||||
| Urbanus procne (Plötz, 1881) | X | - | - | - | - | X | |||||||
| Pyrgus adepta Plötz, 1884 | X | - | - | X | X | X | |||||||
| Epargyreus exadeus (Cramer, 1780) | - | - | - | X | - | X | |||||||
| Heliopetes macaira (Reakirt, [1867]) | - | - | - | - | X | - | |||||||
| Typhedanus undulatus (Hewitson, 1867) | - | - | - | - | X | X | |||||||
| Lycaenidae | Ocaria ocrisia (Hewitson, 1868) | - | X | - | - | - | - | ||||||
| Ministrymon clytie (W. H. Edwards, 1877) | X | - | - | - | - | - | |||||||
| Calycopis beon (Cramer, 1780) | X | - | - | - | - | - | |||||||
| Lamprospilus collucia (Hewitson, 1877) | - | - | - | - | - | X | |||||||
| Strephonota tephraeus (Geyer, 1837) | - | - | - | - | - | X | |||||||
| Cupido comyntas (Godart, [1824]) | X | - | - | - | - | - | |||||||
| Leptotes cassius (Cramer, 1775) | - | - | - | X | - | X | |||||||
| Papilionidae | Heraclides paeon thrason (C. Felder y R. Felder, 1865) | X | - | X | X | X | - | ||||||
| Heraclides anchisiades (Esper, 1788) | X | - | - | - | X | - | |||||||
| Riodinidae | Lasaia agesilas agesilas (Latreille, 1809) | X | X | X | - | - | - | ||||||
| Melanis electron melantho (Ménétriés, 1855) | X | - | - | - | - | - | |||||||
| Parcella amarantina (C. Felder y R. Felder, 1865) | - | - | X | - | - | - | |||||||
Durante los muestreos la actividad o inactividad de los potreros influyó en la actividad, distribución y oferta alimenticia para los lepidópteros; también se observó que las lluvias aumentaron la tasa reproductiva de estos y otros insectos, lo cual generó mayor competencia por parte de odonatos e himenópteros como avispas y algunas hormigas del género Crematogaster. En conjunto, todos aprovecharon la oportunidad cuando algunas mariposas frecuentaban el recurso hídrico acumulado en la matriz para el caso de Las Martas, borde y bosque en forma de lodo, en La Pachuca dentro y fuera del bosque como charcas.
Comparación entre los fragmentos La Pachuca y Las Martas
Nymphalidae registró la mayor riqueza y abundancia. El alto número de especies e individuos aportados por esta familia se explica por la amplia riqueza de especies, que ocupa una diversidad de hábitats y presenta amplios intervalos de distribución (DeVries et al. 1999; Chacón y Montero 2007). Estuvo seguida por Pieridae (Tabla 2), lo que se puede atribuir a que las subfamilias Pierinae y Coliadinae presentan especies altamente heliofílicas (Emmel y Austin 1990), además algunos géneros pueden ser beneficiados por el incremento de la temperatura que reduce el tiempo de desarrollo larval y aumenta las tasas de fecundidad (Chew 1995). Las especies comunes que se encontraron en los tres hábitats (Tabla 3) se han registrado volando en zonas abiertas y cafetales bajo sombra, alimentándose de frutas fermentadas, excrementos de aves y mamíferos, y de compuestos orgánicos en descomposición (Valencia et al. 2005).
Tobar (2000), propone una tendencia de especies de mariposas generalistas en hábitats perturbados o con algún tipo de perturbación o transformación, mientras que las especies de bosque tienden a ser especialistas y prefieren hábitats con estructuras de vegetación más complejas. Las Martas y La Pachuca son fragmentos altamente intervenidos, con una matriz ganadera dominante que ofrece alimento para algunos lepidópteros (Tabla 3). Estudios en diferentes estados de sucesión secundaria y pastizales, sugieren una alta heterogeneidad en los estratos lo que posibilita un mayor número de microhábitats para algunas especies, como T. andromeda indicadora de bosque secundario (Álvarez 1993; Andrade 1998). Este comportamiento ha sido reportado por Simonson et al. (2001) quienes sugirien que la variación microclimática y complejidad del hábitat favorece la composición y diversidad de mariposas. Griffiths (1985), mencionó que la variación de la altitud ejerce una acción sobre el clima, principalmente en la disminución o el aumento de la presión atmosférica, el cambio en la densidad del aire, el descenso de la temperatura y el aumento de la precipitación. Cabe resaltar que La Pachuca registró mayor riqueza y abundancia en la matriz, posiblemente debido a que en diciembre se evidenció la incineración de un ternero, siendo de éste un atractivo para los lepidópteros acimófagos (Figs. 2A-2B).

Figura 2 Riqueza (A), Abundancia relativa (B) de lepidópteros registrados entre los fragmentos de bosque seco La Pachuca y Las Martas, Patía (Cauca, Colombia).
En cuanto a los cambios entre la temporada de sequía y lluvia (Tabla 2 y Figs. 3A-3B), son evidentes en la riqueza y abundancia de lepidópteros. En este caso, las precipitaciones son un factor ambiental que modela la fenología del bosque seco y, por consiguiente, la disponibilidad de refugio y alimento necesarios para estos insectos (Vargas et al. 2011). En la temporada seca no se contó con ningún representante de la familia Papilionidae y Riodinidae, y durante las lluvias la tasa de inmaduros correspondientes a H. anchisiades en los tres hábitat se incrementó. Esta especie fue la más abundante, al menos de octubre - diciembre, tanto en la Pachuca como en las Martas. Hill (1988) indicó que la abundancia estacional de mariposas es un fenómeno complejo, ligado a factores ambientales como la precipitación que reduce la temperatura ambiental e influyen en sus ciclos de vida, sumado a los complejos mecanismos de termorregulación que poseen (Dennis 1993).

Figura 3 Riqueza (A), abundancia relativa (B) de lepidópteros registrada en La Pachuca durante la temporada de sequía y lluvia (Cauca, Colombia).
El cambio estacional en la riqueza de mariposas también parece estar en función del voltinismo y la sincronización generacional con las condiciones ambientales y nutricionales. De acuerdo con Shapiro (1974), las especies univoltinas tienden a ser monófagas y las multivoltinas polífagas, por lo que estas últimas pueden emerger en varias épocas del año y tienen oportunidad de sobrevivir, pues sus requerimientos no son tan específicos como en las primeras, cuya emergencia está sincronizada con la época en que sus recursos alimenticios están presentes. La presencia de las lluvias se correlaciona directamente con la abundancia y la riqueza de los insectos (Wolda 1988), debido a que se puede afectar la fisiología de la reproducción, el desarrollo ontogenético y la conducta de los imagos; indirectamente también puede afectar a las poblaciones por sus efectos sobre la fenología vegetal. Además, las fórmulas y porcentajes de algunos compuestos presentes en las plantas pueden variar en cada estación y no ser palatables en ciertos meses, por lo que no son aprovechables nutricionalmente por los estadios inmaduros de ciertas especies. Esto puede verse reflejado en el tamaño poblacional en la época de no-palatabilidad, o bien, que en esa época sólo se encuentren especies polífagas, pues éstas pueden alimentarse de varias especies o familias de plantas, dado su amplio espectro de recursos alimenticios (Vargas et al. 1999).
Ahora bien, el fragmento Las Martas cuenta con 35 hectáreas, está rodeado de una amplia matriz ganadera y cercas vivas. En su interior se encuentran caminos de herradura frecuentemente usados para el transporte de cincho y ganado vacuno. El potrero se caracterizó por la amplia distribución de Z. fagara y es de resaltar que, en la época de lluvias, se presentaron cúmulos de agua en torno a las cercas vivas lo cual favoreció la permanencia de hespéridos y piéridos. Además, con la actividad del potrero se generaba mayor oferta de alimento para aquellas mariposas copronecrófagas como J. evarete y A. erosus. Por otro lado, se notó que plantas de la familia Asteraceae, Verbenaceae y Poaceae a lado y lado de las cercas vivas formaron parte de la oferta de alimento para lepidópteros por encontrarse en floración durante las lluvias. En cuanto al bosque se encuentra en sucesión avanzada con intervención constante, los transectos al interior están divididos por una quebrada más cercana al transecto 1, con abundancia de odonatos. En el 2, se presentó una dinámica diferente, debido a que el terreno tenía una mayor pendiente, la cual permitía ciertos puntos con gran incidencia de luz y gran cantidad de material orgánico por la tabla 5hojarasca, en esta zona se visualizaron lepidópteros como B. hyperia pacifica, H. amphinome fumosa, A. vanillae, entre otras. Las especies vegetales registradas fueron 15 (Tabla 4). El hábito de crecimiento con mayor presencia en este bosque correspondió a los arbustos (57,14 %) (Erazo et al. 2014).
Tabla 4 Especies vegetales encontradas en los fragmentos de bosque seco bosque seco La Pachuca y Las Martas, Patía (Cauca, Colombia).
| Especie | La Pachuca | Las Martas |
|---|---|---|
| Albizia guachapele (Kunth) Dugand | x | x |
| Cassia grandis L. f., 1781 [1782] | x | x |
| Citharexylum kunthianum Moldenke | - | x |
| Coutarea hexandra (Jacq.) K. Schum., 1889 | - | x |
| Crescentia cujete L., 1753 | x | x |
| Croton hibiscifolius Kunth ex Spreng | x | x |
| Eritroxylum sp. | x | x |
| Eugenia sp. | x | x |
| Guazuma ulmifolia Lam. 1789 | x | x |
| Machaerium sp. | - | x |
| Pithecellobium lanceolatum (Humb. & Bonpl. ex Willd.) Benth | x | x |
| Psidium sartorianum (O. Berg) Nied., 1893 | - | x |
| Zanthoxylum caribaeum Lam., 1786 | x | x |
| Zanthoxylum fagara (L.) Sarg., 1890 | - | x |
| sp. 1 | - | x |
| Bunchosia sp. | x | - |
| Pisonia sp. | x | - |
El bosque La Pachuca está rodeado por una amplia matriz de ganado vacuno (cebú y brahmán) dominada por pastizales, árboles de Crescentia cujete L., 1753 y dos ciénagas, una de ellas empleada para la caza de patos, próxima a ella se estableció el transecto 1. La parte de esta matriz es intervenida por un camino de herradura para el transporte de los pobladores a su zona de trabajo, ahí se estableció el transecto 2, en ella fue muy marcada la presencia de A. amathea, J. evarete, P. orcus, P. adepta y A. monuste entre otras. Alrededor se encuentran algunos cultivos de pan coger (plátano, sandia, papaya, entre otros) y monocultivos como cacao que forman parte de la agricultura de la zona. Llegando al borde se encuentran cercas vivas conformadas por Bromeliaceae. Durante la temporada de lluvias parte de este borde se encontró en floración, con especies de Asteraceae, Fabaceae y Solanaceae que ampliaron la oferta de alimento para los lepidópteros como: Caligo ilioneus oberon (Butler, 1870), S. epaphus, A. amphimachus, entre otros.
El bosque presenta un estado secundario en proceso de sucesión (Erazo et al. 2014), afectado por la ganadería, entre otras actividades antrópicas que han potencializado el impacto ambiental, muestra de ello es la erosión de los suelos, escorrentía y en algunas zonas la poca cobertura vegetal. Por otro lado, se registraron 11 especies vegetales (Tabla 4). El hábito de crecimiento con mayor presencia en este bosque corresponde a los árboles 54,55 % (Erazo et al. 2014). La diferencia que se evidencia en la cantidad de volumen de hojarasca dentro y fuera del bosque corrobora la poca cobertura arbórea que posee el potrero y el espesor está relacionado con la gama de pastizales presentes en la matriz (Tabla 1).
Diversidad beta. Curvas de acumulación e índices de diversidad
Brown (1984) propone que la distribución y abundancia de cada especie está determinada por combinaciones de muchas variables físicas y bióticas para la sobrevivencia y reproducción de sus individuos. Conforme a esto se visualiza que en las curvas de acumulación de especies total y para cada bosque, de acuerdo con los estimadores de riqueza, que la eficiencia de muestreo estuvo entre 48,38 - 67,9 %, por lo que se requiere mayor intensidad de muestreo (Tabla 5). Por otro lado, los coeficientes de similitud cualitativos de Jaccard (0 - 1) obtuvo el 0,43 de similitud en cuanto a la comunidad de lepidópteros diurnos presentes entre La Pachuca y Las Martas, compartiendo treinta y cinco especies de las ochenta y un registradas. Al comparar el índice de diversidad de Shannon (H = 3,4) con el registrado en el Parque Regional El Vínculo que obtuvo H = 4,73 (Gavíria-Ortíz y Henao-Bañol 2011), se infiere una relativa alta diversidad de especies de lepidópteros. Al aplicar el índice de Jost, los valores calculados se mantienen en los dos bosques (Figs. 4A-4C).
Tabla 5. Estimadores de riqueza, índice de diversidad y diversidad beta en los fragmentos de bosque seco La Pachuca y Las Martas, Patía (Cauca, Colombia).
| Riqueza | Estimadores de riqueza | Eficiencia de muestreo | Índice de Shannon | Riqueza verdadera Jost | Coeficiente de similitud | ||||
|---|---|---|---|---|---|---|---|---|---|
| Ace | Chao1 | Ace | Chao1 | Jaccard | Sorensen | ||||
| La Pachuca | 63 | 93,1 | 99,8 | 67,7 % | 63,2 % | 3,1 | 22,9 | 0,43 | 0,60 |
| Las Martas | 53 | 89,6 | 109,8 | 59,2 % | 48,3 % | 3,2 | 24,0 | ||
| Total | 81 | 119,3 | 120,1 | 67,9 % | 67,4 % | 3,4 | 30,3 | ||

Figura 4. Curvas de acumulación de especies de lepidópteros en los fragmentos de bosque seco La Pachuca y Las Martas, Patía (Cauca, Colombia). A. Total. B. Las Martas. C. La Pachuca.
Evaluación ecológica. Los fragmentos de bosque de las Martas y La Pachuca no son ajenos a las actividades de ganadería extensiva y monocultivos llevadas a cabo por intervención humana, cabe resaltar que algunas actividades tensionantes repercuten en gran medida, como es el caso de la incineración de ganado en La Pachuca, para los pobladores es un modo de no contaminar fuentes hídricas con los cuerpos sin vida de terneros. Sin embargo, esta actividad vale la pena evaluarla exhaustivamente dado que al realizarla continuamente influye en el desarrollo sucesional y de regeneración del paisaje. De igual modo pasa con las quemas que se vieron como una actividad con efecto adverso en Las Martas, debido a que el ecosistema de bs-T por las bajas precipitaciones lo hacen más susceptible a fenómenos como éste.
La tala fue otra de las actividades que afectó directamente y se encuentra estrictamente relacionada con la disponibilidad de hábitat. En las dos zonas esta actividad se lleva a cabo con fines comerciales. Lo cual afecta la sucesión vegetal dado que no todas las especies tienen la misma tasa de crecimiento y capacidad de regeneración. A ello se suman actividades tan específicas como el reentrenamiento militar que genera contaminación auditiva y a su vez estrés en la fauna.
Finalmente, cada una de las actividades evaluadas genera de una u otra manera contaminación, como es el caso de la agricultura. En los recorridos dentro del bosque se encontraron restos de envases de plaguicidas. Durante la sequía fue evidente la acumulación de basuras que por la falta de agua no había arrastre de material en las pequeñas quebradas, indicando que no hay buenos mecanismos de recolección y manejo de estos productos a la hora de desecharse.
Conclusiones
La matriz ganadera influye en la dinámica de la comunidad de lepidópteros de los dos fragmentos La Pachuca y Las Martas por al menos dos factores: la oferta alimenticia y el área destinada para dicha actividad la cual es mayor que la que se conserva como parche de bosque, particularmente para La Pachuca. Se observó interacción entre los tres hábitats evaluados bosque, borde y matriz, ampliando el registro de especies euritopas en bosque seco. Su abundancia se corrobora con la dinámica que reportan las especies generalistas, permitiendo recolonizar este tipo de ecosistemas intervenidos.