Introducción
Las infecciones asociadas a la atención en salud (IAAS), anteriormente llamadas nosocomiales o intrahospitalarias, son adquiridas por pacientes mientras reciben algún tipo de atención médica, sin presencia de haberla adquirido anteriormente o previo a su ingreso en algún centro de salud (Serrano et al., 2014). La etiología de las IAAS es de naturaleza diversa; asociándose con causas como: el uso de dispositivos médicos por tiempos prolongados (sondas, catéteres), complicaciones postquirúrgicas, transmisión entre pacientes y trabajadores de la salud, y múltiples factores de riesgo entre los que se encuentran las transmitidas por vectores (mosquitos, moscas y otros), los cuales transmiten microorganismos presentes en ellos (Maia et al., 2009). Cada una de estas fuentes potenciales es sujeto de vigilancia y seguimiento institucional con el fin de implementar las medidas pertinentes para su control (Serrano et al., 2014).
El control realizado sobre cada aspecto relacionado con las IAAS incluye: verificación del origen intrahospitalario de la infección, monitoreo microbiológico y molecular de las áreas críticas y, por último, la implementación y seguimiento de los protocolos de limpieza, desinfección y esterilización en los servicios de la institución (Serrano et al., 2014). No obstante, es importante destacar que se hacen necesarias las vigilancias entomológicas y de pequeños animales con el fin de disminuir su tránsito y/o su permanencia en el área institucional (Pujol & Limón, 2013).
Las IAAS son consideradas un evento adverso producto de una atención en salud que de manera no intencional produce algún daño al paciente (Serrano et al., 2014). Las infecciones más frecuentes son las de tipo respiratorio, seguidas por las infecciones de vías urinarias, piel y partes blandas, tracto gastrointestinal y mucosas, las cuales llegan al paciente por contacto con superficies, alimentos, agua, aire y dispositivos médicos en la institución (Serrano et al., 2014). El desconocimiento de la asociación de las IAAS a la presencia de insectos en los contextos quirúrgicos, cuando estos entran en contacto con el paciente o con los dispositivos usados en su cuidado, puede representar un aumento en los índices de morbimortalidad, falla en el sistema de vigilancia epidemiológica y control adecuado de los vectores (López-Cerero, 2014).
El objetivo de este trabajo fue identificar, mediante una revisión de literatura, el estado actual de la evidencia científica con respecto a los insectos como potenciales vectores de microorganismos y su posible relación como factor de riesgo en la incidencia de IAAS, con el fin de profundizar en el estudio de los microbiomas presentes en los vectores que se encuentren en el área quirúrgica y los microbiomas identificados en los pacientes que desarrollan IAAS. De esta manera, divulgar información científica que permita mejorar los protocolos de vigilancia y control epidemiológico.
Materiales y métodos
Se realizó una revisión bibliográfica, de tipo observacional, descriptiva y retrospectiva en el marco de una metodología hermenéutica como estrategia para el análisis de textos. El proceso incluyó rastreo, selección, organización, sistematización y análisis de 803 publicaciones desde el año 2005 hasta el primer semestre de 2021, con información sobre vectores (insectos) que transitan en las instituciones hospitalarias y son considerados como factores de riesgo asociados a las IAAS, buscando determinar y posteriormente contextualizar los hallazgos con la relación de los microbiomas de los agentes patógenos encontrados en los vectores y su relación con IAAS.
Los criterios de inclusión que se tuvieron en cuenta fueron los siguientes: i) publicaciones que en su contenido reportan presencia de vectores en cualquier servicio del área hospitalaria; ii) publicaciones que reporten el análisis de la presencia de vectores en el área hospitalaria como fuente potencial o real de microorganismos que causan IAAS, iii) publicaciones que reportan la identificación de microorganismos causantes de IAAS por métodos microbiológicos y/o moleculares, en los vectores presentes en área hospitalaria y, iv) artículos que detallan la metodología de identificación de los agentes causantes de IAAS con rigurosidad científica.
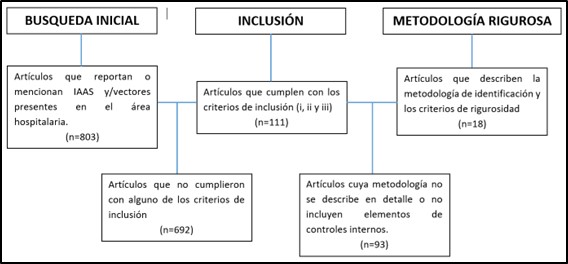
Figura 1 Diagrama CONSORT que ilustra el proceso de selección de los artículos incluidos en la revisión.
Las bases de datos electrónicas revisadas fueron: PubMed (MedLine), Elsevier, Index Medicus, LILAC’S, Embase, SciELO Colombia y Google Académico. Los descriptores usados fueron: “Infecciones Asociadas a la Atención Sanitaria”, “Factores de riesgo”, “Insectos”, “Vectores”, “Área Quirúrgica”, los cuales fueron combinados en inglés y español, mediante el uso de operadores booleanos “AND” y “OR”; permitiendo diseñar varios algoritmos para ampliar la búsqueda. Se preseleccionaron 111 documentos, los cuales se organizaron teniendo en cuenta los siguientes criterios: base de datos de origen, fecha, autores, calidad metodológica y científica. Un total de 18 estudios que cumplieron con los criterios de inclusión y descripción metodológica fueron seleccionados (Figura 1).
Resultados
Vectores de microorganismos e IAAS.
En el contexto de las ciencias biológicas, se denomina vector a un ser vivo que es portador en su superficie o que posee internamente un agente infeccioso, el cual al transmitirlo causa enfermedad en el receptor (Verwoerd, 2015). En el contexto de las IAAS, los vectores artrópodos son agentes portadores de microorganismos que podrían favorecer el desarrollo de infecciones intrahospitalarias. Se debe diferenciar entre vector mecánico y vector biológico; el primero de ellos transporta físicamente un agente infeccioso a un hospedador, pero el agente patógeno no se reproduce en este. Por el contrario, en el vector biológico el artrópodo lo transporta y es intermediario para que el patógeno complete su ciclo biológico. Se deben identificar las áreas que sirvan de reservorio en donde estos vectores pueden transmitir los agentes patógenos y así permitir su propagación (Heras & Sierra, 2016).
La aplicación de los criterios de inclusión y selección permitió seleccionar 18 artículos que reportan la presencia de microorganismos patógenos en insectos, arañas y otro tipo de animales como los roedores presentes en instituciones hospitalarias (Avendaño et al., 2013; Castillo & Martínez, 2011; Olaya-Másmela et al., 2005; Rodríguez et al., 2016). Los microorganismos encontrados en ellos corresponden a especies bacterianas y hongos, los cuales han sido aislados y caracterizados por estudios microbiológicos (Fonseca et al., 2010; Maia et al., 2009; Máximo et al., 2014; Oliveira et al., 2014; Pelli et al., 2007).
No obstante, las técnicas microbiológicas no permiten el crecimiento de todos los microorganismos que puedan estar presentes en un área determinada, haciendo difícil una caracterización amplia de las especies integrantes de la microbiota (Avendaño et al., 2013) y, por lo tanto, un abordaje más efectivo para controlar el desarrollo de IAAS. Las nuevas tecnologías de secuenciación masiva de ADN, como MALDI-TOF, de los genes RecN y ARN16S, brindan identificaciones más precisas y permiten caracterizar la distribución de genes compartidos entre las especies presentes en la microbiota de un ambiente determinado (Werinder et al., 2021). Estos estudios se realizan con el fin de realizar trazabilidad desde el vector, hasta el paciente con IAAS, sin embargo, no hay suficientes estudios que verifiquen la ruta (Oliva et al., 2010).
Identificación de microorganismos asociados a IAAS.
En Brasil se han publicado varios estudios que realizan seguimiento a vectores intrahospitalarios. En el estudio más completo se aislaron 35 cepas de Staphylococcus aureus al analizar muestras de 91 insectos en dos hospitales públicos. El análisis incluyó pruebas microbiológicas para caracterizar las cepas, pruebas moleculares para evaluar la presencia de genes de resistencia a antibióticos específicos y actividad antimicrobiana de productos de desinfección sobre las cepas aisladas. Este estudio ilustra una ruta microbiológica, molecular y química para caracterizar la presencia de agentes potenciales de IAAS (Oliveira et al., 2014). Este tipo de caracterización permite hacer las asociaciones correspondientes ante la aparición de infecciones en los diferentes servicios y en el área quirúrgica, así como implementar los manejos adecuados en caso de presentarse la infección.
Otros estudios, también en Brasil, establecen que las hormigas son un vector importante de agentes causantes de IAAS, por lo tanto, se constituían en un factor de riesgo. En general, destacaron que las bacterias aisladas de ellas son oportunistas en su mayoría, tanto gram negativas como gram positivas; sin embargo, tienen una alta probabilidad de poseer genes de resistencia a antibióticos, lo que dificultaría su manejo al infectar un paciente (Maia et al., 2009; Máximo et al., 2014). Aunque la presencia de las hormigas en las instituciones hospitalarias está asociada a áreas con disponibilidad de alimentos (Fonseca et al., 2010), la institución debe implementar protocolos de limpieza que permitan controlar la presencia y propagación de vectores en sus instalaciones y protocolos de desinfección que minimicen la incidencia de IAAS, lo cual está reglamentado por políticas nacionales en salud pública de cada país y por la Organización Panamericana de la Salud (Acosta-Gnass, 2011).
El monitoreo de insectos voladores en otras instituciones permitió aislar una bacteria del género Nocardia la cual no había sido descrita previamente sobre vectores, únicamente en el aire, la cual está asociada a infecciones respiratorias (Pelli et al., 2007). En estudios en el tracto intestinal y la superficie de cucarachas usando la técnica MALDI-TOF y secuenciación de ARN16S se identificaron 183 especies de bacterias (Mehainaoui et al., 2021).
En otro estudio se analizaron 14 especies distintas de hormigas en hospitales donde identificaron 41 especies diferentes de bacterias en ellas y 18 pacientes (Lima et al., 2013). En otro estudio se analizaron insectos voladores que no pican logrando sólo identificar las bacterias por su morfología y coloración de gram (Kappel et al., 2013). Un estudio de la cucaracha Blatella germanica L. (Blattodea: Blattellidae) presente en un hospital, reporta la comparación de las especies de bacterias presentes en ella, determinadas por crecimiento en medios de cultivos y por coloración de gram; las especies gram negativas identificadas se compararon con los reportes de infecciones nosocomiales en el mismo período del estudio, coincidiendo en 11 especies de las 18 reportadas en los casos (Oliva et al., 2010).
En una investigación en Teherán, Irán, se reportó el estudio de la prevalencia de agentes infecciosos sobre tres tipos de cucarachas, aislando 19 especies diferentes de bacterias e identificándolos microbiológicamente (Zarchi & Vatani, 2009). Otro estudio comparó la población de hongos, bacterias y parásitos sobre y dentro de cucarachas de sitios residenciales como grupo control en instituciones hospitalarias; la identificación de especies se realizó por técnicas microbiológicas (Salehzadeh et al., 2007).
Los estudios publicados abarcan países de diferentes partes del mundo, siendo el continente menos representado el africano, destacándose el sur de Asia y Brasil en Suramérica como las zonas con más reportes al respecto; éstos se han realizado en instituciones especializadas, generales o de formación en medicina; siendo la única diferencia observable la naturaleza endémica de algunos de los vectores en los diferentes reportes, comprendiendo un período disperso de 30 años, con obvias diferencias entre las técnicas de identificación utilizadas (Beatson, 1972; Chadee et al., 1990; da Costa et al., 2006; Daniel et al., 1992; Faulde et al., 2001; Fotedar et al., 1989, 1991a, b, 1992a, b; Lemos et al., 2006; Rady et al., 1992; Pai et al., 2003, 2004; Rahuma et al., 2005; Rodovalho et al., 2007; Stypułkowska-Misiurewicz et al., 2006).
En instituciones de IV nivel, en Colombia, se ha reportado la presencia de hormigas de los géneros Monomorium, Paratrechina, Tapinoma y Tetramorium, como vectores de hongos y bacterias asociados con enfermedades nosocomiales (Olaya-Másmela et al., 2005). Entre los géneros de hongos se encontraron: Acremonium, Aspergillus, Candida, Cladosporium, Exophiala, Gliocladium, Paecilomyces, Penicillium, y Scytalidium (Castillo & Martínez, 2011); para el caso de las bacterias se aislaron los siguientes géneros: Staphylococcus (incluyendo Staphylococcus coagulasa negativo), Bacillus, Enterobacter, Escherichia, y Micrococcus (Rodríguez et al., 2016). Además de esto, se ha logrado determinar la presencia de algunos de estos agentes infecciosos en superficies de las instituciones (Castillo & Martínez, 2011; Olaya-Másmela et al., 2005; Rodríguez et al., 2016).
En otros estudios se reporta en áreas quirúrgicas de las IPS la presencia de vectores, pertenecientes a dos clases (Arachnida e Insecta) y distribuidos en cinco órdenes y seis familias de la siguiente forma: Arachnida: Opilionida; Insecta: Psocoptera, Hymenoptera (Formicidae), Diptera (Culicidae, Muscidae, Sarcophagidae, Tipulidae), y Coleoptera (Carabidae). En estos organismos se aislaron las siguientes especies de bacterias: Staphylococcus sp. coagulasa negativa, Bacillus sp., Burkholderia cepacia y Klebsiella pneumoniae (Avendaño et al., 2013). Lo que demuestra la presencia de bacterias en el cuerpo de artrópodos (arácnidos e insectos), en áreas quirúrgicas de instituciones hospitalarias.
La implementación de los estudios moleculares ha permitido establecer que los microorganismos asociados a IAAS poseen genes de resistencia compartidos, los cuales necesitan monitorearse, como lo demuestran dos estudios realizados en Colombia (Cadena-Zamudio et al., 2016; Villalobos et al., 2014). En un estudio de 2014 se monitoreó la distribución del gen BLAkpc, el cual codifica para enzimas que degradan principios activos de los medicamentos, y al estar presente en un plásmido, es compartido entre diferentes especies que constituyen una misma microbiota (Pacheco et al., 2014). Lograr estos resultados sólo es posible gracias al seguimiento de los fenotipos resistentes de las diferentes bacterias aisladas en los servicios hospitalarios (Villalobos et al., 2011). Este seguimiento permite establecer protocolos de manejo y anticipar la evolución de la resistencia, como se hizo en un estudio sobre Acinetobacter baumanni, una bacteria oportunista que desarrolló resistencia y afectó piel y huesos de pacientes en una unidad hospitalaria (Vanegas et al., 2015).
Asociación entre IAAS e infecciones en el área quirúrgica.
Aunque pueden ser sub registradas, las IAAS del sitio quirúrgico, son de gran relevancia porque pueden contribuir al aumento de las tasas de mortalidad de pacientes. Los protocolos de vigilancia han permitido determinar siempre un origen bacteriano y las especies han sido determinadas por pruebas microbiológicas (Martínez et al., 2014).
Algunos estudios han determinado que existen factores de riesgo de aparición de infección del sitio quirúrgico; estableciendo entre estos: factores propios del paciente (endógenos), factores externos al paciente e inherentes a las actividades prequirúrgicas y postquirúrgicas dentro de la institución (exógenos), y otros factores que incluyen el ambiente hospitalario y sus dinámicas de rotación y circulación (Rael & López, 2016).
Es importante establecer que el origen o reservorio dentro del área quirúrgica de la fuente de infección, no siempre es determinado, dadas las condiciones propias del servicio quirúrgico. Los protocolos establecidos determinan aislar el agente e identificarlo, y aplicar un protocolo de limpieza al quirófano o las áreas donde se realizó la intervención quirúrgica al paciente afectado y por donde éste transitó durante su estancia hospitalaria (Ortíz et al., 2008). Sin embargo, no se tiene en cuenta la vigilancia microbiológica de los vectores presentes en la institución, limitándose al uso de insecticidas o trampas para capturarlos. Las enfermedades causadas por vectores fuera de instituciones hospitalarias pueden ser responsables de hasta un millón de muertes por año (Padilla et al., 2017); por tanto, caracterizar la microbiota de vectores intrahospitalarios podría contribuir a una mejor comprensión del fenómeno de aparición de multirresistencia a antibióticos, e implementar mejores protocolos de vigilancia.
Discusión
Revisadas las bases de datos relacionadas, son pocos los estudios al respecto, y los que se han desarrollado, en su mayoría comprenden la identificación de los agentes patógenos presentes en los vectores que transitan en las instituciones hospitalarias, lo que sugiere la necesidad de profundizar en el tema, para determinar la relación entre los microbiomas de los agentes encontrados en los vectores con IAAS delimitadas al área quirúrgica y considerando que la frecuencia de las IAAS varía según nivel de atención, grado de complejidad de la Institución hospitalaria, el servicio o área evaluado, entre otros aspectos. Respecto al servicio, los quirúrgicos tienen tasas de IAAS casi tres veces mayores que el resto de las áreas hospitalarias; siendo superados por las unidades de cuidados intensivos (Rivera, 2018).
Las IAAS son consideradas un evento adverso producto de una atención en salud que de manera no intencional produce algún daño al paciente; según datos estadísticos, éstas representan una fuente importante de morbilidad y mortalidad, por lo que actualmente constituyen un tema prioritario en investigación y prevención en salud (Rivera, 2018; Rutala & Weber, 2013a, b). De allí la necesidad de profundizar en la asociación de las IAAS y la presencia de insectos en el área quirúrgica; ya que estos representan un potencial factor de riesgo para la salud del paciente, debido a que están relacionados en la trasmisión de microorganismos patógenos al hombre, e incluso es importante considerar la posible relación entre la microbiota aislada en los pacientes y la encontrada en los insectos.
La falta de estudios que asocien las IAAS con la presencia de insectos en el área quirúrgica podría estar generando vacíos en la identificación y el manejo de los agentes causales de estas. Diferentes aspectos deben ser tenidos en cuenta en este escenario como: el contacto del vector con pacientes, superficies y dispositivos médicos utilizados en el cuidado de éste, los cuales podrían pueden representar indicadores epidemiológicos que no se han cuantificado, y que favorecen así el subregistro (Shaw & Catteruccia, 2019).
Es importante tener presente que la cadena de transmisión desde el vector hasta el paciente puede ser tan corta como la interacción directa, y tan larga como la mediación de elementos físicos y humanos presentes en el servicio quirúrgico (Kärki et al., 2019). Estos espacios cuentan con protocolos de limpieza y desinfección de superficies y del personal, y manejo de soluciones químicas según sea lo apropiado para reducir su contribución potencial a la incidencia de infecciones asociadas a la atención de la salud. Sin embargo, no están exentos a la presencia de insectos que generen IAAS (Chauveaux, 2015; Rosales & Cubas, 2020).
La limpieza y desinfección de áreas y dispositivos médicos es un proceso complejo cuya función fundamental es romper los mecanismos de transmisión con el fin de reducir el riesgo de contaminación cruzada y de IAAS. Es importante evaluar la efectividad de los métodos de limpieza y desinfección, de tal manera que se verifique la disminución de microorganismos que puedan estar presentes; lo que representa un desafío en la vigilancia epidemiológica, ya que no hay una estandarización de protocolos debido a la diversidad de productos en el mercado y a la falta de estudios que comparen entre sí a estos productos (Cabral & Rodrigues, 2019; Chauveaux. 2015).
Un elemento clave en este proceso es el uso optimizado y adecuado de los agentes o soluciones químicas, ya que muchos microorganismos producen biopelículas y conglomerados que generan una barrera contra la desinfección, por lo que los preparados deben saturar y actuar por un tiempo para lograr la desinfección (Acosta-Gnass, 2011). Aunque los fabricantes ofrecen recomendaciones para el uso adecuado de sus productos, la mayoría de los estudios evidencian que estos no informan aspectos como la minuciosidad de la limpieza, la adherencia del desinfectante, tiempo de contacto con superficies, tipos de bacterias o virus, entre otros; por lo que esta información permanece en gran parte desconocida en la práctica diaria, afectando los resultados de la vigilancia epidemiológica (Kotb et al., 2020).
Por otra parte, las especies bacterianas pueden permanecer en hospitales y clínicas por mucho tiempo en las superficies húmedas y secas, en conductos de aire y agua, en la indumentaria propia de los profesionales de la salud, en los equipos diagnósticos o instrumental de revisión, y sobre otras especies animales que infestan o transitan por las instalaciones (Blake et al., 2021). Por lo tanto, las instituciones de salud están obligadas a desarrollar programas de vigilancia y control.
Las publicaciones sobre casos de IAAS indican que este fenómeno es global; siendo los mayores reportes de Asia (Alfarawi et al., 2019; Bai et al., 2021; Brinkmann et al., 2019; Goldblatt et al., 2007; Salehzadeh et al., 2007; Stoesser et al., 2014). Sin embargo, se presentan también comparaciones del fenómeno y reportes de Europa (Boyer et al., 2020; Franck et al., 2020; Wall et al., 2009), Norteamérica (Goldblatt et al., 2007) y Suramérica (da Costa et al., 2006), entre otros. Se destaca que sus metodologías de determinación y aislamiento varían desde estudios microbiológicos únicamente, estudios moleculares y en algunos casos combinación de estos. Es importante enfatizar en este punto que esta combinación de pruebas microbiológicas y moleculares parece ser la más completa. Los estudios microbiológicos permiten hacer pruebas de resistencia a antibióticos de las cepas aisladas; mientras que las pruebas moleculares brindan caracterización de especies y cepas, genes de resistencia y su evolución y, por último, aislar y caracterizar los plásmidos con la información de resistencia (Blake et al., 2021). En este sentido, las tecnologías de secuenciación de siguiente generación son las herramientas de elección.
La mayoría de los estudios revisados, realizados en diferentes momentos utilizaron pruebas microbiológicas, las cuales permiten sólo el aislamiento y crecimiento de un porcentaje cercano al 1 % de los microorganismos. Es importante que los estudios actuales utilicen técnicas moleculares que permiten determinar una mayor cantidad de especies. Para ello, se debe aislar la mayor cantidad de material genético de la superficie corporal de los vectores, lo que permitirá obtener los diferentes juegos de ADN que serán secuenciados con técnicas de Secuenciación de Siguiente Generación (NGS). Se podrá determinar así tanto las especies como caracterizar el metagenoma presente (Cadena-Zamudio et al., 2016). Caracterizar el metagenoma ayuda a determinar patrones de tratamiento; ya que, es creciente el número de bacterias intrahospitalarias multirresistentes a antibióticos (Villalobos et al., 2014).
Las herramientas moleculares serán la clave que permita relacionar directamente la composición del microbioma de los vectores presentes en el espacio hospitalario y los casos de IAAS que se presenten, pues sólo así se podrá hacer un rastreo efectivo de la o las fuentes de infecciones (Werinder et al., 2021). Esto será sustancial en las áreas quirúrgicas, pues en ellas se aplican los protocolos de limpieza y desinfección más rigurosos por su condición de ser consideradas áreas restringidas dentro de instituciones hospitalarias y donde los insectos vectores son menos frecuentes, por lo que esta correlación tendría significancia robusta, para la toma de decisiones. Por lo tanto, la implementación rutinaria de esta vigilancia epidemiológica es una necesidad urgente (Kotb et al., 2020).
La incidencia de las IAAS tiende a mantenerse constante en las instituciones de salud. En su esfuerzo por reducir las cargas biológicas, disminuir los riesgos de transmisión de agentes patógenos al paciente y mejorar las técnicas utilizadas en procesos de limpieza y desinfección entre otros, deben mejorar sus protocolos de vigilancia epidemiológica incluyendo una ruta que implemente la valoración microbiológica, molecular y química. Igualmente, debe existir una corresponsabilidad entre los entes gubernamentales de vigilancia de vectores y las instituciones de salud (Rafa et al., 2022).
Para lograr este mejoramiento es necesario el desarrollo de estudios que permitan exponer la problemática aquí descrita para caracterizar el fenómeno de la incidencia de infecciones intrahospitalarias asociadas a vectores en el área quirúrgica de las Instituciones prestadoras de servicios de salud.
Conclusiones
Las IAAS pueden estar presentes en las instituciones de salud debido a que los microorganismos que las causan se mantienen en vectores reservorios. En el interior de éstos, las bacterias pueden intercambiar información genética que los favorezca contra el tratamiento con antibióticos, o genes de adaptabilidad a soluciones desinfectantes.
Los eventos que pueden conducir a la caracterización del fenómeno en cualquier espacio hospitalario dependerán de los controles establecidos y de los protocolos de detección e identificación de los microorganismos en los espacios y vectores presentes. Para ello, son necesarios las técnicas moleculares de identificación y los estudios metagenómicos. De esta manera, se puede dilucidar una probable ruta de infección para la cual se pueden diseñar protocolos de control.
Por último, no hay suficientes reportes de vectores en el área quirúrgica, de manera que se necesitan más estudios que den cuenta de la aparición de infecciones en el sitio quirúrgico, posterior a un procedimiento quirúrgico, de algunos pacientes, y que estos eventos sean observados como IAAS, pudiéndose asociar con la presencia de vectores en estas áreas.















