Los seres humanos han desarrollado a lo largo de los años diferentes procesos industriales que van de la mano con el consumo de agua, estas actividades hoy en día representan uno de los problemas ambientales de mayor importancia en el mundo, debido a la notable reducción del recurso hídrico y a los problemas en la salud pública que acarrea su descontrolado uso, poco aprovechamiento y mala disposición final [1].
En la actualidad se han producido más de 10,000 clases de colorantes, utilizados principalmente en la industria del teñido de prendas, objetos y flores [2], con la problemática de que muchas de las moléculas presentes en estos colorantes son resistentes a la acción de la luz, temperatura y a la degradación microbiana, convirtiéndolos en contaminantes altamente persistentes y perjudiciales para el ambiente [3]. Ahora bien, una gran proporción de los colorantes empleados en el teñido de tejidos, no son directamente tóxicos para los organismos vivos; sin embargo, la fuerte coloración que imparten a los medios de descarga pueden llegar a suprimir los procesos fotosintéticos en los cuerpos de agua e implica un alto riesgo a la salud humana y al ecosistema debido a que algunos de estos colorantes o sus subproductos son altamente tóxicos, mutagénicos o carcinogénicos, haciendo necesario que su presencia sea controlada [4]. La industria textil es una de las principales consumidoras de colorantes sintéticos a nivel mundial [5] y es considerada una de las industrias más contaminantes, ya que genera grandes cantidades de residuos líquidos y a su vez, emplea elevados volúmenes de agua, energía y reactivos químicos para su funcionamiento diario [7]. Por otro lado, existen otras actividades económicas asociadas al uso de colorantes sintéticos, como son los productores de cultivos de flores, los cuales emplean colorantes para teñir las flores, lo que las hace más atractivas para el consumidor [6]. En la industria de la floricultura se embellecen a las flores empleando la tinción por absorción, donde los colorantes deben ser valorados respecto a la afinidad que ellos tengan con los tejidos de la flor y deben ser altamente solubles en agua, de esta manera es importante evaluar las características principales de pH, solubilidad e higroscopicidad previo a su uso [8].
Para lograr el teñido de las flores, éstas son introducidas en una solución acuosa que contiene el colorante, lo que da lugar a un residuo líquido, el cual no puede ser vertido al recurso hídrico sin un previo tratamiento. Por ello, para mitigar la problemática ambiental, es conveniente acudir a sistemas de tratamientos que logren reducir el grado de contaminación de forma eficiente, económica y en lo posible mediante el uso de procesos biológicos, ya que estos permiten tratar el agua sin la adición de agentes químicos, convirtiéndolos en muchos casos en tecnologías sostenibles para el tratamiento de las aguas [9]. Los procesos biológicos de depuración de las aguas residuales utilizan reacciones asociadas con los microorganismos, donde la materia orgánica y los compuestos de nitrógeno y fosforo son eliminados del agua residual por acción de las bacterias presentes, las cuales emplean la materia orgánica con donante de electrones, tanto para producir material celular como para obtener la energía necesaria para su respiración [10], y de esta manera, transforman la materia orgánica a formas inorgánicas las cuales son más inocuas para el medio ambiente [11].
La experiencia ha mostrado que la implementación de los sistemas SBR (Sequencing Batch Reactorpor sus siglas en inglés y Reactor Secuencial en Discontinuo - en español) para el tratamiento de las aguas residuales contaminadas con colorantes, ha dejado resultados confiables en la remoción de estos, facilitando su manipulación, debido a que los SBR son sistemas automatizados, en los cuales se logra una gran flexibilidad ante fluctuaciones de caudal y concentraciones del afluente [12, 13]. Los sistemas SBR son conocidos como sistemas de tratamiento de lodos activados en discontinuo, en el cual el agua residual es adicionada en un solo reactor que trabaja por cargas repitiendo un ciclo o secuencia a lo largo del tiempo, cada una con un periodo de tiempo definido [14, 15]. Las fases secuenciales convencionales de un reactor SBR son: llenado; etapa en la que se suelen combinar fases aeróbicas (en presencia de oxigeno), anóxicas (con agitación) o estáticas (sin aireación y sin agitación), según las características de las aguas residuales a tratar. La duración del llenado suele ser un 25% del total del ciclo y en esta fase se producen procesos importantes para la eliminación biológica de nutrientes y también se elimina parte de la materia orgánica biodegradable que entra en el afluente [16, 17], reacción; esta es una etapa aireada y con buena mezcla, en la que se produce la eliminación biológica de la materia orgánica biodegradable. La duración de este periodo suele ser de un 35% del ciclo [18], sedimentación; en esta etapa se separa el lodo del agua tratada [19], vaciado; se descarga el efluente hasta dejar el volumen inicial en el reactor [20] e inactividad; normalmente se aprovecha este tiempo de espera para realizar la purga y así mantener la edad de lodos del reactor. Las fases se combinan de diferentes formas dependiendo del objetivo de calidad que se requiere en el agua efluente, de esta manera, este proceso es empleado para el tratamiento de aguas residuales debido a sus óptimos resultados registrados en la práctica [17].
En este estudio se evaluó la eficiencia de un reactor SBR sobre la remoción de la materia orgánica, empleando un agua residual sintética contaminada con dos tipos de colorantes específicos provenientes de la industria del teñido de flores, a partir de análisis fisicoquímicos y de la biomasa presente en el reactor.
Materiales y métodos
Reactor SBR
Los experimentos fueron llevados a cabo en un reactor SBR (Figura 1), con un volumen útil de 12 L y una relación altura/diámetro de 4,7. El reactor tenía una (1) válvula de entrada del afluente, dos (2) válvulas situadas a lo largo del reactor para permitir la toma de muestras, una (1) válvula de purga en el fondo del reactor y una (1) válvula de salida del efluente. La aireación era generada mediante tres (3) bombas de aire cada una con una capacidad de oxigenación 1200 cc/ min y dos (2) difusores de burbuja fina, para un total de seis (6) difusores, los cuales mantenían la concentración de oxigeno disuelto en el reactor entre 2-4 mg/L. La agitación era realizada con un agitador de varilla (Heidolph) a 40 RPM. El afluente ingresaba al reactor mediante una bomba peristáltica (Masterflex) con una caudal de 50 ml/ min y el efluente era descargado mediante una electroválvula que permitía la salida automática de este. La edad de los lodos empleada fue 15 d.
Todas las partes descritas se encontraban conectadas a un controlador lógico programable (PLC), mediante el cual se programaron tanto las etapas como los tiempos para el funcionamiento del reactor, de esta manera, la fase llenado se realizó de forma estática durante 2 h, la etapa de reacción se realizó durante 8 h (4 h de aireación y 4 h de mezcla) y finalmente la sedimentación se llevó a cabo durante 2 h, para un total de 12 h por ciclo y 2 ciclos al día. Estas condiciones de operación promueven no solo la remoción material carbonáceo, sino también de material nitrogenaceo, debido a que favorece la formación de etapas combinadas aerobias y anóxicas dentro del mismo sistema.
Caracterización de la biomasa
El reactor fue inoculado con lodo floculento proveniente de un reactor SBR empleado en el tratamiento de las aguas residuales domésticas en el municipio de San Jerónimo, Antioquia. La caracterización inicial del lodo arrojó una concentración de sólidos suspendidos totales (SST) de 3240 mg/L y 2576 mg/L de sólidos suspendidos volátiles (SSV), donde los SSV fueron aproximadamente el 79% de los SST, indicando un alto porcentaje de material orgánico presente. El índice volumétrico de los lodos (IVL) fue 21,45 ml/g, indicando un lodo con buena sedimentabilidad (IVL < 100 ml/g).
Preparación del agua sintética
Se prepararon 20 L diarios de agua sintética, compuesta por el colorante azo (C1 o C2 según el diseño de experimento), 10 ml de macronutrientes y 10 ml de micronutrientes. La preparación de los macronutrientes fue: 6 g/L NH4Cl; 8 g/L KH2PO4; 16 g/L K2HPO4. La preparación de los micronutrientes fue: 0,75 g/L MgSO4·7H2O; 0,05 g/L FeSO4·7H2O; 0,05 g/L ZnSO4; 0,1g/L CaCl2·2H2O [15]. Los dos colorantes azo empleados, fueron suministrados por la empresa Cultivos de San Nicolás, dedicada al teñido de flores, ubicada en el municipio de Rionegro, Antioquia. El colorante azo C1 tenía una DQO de 1200 mg/L, un pH de 6,58, el NH4+ de 2,30 mg/L, el fosforo total menor al límite de detección (< 0,1 mg P/L) y el color era naranjado. El colorante azo C2 tenía una DQO de 1220 mg/L, un pH de 6.8, el NH4+ de 3,14 mg/L, el fosforo total menor al límite de detección (< 0,1 mg P/L) y el color era púrpura.
Diseño de experimentos con los colorantes
El arranque y estabilización del reactor se realizó durante 2 semanas, empleando como sustrato la dextrosa, con el fin de permitir la adaptación de los microorganismos a sus nuevas condiciones de funcionamiento. Posteriormente, los ensayos consistieron en el análisis de dos (2) cargas diferentes para cada colorante (C1 y C2). El diseño de experimentos que se llevó a cabo ocurrió en dos fases; la fase 1 en la que se adicionó el colorante C1 con una carga orgánica volumétrica de 3,0 g DQO/L.d y 7,0 g DQO/L.d (Cada carga se evaluó durante aproximadamente 30 días). Posterior a esto, se realizó un tiempo de espera de una semana donde se alimentaba solo con dextrosa para evitar dejar trazas de C1 en el reactor. En la fase 2 se adicionó el colorante C2 empleando las mismas cargas previamente evaluadas para C1.
Análisis fisicoquímicos
Para el análisis de los parámetros in situ se utilizó un equipo multiparamétrico HQ40d para el seguimiento del oxígeno disuelto dentro del reactor y un pHmetro WTW pH 7110 para la lectura del pH. Adicionalmente, se analizaron los parámetros fisicoquímicos de Demanda Química de Oxígeno (DQO), Nitrógeno Amoniacal (NH4+) y Fósforo total en el afluente y efluente del reactor y Sólidos Suspendidos Totales (SST), Sólidos Suspendidos Volátiles (SSV) en la biomasa, siguiendo los criterios analíticos del Estándar Métodos [21]. Para la determinación del Carbono Orgánico Disuelto (COT) se empleó el método de combustión a alta temperatura, filtrando previamente la muestra a analizar a través de un filtro de membrana de Nylon de 0,45 µm en viales de 40 mL previamente muflados a una temperatura aproximada de 550°C durante al menos una hora, luego cada uno de los viales fueron preservados a pH < 2 utilizando ácido fosfórico H3PO4 , para ser llevados a su posterior lectura en el analizador de carbono orgánico total Apollo 9000.
En el caso de la biomasa contenida en el reactor, se hicieron también observaciones del lodo aerobio empleando un microscopio Axioplan Universal Zeiss para epifluorescencia y luz transmitida con el fin de determinar el estado de los lodos, además, se calculó el Índice Volumétrico de Lodos (IVL) para evaluar la sedimentabilidad de la biomasa que se formaba en el reactor (Rodriguez y Peñuela, 2017). Todos los análisis fueron realizados en el laboratorio del grupo Diagnostico y Control de la Contaminación (GDCON), laboratorio acreditado para el análisis de aguas por el IDEAM bajo la norma NTC-ISO/IEC 17025, Resolución 1665 del 12 de julio de 2011.
Análisis Estadísticos
Para observar la variación en el tiempo de los diferentes puntos de muestreo en las plantas de tratamiento, se hizo un análisis exploratorio de los datos, gráficas de cajas y bigotes y correlaciones entre las variables estudiadas. Los resultados se representan como el promedio ± desviación estándar. El análisis estadístico fue realizado empleando el software Statgraphics plus 5.1.
Resultados y discusión
Análisis de eficiencias
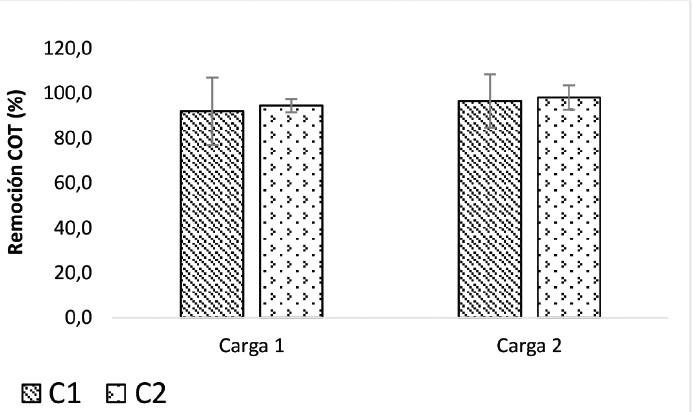
La Figura 2 muestra los resultados de las eficiencias obtenidas con los colorantes C1 y C2, para cada una de las cargas aplicadas. Con la carga 1 (3,0 g DQO/L.d), las eficiencias fueron menores con ambos colorantes comparado con las eficiencias obtenidas empleando la carga 2 (7,0 g DQO/L.d). Los valores promedio fueron 92,02% (C1) y 94,60% (C2) con la carga 1 y 96,69% (C1) y 98,30% (C2) con la carga 2. Estas altas eficiencias encontradas indican que los reactores SBR son sistemas adecuados para el tratamiento de este tipo de aguas, ya que todas las eficiencias fueron superiores al 90% independientemente de la carga aplicada y, por otro lado, comparando las cargas, se evidenció que con la carga 2 es posible potenciar las reacciones metabólicas realizadas por los microorganismos y que dicha carga, más que inhibir los procesos, funciona como fuente de energía para llevar a cabo los procesos metabólicos de catabolismo y anabolismo; en este sentido, Cobos y González [22] definieron que algunos microorganismos son capaces de crecer usando los colorantes azo como única fuente de carbono, donde, estos realizan el rompimiento del enlace azo y utilizan las aminas formadas como fuente de carbono y energía para su crecimiento, adicionalmente, Coughlin et al. [23] sugirieron en su estudio que, los microorganismos adaptados a este tipo de sustrato (Colorantes azo), pueden sintetizar azoreductasas, las cuales se encargan de romper los enlaces azo en presencia de oxígeno molecular, siendo esta una de las vías de degradación de estos colorantes.
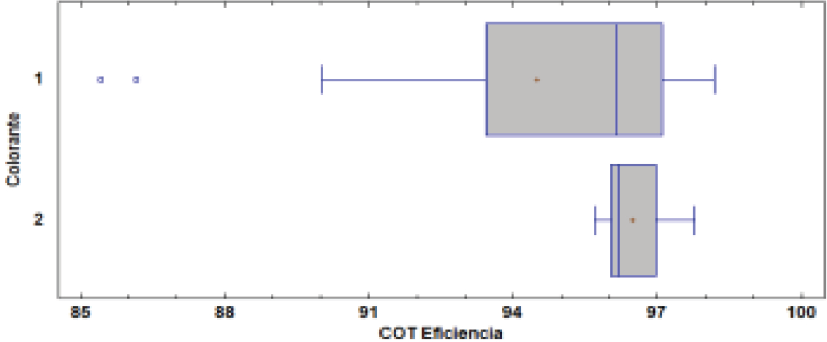
Comparando el comportamiento de los colorantes C1 y C2 (Figura 3), se encuentra que las mayores remociones de COT ocurrieron con el colorante C2, con un promedio de 96,45%, frente a 94,31% para C1, estos resultados permiten establecer que la composición del colorante C1 podría contener agentes químicos inhibitorios de los procesos biológicos, lo que podría explicar, la ligera diferencia de remoción entre ambos colorantes. Por otro lado, para C1, se encontraron algunos valores atípicos (85,21% y 86,43%) y una desviación de los datos mucho mayor, comparado con la desviación para C2, indicando que el reactor operado con C1 pudo sufrir importantes variaciones, lo que sustenta la hipótesis de un compuesto inhibitorio en su composición. Se tiene también, que para C1, la mayoría de los valores estaban por debajo de la media, contrario a C2, donde la mayoría de los valores estaban por encima de ésta. Estadísticamente, la mediana para ambos colorantes tuvo un comportamiento igual, independiente de las condiciones de operación del reactor y el tipo de colorante usado.
La Tabla 1 presenta el análisis estadístico para los porcentajes de remoción representados en términos de COT, para los dos colorantes evaluados con sus respectivas cargas orgánicas. La varianza (σ2) de C2 fue 0,545, indicando un comportamiento más eficiente de remoción del COT, en comparación al colorante C1, donde la varianza fue 15,674. Esta afirmación se corrobora con la desviación estándar, obteniéndose nuevamente un menor valor para C2 (σ = 0,738), comparado con C1 (σ = 3,959), lo que indica que tiene un comportamiento más homogéneo respecto a la mediana que el que describe el colorante C1. Los valores que se muestran del rango para los dos tipos de colorantes permiten analizar la dispersión de sus datos, donde la mayor dispersión se ocurrió para el colorante C1, con un rango de 12,770, en comparación con el colorante C2 donde el rango fue mucho menor (2,082).
En la Figura 4 se hace un análisis del comportamiento general del sistema SBR, en ésta se observa que hay un sesgo significativo desplazado hacia la izquierda, queriendo decir con esto, que gran parte de los datos están por debajo del valor de la mediana de 96,172%, por lo tanto, los valores obtenidos para el experimento en general, tales como: la varianza, la desviación estándar y el rango, permiten clasificar la eficiencia del reactor en términos de remoción del COT como un tratamiento eficiente en cuanto a remoción de materia orgánica. Dado que el p-valor es menor a 0,05, la hipótesis nula (comportamiento igual para ambos colorantes) se acepta, teniéndose entonces, que el reactor SBR es capaz de remover la materia orgánica generada a partir del agua residual sintética tanto para el colorante C1 como para el colorante C2. Autores como Sathian et al. [24], encontraron eficiencias del orden de 79,4% para la remoción de materia orgánica en un reactor SBR con ciclos de 24 horas compuestos por llenado, reacción, sedimentación y espera, empleando aguas residuales de una industria de colorantes, por otro lado, Ong et al. [25] evaluaron la eficiencia en un reactor SBR para la remoción materia orgánica en aguas residuales con el colorante Naranja II, con eficiencias promedio del 80%. Finalmente, Khosravi et al. [26], obtuvieron eficiencias del orden de 98% en un reactor SBR para la remoción de materia orgánica en aguas residuales de una empresa textil con el colorante Ftalocianina, lo anterior demuestra la alta eficacia que tienen los reactores SBR en la remoción de materia orgánica en presencia de colorantes.
En promedio la relación C:N:P para C1 fue 100:2.73:0.64 y 100:3.96:0.78 para las cargas 1 y 2, respectivamente, y para C2 de 100:4.13:0.74 para la carga 1 y 100:5.10:0.84 para la carga 2. En los reactores aerobios la relación óptima se ha establecido en valores de 100:5:1 [27], siendo este el balance ideal, con el cual los microorganismos adquieren los macronutrientes necesarios para incorporar a la célula y realizan el proceso de degradación de la materia orgánica de forma eficiente. En este sentido, al emplear el colorante C1, el balance tanto con la carga 1 como 2 fue menor al teórico, mientras que con C2 el balance fue más elevado con valores más cercanos a la teoría, lo que sustenta las mayores eficiencias alcanzadas con ese colorante. Es importante destacar que los colorantes azo se caracterizan por tener en su estructura el grupo azo -N=N- como cromóforo asociado a grupos auxocromos (-NH3 , -COOH, -OH, -NHR, -SO3Na) [22], por esta razón, es importante la determinación de los nutrientes y en especial del nitrógeno, el cual hace parte de la estructura de estos colorantes.
Análisis de la biomasa
Se encontraron concentraciones promedio de SST con el colorante C1, del orden de 1770 mg/L y 1856 mg/L para las cargas 1 y 2, respectivamente, y de SSV de 1467 mg/L para la carga 1 y 1501 mg/L para la carga 2 (Figura 5a). En cuanto al colorante C2, las concentraciones promedio de SST fueron 1898 mg/L y 1932 mg/L para las cargas 1 y 2, respectivamente, y 1605 mg/L y 1732 mg/L para los SSV con las cargas 1 y 2, respectivamente (Figura 5b). Estos resultados demuestran que la población de microorganismos fue menor cuando se empleó el colorante C1 en el reactor SBR y esta aumentó, cuando se empleó el colorante C2, resultados acordes con lo encontrado en los porcentajes de remoción del COT y que evidencian que el colorante C1 constituye un limitante en el crecimiento de los microorganismos, mientras que el colorante C2 es incorporado en la célula fácilmente por los microorganismos, lo que permite acelerar los procesos metabólicos de catabolismo y anabolismo para el crecimiento celular.
La Figura 6 muestra la variación de la relación SSV/SST de la biomasa analizada durante el tiempo de experimentación. Ambos colorantes tuvieron comportamientos similares en cuanto a esta relación, donde el colorante C1 tuvo una mayor cantidad de sus datos por debajo de la mediana, representada con un valor de SSV/SST de 0,82, mientras que el colorante C2 presentó una concentración bastante homogénea, con la mayor parte de sus datos cercanos a la mediana con un valor de SSV/SST de 0,87. También se encontró que ambos colorantes tuvieron valores atípicos, tanto por debajo como por encima de la media, lo cual demuestra la variabilidad que pueden tener los microorganismos en los diferentes días de monitoreo del reactor. Comparando ambos colorantes se concluye que tanto con C1 como C2, la relación SSV/SST fue en promedio la adecuada para un tratamiento biológico, ya que los resultados indicaron en la mayoría de los casos el 80% de los sólidos suspendidos presentes en el reactor eran de naturaleza orgánica, lo que hace referencia a una adecuada población de microrganismos para llevar a cabo los procesos biológicos, con mejores resultados para el colorante C2, lo que era de esperarse debido a las mayores eficiencias de remoción de materia orgánica presentadas.
La Tabla 2 presenta el análisis estadístico de la biomasa en términos de relación SSV/SST. La varianza (σ2 )de C2 fue 0,007, valor muy por debajo de la varianza de C1 (σ2 = 0.050), indicando un mejor comportamiento de los microorganismos con C2 en comparación al colorante C1. Esta afirmación también se puede afirmar con la desviación estándar (σ), donde para C2 se obtuvo un valor de 0,082, mientras que para C1 fue 0,224, indicando un comportamiento más homogéneo para C2, en cuanto al crecimiento de los microorganismos.
La tendencia general de la relación SSV/ SST (Figura 7), indica que parte de los datos analizados se ubicaron por debajo del valor de la mediana, aunque es un sesgo poco significativo. El promedio general de la relación SSV/SST fue 0,802, indicando con esto que aproximadamente el 80% de los sólidos presentes en el reactor SBR son de naturaleza orgánica, o sea que es un lodo con una alta concentración de microorganismos, hecho que favorece la depuración del agua del afluente.
Dados los resultados obtenidos para los ensayos de sedimentabilidad empleando como indicador el IVL (Figura 8), el valor promedio para el colorante C1 fue 49,792 (ml/g) y para el colorante C2 fue 63,233 (ml/g), indicando para ambos una buena sedimentabilidad debido a que los valores fueron menores a 100 ml/g [27], estos resultados son importantes, ya que la sedimentabilidad del lodo mejora la clarificación del efluente y por lo tanto, la eficiencia final del sistema. Estudios realizados por Sathian et al. [24], encontraron valores de IVL en el rango de 90 – 103 ml/g para un reactor SBR empleado en la remoción de colorantes de una industria textil, lo que corrobora la buena sedimentabilidad que se logra obtener con este tipo de reactores.
En cuanto al análisis estadístico (Tabla 3), el colorante C2 tuvo un comportamiento más homogéneo del IVL, al igual que los parámetros previamente analizados, donde la varianza (σ2 ) de C2 fue 154,484, valor muy por debajo de la varianza de C1 (σ2 = 377,113) y la desviación estándar (σ) fue 12,389 para C2 y 19,419 para C1, indicando que los microorganismos mantuvieron una sedimentabilidad más constante y mejor cuando operó con el colorante C2.
La Figura 9 permite observar el comportamiento general del parámetro IVL en el sistema SBR, con un sesgo poco significativo desplazado hacia la izquierda, lo que indica, que algunos datos se encuentran por debajo del valor de la mediana de 59,310. En general, como se demostró mediante el análisis estadístico, el IVL tuvo un comportamiento bastante homogéneo y óptimo para tratamientos de aguas residuales con este tipo de contaminantes.
La presencia de ciertas especies de protozoos en los tratamientos de aguas residuales brinda información que permite identificar la efectividad de los procesos, consiguiendo de esta manera, monitorear y controlar eventuales dificultades que se presenten en el continuo proceso de funcionamiento. En el monitoreo llevado a cabo al reactor SBR, se identificaron un conjunto de organismos que comparados con la literatura permitieron afirmar que el sistema de tratamiento estaba logrando los objetivos propuestos. Los protozoos encontrados e identificados en el lodo se muestran en la Figura 10, donde la mayor abundancia para el reactor SBR operado con C1 fue de Ciliados fijos y Rotíferos (Figura 10a), mientras que para las condiciones de C2, abundaron principalmente los Ciliados libres (Figura 10b). En cuanto a los Rotíferos y Ciliados fijos encontrados con C1, estos protozoos son indicadores de buena sedimentabilidad, ya que ellos contribuyen a la remoción de las bacterias suspendidas o aquellas no floculadas, y ayudan a la formación del floc, permitiendo con esto que se logre una adecuada clarificación del efluente [28]. Sin embargo, la presencia de ellos también es un indicador de baja concentración de materia orgánica disponible lo que da lugar a procesos de respiración endógena y una edad de lodos elevada, lo que conlleva a un exceso de microorganismos viejos, los cuales tienen poca actividad, esta situación se vio reflejada en las remociones encontradas en C1, las cuales a pesar de ser elevadas comparadas con otros estudios, fueron menores comparadas con el colorante C2. En cuando a los Ciliados libres, estos protozoos son controladores de las bacterias filamentosas, las cuales pueden causar problemas de sedimentabilidad, esto explica los óptimos valores de IVL encontrados en C2, además, estos ciliados son indicadores de la existencia de una buena oxigenación en el reactor [28] y un buen balance de materia orgánica, lo que mejora la eficiencia de los reactores. Los Ciliados libres son considerados la condición más óptima de un proceso de remoción aerobio.
Conclusiones
Los resultados de la investigación permitieron concluir que ambos colorantes se comportaron estadísticamente iguales frente a la remoción del COT, con un valor promedio de remoción de materia orgánica de 94,31% para C1 y 96,45% para C2. La relación SSV/SST determinada para ambos colorantes indicó que los sólidos presentes en el reactor eran de naturaleza orgánica, hecho que favoreció la depuración del efluente. El resultado obtenido del IVL clasificó el lodo de buena sedimentabilidad, lo que contrastó con las altas eficiencias encontradas en la remoción de materia orgánica. Los microorganismos que más abundaron en la biomasa dieron certeza del buen funcionamiento del sistema SBR en cuanto a remoción de la materia orgánica. Por lo tanto, se concluye que el reactor SBR a escala piloto es altamente eficiente para remover la materia orgánica presente en aguas residuales generadas del teñido de flores, ya que es capaz de soportar la carga orgánica de los contaminantes usados en dicha actividad. Es, por esta razón, el sistema SBR una alternativa viable para el tratamiento de este tipo de aguas residuales industriales logrando un efluente de alta calidad, lo que disminuye el impacto ambiental generado por estas actividades industriales frente a los recursos hídricos.