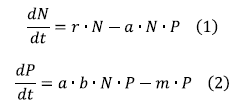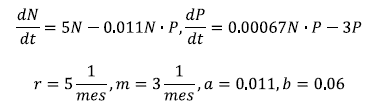INTRODUCCIÓN
Los lagos altoandinos son considerados estratégicos por sus condiciones climáticas, altitudinales y por la ausencia de estacionalidad en el trópico (Gómez et al., 2016). Sin embargo, estos lagos presentan problemas de eutrofización, acidificación, alteraciones hidrológicas y modificaciones geomorfológicas producto de los cambios en los usos del suelo y la explotación de sus servicios ambientales (Poikane et al., 2016; Ríos-Touma et al., 2014).
Estos problemas se reflejan en la zona litoral, que es receptora directa de nutrientes y contribuye al desarrollo de las plantas acuáticas que proporcionan superficie, refugio y alimento a las comunidades bióticas (Caleño Ruiz et al., 2017; Carrillo et al., 2006; Cremona et al., 2008). Dentro de estas comunidades, se encuentran los macroinvertebrados, que son en su mayoría sedentarios, tienen ciclos de vida largos y son muy importantes en la dinámica y funcionalidad de los ecosistemas acuáticos (Prat et al., 2009; Rial et al., 2016). Los macroinvertebrados son bioindicadores de condiciones ambientales, gracias a sus adaptaciones evolutivas y límites de tolerancia que responden a condiciones del ecosistema más que a variables específicas (Álvarez, 2005; Barman y Gupta, 2015; Poikane et al., 2016). Los índices biológicos, por su parte, permiten valorar cuantitativamente la dinámica de la comunidad de macroinvertebrados (Boggero et al., 2020; Poikane et al., 2016; Ríos-Touma et al., 2014), así como su composición y perturbación (Khatri et al., 2021; Soria et al., 2020).
En este contexto, el Lago de Tota, que es el sistema léntico natural más grande de la zona andina de Colombia, ejemplifica la influencia de los factores antropogénicos, el cambio climático y la capacidad hidrológica en la dinámica de los lagos de alta montaña (Cañón y Valdes, 2011; Pedroza-Ramos et al., 2020) El Lago de Tota se clasifica como polimíctico cálido y brinda múltiples servicios ambientales, recreativos e industriales, siendo la principal fuente de agua para consumo humano de 250.000 habitantes (Reyes et al., 2016). Sin embargo, está sometido a un continuo ingreso de nutrientes provenientes de los cultivos aledaños al litoral y de los vertimientos directos de aguas residuales que han favorecido el crecimiento de la macrófita Egeria densa (Figura 1). Esta planta acuática, introducida en el lago, actúa como barrera de contención de nutrientes y bioacumula las entradas de fósforo alóctonas al sistema lacustre. Por su crecimiento rápido, Egeria densa contribuye a la pérdida de espejo de agua, creando barreras para la navegación y disminuyendo la transparencia del agua (Pineda, 2020). En torno a la problemática del Lago de Tota, se han desarrollado estudios ecohidrológicos asociados a actividades humanas y condiciones climáticas (Cañón y Valdes, 2011; González Morales, 2016), que incluyen el estudio de los macroinvertebrados acuáticos y el crecimiento de la macrófita Egeria densa (Gil Padilla et al., 2016; Pedroza-Ramos et al., 2016; Pineda, 2020) que determinan el estado trófico del lago (Pedroza-Ramos et al., 2020) En línea con estos estudios previos, este artículo aborda dos preguntas orientadoras: ¿Cuál es la condición actual de la calidad del agua a lo largo del litoral del Lago de Tota? y ¿Cómo es la dinámica trófica de comunidades de macroinvertebrados en el litoral, asociados al crecimiento dominante de la macrófita Egeria densa? Para responderlas, se hizo un seguimiento espacial y temporal de la calidad ecológica del litoral del lago y del recurso hídrico en tres campañas de campo entre 2016 y 2018, analizando estadísticamente índices hidrobiológicos y variables físico-químicas del agua y de la macrófita, Se consideran como hipótesis que la calidad del agua varía a lo largo del litoral, viéndose más afectada en los puntos de vertimiento directo de los afluentes y que la dinámica de la relación predador-presa de los macroinvertebrados asociados a Egeria densa es un mejor reflejo de las condiciones de calidad a largo plazo en el lago, comparada con observaciones de abundancias de organismos en muestreos puntuales.
MATERIALES Y MÉTODOS
Fase de campo
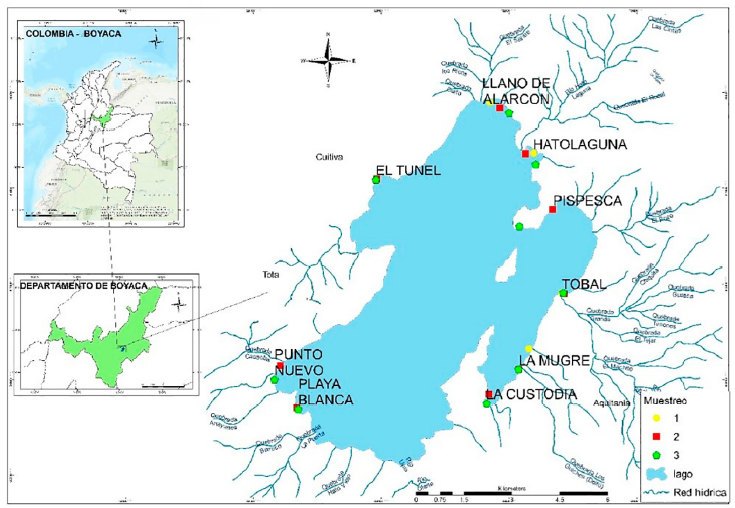
Para determinar el estado del Lago de Tota y recolectar la información biológica, físicoquímica y de georreferenciación, se realizaron tres campañas de muestreo: 30 de octubre de 2016, 28 de noviembre de 2017 y 19 de marzo de 2018. Estas campañas se hicieron en nueve estaciones de monitoreo que abarcaron el perímetro del Lago de Tota (entre 5°28'13" y 5°39'14"-N, entre 72°51'38" y 73°0'00" O.) (Figura 2). El Lago de Tota se encuentra a 3015 m.s.n.m en la vertiente nororiental de la cordillera de los Andes, entre los municipios de Aquitania, Cuitiva y Tota, en el departamento de Boyacá (Cordero et al., 2005). El lago tiene un área de 5620 hectáreas y 1920 millones de m3 de volumen medio. La definición de las estaciones de muestreo tuvo en cuenta el uso del suelo, la influencia del casco urbano, los servicios ecosistémicos, la entrada de afluentes y recomendaciones de estudios previos. Igualmente, se delimitó el área superficial de Egeria densa, georreferenciando la presencia de la planta en el límite interno a lo largo del margen litoral. Las muestras biológicas se recolectaron con una red de 50 cm de diámetro de boca y poro de malla de 3 mm, extrayendo 1 kg de material vegetal (kg MV) de la planta. Las muestras se fijaron con alcohol al 70 %, midiendo in situ: pH, conductividad, oxígeno disuelto, temperatura, sólidos disueltos totales (SDT) y coordenadas geográficas, con un medidor multiparamétrico HANNA 9829. La toma de muestras para nitritos, fósforo total, dureza total y alcalinidad (en el agua) y para fósforo total y nitrógeno total en Egeria densa siguió el protocolo del laboratorio GAIA de la Universidad de Antioquia (Baird et al., 2017). Para establecer el predador y la presa representativos del litoral del lago, se tuvo en cuenta la red trófica identificada por el trabajo de Pedroza-Ramos et al., (2016).
Análisis de laboratorio
En el Laboratorio de Hidrobiología de la Facultad de Ingeniería de la Universidad de Antioquia, se determinaron y contaron los taxones de macroinvertebrados con ayuda de claves taxonómicas especializadas (Domínguez y Fernández, 2009; González y Watling, 2003; Merritt y Cummins, 1996; Pennak, 1955; Roldán-Pérez, 1988; Stebbing, 1899) y posteriormente se establecieron los datos de riqueza y abundancia.
Análisis de información y bioindicadores
Para la determinación espacial y temporal de la información de bioindicadores en el Lago de Tota, respecto a la comunidad de macroinvertebrados, se aplicaron los índices: BMWP adaptado a zona andinas (Álvarez, 2005), diversidad de Shannon Wiener, dominancia de Simpson, riqueza de Margalef y equidad de Pielou (Alba-Hincapié et al., 2016; Kumari y Maiti, 2020; Roveri et al., 2020).
El análisis espacial de los índices se hizo con el método de interpolación distancia inversa ponderada (IDW) y el análisis de las variables consideradas por medio de Box-Plot. Para establecer diferencias estadísticamente significativas en las abundancias y variables ambientales se utilizó el análisis multivariado ANOVA con un nivel de confianza del 95 %, verificando previamente la normalidad de las variables con la prueba Kolmogorov-Smirnov, y realizando las transformaciones de potencia necesarias para validar los supuestos de los valores residuales. El diseño de los mapas se hizo en el programa ArcGIS 10.2.2 (licenciado por la Universidad de Antioquia). Para el análisis estadístico se usaron los programas R 3.4.2 y para la modelación, Python 3.7.1.
Modelo predador-presa
Para elucidar las relaciones tróficas básicas dentro de la dinámica poblacional de los macroinvertebrados en el lago como reflejo de las condiciones ambientales de acumulación de nutrientes en el litoral, se presenta un modelo Lotka-Volterra de la relación predador-presa de los dos géneros dominantes dentro de la comunidad del Lago de Tota: el anfípodo Hyalella sp. (González y Watling, 2003; Stebbing, 1899) y las larvas del odonato Ischnura sp.
Las ecuaciones de Lotka-Volterra son la base de estudios de sistemas dinámicos con modelos ecológicos simples que consideran las densidades de población y las variables continuas asociadas al comportamiento poblacional (Bunin, 2017; Kumar et al., 2020). Estas ecuaciones permiten evaluar y predecir el comportamiento de interacciones poblacionales (Dannemann et al., 2018; Gavina et al., 2018; Jiao et al., 2015; Pintar y Resetarits, 2021). El modelo Lotka-Volterra describe la interacción del depredador (larva de odonato Ischnura sp.) con la presa (Hyalella sp.) a través de dos ecuaciones diferenciales simultáneas para simular el comportamiento con respecto a las abundancias medidas en un periodo de 10 años:
La ecuación 1 describe el comportamiento de las presas, mientras que la ecuación 2 describe el de los predadores. N es el número de presas y P es el número de individuos predadores. Se consideran los parámetros r: tasa per-cápita de reproducción de las presas, a: coeficiente de eficiencia predadora, b: eficiencia de convertir una presa en un nuevo predador y m: la tasa per-cápita de muerte de los predadores (Gotelli, 2008). Para solucionar las ecuaciones se utilizó el método numérico de Runge-Kutta de cuarto orden, y para garantizar la convergencia de los resultados se escogió un paso de tiempo dt=0.01 días.
Para calibrar el modelo, se relacionan las tasas de cambio de ambas poblaciones con las tasas intrínsecas de crecimiento y la tasa de la interacción de las especies, lo cual resulta favorable para el predador y desfavorable para la presa (Amaya Cedrón, 2020). La relación predador-presa proyecta las relaciones y el comportamiento de las comunidades con relación a las abundancias en el tiempo, las cuales igualmente se relacionan con las variables físicas y químicas del agua y las condiciones de enriquecimiento del litoral.
Los muestreos realizados en esta investigación permitieron cuantificar el número de individuos por kg MV (individuos en 1 kg de material vegetal), y para complementar la calibración del modelo se incorporaron los cálculos de biomasas calculados por Pineda, (2004) que corresponden a datos del predador y la presa en 6 meses consecutivos, que son similares a los medidos entre 2016 y 2018, los cuales contribuyeron al ajuste de la serie de datos del modelo Lotka-Volterra. Para estandarizar la información y hacer las conversiones de los datos, se tuvieron en cuenta los resultados de Rivera-Usme, (2011), que considera abundancias y biomasas de anfípodos del género Hyalella y de larvas de odonatos de la familia Coenagrionidae, en el humedal Jaboque, ubicado en la zona Andina, en la ciudad de Bogotá, con condiciones altitudinales y medioambientales similares a las del Lago de Tota.
RESULTADOS
Las campañas de campo permitieron identificar un total de 12526 individuos pertenecientes a 11 órdenes, 18 familias y 21 géneros. Los taxones más abundantes fueron: Hyalella sp., con 7770 individuos y larvas de quironómidos del género Dicrotendipes, con 6836 individuos, seguidos de larvas de odonatos de los géneros Neosigara, Hidrozetes e Ischnura sp., este último con 372 de individuos (Tabla 1). El mayor aporte de Hyalella sp. provino de la estación La Mugre (1931 individuos). Los anfípodos del género Hyalella son característicos de aguas con alta conductividad, alta transparencia, presencia de macrófitas como biotopo y presencia de materia orgánica en descomposición (Alba-Hincapié et al., 2016; Rivera-Usme et al., 2013). El género Dicrotendipes, presente mayormente en La Mugre con 755 individuos, es tolerante a bajas concentraciones de oxígeno y altas cargas de materia orgánica y por lo tanto es bioindicador de contaminación (Gómez et al., 2016). La abundancia promedio por estación fue mayor en La Mugre con 934 individuos, seguida por Pispesca con 811 individuos y la más baja en Llano de Alarcón, con 325 individuos, seguido por Playa Blanca con 327. A nivel temporal, el primer muestreo tuvo las máximas abundancias. No se registraron diferencias estadísticamente significativas entre estaciones (p=0,41), ni entre muestreos (p=0,25).
Tabla 1 Clasificación taxonómica y abundancia total por morfotipo de los macroinvertebrados del Lago de Tota (MV: material vegetal)

Para delimitar el análisis espacial de las variables biológicas y ambientales, se georreferenció el cinturón de la macrófita Egeria densa, estableciendo un área de ocupación de la macrófita de 6,63 km2, correspondiente a la diferencia entre el perímetro del lago (56,04 km) y el polígono del límite interno de la macrófita (49,41km).
Índices bióticos
En los monitoreos de 2016 a 2018 se encontró que la diversidad de Shannon en general es muy baja con respecto a la calidad del agua (Magurran, 1988), con valores entre 0,41 y 1,83, que reflejan condiciones de calidad entre moderadamente contaminada y muy contaminada (Figura 3a). La estación La Mugre tuvo los valores más bajos del índice en las tres campañas de muestreo, mientras que las estaciones Pispesca, El Túnel, La Custodia, Llano de Alarcón y Hatolaguna mostraron condiciones de contaminación considerable. Las estaciones Punto Nuevo y Playa Blanca, por su parte, tienen la máxima diversidad y una contaminación moderada (Pérez y Restrepo, 2008). La diversidad fue mayor en el tercer muestreo y menor en el primero. La dominancia de Simpson, con valores entre 0,21 y 0,86, tuvo un comportamiento opuesto a la diversidad como se observó en El Túnel y El Tobal (diversidad baja, dominancia alta) y Playa Blanca y Punto Nuevo (dominancias bajas, diversidades altas) (Figura 3b). La dominancia fue mayor en el primer muestreo y menor en el tercero. La equidad osciló entre 0,17 y 0,80 (Figura 3c).
La riqueza de Margalef fue más baja en La Mugre, La Custodia y Hatolaguna y mayor en Punto Nuevo y Playa Blanca con valores entre 0,86 y 1,89. Este fue el único índice que registró diferencias significativas entre muestreos (p= 0,02), con valores de rango muy amplio, especialmente en el segundo muestreo (Figura 3d). El índice BMWP, con puntajes de 19 a 51, corresponde a aguas contaminadas a moderadamente contaminadas. Los valores más bajos del índice BMWP se obtuvieron en las estaciones Llano de Alarcón, El Túnel y La Mugre (Figura 3e).
Variables ambientales
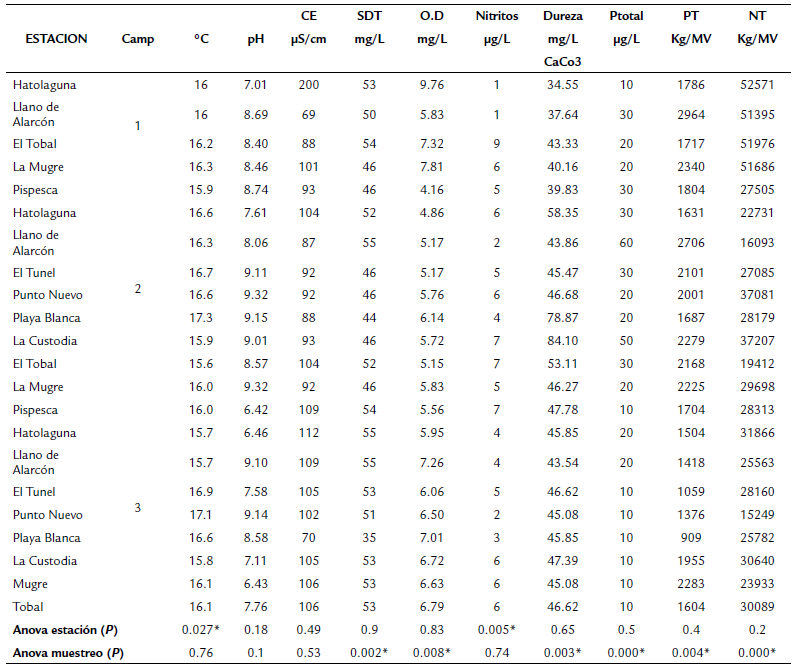
En la Tabla 2 se presentan los resultados del análisis ANOVA de las variables fisicoquímicas del estudio a un nivel de significancia del 95 %. Los resultados muestran diferencias estadísticamente significativas por estación para la temperatura, que osciló entre 15.6 y 17.2 °C con máximos valores en Playa Blanca y Punto Nuevo, y para los nitritos, que presentaron concentraciones muy bajas (<0.1 mg/L) en la mayoría de las estaciones, excepto en El Tobal y La Custodia que presentan los valores más altos, debido probablemente al ingreso de aguas negras del municipio de Aquitania y al arrastre de sedimentos de la cuenca por los tributarios. En estas dos estaciones se encontraron los menores índices de diversidad. El oxígeno disuelto (OD) estuvo entre 4,16 y 9,76 mg/l, con máximos valores en Hatolaguna y La Mugre en el primer muestreo, asociado con el inicio del periodo de lluvias e incremento del nivel del lago. Las concentraciones más bajas de OD las tuvo Pispesca, estación cercana a una de las truchifactorías, lo que puede relacionarse con alta demanda de oxígeno. El fósforo total en el agua tuvo concentraciones muy bajas (entre 0,01 y 0,07 mg/l), aunque debe tenerse presente que el fósforo se bioacumula en Egeria densa. Los máximos valores de fósforo los tuvo Llano de Alarcón y La Custodia (sectores con vertimientos y actividad agrícola), mientras que los valores más bajos se presentaron en Punto Nuevo, El Túnel y Playa Blanca, sectores con baja intervención. A nivel temporal, en el segundo muestreo se presentaron los valores más altos de fósforo total. Para Egeria densa, el nitrógeno osciló entre 15249 y 52571 mg/Kg MV, con máximos valores en Hatolaguna, Llano de Alarcón, La Mugre y El Tobal y con un rango más estable en Punto Nuevo, Playa Blanca, Pispesca, El Túnel y La Custodia. La concentración de fósforo en la macrófita, con valores entre 909 y 2964 mg/Kg MV, fue mayor en Llano de Alarcón y La Mugre, y baja en Playa Blanca, El Túnel y Punto Nuevo. En el primer muestreo se presentaron los valores más altos de fósforo y en el segundo muestreo los menores. En general, la conductividad eléctrica registró valores entre 69 y 200 µS/cm que son considerados altos (Hernández et al., 2013)
Modelo predador-presa
Dentro de la dinámica trófica general de las comunidades de macroinvertebrados, se consideró la modelación de Ischnura sp. como predador de la Hyalella sp., taxones abundantes en el Lago de Tota, que coexisten en asociación con la Egeria densa, la cual les provee refugio y alimento (Pedroza-Ramos et al., 2016).
Los datos que alimentan el modelo predador-presa corresponden al número de individuos y su equivalencia en biomasa la cual fue obtenida de los tres muestreos hechos en este estudio (correspondientes a 2016, 2017, 2018). Estos datos fueron complementados con los datos del estudio de Pineda (2004), en las estaciones El Tobal y Llano de Alarcón efectuado en el primer semestre del 2004 (Tabla 3). Se pudo observar que los individuos son mucho más abundantes en la estación El Tobal tanto para el predador como para la presa (Tabla 3).
Las ecuaciones dinámicas calibradas con los datos mensuales de 2004 fueron:
Los parámetros r y m son propios de la fisiología de los organismos y una vez calibrados no cambian en las simulaciones. Los parámetros a y b están más relacionados con las condiciones del ecosistema y pueden variar entre estaciones y épocas del año.
A pesar de que los odonatos son buenos cazadores, la eficiencia predadora es baja en El Tobal, debido a la baja transparencia del agua causada por factores como la turbidez de la corriente del tributario, los cambios de temperatura del agua y la presencia de vegetación, que dificultan el éxito de caza. El parámetro b, que es el porcentaje de las presas consumidas por los predadores que puede resultar en el nacimiento de un predador nuevo, para el Tobal se asume en seis nuevos predadores por cada 100 presas comidas. Las condiciones iniciales son las mismas para los dos periodos del Tobal: (t0 = 0, N0 = 80, P0 = 50). N0 y P0 son las condiciones iniciales de las poblaciones de presa y predador respectivamente y son un estimativo del número de individuos al comienzo de la simulación. En este caso, las condiciones se han escogido de tal forma que coincidan aproximadamente con los datos de las abundancias observadas. El último parámetro es el ajuste a la fecha de inicio, que coincide con la toma de los datos, con lo cual se puede representar la dinámica de las poblaciones. Este valor si varía entre épocas, teniendo en cuenta intervalos mensuales (figuras 4 y 5).
Para el periodo 2014, los datos mensuales (correspondientes a seis meses) se ajustan muy bien al comportamiento del modelo, con un pico de presas entre agosto y septiembre para ambas estaciones (Figura 5a).
Para la estación Llano de Alarcón, tanto en 2004 como en 2016-2018, la condición inicial que aumenta es la eficiencia predadora α = 0.033 porque las condiciones de Llano de Alarcón facilitan los encuentros entre predador y presa (Figura 5b).
Se encontró que, hacia el mes de septiembre, al igual que en el Tobal, se da el pico más alto de abundancia de presas e inmediatamente el aumento de los predadores, esto respecto a las dinámicas de las especies y al modelo Lotka-Volterra. Hay que tener en cuenta el cambio de escala, ya que El Tobal tiene mayores abundancias (Figura 4).
A pesar de que hay puntos que quedan por fuera de las curvas modeladas debido a que la reproducción es continua y pueden presentarse varias dinámicas al mismo tiempo, el modelo pudo relacionar el comportamiento de las abundancias con las dinámicas poblacionales de estas especies.
DISCUSIÓN
Las elevadas abundancias de los géneros Hyalella y Dicrotendipes identificadas en los muestreos de 2016 a 2018, son indicadoras de baja calidad del agua y alta carga orgánica, lo que corrobora los hallazgos de otras investigaciones en sistemas lénticos de alta montaña (Alba-Hincapié et al., 2016; Gómez et al., 2016; Pedroza-Ramos et al., 2020; Rivera-Usme et al., 2015) Por su parte, las larvas del odonato del género Ischnura, presentes en los diferentes muestreos y consideradas como predadoras en el modelo, son indicadoras de la presencia de presas suficientes para su alimentación. Las plantas acuáticas son un excelente hábitat para el desarrollo de estas larvas que son también tolerantes a cambios de temperatura (Bota-Sierra et al., 2019).
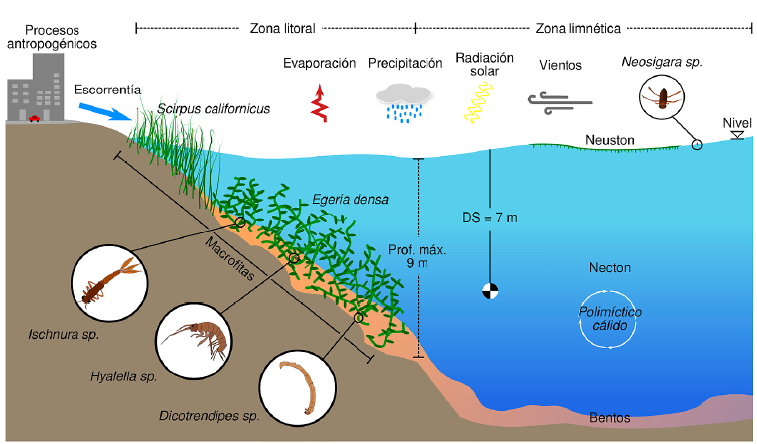
Figura 1 Esquema de las variables ambientales, físicas y bióticas que inciden en el comportamiento de la comunidad de macroinvertebrados
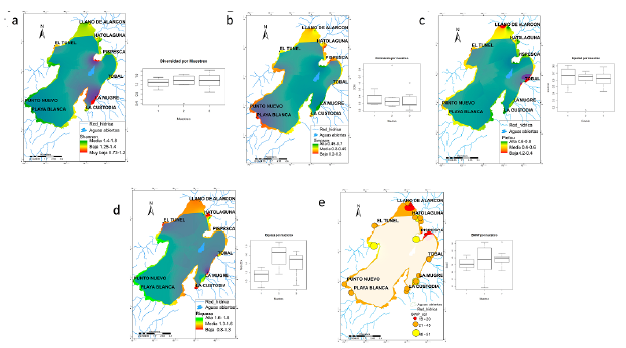
Figura 3 Comportamiento espacio-temporal de los índices bióticos en el litoral del Lago de Tota. (a) Diversidad de Shannon; (b) Dominancia de Simpson; (c) Equidad de Pielou; (d) Riqueza de Margalef; (e) BMWP.
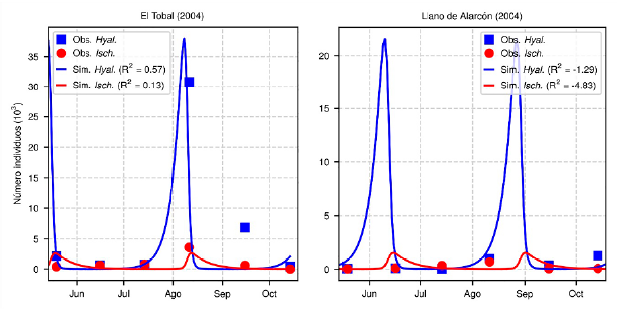
Figura 4 Comparación del comportamiento de la dinámica predador-presa en las estaciones El Tobal y Llano de Alarcón (calibración con datos de Pineda (2004).
El impacto del incremento de nutrientes y de los procesos antrópicos en la cuenca se evidencia en las grandes densidades de Egeria densa (Carrillo et al., 2006), a lo largo del litoral del lago, especialmente en el litoral oriental, ya que el aporte constante de fósforo y nitrógeno desde los cultivos a orillas del lago favorece el crecimiento acelerado de la macrófita. Esto se corroboró con las concentraciones de fósforo encontradas en la planta y con las diferencias espaciales asociadas a altas densidades en zonas de amplio desarrollo agropecuario.
En términos de índices bióticos, la alteración de la dinámica natural de la cuenca de un lago de alta montaña se traduce en baja diversidad, alta dominancia y bajos valores del índice BMWP, lo que implica baja calidad del agua en sectores críticos que requieren atención, según los límites que establecen dichos índices (Ríos-Touma et al., 2014; Roveri et al., 2020; Roldán-Pérez, 2016). Los índices evaluados en Tota reflejan procesos sectorizados de contaminación en el litoral, con condiciones desfavorables en el flanco oriental del lago y condiciones aceptables hacia el suroccidente.
Con respecto a las variables fisicoquímicas, los altos valores de conductividad eléctrica se deben probablemente a las características de recepción de nutrientes del litoral y a los procesos de degradación de la materia orgánica propios de las plantas acuáticas, que aceleran la concentración de iones en el agua. También hay que tener en cuenta que, bajo condiciones naturales en ecosistemas acuáticos de alta montaña, a medida que aumenta la conductividad disminuye la diversidad de especies (Roldán-Pérez, 2012).
Igualmente, la relación de bajos valores de abundancia y de oxígeno disuelto puede deberse a que los procesos de degradación de la materia orgánica agotan el oxígeno, generando condiciones inadecuadas para la supervivencia de la mayoría de los invertebrados acuáticos (Rivera-Usme et al., 2015).
El exceso de nitrógeno se manifiesta en la proliferación masiva de macrófitas que induce a la reducción de la diversidad, a la producción de cianotoxinas, desoxigenación del agua y a la pérdida de servicios ecosistémicos (Pedroza-Ramos et al., 2020) se puede deducir que los altos valores encontrados de nitrógeno acumulado en Egeria densa son evidencia del proceso de eutrofización que afronta el lago.
En estudios limnológicos, tener abundancias muy grandes de un morfotipo con un rango bajo de tolerancia generalmente se asocia a un incremento de contaminación. Sin embargo, al desconocer el comportamiento poblacional de las comunidades de macroinvertebrados puede darse un diagnóstico incompleto, ya que pueden ser abundancias momentáneas que no siempre tienen relación directa con las condiciones ambientales. Igualmente, un cambio en las tasas de crecimiento o mortalidad de las poblaciones puede mostrar el impacto de un evento catastrófico en la calidad del agua e indicar el tiempo de recuperación según sus dinámicas tróficas y reproductivas.
Así mismo, se pueden modelar escenarios futuros o intermedios como fue el caso del modelo del presente trabajo, que cuenta con datos medidos de la comunidad escogida, lo que ayuda a pronosticar un comportamiento futuro de las relaciones de la presa Hyalella sp. y del predador Ischnura sp.
La dinámica predador-presa de los géneros Hyalella sp. e Ischnura sp. muestra la estabilidad de las relaciones en el ecosistema y la influencia del medio ambiente, ya que los incrementos de presas o predadores pueden obedecer a un pico reproductivo o a un descenso por depredación en el caso de las presas (Asencio Oganician, 2017).
Por ejemplo, los predadores Ischnura, al tener un rango limitado de tolerancia a alteraciones ambientales y por efectos de contaminación, se pueden ver drásticamente reducidos (Chiriboga-Ortega et al., 2021; Nasirian y Irvine, 2017; Roldán-Pérez, 2016b). Esta reducción puede disparar a su vez la tasa de crecimiento de presas. Por otra parte, el desarrollo exponencial de la vegetación acuática afecta la dinámica de estas comunidades, ya que Hyalella es herbívoro-raspador y la vegetación le sirve de refugio (Acosta y Prat, 2011; Castiglioni et al., 2020; Zhang et al., 2017) lo que dificultaría la actividad predadora y favorecería su crecimiento.
Por lo anterior, es importante relacionar los incrementos de materia orgánica con factores como la oferta de alimento, las condiciones hidrológicas y las condiciones fisicoquímicas de la cuenca. Estas relaciones ayudarían a comprender el comportamiento de las comunidades litorales a la hora de tomar decisiones ambientales respecto a los macroinvertebrados como indicadores de calidad en una época determinada.
Para analizar el comportamiento de la relación trófica en el tiempo, el modelo que se empleó en este estudio simula continuamente la relación predador-presa a lo largo de 14 años, ajustándose al conjunto de datos medidos, aunque se reconoce que la cantidad de mediciones es reducida y no permite identificar en campo todo el ciclo completo del proceso. Un mayor número de mediciones sería ideal para corroborar las suposiciones del modelo. A pesar de esta limitación, este tipo de modelos brinda la oportunidad de analizar dinámicamente los procesos tróficos y de calidad de aguas en ambientes lacustres como el del Lago de Tota, más allá de los tradicionales muestreos estáticos que suelen tomarse de base para los análisis y cuyas mediciones distantes en el tiempo puede ocultar los verdaderos mecanismos de relación y de abundancias de las poblaciones.
El modelo predador-presa puede perfeccionarse añadiendo variables como capacidad de carga y cambios de temperatura para simular el comportamiento de los ecosistemas y observar cómo interactúan sus variables. Los modelos de interacción deben apoyarse en muestreos continuos para calibrarse adecuadamente, percibir dinámicas significativas de las poblaciones y proyectar comportamientos futuros. Por lo tanto, es recomendable diseñar experimentos donde se midan tasas de crecimiento y mortalidad para hacer una evaluación poblacional de los organismos y relacionarlos en futuros modelos.
CONCLUSIONES
De acuerdo con los resultados (abundancias, composición fisicoquímica, índices bióticos y métodos multivariados), el litoral del Lago de Tota está en proceso deterioro, reflejado en su composición biótica y la calidad del agua. El estudio identificó zonas críticas como El Tobal, La Mugre, Llano de Alarcón, La Custodia y Hatolaguna,y zonas con mejor calidad relativa del agua como El Túnel, Playa Blanca y Punto Nuevo. Por lo tanto, es importante la delimitación de zonas de protección del ecosistema litoral que se basen en la calidad del agua según los índices bióticos, las variables ambientales y las relaciones entre organismos.
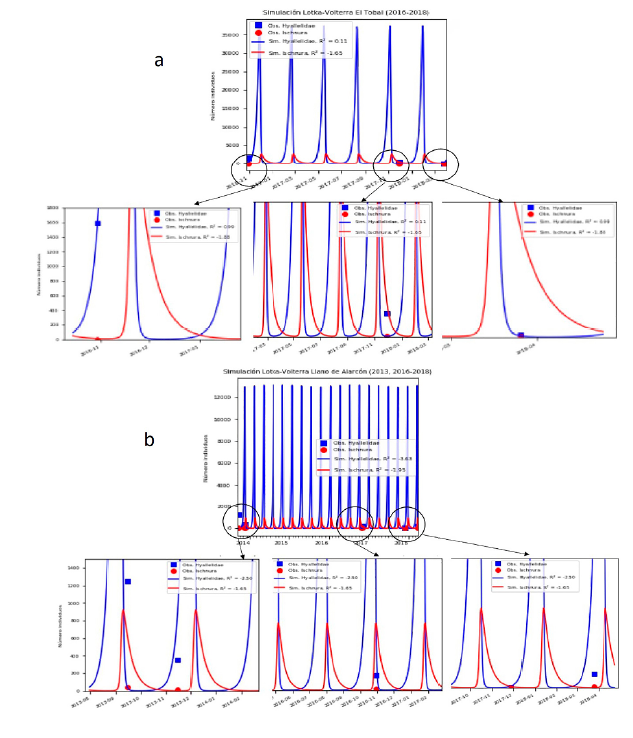
Figura 5 Comportamiento de la dinámica predador-presa en Hyalella sp. (cuadros azules) e Ischnura sp. (círculos rojos) para las estaciones (a) El Tobal (2016-2018) y (b) Llano de Alarcón (2013-2018).
Los géneros Hyalella y Dicrotendipes, que dan un primer indicio de la salud del ecosistema, son indicadores de alta carga orgánica y están presentes en todas las estaciones y muestreos. Se recomienda en particular el seguimiento de los géneros Hyalella sp. e Ischnura sp. en futuros estudios ecotoxicológicos y poblacionales, teniendo en cuenta sus abundancias, ciclos de vida y relaciones tróficas.
Las diferencias estadísticas de las variables fisicoquímicas a nivel temporal están determinadas por cambios de precipitación y de nivel del agua en el Lago de Tota, por lo que es importante monitorear el sistema, dados los múltiples servicios ecosistémicos que presta a la región, como suministro de agua para riego y consumo humano, acuicultura, pesca, ecoturismo y paisajismo.
Los resultados de la simulación del modelo Lotka-Volterra y el seguimiento de la relación predador-presa basada en abundancias reales, puede ayudar a establecer la vulnerabilidad de las especies a cambios en la calidad de agua del Lago de Tota por diferentes factores antrópicos. Un modelo dinámico como el planteado en este estudio facilita la comprensión de los comportamientos en el tiempo de dos especies representativas de la zona litoral del Lago de Tota y su condición de bioindicadores, pudiendo explicar los cambios observados en las abundancias de las poblaciones a través del tiempo.