Introducción
Alnus acuminata Kunth (Betulaceae) o Aliso (Tropicos, 2022) es una especie forestal arbórea con un amplio rango de distribución desde los 20° de latitud norte en México hasta los 28° de latitud sur en Argentina, encontrándose en los bosques premontanos, montanos y montanos bajos (Holdridge, 1966). Esta especie crece entre los 2000 y los 3000 m s.n.m., especialmente en las riberas de los ríos y en suelos muy húmedos (Erazo et al., 2019), prospera en un rango de temperatura entre 4 °C a 26 °C con pluviosidad variable de 1000 a 3000 mm y tiene valor económico para los habitantes locales por los diferentes usos en la fabricación de mangos de herramientas, en construcción, mueblería y artesanía. La madera de “aliso” es ligera y usada en construcciones livianas, con elementos estructurales sometidos a cargas pequeñas, tiene buena trabajabilidad, es de fácil tallado y no tiende a torcerse ni rajarse. Además, tiene un buen acabado, por lo que se puede utilizar en la elaboración de muebles decorativos y artesanías (Pacheco-Agudo & Quisbert-Guarachi, 2016).
Los alisos son plantas leñosas que varían en tamaño, desde pequeños arbustos hasta árboles grandes; poseen copas estrechas e irregulares, con alturas variables que alcanzan hasta los 30 m y hasta 60 cm de diámetro; sus troncos tienen cortezas de lisas a ligeramente ásperas, aunque escamosas en individuos viejos y son de colores de gris a marrón grisáceo y a veces plateados. En la región de la sierra en Perú (Serfor, 2019), A. acuminata tiene un estrato fustal con un índice de valor de importancia alto (55,59 de 300,00); es una especie amenazada en la categoría vulnerable, con un mayor peso ecológico (2,66) y con una gran abundancia y frecuencia. En el valle del Mantaro en Perú, A. acuminata tiene una densidad de 1267 plantas por hectárea en forma natural. Además, Lazo y Rodríguez (2021) refieren que A. acuminata tiene agentes biológicos perjudiciales, siendo el 73,7% coleópteros y lepidópteros (Arguedas & Espinoza, 2012). Dentro de las especies que afectan a A. acuminata está Eurysthea sordida y esta tiene sinonimias taxonómicas que incluyen a Mallocera sordida, Paramallocera sordida a Trichoporus dysoni (Species 2000, 2007; Irmng, 2022). El género Eurysthea fue descrito por Thomson en 1860 y recientemente fue revisado por Botero et al. (2019).
Eurysthea sordida está distribuida entre Colombia, Bolivia, Ecuador, Perú y Venezuela (Species 2000, 2007; Mindat.org, 2021; Monné, 2017; Taboada-Verona & Botero, 2018) y se ha reportado su presencia en Perú, atacando a A. acuminata, cuya identificación de E. sordida fue realizada por el doctor Ubirajara Martins de Souza del Museo de Zoología de la Universidad de Sao Paulo, Brasil, quien observó algunos estados de desarrollo en Huanchar (Concepción), Quichuay (Huancayo) (Medina Porta & Sarmiento Galván, 2008; Reátegui, 2010) y en Kayra, Valle de Cusco en Perú, a 3229 m s.n.m., con distribución en varias microcuencas con alta diversidad de flora y fauna (Yabar-Landa, 2016). Baltazar (2008), este lo describe como el escarabajo longicornio perforador de la corteza y el barrenador de la albura de A. acuminata, además, el autor describió las características morfológicas de sus estados de larva, pupa y adulto, además de registrar los daños realizados por estos en el “aliso” en Quichuay, provincia de Huancayo en la región andina de Perú, sin embargo, el autor no logró observar el estado de huevo y no identificó a la especie.
Actualmente, no se ha logrado controlar a E. sordida y el daño que ocasiona en A. acuminata en el valle del Mantaro, además de que persisten registros dudosos de la especie; por consiguiente, el objetivo de esta investigación es describir la morfología de los estados inmaduros de E. sordida recolectados en A. acuminata, como apoyo para la identificación de este, así como caracterizar el daño causado a A. acuminata por E. sordida.
Materiales y métodos
Área de estudio
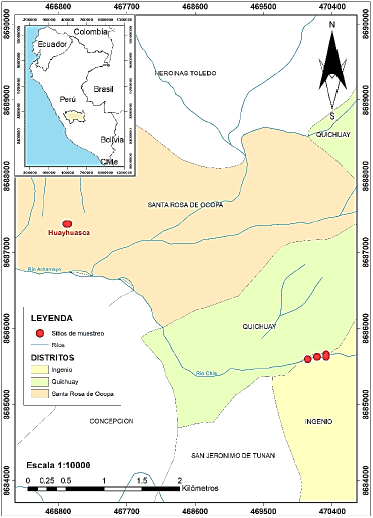
El área de estudio se localiza en los distritos de Ingenio y Quichuay (11° 53′ 23″ S, 75° 16′ 24″ O) en la provincia de Huancayo y en Santa Rosa de Ocopa (11° 52′ 38″ S, 75° 19′ 07″ O) en la provincia de Concepción, ambas ubicadas en la parte central del valle del Mantaro, en el departamento de Junín, Perú. El área tiene altitudes desde los 3360 hasta los 3444 ms.n.m. (figura 1).
Colección de muestras
La población de A. acuminata estuvo constituida por los árboles atacados por E. sordida en los distritos de Ingenio, Quichuay y Santa Rosa de Ocopa. La muestra para la evaluación fue de 12 árboles (10%) que presentaron diversos grados de daño por E. sordida.
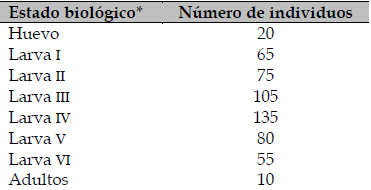
Se colectaron muestras de huevo, larva, pupa y adulto (tabla 1) desde abril del 2021 hasta marzo del 2022, en los distritos de Ingenio, Quichuay y Santa Rosa de Ocopa (11° 52′ 38″ S, 75° 19′ 07″ W) en el departamento de Junín, Perú.
Identificación taxonómica
Para la identificación de E. sordida, se consideró la distribución de las setas en los élitros en insectos adultos (Fonseca-Gessner, 1990; Martins, 2005; Santos-Silva et al., 2021); la descripción de tercer antenómero (Yabar-Landa, 2016) y la descripción realizada por Medina Porta y Sarmiento Galván (2008).
Se enviaron cinco individuos adultos de E. sordida para su identificación al Laboratorio de Entomología de la Unidad Centro de Diagnóstico de Sanidad Vegetal (Ucdsv), (colección entomológica depositada “Billie”) del Servicio Nacional de Sanidad Agraria (Senasa) en Lima. También se depositaron cinco ejemplares en la colección entomológica del Laboratorio de Biodiversidad y Manejo Forestal de la Universidad Nacional del Centro del Perú.
Evaluación del daño a la corteza y albura de A. acuminata
En el Laboratorio de Biodiversidad y Manejo Forestal de la Universidad Nacional del Centro del Perú (UNCP) se realizaron mediciones del diámetro (D) de los orificios de entrada y salida en la corteza y la albura de A. acuminata, realizados por E. sordida. Para caracterizar el daño producido de .. sordida a A. acuminata, se elaboró una escala tomada de Morillo et al. (2008) (tabla 2).
Evaluación y descripción morfológica de los estados biológicos de E. sordida
En condición de campo, se describió la presencia de A. sordida y el hábitat de los estados biológicos cuando ataca a A. acuminata. Se observó el comportamiento de los estados biológicos de A. sordida en A. acuminata, describiendo los signos y los síntomas observados durante la estación lluviosa (de diciembre a marzo) y estación seca (de abril a noviembre), donde se realizaron muestreos en árbol en pie, colectando partes de corteza dañada y desprendida, con orificios de entrada y salida de A. sordida, y la formación de galerías en túneles de longitud y diámetro variable, realizados por las larvas del barrenador. Se describieron los huevos depositados debajo de partes secas de corteza, las larvas de los estadios del I al VI localizadas debajo de la corteza y entre la albura, además de las pupas y los adultos localizados en la cámara pupal y en las galerías de crecimiento y salida. Los adultos de E. sordida pueden observarse caminando entre la corteza, las hojas y la hojarasca en las plantaciones de A. acuminata durante el día, bajo la sombra y con baja luminosidad, ya que son de hábito crepuscular y preferentemente buscan refugio.
En el Laboratorio de Biodiversidad y Manejo Forestal de la UNCP, los individuos que se encontraron fueron separados y clasificados por estados biológicos (huevo, larva, pupa y adulto) para medir la longitud total (L) y el ancho (A), según la metodología de Bellotti y Villegas (1985). Las muestras entomológicas fueron preparadas para realizar las descripciones morfológicas utilizando un estereoscopio de 110X de aumento (Leica modelo S9i, Alemania, con el software Leica LAS EZ versión 3.4).
Análisis estadístico
Se determinó el promedio y la desviación estándar (DE) de las mediciones, se aplicó la prueba de normalidad de Shapiro-Wilk (p > 0,05) a los parámetros morfológicos de los estadios biológicos encontrados (huevo, larva, pupa y adulto) con el software SPSS versión 25 (IBM, 2022).
Resultados y discusión
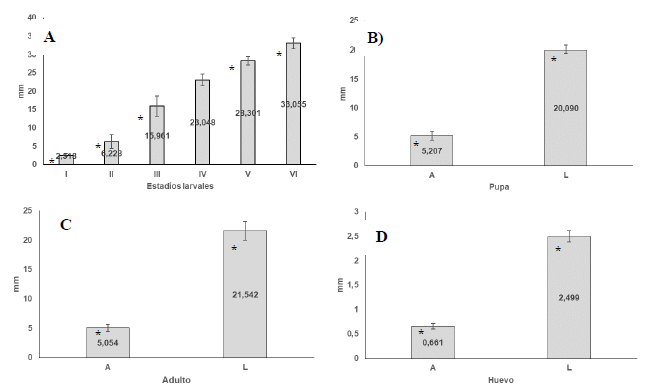
Eurysthea sordida presenta seis estadios de larva (I, II, III, IV, V y VI), con longitud total (L) promedio que incrementa del estadio larval del I al VI (figura 2A). El estadio de pupa tiene en promedio un A de 5,207 ± 0,754 mm y una L de 20,090 ± 0,659 mm (figura 2B), y el estadio de adulto tiene en promedio un A de 5,054 ± 0,617 mm y una L de 21,542 ± 1,579 mm (figura 2C). Los adultos pueden variar de 1,7 mm a 2,70 mm en longitud (Baltazar, 2008; Reátegui, 2010) y, muy probablemente, la diferencia encontrada en las dimensiones de L y A en esta investigación se deba a una variación de las condiciones climáticas y el hábito de alimentación durante el periodo evaluado. Al contrario de estudios como el de Baltazar (2008), en esta investigación se encontraron huevos de E. sordida, los cuales tienen, en promedio, un ancho de 0,661 ± 0,057 mm y una longitud total de 2,499 ± 0,112 mm (figura 2D).
Fuente: Elaboración propia
Figuras 2. Morfometría de E. sordida. Estadios larvales (2A) y estados de pupa (2B), adulto (2C) y huevo (2D), medidos en mm(*) Test de Shapiro-Wilk, n = 50, (p > 0,05).
Descripción morfológica de Eurysthea sordida
El adulto de E. sordidaes de forma cilíndrica, alargado, duro y compacto; tiene cabeza prognata y aparato bucal masticador (Medina Porta & Sarmiento Galván, 2008) y se alimenta del tejido vivo de hojas y corteza de A. acuminata. Hay dimorfismo sexual, la hembra (figura 3A) es más grande que el macho (figura 3B); el tamaño de la antena del macho (figura 3B) cubre todo el cuerpo e incluso rodea el ápice apical del lado opuesto, en cambio, la hembra (figura 3A) puede llegar a cubrir solo hasta el final del margen apical alar (Santos-Silva et al., 2021). El adulto presenta antenas con 11 antenómeros y su tamaño puede variar de 13 mm a 34 mm (Medina Porta & Sarmiento Galván, 2008), cubierto con abundantes setas finas, el escapo es lobulado, el pedicelo es corto y el flagelo es filiforme. Además, el tercer segmento antenal es 1,5 veces la longitud del escapo (Medina Porta & Sarmiento Galván, 2008; Yabar-Landa, 2016), presenta ojos compuestos reniformes de color amarillo castaño a gris oscuro (figura 3A) y las alas anteriores son élitros con terminación marginal y con borde lateral ligeramente atenuado, donde el margen humeral es lobulado y redondeado, que cubre hasta el margen apical; por otro lado, tiene sutura elitral recta en el lado del tercio basal, con superficie de escasa puntuación circular con distribución intersticial, muestra abundante pilosidad con dos tipos de setas amarillentas distribuidas uniformemente: decumbentes, muy cortas y finas, y setas ligeramente más largas e inclinadas (Fonseca-Gessner, 1990).
También los élitros tienen dos tipos de setas: en el macho, con setas cortas y abundantes, y setas largas intercaladas, más abundantes en la mitad posterior (Martins, 2005) (figuras 3A y 3B), son de color castaño claro a marrón oscuro, siendo más oscuro en el lado medio posterior, este tiene una estría elitral decurrente hacia el margen apical, es ligeramente cóncavo y algo curvado en toda su extensión, además, presenta un escutelo piloso lobulado, con ápice redondeado y con setas de color castaño claro de L (0,75 mm) y A (1,15 mm), con un pronoto de superficie glabra, de color marrón oscuro, con cinco tubérculos espinulados y con borde lobulado (figura 3B) y el ala posterior es membranosa y con venación reducida (Medina Porta & Sarmiento Galván, 2008). Además, este tiene patas caminadoras, con coxas fuertemente lobuladas y setas abundantes, con uñas, unguis y arolio (figura 3A); el tórax presenta el dorso tuberculado, de color marrón oscuro y con abundantes setas en el lado pleural y ventral (Fonseca-Gessner, 1990; Santos-Silva et al., 2021); el lado ventral del mesotórax es lobulado y en el metaesterno presenta una sutura discrimen en el metaventrito (Alonso, 2015) y en el abdomen se distinguen cinco segmentos abdominales en el lado ventral, tiene ventrito IV y en el ventrito V se observa el pigidio (figura 3C).

Fuente: Elaboración propia
Figuras 3. Adulto de E. sordida: vista (3A) pleural (hembra), (3B) dorsal (macho) y (3C) ventral (macho)
Fuente: Elaboración propia
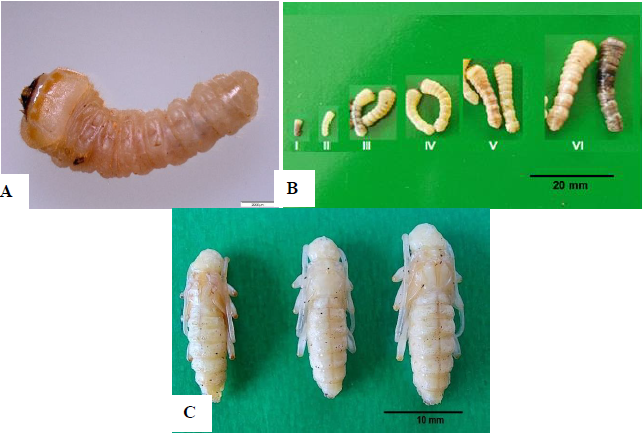
Figuras 4. Larva y pupa de E. sordida: (4A) estado de larva y (4B) estadios larvales I, II, III, IV, V y VI y (4C) estado de pupa
Las larvas de E. sordidason criptocéfalas, de color blanco cremoso a rosado, de forma cilíndrica, ligeramente encorvadas, cubiertas por setas finas y abundantes sobre el tergum de los segmentos abdominales; la cabeza es fuertemente esclerosada, aplanada con pronoto deprimido y no presenta ojo compuesto; el aparato bucal es masticador con mandíbulas gruesas y cuadrangulares, con tres dentículos en el área incisora y con 10 segmentos abdominales; son de hábito nocturno y endófitos, porque viven entre la corteza y la albura formando galerías, como refiere Medina Porta y Sarmiento Galván (2008). La coloración observada probablemente es respuesta a la ingesta de taninos de la corteza de A. acuminata (Janceva et al., 2015). Varían en L de 2,518 mm a 33,055 mm; el ancho de la cabeza es mayor con relación al tórax y el abdomen y presentan 10 segmentos abdominales situados en el lado dorso-pleural. Estos viven en el tejido vivo de la corteza y la albura de A. acuminata (Casari & Teixeira, 2014), se alimentan del tejido vivo de los árboles y son barrenadores primarios con un hábito de alimentación que se da en las galerías o los túneles debajo de la corteza o dentro de la albura de la planta huésped y estos túneles terminan en una cámara pupal, donde tiene lugar la metamorfosis de la larva del último estadio a pupa y luego a adulto. Además, tienen mandíbulas grandes y fuertes para barrenar y formar galerías y la cámara pupal (figura 4A) y se les observan seis estadios larvales: I (2,518 ± 0,421 mm), II (6,228 ± 1,858 mm), III (15,961 ± 2,752 mm), IV (23,048 ± 1,581 mm), V (28,301 ± 1,170 mm), y VI (33,055 ± 1,412 mm); las larvas del estado I hasta el estado IV presentan setas de color pardo amarillento que cubren todo el lado dorsal-pleural, desde la cabeza hasta el último segmento abdominal y, en el lado ventral, el protórax es más ancho que los ventritos I, II y III, y es de forma de subcilíndrica a ligeramente aplanada (figura 4B).
Las pupas de E. sordidason exaratas de color blanco cremoso brillante, sin presencia de setas; muestran formación de patas, antenas y ocelos (figura 4C); son inmóviles en las primeras etapas de crecimiento; muestran movimiento hacia el momento de la emergencia del adulto y viven entre la corteza, el aserrín y las galerías formadas en la albura.
Los huevos de E. sordida son colocados por las hembras en la albura debajo de la corteza en un lugar seco y en la parte media del fuste afectado (figuras 5A y 5B). Estos huevos son blanquecinos con un brillo perlado y tienen forma oval fusiforme, presentan dos ápices más delgados hacia los extremos y son ensanchados ecuatorialmente en el centro, se les observa la formación de ocelos y el aparato bucal antes de la emergencia (figura 5C). Cuando el huevo se conserva por un periodo mayor a 72 horas, el color de este cambia de blanco cremoso a amarillento (figura 5D), probablemente debido por el envejecimiento (Ric et al., 2006) y también por el desarrollo de la larva en el huevo.

Fuente: Elaboración propia
Figuras 5. Huevos de E. sordida: (5A) postura de huevos agrupados irregularmente debajo de la corteza, (5B) hembra en plena ovoposición, (5C) huevo oval fusiforme con ápices más delgados hacia un extremo y (5D) huevo que cambió a un color amarillento al conservarlo por un periodo mayor a 72 horas.
Daños en la corteza y albura de A. acuminata (T2)
El 100% de los árboles de A. acuminata evaluados en los distritos de Quichuay y Santa de Rosa de Ocopa presentaron daños por E. sordida (figura 7A), estos se observaron en la corteza, el cámbium y la albura, mostrando aberturas de ingreso de forma circular a irregular y desprendimiento de corteza en la etapa inicial (figura 7B). Durante la etapa intermedia de daño, se presentaron orificios de entrada de 2,0 mm hasta 3,0 mm en la parte inferior del fuste (figura 7C); en la etapa intermedia los orificios variaron de 4,0 mm a 5,0 mm, observando aserrín expulsado por la larva (figura 7E) y en la etapa final se presentaron orificios de salida del adulto que variaron de 11,0 mm hasta 21,0 mm, situados a diferentes alturas del árbol desde 0,6 m hasta 4,0 m (Medina Porta & Sarmiento Galván, 2008); y en la etapa final formaron galerías sinuosas e irregulares que llegaron hasta el cámbium y la albura (figura 7D). Las larvas se desarrollaron debajo de la corteza ya que son xilófagas y se detectó su presencia por la aparición de aserrín en la base del árbol (figura 7E). El insecto prefirió el hábito en madera húmeda (figura 7F), como también fue registrado por Martínez (2000) y el árbol atacado mostró un decaimiento desde la base, que avanzó hacia el fuste medio del árbol. Manifestó, adicionalmente, desprendimiento de la corteza en gran tamaño cuando el daño fue muy severo (figura 7B).
Se ha observado la presencia de individuos durante todo el año (Enriquez, 2007), sin embargo, hubo un aumento de individuos y daños de los estados de larva, pupa y adulto en los meses de diciembre a marzo. Esta variación de la población estuvo asociada al incremento de la precipitación (Evangelista et al., 2021) en el valle del Mantaro. Se ha observado que en algunos árboles de A. acuminata, cuando el daño afecta más del 70% de las ramas y el fuste, ocurre su muerte.
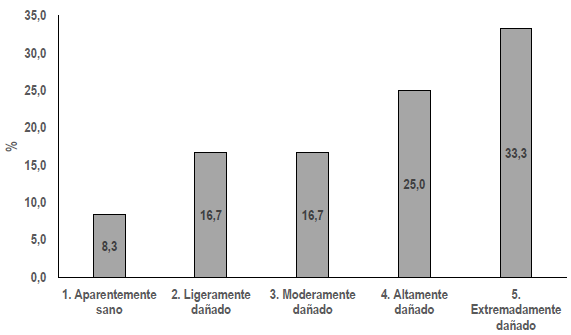
La incidencia de daños de E. sordida en A. acuminata ha detectado valores de escala 1 a 5, siendo similar a lo descrito por Morillo et al. (2008) (figura 6 y tabla 2). Los daños expresan una incidencia del 8,3% (aparentemente sano, figura 7A), una incidencia del 16,7% (ligeramente dañado y moderadamente dañado, figuras 7B y 8C), una incidencia del 25% al 33,3% (de altamente dañado a extremadamente dañado, respectivamente figuras 7C y 7D). Además, todas las plantas de A. acuminata presentaron incidencia de daños desde el ingreso del insecto hasta la emergencia del adulto, inclusive pudiendo provocar la muerte.

Fuente: Elaboración propia
Figuras 7. Daños en A. acuminata por larvas de E. sordida: (7A) árbol aparentemente sano, (7B) árbol de A. acuminata con daño severo y desprendimiento de corteza en la base del árbol etapa inicial, (7C) perforación en la corteza de forma circular (etapa intermedia), (7D) perforación de forma irregular (etapa final), (7E) perforaciones con signos de aserrín en el fuste y la base del árbol por presencia de larvas de E. sordida y (7F) larvas de E. sordida en el cámbium de la corteza.
El conocimiento de la descripción morfológica y los daños ocasionados por E. sordida a A. acuminata aportan una base científica para desarrollar un control integrado, a fin de conservar al aliso que habita en el valle del Mantaro y la región andina de Perú.
Conclusiones
Se realizó la descripción morfológica completa de los estados de huevo, larva, pupa y adulto de E. sordida, encontrando seis estadios larvales (I, II, III, IV, V y VI) y confirmando su identidad taxonómica.
Todos los ejemplares de A. acuminata evaluados en el valle del Mantaro, región de Junín, Perú, resultaron atacados por individuos de E. sordida, mostrando daños en la corteza, el cámbium y la albura, donde se encontró su preferencia por las maderas húmedas. Los daños, desde leves hasta muy severos, se muestran desde la base hasta el fuste medio.
El presente es el primer registro de los aspectos morfológicos de A. sordida y su daño severo en A. acuminata en el valle del Mantaro.
Contribución de los autores
Hernán Baltazar: análisis estadístico y tomas fotográficas de los estados de huevo, larva, pupa y adultos de E. sordida, y daños en corteza y albura de A. acuminata; Joan Blanco: colección de campo y mediciones microscópicas en laboratorio; Sthefany Quispe: preparaciones macroscópicas y microscópicas para la observación; Danilo Baltazar: contribución en las colectas de campo y Neddy Baltazar: contribución en las colectas de campo. Adicionalmente, todos los autores aportaron en la redacción del manuscrito.
Implicaciones éticas
El presente articulo cuenta con el aval de la Resolución n.° 4600-CU-2018, aprobado el 8 de noviembre del 2018, del Código de Ética para el Investigador UNCP, del Instituto General de Investigación, Vicerrectorado de Investigación de la Universidad Nacional del Centro del Perú. También se obtuvo el consentimiento de los colaboradores para usar la información suministrada en la documentación del proceso presentado en el artículo.