1. Introducción
La baja fijación de los colorantes sintéticos a las fibras textiles ocasiona la aparición de estos compuestos en las aguas residuales 1. En efecto, se generan altos volúmenes de aguas coloreadas, que sin un tratamiento eficiente representan una grave amenaza para el ecosistema acuático. Específicamente, en los procesos de teñido y acabado se estima que aproximadamente un 15% de los colorantes se pierden y se liberan al medio ambiente 2. La descarga de estos efluentes a los medios receptores conlleva varias implicaciones ambientales debido a la alta toxicidad y baja biodegradabilidad de los colorantes. Además de afectar el aspecto estético de los medios receptores, los colorantes interfieren en la penetración de la luz solar en el agua, lo que reduce la tasa de fotosíntesis y afecta negativamente la diversidad acuática 3.
Por otra parte, los efectos contaminantes de estos compuestos se reflejan en la acumulación en sedimentos, en peces y en otras formas de vida acuática4. Se ha evidenciado, por ejemplo, que la biotransformación de los colorantes azoicos causada por bacterias a través de la enzima azoreductasa, resulta en la liberación al ambiente de aminas aromáticas altamente dañinas, las cuales son absorbidas por los organismos a través de la piel, el tracto gastrointestinal o por inhalación 5,6. De igual forma, estos grupos amina también representan riesgos para la salud humana por los efectos carcinógenos y mutagénicos7 . En este sentido, es importante garantizar un tratamiento adecuado de los efluentes coloreados.
Varios métodos de tratamiento que van desde métodos físicos, químicos y biológicos han sido empleados para la eliminación de los colorantes del medio acuoso con el fin de disminuir su impacto en el medio ambiente 8,9. Sin embargo, por la complejidad de la estructura de los colorantes y las limitaciones de cada técnica es difícil seleccionar un tratamiento seguro y eficiente. En este sentido, procesos como la coagulación, la filtración y la adsorción por carbón activado son inapropiadas para la remoción de colorantes pues solamente transfieren al contaminante de una fase a otra10. En el caso de los procesos de degradación biológica, la toxicidad de la mayoría de los tintes comerciales para los organismos utilizados en el proceso, así como los tiempos prolongados requeridos desestimaría la aplicación de esta técnica 11,12. Por lo tanto, se necesita proceso de oxidación más fuerte que permita una completa mineralización de estas estructuras 13.
Al respecto, los Procesos de Oxidación Avanzada (POAs) se presentan como una opción altamente competitiva para la mineralización completa y segura de compuestos que, por su naturaleza persistente y recalcitrante, no son susceptibles de degradación por métodos convencionales. Entre los AOP disponibles, las reacciones de Fenton o similares a Fenton son atractivas porque la reacción produce radicales •OH altamente reactivos a través de la reacción de Fe+2 con H2O2 a temperatura y presión ambiente con un potencial redox de aproximadamente 2.73 eV, que se requiere para descomponer la mayoría de los tintes recalcitrantes 14,15.
Dentro de los materiales utilizados como catalizadores en el proceso Fenton, llaman la atención, los subproductos derivados de actividades industriales, por su bajo costo y su contenido en hierro. Particularmente, en la industria siderúrgica se producen grandes cantidades de una cascarilla de laminación o calamina que por su alto contenido en óxidos de hierro como hematita (Fe2O3), magnetita (Fe2O4) y wustita (FeO)16, se convierte en una alternativa de interés para emplearse como sustituto económico en tecnologías de tratamiento de aguas residuales como el proceso Fenton. Con frecuencia, este subproducto industrial se reincorpora nuevamente al proceso de generación del acero; sin embargo, una fracción de la calamina se dispone en rellenos sanitarios, representando una amenaza para las aguas subterráneas y el suelo, por la lixiviación de metales de la calamina 17. En este sentido, es esencial encontrar alternativas de aprovechamiento adecuadas para este subproducto dada su enorme producción dentro del mercado del acero en Colombia.
El objetivo de esta investigación fue determinar la eficiencia del proceso Fenton heterogéneo para la degradación del colorante azul de metileno, empleando calamina como catalizador.
2. Metodología
2.1 Reactivos
Peróxido de hidrógeno (30% p/v) Marca: Chemi, azul de metileno Marca: Chemi, ácido ortofosfórico Marca: Panreac, sulfato de hierro heptahidratado Marca: Merck y agua destilada.
El azul de metileno se seleccionó como compuesto de estudio debido a que es un colorante catiónico que, por su carácter aromático y aplicación en distintos campos, requiere una eliminación adecuada del medio acuoso, con el fin de evitar efectos adversos en el ecosistema.
El material empleado como fuente de hierro y catalizador de la reacción de Fenton heterogéneo corresponde a la cascarilla de laminación (calamina) proveniente de la elaboración de productos siderúrgicos. Se utilizaron tres muestras de calamina, las muestras tipo 1 y tipo 2 se identifican como de bajo y alto carbono, y la muestra tipo 3 corresponde a la calamina seca. Las muestras de calamina se trituraron suavemente en un mortero de porcelana con el fin de mejorar la uniformidad de las partículas y aumentar el área de superficie. Las muestras tipo 1 y tipo 2 presentaron un tamaño de partículas de 0.425 milímetros, y la muestra de calamina tipo 3 registró un tamaño promedio de 0.6 milímetros.
2.2 Determinación de la máxima longitud de onda de azul de metileno
Para estimar la máxima absorbancia bajo espectrofotometría visible, se realizó un barrido espectral con concentraciones inferiores a 10 ppm de azul de metileno debido a que favorecen la observación del espectro de absorción del colorante por el equilibrio monómero-dímero.
2.3 Elaboración de la curva de calibración de azul de metileno
Para realizar la curva de calibración de azul de metileno se preparó una solución stock de 100 mg/L del colorante. Posteriormente, se hicieron disoluciones para obtener concentraciones entre 0.5 a 11 mg/L, y se realizó la lectura de absorbancia en espectrofotómetro NANOCOLOR VIS II fijando el cero (blanco) con agua destilada.
24 2.4 Ejecución de los experimentos de Fenton homogéneo y Fenton heterogéneo
2.4.1 Descripción del procedimiento experimental
Cada experimento de oxidación se llevó a cabo en un beaker de vidrio de 600 mL para simular un reactor de tipo discontinuo. Inicialmente, se midieron 200 mililitros de la solución de agua coloreada (10mg/L de azul de metileno), previamente preparada en solución buffer de pH 3. Se realizó una estimación de la absorbancia y el pH de la muestra inicial. Posteriormente, se agitó la muestra a 100 rpm en un equipo de jarras, y se adicionó el volumen requerido de la solución concentrada del catalizador sulfato ferroso (10 g/L) y el volumen necesario de peróxido de hidrógeno. El tiempo de reacción se empezó a contabilizar luego de adicionar este último. Se tomaron alícuotas de 5 mililitros cada 20 minutos y se registró la absorbancia a 664 nm en el espectrofotómetro NANOCOLOR VIS II.
Para efectuar los experimentos de Fenton heterogéneo con la calamina como catalizador se aplicó el proceso descrito anteriormente, pero se utilizaron 300 mililitros de solución coloreada y el volumen de peróxido de hidrógeno se adicionó a la muestra 10 minutos después de agregar la calamina.
Así mismo, con el objetivo de realizar el seguimiento de la oxidación catalítica del colorante en función del tiempo en el proceso heterogéneo, se tomaron muestras cada 20 minutos durante 6 horas de reacción. Cada muestra extraída de la solución se centrifugó durante 5 minutos a 1000 rpm con el fin de remover las partículas de la solución. Finalmente, se realizó la lectura de absorbancia en el espectrofotómetro NANOCOLOR UV-VIS.
2.4.2 Condiciones de operación de los experimentos de Fenton homogéneo
En la Tabla 1 se muestran los parámetros que se tuvieron en cuenta para la ejecución de los experimentos. Se estableció un rango de pH ácido, debido a que favorecía la reacción de oxidación. Adicionalmente, se estableció un tiempo de reacción de una hora para la degradación del colorante.
Por otra parte, la selección de la concentración inicial de peróxido de hidrógeno que corresponde a 2.94 mM 100mg/L se realizó con base en las dosis óptimas reportadas en estudios en los que se evalúa el desempeño del proceso Fenton para la degradación de 10 mg/L de azul de metileno (18,19. Así mismo, se decidió evaluar menores concentraciones de peróxido de hidrógeno, pues este parámetro es uno de los limitantes en el proceso Fenton dado su alto costo.
Tabla 1 Condiciones del procedimiento experimental
| Parámetro | Unidades | Valor |
|---|---|---|
| Ph | - | 2.5-3.0 |
| Relación molar FeSO4 /H2O2 | - | 1:10; 1:15; 1:20 |
| Concentración de H2O2 | mg/L | 40; 70; 100 |
| mM | 1.176; 2.058; 2.94 | |
| Velocidad de agitación | rpm | 100 |
| Tiempo total de reacción | minutos | 60 |
Fuente: Elaboración propia
De igual forma, se tuvo en cuenta la relación molar FeSO4:H2O2 para el diseño de los experimentos, debido a que este parámetro se relaciona con la eficiencia del proceso Fenton, evitando reacciones secundarias indeseables. Como se aprecia en la Tabla 2 se fijaron relaciones molares entre (1:10 a 1:20) las cuales coindicen con los rangos de evaluación descritos en artículos referentes a degradación por Fenton para colorantes azoicos y para otros compuestos orgánicos persistentes 15,20,21). Específicamente, para la degradación de 10 ppm de azul de metileno mediante Fenton a un pH de 3 se han reportado relaciones molares óptimas de (1:15) y (1:17.5) 16,22,23.
2.4.3 Diseño experimental
Para estudiar los efectos en la degradación del colorante en la solución, se plantea un diseño experimental de tipo factorial 23 (Tabla 2), es decir, 2 factores con 3 niveles cada uno, para un total de 9 experimentos, en donde se evalúan todas las combinaciones posibles modificando diferentes concentraciones de los reactivos del proceso Fenton (peróxido de hidrógeno y sulfato ferroso). Se emplearon soluciones de 30.000 mg/L de H2O2 (0.88 M) y de 10 g/L de FeSO4 (65.83mM) para la aplicación de los volúmenes requeridos en cada muestra.
Tabla 2 Diseño de los experimentos tipo factorial 23
| H2O2 (mM) FeSO4:H2O2 (molar) | 2.94 | 2.058 | 1.176 |
|---|---|---|---|
| 1:10 | Experimento 1 FeSO4=0.294mM H2O2= 0.67mL; FeSO4=0.89Ml | Experimento 4 FeSO4 =0.206 mM H2O2= 0.47 mL; FeSO4=0,63mL | Experimento 7 FeSO4 =0.1176 mM H2O2= 0.27 mL; FeSO4= 0.36 mL |
| 1:15 | Experimento 2 FeSO4 =0.196 mM H2O2= 0.67 mL FeSO4=0.60mL | Experimento 5 FeSO4 =0,137 mM H2O2= 0.47 mL; FeSO4= 0.42mL | Experimento 8 FeSO4 =0.08 mM H2O2= 0.27 mL; FeSO4=0.24mL |
| 1:20 | Experimento 3 FeSO4 =0.147 mM H2O2=0.67 mL; FeSO4=0.45mL | Experimento 6 FeSO4 =0.103 mM H2O2= 0.47 mL; FeSO4=0.31mL | Experimento 9 FeSO4 =0.059 mM H2O2= 0.27 mL; FeSO4=0.18 mL |
Fuente: Elaboración propia
2.4.4 Condiciones de operación de experimentos de Fenton heterogéneo
De acuerdo con la Tabla 3, los experimentos de tipo heterogéneo se plantean para tres dosis de calamina, una concentración de peróxido de hidrógeno y con pH de 3 y de 7. Para garantizar la reproducibilidad de los experimentos, se lleva a cabo un duplicado de cada uno estos y, posteriormente, se calcula el promedio de los resultados obtenidos con el fin de asegurar un manejo adecuado de los datos.
Tabla 3 Condiciones de operación para experimentos Fenton heterogéneo.
| Variable | Unidades | Valor |
|---|---|---|
| Volumen de muestra | mL | 300 |
| Concentración de peróxido de hidrógeno H2O2 | mg/L | 100 |
| mM | 2.94 | |
| Concentración de calamina | g/L | 5; 10; 15 |
| pH | - | 3; 7 |
| Tiempo de reacción | Horas | 6 |
| Velocidad de agitación | rpm | 100 |
Fuente: Elaboración propia
2.5 Determinación de los porcentajes de remoción de DQO y COT
Con el fin de determinar la biodegradabilidad y la mineralización de las soluciones luego del tratamiento de oxidación, se evaluaron los parámetros de la Demanda Química de Oxígeno y de Carbono Orgánico Total para los experimentos óptimos en la remoción de azul de metileno mediante el proceso Fenton heterogéneo.
Para la determinación de la DQO se siguió el método colorimétrico, utilizando viales de digestión de Hach del rango entre 0.7 a 40 mg/L. Por la interferencia causada por el peróxido de hidrógeno en el resultado de la DQO de las muestras finales, se determinó la DQO para 2.94 mM (100 mg/L) de peróxido de hidrógeno. De esta forma, la DQO para cada muestra corresponde al valor obtenido menos el valor de la DQO del peróxido de hidrógeno. La determinación de Carbono Orgánico Total se realizó con base en el método de oxidación con persulfato, utilizando viales de digestión de Hach de rango bajo (0.3-20 mg/L). Los porcentajes de remoción de la DQO y de COT se obtienen de acuerdo con las Ecs. (1) y (2).
2.6 Estudio de la cinética de reacción para la degradación del azul de metileno
Para la determinación de la cinética de las reacciones de degradación del colorante azul de metileno se utilizó el método de la ley integral de velocidad. La tasa inicial de degradación del colorante está dada por la Ec. (3)
Donde A0, B0 y C0 son las concentraciones del colorante, catalizador y H2O2 respectivamente, m, n y p los respectivos órdenes. Manteniendo B0 y C0 constantes, la tasa isp. l de degradación del colorante esta dada por el producto de la constante de velocidad y la concentración inicial del colorante Ec. (4)
Los modelos de orden cero, primer y segundo se definen de acuerdo con las Ecs.5, 6 y 7:
Donde k0, k1 y k2 son las constantes de velocidad de orden 0, primer y segundo orden respectivamente, t es el tiempo de reacción y Ct es la concentración del colorante para un tiempo dado. Para representar cada modelo se lleva a cabo el seguimiento de la oxidación del colorante para el experimento óptimo, mediante la lectura continua de la absorbancia en el espectrofotómetro NANOCOLOR UV-VIS. Posteriormente, son construidos los respectivos perfiles cinéticos de cada modelo. El de orden cero representa el comportamiento de la concentración para el tiempo de reacción; en el modelo de primer orden, se relaciona el logaritmo de la concentración con el tiempo definido y, finalmente, para el modelo de segundo orden se presenta el comportamiento del inverso de la concentración para el tiempo de la reacción. A partir del coeficiente de correlación más próximo a la unidad determinado en cada perfil, se define el modelo que mejor representa la degradación de azul de metileno mediante el proceso Fenton
3. Resultados y discusión
3.1 Barridos espectrales del azul de metileno
En las Figuras 1 y 2se aprecian los resultados de los barridos determinados entre un rango de 320 a 900 nanómetros. Como se observa, es más notorio un pico a 610nm con el aumento de la concentración, lo cual se relaciona con la agregación de los colorantes en solución. De igual forma, se determina que el máximo de la banda de absorción para este colorante corresponde a 664nm.
3.2 Curva de calibración
La Figura 3 presenta la curva de calibración de azul de metileno.
Como se aprecia en la Figura 3, la absorbancia y la concentración del colorante tienen una respuesta directamente proporcional, lo cual evidencia el cumplimiento con la Ley de Lambert-Beer y, por tanto, es posible hacer uso de la Ec. (8) para determinar la concentración de azul de metileno en los experimentos.
3.3 Porcentajes de degradación del colorante mediante Fenton homogéneo
Las Figura 4, 5 y 6 muestran los porcentajes de degradación de azul de metileno para los 9 experimentos en 60 minutos de reacción mediante el proceso de Fenton homogéneo.

Fuente: Elaboración propia.
Figura 4 Porcentajes de degradación de 10 mg/L de azul de metileno con 2.94mM (100mg/L) de H2O2.

Fuente: Elaboración propia.
Figura 5 Porcentajes de degradación de 10 mg/L de azul de metileno con 2.058 mM (70 mg/L) de H2O2.

Fuente: Elaboración propia.
Figura 6 Porcentajes de degradación de 10 mg/L de azul de metileno con 1.176 mM (40 mg/L) de H2O2.
Según las Figuras 4, 5y 6 es evidente que utilizando una relación más alta de Fe:H2O2 se obtienen mayores porcentajes de degradación del colorante para cada tiempo evaluado. También es notorio que, durante los primeros 20 minutos se consigue la mayor degradación en cada experimento. Esto concuerda con el hecho de que la reacción de Fenton domina los primeros minutos a través de Fe+2, y que una mayor concentración de reactantes aumenta la velocidad de degradación.
De igual forma, los resultados indican que el experimento 1 utilizando Fe:H2O2 de 1:10, 100 mg/L (2.94 mM) de peróxido de hidrógeno y 44.6 mg/L (0.294 mM) de sulfato de hierro es el más eficiente para la degradación de 10 mg/L del colorante azul de metileno en 60 minutos de reacción a pH 3, pues alcanza un 99.9% de remoción del colorante.
3.4 Porcentajes de degradación del colorante mediante Proceso Fenton heterogéneo
Las Figuras 7 y 8 muestran las eficiencias de remoción de azul de metileno mediante el proceso de Fenton heterogéneo utilizando la calamina tipo 1 (bajo carbono) con pH ácido y neutro.

Fuente: Elaboración propia.
Figura 7 Porcentajes de remoción de azul de metileno con pH 3 y 2.94 mM de H2O2.

Fuente: Elaboración propia.
Figura 8 Porcentajes de remoción de azul de metileno con pH 7 y 2.94 mM de H2O2.
Las Figuras 9 y 10 muestran la remoción de azul de metileno con el proceso Fenton heterogéneo utilizando la calamina tipo 2 (alto carbono) con pH ácido y neutro.

Fuente: Elaboración propia.
Figura 9 Porcentaje de remoción de azul de metileno utilizando, pH 3 y 2.94 mM de H2O2.
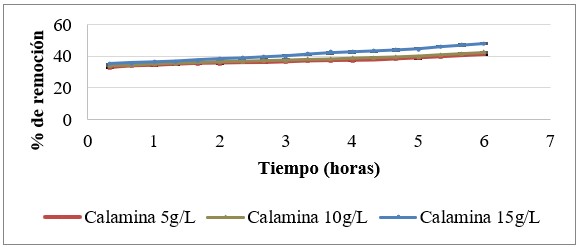
Fuente: Elaboración propia.
Figura 10 Porcentaje de remoción de azul de metileno utilizando pH 7 y 2.94 mM de H2O2.
Las Figuras 11 y 12 presentan las eficiencias de remoción azul de metileno mediante el proceso Fenton heterogéneo utilizando la calamina tipo 3 (calamina seca) con pH ácido y neutro.

Fuente: Elaboración propia.
Figura 11 Porcentajes de remoción del colorante con pH de 3 y 2.94 mM (100 mg/L) de H2O2.

Fuente: Elaboración propia.
Figura 12 Porcentajes de remoción del colorante 3 con pH 7 y 2.94 mM (100 mg/L) de H2O2.
De acuerdo con los resultados obtenidos en los experimentos de pH 3, a medida que aumenta la dosis de catalizador y transcurre el tiempo de reacción existe una mejor remoción del colorante. Específicamente, los experimentos realizados con la dosis de 15 g/L de calamina tipo 2 presentaron una mayor remoción. De esta forma, se obtienen remociones totales de 89.16% con la calamina tipo 1, de 99.8% con la calamina tipo 2 y de 92.58% con la calamina tipo 3 en 6 horas de reacción. Por su parte, los experimentos efectuados con pH neutro no alcanzan más del 50% de remoción de azul de metileno. El comportamiento que se evidencia en los experimentos de pH bajo puede atribuirse a una mayor disolución de especies de hierro y el incremento en la estabilidad del peróxido de hidrógeno en solución ácida 24.
3.5 Porcentajes de remoción de DQO y COT en Fenton heterogéneo con calamina tipo 2
Las Figuras 13 y 14 presentan la remoción de la Demanda Química de Oxígeno y de Carbono Orgánico Total para los experimentos de Fenton heterogéneo con 10 y 15 g/L de calamina tipo 2, 2.94 mM (100mg/L) de H2O2 y con pH 3.
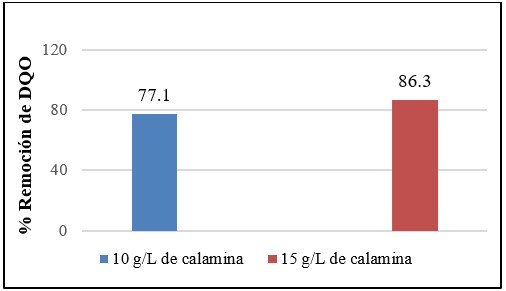
Fuente: Elaboración propia.
Figura 13 Porcentaje de remoción de DQO para experimentos con calamina tipo 2.
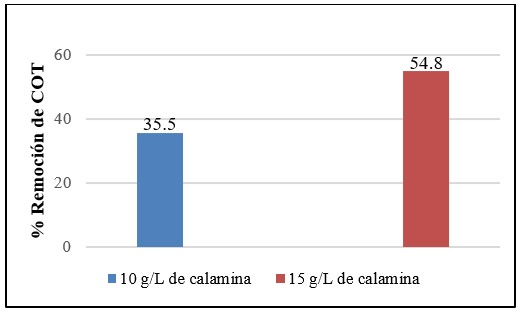
Fuente: Elaboración propia.
Figura 14 Porcentaje de remoción de COT para experimentos con calamina tipo 2.
De acuerdo con los resultados anteriores se evidencia una mejor eficiencia de remoción tanto de la Demanda Química de Oxígeno como de Carbono Orgánico Total para el experimento evaluado con la concentración más alta de calamina que corresponde a 15 g/L. Este resultado puede sugerir la mineralización del colorante en las muestras tratadas mediante el proceso Fenton heterogéneo bajo un pH ácido.
3.6 Resultados del estudio cinético para el proceso Fenton homogéneo
Con las mejores condiciones de degradación establecidas para azul de metileno mediante el proceso Fenton homogéneo, las cuales fueron producidas por el experimento 1, se realizaron los perfiles (Figuras 15, 16 y 17) que evidencian el comportamiento de los modelos de cero, primer y segundo orden.
La Tabla 4 presenta la constante de velocidad y el coeficiente de correlación obtenidos para el modelo de primer orden.
Tabla 4 Datos obtenidos del modelo de primer orden
| Condiciones | Primer orden | |
|---|---|---|
| Fe(II):H2O2= [1:10] pH: 2.8 | R2 | k1 (min-1) |
| 0.9815 | 0.036 | |
Fuente: Elaboración propia.
De acuerdo con el comportamiento de cada modelo cinético se evidencia que el de primer orden tiene una mayor aproximación lineal y, por tanto, describe más apropiadamente la cinética de degradación del colorante. Lo anterior coincide con los estudios de Dutta et al.22 y Melgoza et al.25 los cuales demostraron que una cinética de primer orden representa de manera apropiada la degradación del azul de metileno bajo el sistema homogéneo.
Reemplazando la constante de velocidad y el orden de reacción, la ley de velocidad se expresa como:
Dado que es una ecuación de primer orden respecto a la concentración de azul de metileno, la concentración de azul de metileno [𝐴𝑀]𝑡 en un tiempo dado esta dada por la siguiente expresión:
3.7 Resultados de la cinética de degradación mediante Fenton heterogéneo
El estudio cinético del proceso Fenton heterogéneo (Figuras 18, 19 y 20) se evaluó para el experimento más eficiente en la degradación del colorante, el cual se realizó con pH 3, 15g/L de calamina tipo 2 y 2.94 mM (100mg/L) de peróxido de hidrógeno.
De acuerdo con los resultados del estudio cinético mediante el proceso heterogéneo (Figuras 18, 19 y 20), el modelo que se ajusta más adecuadamente para la degradación de azul de metileno es el de primer orden. La Tabla 5 muestra el coeficiente de correlación y la constante de velocidad obtenida para el modelo de primer orden.
Tabla 5 Datos obtenidos del modelo de primer orden para Fenton heterogéneo
| Condiciones | Primer orden | |
|---|---|---|
| Calamina tipo 2: 15 g/L H2O2: 2.94 mM pH: 2.8 | R2 | k1 (min-1) |
| 0.9269 | 0.0122 | |
Fuente: Elaboración propia.
Al comparar la cinética de los procesos homogéneo y heterogéneo, se puede apreciar que el modelo de primer orden representa apropiadamente la degradación del colorante con los dos métodos utilizados; aun así, existe una mayor correlación de las variables con el proceso homogéneo. Por otra parte, los resultados muestran una constante de velocidad superior para el proceso homogéneo, lo que confirma el incremento de la degradación de azul de metileno en menor tiempo mediante dicho método.
4. Conclusiones
En este estudio, la aplicación de los procesos de Fenton homogéneo y heterogéneo resultó apropiada para la degradación de azul de metileno de la solución sintética. Los experimentos de Fenton homogéneo indicaron que el aumento de la relación Fe:H2O2 genera una mayor velocidad de degradación del colorante azul de metileno. A partir de los experimentos de Fenton homogéneo se seleccionó una concentración óptima de 2.94 mM de peróxido de hidrógeno y una relación molar óptima de Fe(II): H2O2 de 1:10.
Por su parte, los experimentos de Fenton heterogéneo con el uso de la calamina, demostraron que se requieren largos periodos de reacción y un pH ácido para obtener una mayor degradación del colorante azul de metileno. Con este proceso, se alcanzó una remoción del 99,8 % del colorante en 6 horas, utilizando 2.94 mM de H2O2, 15 g/L de calamina tipo 2 y en condiciones de pH 3. Para estas concentraciones, se obtuvieron también remociones de 86.3% para DQO y 54.8% para COT. En relación con la determinación de la cinética de la reacción, se pudo establecer que el modelo de primer orden se ajusta en mayor medida para la degradación de azul de metileno mediante los procesos de Fenton homogéneo y Fenton heterogéneo.
Como recomendaciones y observaciones finales de esta investigación, se aconseja determinar los compuestos secundarios producidos y su nivel de toxicidad para la valoración adecuada de la calidad del efluente obtenido con el tratamiento de oxidación. De igual forma, se recomienda evaluar procesos de activación de la calamina que permitan disminuir el tiempo de reacción en los experimentos de Fenton heterogéneo. Para la recuperación del catalizador se puede realizar una etapa de sedimentación, que permita separar la fase líquida de la sólida. En caso de aplicarse el proceso Fenton para el tratamiento de aguas residuales industriales, se recomienda neutralizar el pH del agua antes de realizar la descarga a los cuerpos de agua con el fin de cumplir la norma de vertimientos y evitar efectos adversos en los ecosistemas.
























