INTRODUCCIÓN
La generación de residuos es una problemática, a nivel mundial, que viene aumentando (Mojumdar & Deka, 2019) y que, a su vez, impulsa la creación de múltiples estrategias para su valorización en procesos de reciclaje, compostaje o de producción de energía (Matei et al. 2021). Debido a que los residuos agroindustriales representan una fuente importante de lignina, celulosa, almidón y otros polímeros, son utilizados como materia prima para el desarrollo de productos obtenidos a partir de su biodegradación, como bioetanol, biogás, bioabonos, sustancias bioactivas y ácidos orgánicos (Speda et al. 2017; Carrillo-Nieves et al. 2019; Halimah et al. 2019; Mazzoli, 2021; Lemes et al. 2022).
Los residuos agrícolas y agroindustriales se consideran sustratos de bajo costo en la producción de enzimas microbianas, aprovechando su composición química, disminuyendo costos de producción y minimizando los impactos ambientales asociados. Residuos, como el bagazo de caña de azúcar, las cáscaras de naranja, la cascarilla de arroz, el salvado de trigo y el raquis de maíz, se emplean en la producción de enzimas, como amilasas, pectinasas, ligninasas, proteasas y celulasas (Poondla et al. 2016; Akpinar & Urek, 2017).
Las celulasas son un complejo de enzimas conformado por endoglucanasas, exoglucanasas y β - glucosidasas, que catalizan la hidrólisis de los enlaces β 1-4 de la celulosa, produciendo monómeros de glucosa (Miranda Zoppas et al. 2013). Esta actividad catalítica es aprovechada, tanto en la producción de bioetanol y jarabes de glucosa a partir de material lignocelulósico como en la extracción de jugos de frutas y aceites de semillas. Asimismo, en la industria detergente, textil y del papel estas enzimas son aplicadas para mejorar la calidad de los productos, reduciendo el tiempo y el uso de energía en los procesos de fabricación (Miranda Zoppas et al. 2013; Muhammad et al. 2016; Niyonzima, 2021).
A pesar de las diversas aplicaciones y beneficios de las enzimas tienen un uso limitado, debido a sus elevados precios, ocasionados por los costos de producción, representados en los procesos de fermentación y de purificación (Ravindran et al. 2018). La producción de celulasas a partir de residuos agroindustriales permitiría disminuir los costos de producción, ampliando las oportunidades de aplicación, a nivel industrial, sobre todo en países en desarrollo, como Colombia.
Teniendo en cuenta que existe un bajo aprovechamiento de residuos orgánicos generados en las plazas de mercado y que se limita a la producción de compost, vermicompost, biogás y alimento para animales (Civelek Yoruklu et al. 2018; Das et al. 2018; Saranraj et al. 2018), se propone la obtención de celulasas bacterianas a partir de los residuos agrícolas, generados en las plazas de mercado.
MATERIALES Y MÉTODOS
Elaboración del medio de cultivo. A partir de ameros de mazorca y vainas de leguminosas recolectadas en el cuarto de almacenamiento de residuos de la plaza Distrital de mercado El Restrepo, en Bogotá, se realizaron dos medios de cultivo para la producción de celulasas. Para cada medio se pesaron 14,5 g de residuos lavados, troceados, deshidratados y licuados, con un contenido de celulosa de 35,3 ± 0,7 %, previamente determinado (Sánchez-Castelblanco & Heredia-Martín, 2022). Estos se suspendieron en 450 mL de una solución de nutrientes ((NH4)2SO4 0,31 g/L; KH2PO4 1,5 g/L; UREA 0,065 g/L; CaCl2·2H2O 0,4 g/L; MgSO4 0,3 g/L; Peptona 0,168 g/L), obteniendo una concentración final de 1 % de celulosa. A un medio, se le ajustó el pH a 7,0 (Medio A1), con NaOH 1M y, al otro, se le dejó su pH inicial de 5,0 (Medio A2). Los medios se llevaron a esterilización, a 115 ºC, por 7 minutos.
Producción del inoculo microbiano. Para la producción de los inóculos se utilizó la cepa C6M2, correspondiente a una bacteria celulolítica Gram negativa de la familia Enterobacteriaceae, previamente aislada de residuos orgánicos, generados en la plaza Distrital de mercado El Restrepo. En 150 mL de caldo BHI se adicionaron 2 mL de la cepa ultracongelada, se incubó en un shaker INNOVA 40, a 37 ºC y 100 rpm, por 18 horas. A partir de este cultivo se prepararon 2 inóculos de 50 mL, con una concentración correspondiente al tubo Nº 3, de la escala de McFarland.
Fermentación. Para la producción de celulasas microbianas se realizó una fermentación en el Medio A1 y otra en el Medio A2, a partir de la cepa C6M2. A 450 mL de medio se le adicionaron 50 mL del inóculo y se incubaron en shaker INNOVA 40, a 37 ºC y 150 rpm, por 75 horas. Se tomaron muestras de 4 mL a las 0, 24, 32, 48, 56, 60, 72 y 75 horas, para determinar azúcares reductores (AR), concentración bacteriana, actividad enzimática (AE) y celulosa residual.
Determinación de azúcares reductores en el medio. Las muestras se llevaron a una centrifuga Hettich - Rotanta 460R, a 4.500 rpm y 7 ºC, por 30 minutos. El sobrenadante se recuperó y se utilizaron 500 μL, para determinar AR, por la técnica del ácido 3-5 dinitrosalicílico (DNS), según Olanbiwoninu & Fasiku (2015). La absorbancia de las muestras se leyó a 540 nm, utilizando un lector de multimicroplacas marca BIOTEK - SYNERGY H1MG.
Determinación de la concentración bacteriana. Para verificar la viabilidad y la concentración bacteriana se tomaron muestras a las 0, 24, 32, 48 y 56 horas de la fermentación; se sembraron en agar Plate Count Merck®, por la técnica de recuento en placa en superficie y se llevaron a incubar a 37 ºC, por 24 horas.
Evaluación de la actividad enzimática. Las muestras provenientes de la fermentación fueron centrifugadas a 4.500 rpm y 7 ºC, por 30 minutos, en una centrifuga Hettich - Rotanta 460R; luego, en un microtubo, se tomaron 750 μL de sobrenadante (extracto enzimático) y se mezclaron con 750 μL, de una solución de carboximetilcelulosa (CMC), al 1 %p/v, en una solución buffer fosfato, para determinar la AE a pH 7,0 y para evaluarla, a pH 5,0, se utilizó una solución de CMC al 1 %p/v, en buffer citrato. Los tubos se llevaron a baño termostatado marca Memmert, a 50 ºC, por 30 minutos; después se detuvo la reacción enzimática en un baño de hielo por 5 minutos y se llevaron a centrifugar a 5.000 rpm, 20 minutos y 7 ºC, en una centrifuga Benchmark Z326K. En 500 μL de sobrenadante se cuantificaron los AR producidos durante la reacción enzimática, por la técnica descrita en el ítem de la determinación de AR. Para calcular la AE, a las absorbancias de las muestras, se les restó la absorbancia del punto 0 de la curva de calibración de glucosa y la de un blanco realizado con 750 μL del extracto enzimático más 750 μL de buffer fosfato o citrato, sometido a las mismas condiciones de la reacción enzimática. La AE se definió como la cantidad de enzima capaz de liberar una μmol de glucosa por mL por minuto, bajo las condiciones de ensayo establecidas. Las reacciones enzimáticas y la determinación de AR se realizaron por triplicado.
Obtención de extractos de celulasas. Después de las 75 horas de fermentación, los cultivos se centrifugaron a 4.500 rpm y 7 ºC, por 30 minutos, en una centrifuga Hettich - Rotanta 460. La biomasa se preservó para cuantificar la celulosa residual, mientras que el sobrenadante (extracto enzimático de celulasas), se prefiltró en una membrana de 0,45 μm y, posteriormente, se determinó su AE.
Determinación de celulosa residual. La concentración de celulosa residual se determinó a las 60 y 75 horas de la fermentación realizada en el medio. 150 mL de muestra se centrifugaron a 4.500 rpm y 7 ºC, por 30 minutos, en una centrifuga Hettich - Rotanta 460; el pellet obtenido y deshidratado, en horno Binder FED 115, a 90 ºC, por 8 a 12 horas; se digirió en medio alcalino por reflujo abierto, con una solución de NaOH 17,5 %, por 2 horas. Después de neutralizar con HCl concentrado, se centrifugó a 4.500 rpm, 7 ºC y 20 minutos, en una centrifuga Hettich - Rotanta 460R; se filtró al vacío y se llevó a 105 ºC, hasta peso constante, para determinar el contenido de celulosa gravimétricamente (Kulic & Radojičić, 2011).
Precipitación con sulfato de amonio (NH4)2SO4. La precipitación de la enzima se realizó con un porcentaje de saturación del 80 % de (NH4)2SO4 (JTBaker 99,9 %). A 180 mL del extracto de celulasas prefiltrado se le adicionaron lentamente 95,91 g de (NH4)2SO4 y se dejó en agitación a 4 ºC, durante 18 horas, aproximadamente.
Diálisis. La muestra precipitada con (NH4)2SO4 se centrifugó por 15 minutos, a 8.000 xg y 7 ºC, en una centrifuga Benchmark Z326K. El pellet fue resuspendido en buffer TRIS-HCl pH 8,0; posteriormente, se llevó a diálisis en una membrana de 12 a 14 MWCO (kDa), en buffer TRIS-HCl pH 8,0, se dejó en agitación a 4 ºC, por 48 horas y, finalmente ,se determinó la AE.
Ultrafiltración. El extracto de celulasas dializado se filtró utilizando una membrana de 0,22 μm.; al filtrado se le determinó la AE y se pasó a través de un cassette de ultrafiltación SARTORIUS VIVAFLOW 200, de 30.000 MWCO (Da). La AE de las celulasas se evaluó en el concentrado obtenido en la ultrafiltración.
Análisis estadístico. Las diferencias significativas entre las actividades enzimáticas evaluadas en los extractos enzimáticos de los medios A1 y A2 a pH 5,0 y 7,0 fueron determinadas, a través de un análisis de varianza (ANOVA), de un factor con un nivel de significancia (α) de 0,05, considerando diferencias significativas para p < 0,46. Estas diferencias entre la variabilidad de las medias se comprobaron por la prueba estadística de Tukey.
RESULTADOS Y DISCUSIÓN
En las figuras 1 y 2 se presentan los resultados de la producción de celulasas a partir de la cepa bacteriana nativa C6M2, aislada de residuos vegetales, generados en una plaza de mercado, utilizando medios de cultivo preparados con ameros de mazorca y con cáscaras de leguminosas, con una concentración final de celulosa al 1 %.
Los AR presentes en el medio A1, con una concentración inicial de 0,81 ± 0,02 mg/mL (Hora 0), presentaron un descenso considerable, a partir de las 24 las 32 horas de fermentación (0,34 ± 0,02 y 0,28 ± 0,01 mg/mL); sin embargo, no se presentaron concentraciones inferiores a 0,28 ± 0,01 mg/mL y en ocasiones hubo aumentos de AR, como el caso de la hora 72 (0,96 ± 0,02 mg/mL). Dichos cambios en la concentración se pueden explicar por el consumo de carbohidratos por parte de las bacterias, seguida por la continua hidrólisis de la celulosa, cuando los AR no estaban disponibles para su metabolismo. Es, por esta razón, que se presentaron dos picos de producción de celulasas, uno a la hora 32, con actividades de 25,56 ± 2,20 U/mL a pH 5,0 y 27,78 ± 0,06 U/mL a pH 7,0 y, otro, a la hora 56, con 24,07 ± 1,41 U/mL a pH 5,0 y 30,19 ±0,61 U/mL a pH 7,0 (Figura 1).
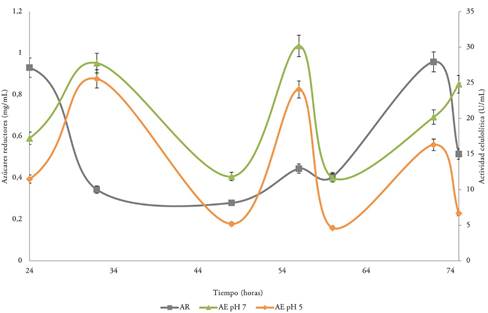
Figura 1 Concentración de azúcares reductores (AR) y actividad enzimática (AE), a 50 ºC, a pH 5,0 y 7,0 ,durante la fermentación del Medio A1, a pH 7.0.
La obtención de celulasas y la concentración de AR en el medio A2 tuvo un comportamiento similar al presentado en el medio A1, en el que también se presentaron dos picos de producción a las mismas horas de fermentación, lográndose la mayor producción a las 32 horas (30,74 ± 0,95 U/mL a pH 7,0); sin embargo, en A2 el segundo pico (56 horas) presentó menor AE, a pH 7,0 (18,15 ± 0,73 U/mL) y cuando la AE se evaluó a pH 5,0, este pico no se evidenció. Adicionalmente, la AE registrada en las dos horas consecutivas a estos picos de actividad (60 y 72) tuvieron valores similares, entre ellas, de 11,85 ± 0,01 a 14,63 ± 0,73 U/mL. Respecto a la concentración inicial de AR en la fermentación del medio A2 (0,74 ±0,02 mg/mL), se evidenció una disminución a partir de la hora 24 (0,40 ± 0,01 mg/mL) hasta la hora 48 (0,24 ± 0,01 mg/mL) (Figura 2).
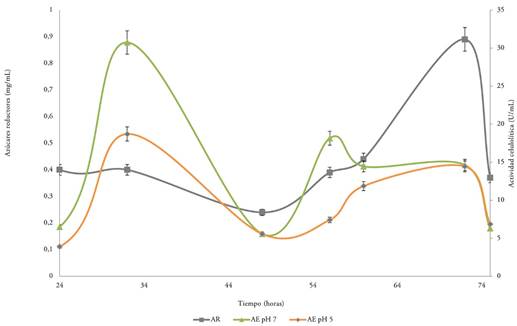
Figura 2 Concentración de azúcares reductores (AR) y actividad enzimática (AE), a 50 ºC, a pH 5,0 y 7,0, durante la fermentación del Medio A2, a pH 5,0.
Aunque los tiempos de máxima producción de celulasas son diferentes en los medios A1 (H56) y A2 (H32), las AE obtenidas en estos tiempos no presentan diferencias significativas, de acuerdo con el análisis de varianza de un factor (p valor = 0,49). Esto indica, que se obtienen AE similares realizando la fermentación, tanto a pH 5.0 como a pH 7,0. La utilización del medio A2 evitaría el uso de bases para ajustar el pH y la utilización del medio A1 permitiría la producción de celulasas en dos tiempos de la fermentación, con AE de 27,78 ± 0,06 U/mL y 30,19 ±0,61 U/mL.
Durante la fermentación de los medios formulados con ameros de mazorca y cáscaras de leguminosas, la obtención máxima de celulasas se observó en dos momentos, cada uno de estos fue precedido por una reducción en esta producción. De la misma forma, Sharma & Kaur (2019) evidenciaron incrementos y descensos consecutivos en la producción de celulasas, a partir de la fermentación de residuos sólidos agrícolas durante 7 días de cultivo. Es así como, por ejemplo, durante la fermentación de salvado de arroz y trigo, a partir de Staphylococcus sp., se observaron dos picos de actividad máxima en los días 1 y 3.
En la fermentación del medio A2, los dos picos de producción de celulasas se registraron durante la fase estacionaria del crecimiento bacteriano, mientras que en el medio A1, el primer pico ocurrió durante esta fase; el segundo, se presentó junto con una disminución de las UFC/mL (Figura 3). De manera similar, las celulasas producidas por B. licheniformis 2D55, en una mezcla de residuos agroindustriales, obtuvieron la máxima producción de FPasa y CMCasa, en la fase estacionaria y de xilanasa, en la fase de muerte (Kazeem et al. 2017).
La presencia de dos picos de producción de celulasas, a partir de residuos agrícolas, facilitaría el paso desde una fermentación discontinua, como la realizada en este estudio, a una discontinua alimentada en el que se realicen procesos de recuperación y separación de las enzimas, en los tiempos en los que se observen aumentos en la AE.
Las celulasas producidas en ambos medios de cultivo presentaron mayores AE cuando la reacción se realizó a pH 7,0 (Figuras 1 y 2), evidenciándose que presentan una mejor actividad que a pH 5,0. Estos resultados coinciden con los publicados para las celulasas producidas por B. licheniformis MTCC429, a partir de residuos agroindustriales (Bala Kumaran et al. 2015), por las obtenidas por Pseudomonas sp. y Serratia sp., aisladas de residuos de salvado de trigo (Prabesh et al. 2016) y para la producida a partir de Acinetobacter junii GAC 16.2 (Banerjee et al. 2020).
La producción de celulasas en medios a partir de ameros de mazorca y de cáscaras de leguminosas fueron mayores a las producidas en medios estándar en las que se utilizaron medios formulados a partir de CMC. Nagaiah et al. (2015) obtuvieron la máxima actividad de celulasas por Enhydrobacter sp. (ACCA2), de 3,50 U/mL; luego de 3 días de fermentación, Farjana & Narayan (2018) lograron una producción de 1,00 U/mL, a partir de Paenibacullus sp., a las 24 horas de cultivo y Prabesh et al. (2016), obtuvieron celulasas de 0,35 U/mL, usando Pseudomonas spp. (PA2).
Los medios A1 y A2 permiten la producción de celulasas a partir de la cepa C6M2 obteniendo actividades de 30,19 ± 0,61 U/mL y 30,74 ± 0,95 U/mL, que son superiores a las producidas en otros sustratos formulados con residuos agroindustriales. Es así, como las celulasas producidas por B. licheniformis 2D55, en un medio preparado con cáscaras de arroz y bagazo de caña, obtuvieron una actividad CMCasa 0,38 U/mL (Kazeem et al. 2017) y otro estudio reportó 0,50 U/mL, para celulasas obtenidas en un caldo CMC con un hidrolizado de bagazo de caña al 5 %, a partir de B. licheniformis MTCC 429 (Bala Kumaran et al. 2015).
En la tabla 1, se evidencia que el 60 % de la celulosa fue consumida por C6M2 durante las primeras 60 horas de la fermentación, período de tiempo, dentro del cual, se obtuvieron los dos picos de producción de celulasas (Figura 1). En las 15 horas subsecuentes se presentó un consumo de 5 % de celulosa que, a su vez, correspondió con un aumento en la producción de celulasa de 13,14 U/mL. La disponibilidad de celulosa en el medio, la AE y la concentración bacteriana deberían condicionar la parada de la fermentación, por ello, el porcentaje de celulosa residual en el medio se debería medir de manera continua e incluirse como variable de control en la optimización del proceso de producción de celulasas.
Las celulasas obtenidas a las 75 horas de fermentación en el medio A1 fueron recuperadas por centrifugación seguida de una filtración; posteriormente, estas se purificaron en tres pasos, obteniendo, al final, una reducción aproximada en la AE de 72,9 % (Tabla 2). Cuando las celulasas producidas se pretendan utilizar en industrias, como las de bebidas y alimentos, será necesario mejorar el proceso de purificación, considerando la inclusión de pasos adicionales y, de esta forma, lograr rendimientos similares a los obtenidos por Yin et al. (2010), Yassien et al. (2014) y Farjana & Narayan (2018), en la purificación de celulasas. De lo contrario, es conveniente utilizar el extracto crudo filtrado sin realizar procesos adicionales de purificación en aplicaciones que no requieran altos grados de pureza, como por ejemplo, la hidrólisis enzimática de residuos en procesos de extracción de biomoléculas.
Se concluye, que los medios formulados con ameros de mazorca y de cáscaras de leguminosas permitieron la obtención de celulasas, mediante una fermentación sumergida a partir de la cepa bacteriana C6M2, aislada previamente de residuos orgánicos, generados en plazas de mercado, lográndose dos picos de máxima producción de enzimas con mejores actividades a las reportadas en estudios previos, en los que también se utilizaron residuos agroindustriales como sustrato.
En la fermentación realizada en los medios a pH 5,0 (A2), como a pH 7,0 (A1), se obtuvieron valores similares de AE, aunque en este último, se debe prolongar el tiempo de fermentación para lograr la máxima producción de celulasas.
Indistintamente del pH en el que se hayan producido las celulasas, estas presentaron mayor actividad cuando la reacción enzimática se realizó a pH 7,0, por lo que se evidencia que las enzimas producidas en este estudio son más activas a este pH.
Aunque el proceso de purificación (precipitación, diálisis y ultrafiltración) de las celulasas obtenidas a partir de residuos agrícolas requiere ser mejorado para obtener mayores rendimientos del proceso, en este estudio, se demuestra que los residuos generados en plazas de mercado, como los ameros de mazorca y cáscaras de leguminosas, son una fuente de celulosa con potencial de aprovechamiento en la formulación de sustratos para la obtención de enzimas celulolíticas, reduciendo costos de producción.


















