Introducción
La embolia paradójica (EP) se describe como un evento trombótico a nivel arterial, que se origina en la circulación venosa y se produce por el paso de un émbolo a través de un defecto pulmonar o cardiaco 1. Estos episodios suelen presentarse como eventos cerebrovasculares (ECV) isquémicos. Aunque no se ha estimado una incidencia real, se considera que aproximadamente el 45 % de los eventos criptogénicos se pueden atribuir al EP. Así mismo, se han descrito casos de infarto agudo de miocardio, infarto renal, infartos periféricos e isquemia mesentérica 2. Para el diagnóstico de EP se requiere de un posible sitio de origen del trombo, evidencia de embolia arterial y presencia de un cortocircuito, siendo los más comunes el foramen oval permeable, los defectos septales y las malformaciones arteriovenosas pulmonares 3.
La isquemia mesentérica (IM) es una patología caracterizada por la disminución del flujo sanguíneo hacia los órganos viscerales, impidiendo llevar a cabo las distintas actividades metabólicas 4. La causa más común son los embolismos arteriales, hasta en un 50 % de los casos, seguido por estenosis de los vasos mesentéricos (35 %) y otras causas (5 %) 5. La relación entre ambas entidades es poco conocida. El objetivo de este artículo fue presentar el caso de un paciente que consultó con isquemia mesentérica, presumiblemente secundaria a embolia paradójica.
Caso clínico
Paciente masculino de 47 años, con cuadro clínico de 3 días de evolución consistente en deposiciones diarreicas, que 24 horas antes del ingreso se asociaron a deposiciones melénicas y emesis en cuncho de café. A la valoración inicial se encontró el paciente diaforético, con frialdad distal y dolor a la palpación de fosa iliaca derecha, sin claros signos de irritación peritoneal. Se tomaron paraclínicos con hallazgo de creatinina en rangos de injuria renal aguda AKIN III y gases arteriales con acidosis metabólica compensada.
Se inició anticoagulación con heparinas de bajo peso molecular. Por sospecha de patología quirúrgica intrabdominal se optó por tomar una tomografía computarizada (TC) de abdomen simple, debido a la injuria renal concomitante, encontrando signos de Íleo como único hallazgo patológico (Figura 1).
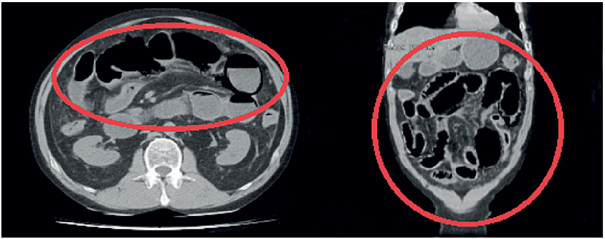
Figura 1. Tomografía computarizada de abdomen simple (cortes axial y coronal) en la cual se observan signos inespecíficos de íleo.
El paciente tuvo deterioro progresivo y a la valoración por el cirujano general ya presentaba signos francos de irritación peritoneal, por lo que se indicó trasladar a salas de cirugía como urgencia vital para laparotomía exploratoria. En la cirugía se encontró necrosis de intestino delgado en parches, desde 15 cm del asa fija hasta el tercio medio, con aproximadamente 150 cm de intestino comprometido (Figura 2). Se procedió a realizar resección intestinal y cierre con bolsa de Bogotá. La patología de la pieza quirúrgica mostró cambios por isquemia, sin evidencia de patología neoplásica.
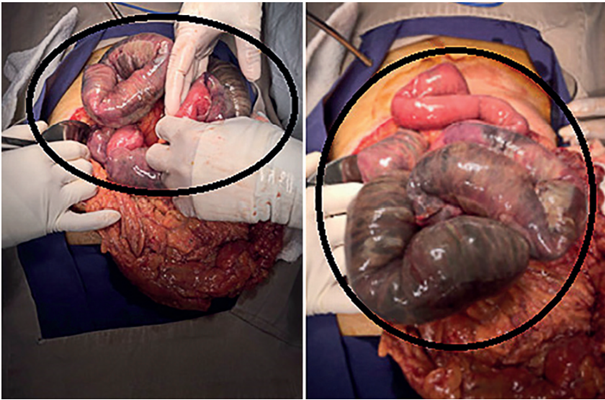
Figura 2. Hallazgos intraoperatorios de isquemia intestinal por parches, con compromiso de 150 cm de intestino delgado.
Se consideró como posible etiología del cuadro abdominal un evento cardioembólico versus trombofilia de base. En los estudios de extensión, el ecocardiograma describió un foramen oval permeable de 2 mm, con paso importante de microburbujas, reborde aórtico de 10 mm con alto potencial cardioembólico, sin trombos intracavitarios; la angiografía de vasos abdominales descartó trombos arteriales y el doppler de miembros inferiores no mostró trombos.
En cuanto a los estudios de coagulación iniciales, se encontró tiempo de tromboplastina 21,4 seg, tiempo de protrombina 11,2 seg e INR 1,05. Los estudios adicionales descartaron enfermedad autoinmune, con perfil para lupus eritematoso sistémico y síndrome antifosfolípido negativos; llamó la atención la disminución leve (69 %) de la actividad de la proteína C de la coagulación (valor normal 70-130 %) y una marcada disminución (15 %) de la proteína S (valor normal 77-143 %).
Fue llevado a revisión de cavidad abdominal 72 horas después del procedimiento inicial, encontrando el intestino bien perfundido; se logró realizar anastomosis intestinal y cierre de la pared abdominal. El paciente cursó con una evolución tórpida y requirió múltiples tiempos quirúrgicos para lavados peritoneal terapéutico. Luego de ocho días del cierre de la pared se encontró nueva isquemia a nivel de la anastomosis intestinal, por lo que requirió ampliar la resección.
El paciente desarrolló sepsis de origen abdominal, sin posibilidad de control del foco dado el hallazgo intraoperatorio de abdomen bloqueado, y evolucionó a choque séptico, con requerimiento de soporte vasopresor dual (noradrenalina y vasopresina) a dosis tope, por lo que se inició esquema de corticoide sistémico, antibiótico de amplio espectro y antimicótico.
El día 35 de hospitalización presentó un episodio convulsivo tónico clónico generalizado, fue llevado a TC de cráneo donde se identificó un infarto parietal derecho, sin indicación de manejo quirúrgico por el estado del paciente, quien finalmente falleció 38 días después del ingreso a la institución.
Discusión
La formación de trombos es un evento multifactorial, el cual suele ocurrir a nivel de la circulación venosa de miembros inferiores, con una incidencia de 104 casos x 100.000 habitantes. Tras un primer episodio, se estima que el 30 % de los pacientes presentarán nuevos eventos en un plazo de 6-12 meses a pesar del manejo adecuado 6.
Cuando se evidencia compromiso de senos venosos, miembros superiores o lecho esplácnico, se considera una trombosis de sitios inusuales, que es una patología rara, con una incidencia de 2 casos x 100.000 habitantes, siendo responsable de aproximadamente el 5 % de todos los eventos trombóticos 7.
Este caso clínico corresponde a un paciente que se presentó con isquemia intestinal por parches, sugestiva de varios eventos trombóticos en vasos de pequeño calibre, sin un origen aparente. Se consideró que era un caso inicial de trombosis de sitio inusual, y en estos casos se deben realizar estudios exhaustivos dada la alta asociación con trombofilias. Se descartaron patológicas autoinmunes y las trombofilias más comunes, aunque presentaba una importante disminución de la actividad de la proteína C y S de la coagulación.
La proteína C de la coagulación, regula la cascada mediante la proteólisis de los factores V y VIII. El déficit congénito de esta proteína causa un rango amplio de manifestaciones, desde eventos trombóticos leves hasta purpura fulminante en el neonato 8. Se diagnostica con valores < 70 %, pero en este caso con 69 % es poco probable que se asociara a los eventos presentados.
La proteína S es un factor dependiente de la vitamina K, que actúa inhibiendo el factor V activado, además de liberar factor activador de plasminógeno. Su actividad normal se reporta entre el 70 y 150 %; nuestro caso tenía una actividad severamente comprometida, con valor de solo 15 % 9. El déficit congénito de proteína S (DPS) tiene una incidencia de 1 en 20.000 personas y existen 2 tipos de presentación: homocigótica, que causa purpura fulminante a los pocos días de nacimiento, y heterocigota, la cual progresa a la vida adulta presentando eventos trombóticos venosos a repetición 10.
Además de las alteraciones descritas, se encontró un foramen oval permeable; por ende, teniendo un estado protrombótico asociado a un cortocircuito cardiaco, se consideró una alta probabilidad de embolia paradójica.
La EP es un estado patológico caracterizado por el paso de un trombo del sistema venoso hacia la circulación arterial, por medio de un defecto anatómico, usualmente a nivel cardiaco 11. Se asocia principalmente con el ECV, estimándose unos 60.000 casos secundarios a EP. Igualmente, se han descrito casos de infarto agudo de miocardio, infartos renales y enfermedad trombótica periférica.
La relación real entre la EP y la IM es desconocida 12. Se han descrito múltiples criterios para EP, pero se considera necesario la presencia de embolia arterial, un defecto anatómico que permita el paso del embolo y un posible origen venoso del trombo 13. Los estudios de imagen son primordiales para la estratificación de esta patología, el ecocardiograma además de establecer los defectos anatómicos, permite descartar trombos intracardiacos y posibles embolias paradójicas inminentes. Así mismo, es necesario realizar doppler de miembros inferiores para determinar la presencia de trombosis venosa profunda. Otros estudios adicionales se deben solicitar en función del órgano afectado 14.
En este paciente con IM, la edad de 47 años no se asocia a este cuadro en ausencia de los factores de riesgo tradicionales. Se identificó un foramen oval permeable, sin evidencia de trombos intracardiacos; si bien, no se encontró trombosis venosa profunda, padece una trombofilia que se asocia a eventos trombóticos venosos (DPS). Se descartaron trombos arteriales mediante arteriografía, y a pesar del manejo anticoagulante, el paciente presentó un nuevo evento trombótico cerebrovascular parietal 15-17.
El manejo propio de la isquemia mesentérica se basa en manejo de soporte, evitando vasoconstrictores y corrigiendo la acidosis durante el primer contacto médico. En todos los pacientes se debe plantear la revascularización del territorio afectado, siempre que sea viable, preferiblemente por vía endovascular. Nuestro paciente presentó deterioro clínico acelerado, con signos de irritación peritoneal, por lo que la laparotomía exploratoria con resección de las asas necróticas fue el manejo de elección, siempre intentando conservar la mayor cantidad de intestino posible 18.
Una vez manejada la situación crítica, se debe realizar una correcta estratificación de la EP. Estos pacientes tienen un alto riesgo de recurrencia de eventos trombóticos, por lo cual, la anticoagulación plena debe ser la primera estrategia implementada en estos pacientes. No hay estudios disponibles que favorezcan un tipo de anticoagulante sobre el otro en el contexto de EP 19. El siguiente paso es el manejo del defecto anatómico. En cuanto al foramen oval permeable, el cierre endovascular es la terapia más recomendada en la literatura, con el fin de evitar recurrencias 20- 21. En nuestro caso no fue posible realizar este procedimiento dado el continuo deterioro que presentó el paciente.
Conclusión
La embolia paradójica es una patología rara, que se debe sospechar en casos de trombosis de sitios inusuales, en los cuales se documentan cortocircuitos arteriovenosos que hagan posible el paso de trombos de la circulación venosa a la arterial. Es necesario en todos los casos descartar trombofilias u otros estados protrombóticos, con el fin de estratificar el riesgo de recurrencia. A la par del manejo de las manifestaciones trombóticas, se debe iniciar manejo anticoagulante a dosis plena y plantear corrección del defecto anatómico.















