Introducción
El tumor sólido pseudopapilar de páncreas (TSSP), conocido también como tumor de Frantz, es una entidad poco frecuente, que corresponde al 5 % de los tumores quísticos pancreáticos, al 0,9-2,7 % de todos los tumores exocrinos y al 0,2-0,7 % de todos los tumores del páncreas 1. Suele presentarse con mayor frecuencia en mujeres jóvenes, entre la tercera y cuarta década de la vida 1 y su origen aún no se conoce completamente.
Los síntomas más frecuentes son dolor abdominal, hasta en el 35 % de los casos, masa abdominal, náuseas, vómito, pérdida de peso, anorexia e ictericia 2. Cuando la lesión se encuentra localizada, el tratamiento de elección es la cirugía sin linfadenectomía, dejando márgenes negativos; mientras que, en casos de enfermedad localmente avanzada o metastásica, se debe individualizar el manejo y discutir la cirugía como opción terapéutica 3.
El interés especial de este reporte de caso es dar a conocer la presentación de un tipo de tumor de páncreas infrecuente, con una clínica inespecífica, cuya adecuada sospecha diagnóstica resultó en un abordaje terapéutico óptimo, con buenos resultados oncológicos y pronóstico favorable.
Caso clínico
Paciente femenina de 24 años de edad, quien consultó por sensación de masa dolorosa en región epigástrica de tres semanas de evolución, aumento progresivo del tamaño y síntomas dispépticos, asociado a disminución de ingesta alimentaria por plenitud gástrica temprana y emesis ocasional de contenido biliar.
Al examen físico abdominal la paciente presentaba leve dolor a la palpación en epigastrio y flanco izquierdo, sin signos de irritación peritoneal y no se palpaban masas ni megalias. Dado los hallazgos del examen físico se solicitó una tomografía computarizada (TC) de abdomen con medio de contraste, que documentó una lesión hipodensa de características heterogéneas, con bordes bien definidos y dimensiones de 108 x 90 x 98 mm, la cual se encontraba en íntimo contacto con la cola de páncreas (Figura 1).
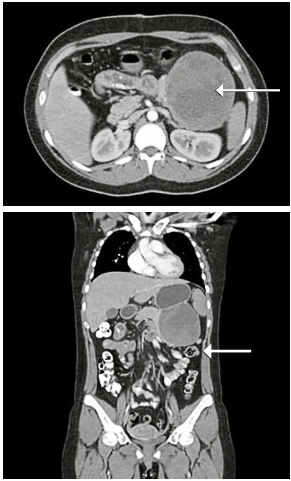
Figura 1. Tomografía computarizada de abdomen con medio de contraste, cortes axial y coronal, donde se observa la lesión en el hipocondrio izquierdo, en vecindad al bazo.
Con la presunción diagnóstica de un tumor de origen pancreático, se realizó una laparotomía mediana supraumbilical, encontrando una masa de 14 x 13 cm, dependiente del cuerpo del páncreas, en íntimo contacto con el meso del colon transverso, la fascia de Gerota, la glándula suprarrenal e infiltración del hilio esplénico. Se realizó pancreatectomía distal radical con esplenectomía y omentectomía parcial en bloque (Figura 2). La paciente tuvo una adecuada evolución postoperatoria, sin complicaciones y egresó al séptimo día.
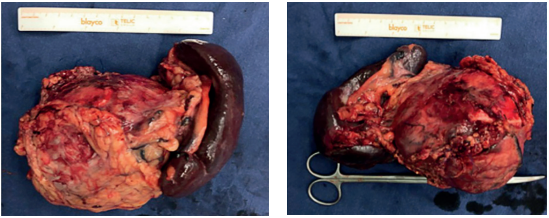
Figura 2. Pieza quirúrgica. Tumor de 14 x 13 cm dependiente del cuerpo del páncreas, en contacto con el meso del colon transverso, la fascia de Gerota, la glándula suprarrenal e infiltración del hilio esplénico.
El estudio histopatológico informó una masa de 140 mm de diámetro mayor, con componente sólido y quístico, con pseudocápsula, compatible con neoplasia sólida pseudopapilar del páncreas en la tinción de hematoxilina y eosina. Los márgenes de sección estaban libres de tumor y la inmunohistoquímica evidenció positividad para betacatenina, receptores de progesterona y andrógenos. A nivel local se expuso positividad para Ciclina D1 y CKAE1AE3, con un índice de proliferación celular Ki-67 del 5 % (Figura 3).
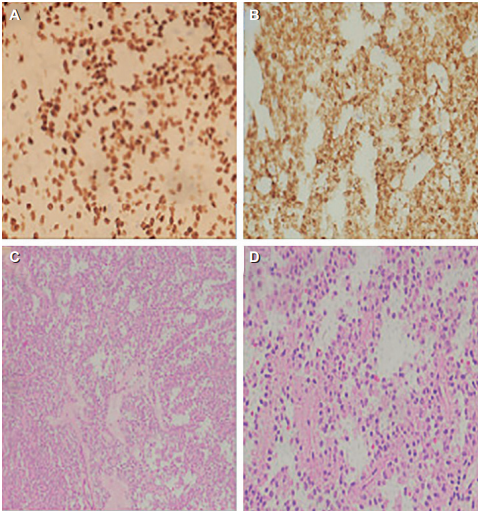
Figura 3. A: positividad de receptores de progesterona nuclear. B: betacatenina positividad nuclear. C y D: tinción de hematoxilina y eosina mostrando el patrón pseudopapilar.
Se hizo seguimiento a los tres y seis meses, con una evolución favorable y adecuada calidad de vida. Hasta el momento permanece sin signos clínicos de recaída local o a distancia.
Discusión
Dentro de las neoplasias pancreáticas poco frecuentes y de bajo potencial de malignidad podemos encontrar el tumor sólido pseudopapilar de páncreas, conocido también por los nombres de “tumor de Frantz”, “neoplasia quística papilar”, o “neoplasia epitelial papilar sólida”. Fue descrito por la patóloga Virginia Kneeland Frantz en 1959 y denominado en 1996 por la Organización Mundial de la Salud (OMS) como tumor sólido pseudopapilar 4.
La etiología del TSSP no es del todo conocida. Existen teorías que sugieren una posible relación hormonal en el desarrollo de esta neoplasia, debido a la frecuente presencia de receptores de progesterona evidenciados en los estudios de inmunohistoquímica 3, sin embargo, otros reportes han asociado este tipo de neoplasia a alteraciones genéticas, ya que se han descrito casos asociados de poliposis adenomatosa y mutaciones en el exón-3 del gen β-catenina 2.
La β-catenina es una molécula que mantiene la adhesión entre células epiteliales y regula la transcripción genética de algunas vías de señalización celular como la vía Wnt/ β-catenina. Mutaciones en este exón se asocian con una alteración en la regulación del ciclo celular y aumento de la degradación de β-catenina que desencadena sobreexpresión de ciclina D1, ciclina D3 y perdida de la unión entre β-catenina y E-Cadherina, hallazgos asociados según el reporte de la inmunohistoquímica de este caso, lo que produce adhesividad celular reducida y formaciones pseudopapilares 5.
Los análisis proteómicos en el TSSP muestran que las proteínas implicadas en la señalización de Wnt/β-catenina (CTNNB1 y DKK4) y las proteínas que se unen directamente a la β-catenina (FUS, hnRNPM, BGN, NONO, YWHAZ, DDX5, SELENBP1 y FN1) están elevados en estos tumores. Los índices de proliferación tumoral como el Ki-67 suelen ser bajos e inferiores al 5 %, indicando un crecimiento tumoral lento y un buen pronóstico 2.
Macroscópicamente, este tipo de tumores exhiben características similares a las observadas en el caso presentado, con un componente sólido y quístico con áreas de hemorragia, calcificaciones, y una cápsula fibrosa. Los hallazgos histopatológicos describen células epitelioides poligonales de aspecto neoplásico, pequeñas, monomorfas, que no tienen una disposición cohesiva, de citoplasma eosinofílico carente de mucina, con núcleos ovalados o redondos, con un patrón de cromatina fino y nucleósidos ausentes. Dichas células se encuentran dispuestas libremente alrededor de un estroma hialinizado, vascularizado, con vasos sanguíneos de paredes delgadas 6.
Respecto a la presentación de esta entidad, los síntomas de nuestra paciente coinciden con los más frecuentes descritos en la literatura 2. Los estudios de imágenes habitualmente revelan la presencia de una masa única de gran tamaño, con un promedio de 7-9 cm y características heterogéneas debido a su composición mixta con elementos sólidos y quísticos. Esta masa presenta una forma redondeada, bien definida y está rodeada por una pseudocápsula fibrosa. En la resonancia nuclear magnética abdominal, es posible observar cambios en la intensidad de señal en las secuencias de T1 y T2, que varían en función de la proporción de componentes sólidos, quísticos o hemorrágicos del tumor 6.
En la mayoría de los casos y según la disponibilidad, se prefiere complementar el estudio preoperatorio con ultrasonografía endoscópica y citología por aspiración con aguja fina, con el objetivo de tener un diagnóstico histológico previo al manejo quirúrgico. También es importante resaltar que hasta un tercio de los casos son asintomáticos, y su detección se logra de forma incidental por medio de exámenes imagenológicos realizados por otros motivos 6.
En cuanto al tratamiento de elección para este tipo de tumores, la resección quirúrgica con márgenes negativos sigue siendo la opción preferida, tanto en la enfermedad primaria como en las recurrencias tumorales, debido a su impacto significativo en el pronóstico del paciente. La elección de la técnica depende del tamaño y la ubicación del tumor. En el caso de tumores localizados en la cabeza del páncreas, generalmente se prefiere la pancreatoduodenectomía proximal, mientras que, en los tumores del cuerpo y la cola del páncreas, se recomienda la pancreatectomía distal sin o con esplenectomía, como en este caso 7,8.
A pesar de ser considerado actualmente un tumor maligno, el TSSP se caracteriza por tener un buen pronóstico, con una tasa de supervivencia a 5 años superior al 90 %. Solo entre el 10-15 % de los pacientes presentan la enfermedad con metástasis en su inicio 9. Uno de los estudios con mayor número de pacientes con TSSP, es un metaanálisis coreano publicado en el 2018 10 que buscó describir la evolución clínica y la supervivencia de los pacientes con este tipo de tumor, encontrando metástasis en el 81,4 % y recurrencia de la enfermedad en el 11,9 % de los pacientes. La supervivencia libre de enfermedad fue de 45 ± 6,2 meses y la supervivencia específica de la enfermedad de 152,6 ± 12,8 meses. En el caso descrito, el pronóstico de la paciente ha sido concordante a su estadio clínico, lo cual confirma lo reportado en la literatura al recibir una terapia oportuna.
De acuerdo con varios autores y reportes de caso, se puede presumir que el rol de la quimioterapia y radioterapia no está bien definido en la literatura, existen pocos reportes que describen su uso. Los casos de TSSP tratados con quimioterapia y radioterapia muestran beneficio en un número limitado de pacientes. En cuanto a la quimioterapia se ha descrito el uso de Gemcitabine, 5-Fluoracilo, Adriamicina, Mitomicina C y Cisplatino 11,12.
Los sitios más frecuentemente afectados en la enfermedad con progresión local o regional son duodeno, bazo, vena porta, vasos mesentéricos superiores, vías biliares y ganglios linfáticos. La presentación con compromiso metastásico suele afectar hígado, pulmón, peritoneo y piel. Se ha visto que en aquellos casos en donde existe documentación de enfermedad metastásica o progresión local avanzada, se conserva una adecuada tasa de supervivencia, debido a la lenta progresión de la enfermedad 13,14.
Conclusiones
El tumor sólido pseudopapilar es una neoplasia quística exocrina poco común, que presenta desafíos en su diagnóstico y tratamiento debido a sus manifestaciones clínicas inespecíficas. Este caso resalta la importancia de reconocer y abordar esta patología de manera temprana y adecuada, lo cual proporciona oportunidades para una intervención quirúrgica oportuna y reduce el riesgo de progresión local o metastásica de la enfermedad, mejorando el pronóstico y la calidad de vida del paciente.















