INTRODUÇÃO
O craveiro-da-índia é uma árvore de ciclo perene, que cresce a uma altura que varia de 10 a 12 metros, possui folhas ovais grandes e flores de cor vermelha que se apresentam em numerosos grupos de cachos terminais [1]. Essa planta vive por cerca de 100 anos e há alguns recordes de árvores atingindo 150 anos [2].
O cravo-da-índia é colhido na forma de botão floral maduro e comercializado na forma de botão floral seco, sendo a qualidade do produto (cravo com cabeça proveniente de botão colhido antes da antese) primordial para a obtenção de melhores preços no mercado nacional e internacional. Os botões florais do craveiro-da-índia são colhi dos com pedicelo, e estes são eliminados durante o processo de destalamento. Além disso, grande quantidade de folhas é derrubada durante o processo de colheita, seja ele manual ou químico. Tais resíduos provenientes da colheita também constituem fonte de óleos essenciais [3]. Os botões florais adquirem primeiro uma cor pálida e, gradual mente tornam-se verdes, então eles se tornam vermelho brilhante quando prontos para a coleta. Os botões são colhidas quando chegam a ter 1,5 - 2 cm de comprimento [1]. Das sementes de aroma ativo, extrai-se o ácido eugênico, incolor e de sabor picante. Sua composição química é constituída principalmente por eugenol, acetato de eugenol, [3]-cariofileno, ácido oleânico, e substâncias das classes: triterpeno, ceras vegetais, cetonas, resinas, taninos e esteróis [4].
O óleo essencial do botão do cravo é pouco produzido, embora sua procura seja grande. O botão contém 17% de óleo essencial e o talo que o acompanha contém 4,5 - 6,0% [5]. O principal componente do óleo de cravo é geralmente considerado como eugenol seguido pelo (3-cariofileno e menores quantidades de outros componentes, tais como álcool benzílico, mas as proporções variam amplamente [6].
Com a finalidade de manter os pesquisadores ou mesmo leitores leigos informados, Affonso e colaboradores [7] descrevem em seu trabalho informações uteis sobre o Syzygium aromaticum, tais como: os aspectos históricos, a composição química, aplicações e as principais atividades que foram obtidas a partir do óleo essencial dessa espécie.
Nesse contexto, este trabalho avalia analiticamente as propriedades físico-químicas e a citotoxicidade do óleo essencial dos botões do cravo-da-índia (Syzygium aromaticum) que são comercializadas em supermercados da rede varejista do Munícipio de São Luís.
METODOLOGIA
Obtenção dos botões florais
Os botões florais foram obtidos em supermercado da rede varejista de São Luís, iden tificados como (Syzygium aromaticum) e levados ao laboratório de Físico-Química de Alimentos do Pavilhão Tecnológico da Universidade Federal do Maranhão (UFMA), para extração do óleo essencial.
Extração do óleo essencial
Para a extração do óleo essencial do Syzygium aromaticum, 68,79 g desses botões florais foram triturados em um moinho elétrico de facas da marca Tecnal-modelo TE340.
Após esse procedimento, o material foi transferido para um balão de fundo redondo com capacidade de 1000 mL, onde efetuou-se a adição de 200 mL de água destilada e o acoplamento ao extrator de Clevenger.
Em seguida ligava-se a manta elétrica e mantinha-se a temperatura em 100 °C. Após 4 horas, encerrava-se a destilação recolhendo-se o óleo essencial. O óleo foi seco por meio de percolação em sulfato de sódio anidro (Na2SO4). Essas operações foram realizadas em triplicatas e as amostras armazenadas em ampolas de vidro âmbar sob refrigeração para evitar possíveis perdas de constituintes voláteis. Posteriormente esses óleos foram submetidos às análises.
O rendimento do óleo essencial foi expresso em porcentagem na relação massa/volume pela medida da densidade, observando o volume (mL) de óleo essencial obtido após a extração do óleo por massa (g) de material vegetal, conforme descrito pela Farmaco peia Brasileira [8] e Fabrowski [9].
Análise físico-química do óleo essencial
As propriedades físico-químicas do óleo essencial determinadas foram: densidade, solubilidade em etanol a 70% v/v, índice de refração, cor e aparência.
Análise química do óleo essencial
Para as análises químicas, utilizou-se a técnica cromatografia em fase gasosa acoplada ao espectrómetro de massas por impacto de elétrons e analisador íon trap (CG-EM-IE -Ion trap). O equipamento utilizado foi da marca Varian 2100, utilizando hélio como gás de arraste com fluxo na coluna de 1mL min-1; temperatura do injetor de 280 °C, split 1:10; coluna capilar (15 m x 0,25 mm) com fase estacionária VF-1ms (100 % metilsiloxano 0,25 µm) e programação de temperatura do forno de 40 °C a 240 °C com taxa de aquecimento de 8° C min-1. No Espectrómetro de Massas, as temperaturas do mainfold, ion trap e da linha de transferência foi de 280 °C. Foram injetadas alíquotas de 0,3 µL (injetor automático CP-8410) das amostras diluídas na proporção de 1mg da amostra em 1000 µL de diclorometano.
A determinação da concentração do eugenol e dos demais componentes do óleo essen cial por esse método foi obtida através da integração eletrónica das áreas dos picos cromatográficos, utilizando o programa AMDIS (Automated Mass Spectral Deconvolution Mass & Identification System): Programa utilizado para a interpretação dos espectros de massas quando havia diferenças significativas entre o espectro de massas obtido e o encontrado na biblioteca do CG/EM.
Bioensaio do óleo essencial frente a Artemia salina
A metodologia utilizada para os ensaios de citotoxicidade utilizando Artemia salina foi baseada em Meyer et al. [ 10] e em Nascimento et al. [ 11].
Em um recipiente retangular, com uma divisória contendo furos de aproximadamente 0,02 cm de espessura espaçada por 0,5 cm e distribuídos uniformemente, foram adi cionados (60 g de sal marinho/ 1 L de água destilada) de solução salina artificial. O recipiente foi colocado dentro de uma incubadora iluminada por uma lâmpada fluo rescente, com aeração (figura 1). Em um dos lados desse recipiente, adicionou-se cerca e 64 mg de cistos de Artemia salina, tomando-se o cuidado para que os mesmos não ultrapassassem a divisória. A parte do sistema contendo os cistos de Artemia salina foi coberta com papel alumínio, para que os organismos ao nascerem, fossem atraídos pela luz do outro lado do sistema, forçando-os a atravessar à divisória. Tal procedimento visa uma homogeneização das condições físicas dos organismos-teste. A incubação foi feita por um período de 48 horas. Durante todo o ensaio a temperatura foi monitorada.
Após o período de incubação, os organismos-testes (náuplios de Artemia salina) foram expostos ao óleo essencial do cravo-da-índia por 24 horas, utilizando-se tubos de ensaio graduados, cada um contendo 10 náuplios de Artemia salina, previamente seleciona dos. Os testes foram feitos em triplicata para cada concentração de cada composto. Além disso, o óleo foi testado, no mínimo, três vezes, totalizando um mínimo de 9 ensaios por concentração do composto. Determinou-se a faixa de concentração a ser testada (correspondente à concentração de 1000, 100, 10 μg/mL), buscando sempre a maior concentração em que se observasse 0% de mortalidade e a menor concentração em que se deflagrasse 100 % de mortalidade, de modo a obter a DL50; 24 h (dosagem letal para 50 % da população em 24 h) do composto testado. As soluções dos com postos a serem testadas foram preparadas em 1 a 3 % de DMSO (dimetilsulfóxido) e avolumadas com solução salina. Os testes para o controle também foram realizados em triplicata, utilizando-se uma solução de DMSO 1 a 3 % diluído em solução salina. Os controles foram utilizados também para se ter certeza de que a mortalidade obser vada nos náuplios de Artemia salina fosse resultante da toxicidade aos compostos e não devido à falta de alimentação [12].
Após 24 horas de exposição, foi feita a contagem de náuplios vivos e mortos, sendo con siderados vivos todos aqueles que apresentassem qualquer tipo de movimento quando observados próximos a uma fonte luminosa por 10 segundos. Só foram considerados válidos os testes nos quais o controle apresentou uma mortalidade igual ou inferior a 10 % da população. Os resultados foram submetidos a tratamento estatístico utilizando a regressão linear, o qual forneceu os valores de DL50; 24 h.
RESULTADOS E DISCUSSÃO
Características físico-químicas
A qualidade dos óleos essenciais depende de vários parâmetros tais como índice de refração, solubilidade em diferentes solventes orgânicos, densidade, dentre outros, os quais são utilizados para a avaliação da qualidade da matéria prima vegetal, além do controle da identidade e da pureza do óleo. Segundo Mouchrek Filho [13] o tempo de extração do óleo essencial é um dos principais parâmetros físico-químicos da indústria de essências, no que se refere à qualidade e à natureza económica. Por isso, uma desti lação rápida pode conduzir a um produto contendo predominantemente constituintes mais voláteis, porém destituído das melhores características; ao contrário, uma extra ção prolongada encarece o produto e também pode sobrecarregá-lo de compostos de aromas indesejáveis [14].
Os resultados referentes aos parâmetros físico-químicos do óleo essencial do cravo-da-índia estão representados na tabela 1.
Os resultados mostraram valores de 1,526 e 0,973 g mL-1 para o índice de refração e densidade do óleo essencial do cravo-da-índia respectivamente. No que se refere à solubilidade em etanol 90 %, o resultado demonstrou que o óleo essencial foi solúvel na proporção 1:2. A cor e aparência apresentada pelo óleo analisado foram consideradas sendo típica, ou seja, transparente e límpido como foi mostrado na tabela 1, afirmando que o óleo essencial estudado possui uma cinética de extração e qualidade muito eficaz, quando comparado a outros óleos, principalmente em relação à quantidade de óleo extraído (volume) e tempo de extração.
Reis [15] investigando os óleos essenciais extraídos dos talos e frutos secos do cra-vo-da-índia, relatou um índice de refração 1,5230 e 1,5252 respectivamente, valores semelhante ao encontrado nesta pesquisa. Valores esses, próximos ao índice de refração descrito para o eugenol, que é de 1,5410 [16]. A proximidade entre os valores do índice de refração descrito para o eugenol com os valores encontrados para os óleos essenciais dos talos e dos frutos evidenciam que o óleo em estudo é realmente rico em eugenol.
O rendimento da extração pode ser calculado a partir da quantidade de óleo que se obteve com uma determinada massa vegetal. Como nesse experimento, partiu-se de uma massa de 68,79 g dos botões florais secos e moídos do cravo-da-índia e obtiveram-se em média 2,5 mL de óleo essencial em cada extração o rendimento m/v foi de 3,63 %, um bom rendimento. Como a densidade do óleo foi determinada em 0,973 g.mL-1, rendimento m/m foi calculado em 3,54 %.
Segundo Ozcan e Chalchat [17] o rendimento do óleo essencial de diferentes varie dades de plantas é dependente da variação sazonal e da localidade. Sendo assim, de acordo com Reis [15] que apresenta rendimentos de massa/volume do óleo essen cial dos talos e frutos secos do cravo-da-índia em torno de 15 %, o baixo rendimento quando comparado ao estudo acima do óleo essencial dos botões do cravo pode ser atribuído ao fato do período da coleta das amostras e estocagem, ou seja, do clima com altas temperaturas que podem ter favorecido a evaporação parcial de alguns consti tuintes do óleo.
Caracterização química (análise por cromatografia gasosa acoplada a espectrometria de massas)
Por meio da cromatografia gasosa acoplada à espectrometria de massas foi possível separar e identificar cinco constituintes do óleo essencial, os quais são apresentados na figura 2, seguindo a ordem de eluição.
A tabela 2 mostra a identificação de cada pico apresentados na figura 2, assim como o seu tempo de retenção (Tr) na coluna e o respectivo teor na mistura de óleos essen ciais, sendo que a quantificação dos cinco picos cromatográficos foi determinada pelo método de normalização (integração da área do pico correspondente). Nota-se que o eugenol apareceu com 52,53 %, e o cariofileno com 37,25 %, o que caracteriza serem estes os principais componentes majoritários.
Bioensaio da citotoxicidade frente à Artemia salina
Os ensaios de letalidade permitem a avaliação da toxicidade geral e é considerado como um bioensaio preliminar no estudo do potencial biológico de um composto ou pro duto [10]. Atualmente, um dos ensaios mais empregado é o teste com larvas de Artemia salina e vem sendo reportado na literatura, não só para avaliar a toxicidade de substân cias, óleos, produtos e extratos vegetais, como também para determinar grau de conta minações ambientais [18].
O critério de classificação do óleo do Syzygium aromaticum (cravo-da-índia) frente Artemia salina com base nos valores das DL50 foi estabelecido por Dolabella [19] como DL50 < 80 μg/mL, o produto é altamente tóxico; DL50 entre 80 a 250 μg/mL, o pro duto é moderadamente tóxico e DL50 > 250 μg/mL, o produto é levemente tóxico ou atóxico. [10] utilizam o critério de avaliação em que considera a amostra tóxica ou ativa as que apresentarem DL50 < 1000 µg/mL e amostras atóxicas ou inativas as que apresen tarem DL50 > 1000 μg/mL. (Cálculos de DL50).
A importância deste ensaio de toxicidade deve-se ao fato de que vários autores buscam correlacionar a toxicidade sobre Artemia salina com atividades anticancerígena, anti-fúngica, inseticida e tripanossomicida [3,10,20,21,22].
Na tabela 3 e na figura 3 estão expostos os resultados obtidos para o bioensaio frente à Artemia salina para o óleo essencial do cravo-da-índia.
Tabela 3 Porcentagem de mortalidade por doses analisadas e valores de DL50 obtidos no bioensaio com Artemia salina para o oleo essencial do cravo-da-india (Syzygium aromaticum).
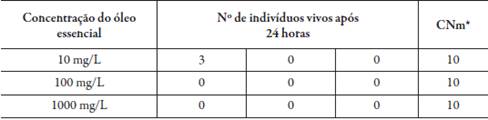
*CNm: media do controle negativo.

Figura 3 (A) Regressão linear do percentual de animais mortos do óleo essencial do cravo-da-índia (DL50); (B) Regressão linear do percentual de animais mortos do padrão de eugenol (DL50).
A dose letal a 50 % (DL50) do óleo essencial do cravo-da-índia (Sygygium aromaticum) a partir do teste de toxicidade (a atividade larvicida frente à Artemia salina, avaliando o grau de letalidade pelo produto) foi igual a 1 μg/mL, considerado altamente tóxico de acordo com [19].
Na tabela 4 estão expostos os valores encontrados para o bioensaio frente à Artemia salina com o componente majoritário do óleo, o eugenol.
Tabela 4 Porcentagem de mortalidade por doses analisadas e valores de DL50 obtidos no bioensaio com Artemia salina para o padrao de eugenol.

*CNm: media do controle negativo.
A dose letal a 50 % (DL50) do padrão de eugenol a partir do teste de toxicidade (a ativi dade larvicida frente à Artemia salina, avaliando o grau de letalidade pelo produto) foi igual a 18,53 μg/mL, considerado altamente tóxico, ou seja ativo, de acordo com [19].
Comparando os resultados tanto do óleo quanto somente do seu componente majori tário, o eugenol, observa-se que ambos são ativos, ou seja, tóxicos frente aos testes com Artemia salina, mostrando eficiência na sua citotoxicidade. Pode-se observar também que o óleo é bem mais tóxico quando comparado ao padrão de eugenol, mostrado nos gráficos de regressão linear para mortalidade do microcrustáceo frente ao óleo testado.
A alta toxicidade do óleo do Cravo-da-índia frente à Artemia salina pode ser apontada pela presença do eugenol que é um forte agente bactericida, fungicida, antimicrobiano, anti-séptico e antialérgico, mas também pela mistura de outros componentes presentes nesse óleo, como por exemplo, o cariofileno e o copaeno que possuem um ótimo poder cicatrizante, diurético, antiinflamatório, aumentando assim o poder de toxicidade do óleo essencial.
Alguns estudos reafirmam o poder do sesquiterpeno cariofileno. Quando isolado do óleo essencial de Cordia verbenacea, este componente mostrou atividade antiinflamatória em diferentes modelos experimentais, utilizando-se nesse caso ratos [23]. Esta atividade do cariofileno também foi demonstrada no estudo da espécie Bupleurum fruticescens, cujo óleo essencial mostrou forte ação antiinflamatória atribuída aos seus dois principais constituintes, α-pineno e cariofileno. A ação farmacológica desses compos tos quando administrados juntos tornou-se similar à do óleo essencial completo de B. fruticescens [ 24]. A administração oral de cariofileno em ratos inibiu significativamente a colite ulcerativa experimental induzida por dextran sulfato de sódio, abrindo cami nho para a prevenção e o tratamento da colite [25].
Também [26] relatou que a administração oral do cariofileno em ratos inibiu signifi cantemente a irritação da mucosa gástrica. Além disto, o composto mostrou atividade antiinflamatória sem nenhuma indicação de causar danos à mucosa gástrica, típicos de agentes antiinflamatórios não esteroidais. O composto óxido de cariofileno, tam bém encontrado em alta proporção no óleo essencial de P. neochilus (15,54 %), é um reconhecido conservante de alimentos e cosméticos. Este sesquiterpeno mostrou ati vidade antifúngica em modelo experimental "in vitro" contra três espécies Trichophyton que causam infestações micóticas nos pés [27]. Vários constituintes de Eugenia caryophyllata foram isolados, identificados e tiveram sua bioatividade analisada. Dentre estes, óxido de cariofileno, cariofileno e α-humuleno mostraram-se potentes agentes anticarcinogênicos [28].
Logo, como teste de triagem, os ensaios com Artemia salina estão se destacando na "indicação de atividade antitumoral". A literatura vem trazendo correlações entre a toxicidade geral com esse microcrustáceo e a citotoxicidade diante de linhagens de células humanas de tumores sólidos [29].
Segundo Mclaughlin [29], o fato de se trabalhar com organismos relativamente sim ples torna mais fácil a indução de um retardo ou paralisação do ciclo celular normal por provocar alteração do processo mitótico, observou uma ótima correlação entre o teste de toxicidade frente Artemia salina e o teste de citotoxicidade, usando células 9 K (car cinoma humano de nasofaringe) e a partir desses resultados, utilizam o teste de Artemia salina como pré-clinico para testes de citotoxicidade com seis linhagens de células tumorais sólidas humanas. Estes autores observaram que a ED50 (dose eficiente 50 %) nos testes de citotoxicidade é geralmente em torno de um décimo da DL50 encontrada no teste com esse microcrustáceo.
CONCLUSÃO
No presente estudo, conclui-se que os parâmetros físico-químicos do óleo essencial do Cravo-da-índia (Syzygium aromaticum) apresentaram resultados satisfatório no que se diz respeito a avaliação da qualidade do óleo extraído. Além disso, houve a iden tificação segura e positiva do componente majoritário pela técnica de Cromatografia Gasosa acoplada à Espectrometria de Massas, CG-EM (baseando-se nos seus tempos de retenção) no qual os botões florais do Syzygium aromaticum, forneceram um óleo essencial cujo rendimento foi de 3,63%, m/v, um valor considerável bom para extração por hidrodestilação. No teste do bioensaio, os resultados mostraram a alta toxicidade do óleo essencial frente às larvas de Artemia salina.


















