Introducción
El citomegalovirus (CMV) es la causa más frecuente de infecciones virales en el postrasplante renal, el CDC de Atlanta establece su prevalencia en 50-80% en adultos mayores de 40 años, con tendencia a aumentar con la edad 1. Su presentación en el postrasplante obedece en la mayoría de los casos, a la reactivación de la infección, favorecida por el estado de inmunosupresión del receptor. Se establece una condición de riesgo, dependiente del estado serológico (IgG para CMV), los receptores que tienen Ig G positiva (R+) son clasificados de riesgo intermedio para reactivación, los receptores Ig G negativa (R-) con donante Ig G negativa (D-) son de bajo riesgo y los R- con D+ son de alto riesgo. En Colombia un estudio realizado en Medellín documentó la presencia de Ig G positiva para CMV en 89% de los pacientes con trasplante renal y en 81% de los donantes 1. Un estudio recientemente publicado que evaluó donantes y receptores en el periodo 2010-2014, incluyó todo el territorio nacional y documentó seroprevalencia para CMV en donantes de 86.2% y en receptores de trasplantes renales de 91% 2, similar a otros países en vías de desarrollo. La distribución del riesgo en este estudio fue 7.3, 91.4 y 1.3% para alto, intermedio y bajo riesgo respectivamente 2.
Otros factores de riesgo identificados son: edad avanzada (>60 años), trasplante riñón-páncreas, antecedente de rechazo agudo y el uso de medicamentos como ciclosporina e inmunoglobulina antitimocito, la cual aumenta dos a cinco veces el riesgo 3.
La reactivación de infecciones ocurre frecuentemente entre el primero y cuarto mes, coincidiendo con las dosis más elevadas de terapia inmunosupresora; sin embargo, pasados los seis primeros meses puede ocurrir infección o enfermedad tardía 4. Los pacientes trasplantados desarrollan infección o enfermedad 5, el diagnóstico de infección es basado en la detección de CMV en sangre periférica (virus, proteínas virales o ácidos nucleicos) y el de enfermedad por la presencia de síntomas y signos clínicos.
En ausencia de medidas preventivas, la frecuencia de reactivación de infección es de 40-100% y de enfermedad a 67% 6; por esto se diseñaron estrategias de prevención, siendo al momento las dos principales: profilaxis universal y terapia anticipada o preemptive7. La profilaxis universal implica la administración de antivirales después de los 10 días del trasplante por un tiempo definido de tres a seis meses, ganciclovir y valganciclovir tienen similar efectividad 8 con la preferencia de este último, debido a su biodisponibilidad y vía de administración.
La literatura muestra diferentes porcentajes de infección y enfermedad, dependientes del medicamento que se haya usado para la inducción. Grecia reporta datos de infección de 12.8% y enfermedad 3.9% 6; modelos previos con pacientes de riesgo intermedio en Estados Unidos determinan infección en profilaxis universal 5.7% y en anticipada 55.5%, con enfermedad en 6.3% de los casos en el primer año 9.
La importancia del estudio de esta entidad, no sólo radica en su alta prevalencia e incidencia, sino en la asociación que ha tenido con varios desenlaces adversos, derivados de la presentación de enfermedad o efectos indirectos asociados a la infección. El más frecuentemente descrito es el aumento en la incidencia de rechazo del injerto. También se asocia con fibrosis intersticial y atrofia tubular en los tres meses postrasplante; aumento del riesgo de infecciones asociadas como Candida, Pneumocystis jirovecci, Aspergillus y virus como Epstein Barr, herpes virus seis y ocho; mayor riesgo cardiovascular y estenosis de la arteria renal 5. Por último, puede producir un aumento de la mortalidad de 2.5-2.9 veces mayor en los pacientes trasplantados 3.
Es importante conocer estadísticas locales, por ello se realiza la descripción de las características clínicas de los pacientes trasplantados renales en nuestra institución que presentan infección- enfermedad por citomegalovirus y comparar nuestros resultados con los datos de otros grupos de trasplante tanto a nivel nacional como internacional dado que la incidencia y prevalencia tiene variación económica, geográfica y factores étnicos. Adicionalmente, no hay datos en nuestro país sobre la densidad de incidencia.
Material y métodos
Se realiza un estudio observacional analítico, tomando una cohorte retrospectiva de pacientes mayores de 18 años, trasplantados renales de donante vivo o cadavérico entre 2004 y 2015, con al menos seis meses de seguimiento. Los datos se obtuvieron de los registros de la historia clínica electrónica y de los resultados de los laboratorios que se les ha practicado a los pacientes durante el seguimiento.
Se realizó el análisis descriptivo de las variables socio-demográficas y clínicas de la población del estudio. Para las variables categóricas se usaron medidas de frecuencias absolutas y relativas. Para las variables continuas se utilizaron medidas de dispersión y de tendencia central de acuerdo con su distribución. En casos de distribución normal se utilizaron promedios y desviaciones estándar, para variables con distribución no normal se utilizaron medianas y rangos. Se estimó la densidad de incidencia para enfermedad e infección por citomegalovirus, tomando como numerador el número de eventos y como denominador el tiempo a riesgo de cada paciente hasta la fecha en que culminó el seguimiento, tuvo el último control en la institución o hasta la muerte. El análisis se realizó en el programa STATA 12.0.
Criterios de inclusión
Pacientes mayores de 18 años trasplantados renales de donante vivo y cadavérico en un centro de trasplante en el periodo 2004-2015.
Criterios de exclusión
Paciente que no tenga datos de seguimiento en este centro de trasplante
Pacientes con menos de seis meses de trasplante a la fecha final del estudio.
Para efectos de este trabajo, se emplearon las siguientes definiciones:
Trasplante renal riesgo intermedio para CMV: estado serológico usando IgG para CMV, todos los receptores con IgG positiva (R+).
Riesgo Alto para CMV: D+/R-
Riesgo Bajo para CMV: D-/R-
Infección por CMV: positividad en la reacción en cadena de la polimerasa (PCR) para CMV en ausencia de síntomas 11.
Enfermedad por CMV: Positividad en la PCR para CMV con presencia de síntomas, sea síndrome viral con fiebre, malestar, leucopenia o invasiva 11.
Resultados
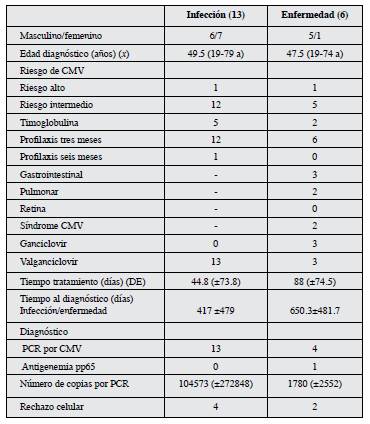
Se realizaron 254 trasplantes renales desde enero 1°. de 2004 hasta 31 diciembre de 2015; de éstos 252 cumplieron los criterios de inclusión. La seroprevalencia para Ig G se distribuyó en: riesgo intermedio 92.4% (233 pacientes) y 7.5% riesgo alto (19 pacientes), no se encontraron pacientes de bajo riesgo en esta cohorte. Doscientos cincuenta pacientes recibieron profilaxis universal con valganciclovir durante 90 días y dos pacientes clasificados como riesgo alto se extendieron a 180 días. Se identificaron 19 casos, 13 con infección (5.1%) y seis con enfermedad (2.3%) (Tabla 1).
La tasa de infección 10.08 casos por 1000 pacientes/año y la tasa de enfermedad 5.88 por 1000 pacientes/año. Se presentaron dos casos de infección temprana, antes de los 100 días y tres casos de enfermedad tardía, después de un año de trasplante.
El compromiso gastrointestinal fue el más frecuente (tres de seis pacientes), manifestándose como colitis, seguido por el compromiso pulmonar que se presentó como neumonitis por CMV (dos de seis pacientes).
El efecto adverso asociado al tratamiento que se presentó con mayor frecuencia fue leucopenia en 25% de los casos. La mortalidad fue 5%, correspondiente a un paciente con compromiso gastrointestinal, dado por úlceras gastrointestinales.
Discusión
La infección por CMV es la infección viral que se presenta con mayor frecuencia en el postrasplante renal. La distribución de riesgo intermedio y alto para reactivación de infección en el postrasplante, es similar a la reportada en estudios a nivel nacional e internacional 2,5. Ningún paciente fue de bajo riesgo, por ello todos los pacientes recibieron profilaxis universal. La densidad de incidencia de infección y enfermedad por CMV fue baja, lo que probablemente se explica por el uso de profilaxis universal. El medicamento utilizado para este fin, fue valganciclovir, de acuerdo con las guías internacionales. Dada la baja frecuencia de eventos, no fue posible establecer asociación con la terapia de inducción utilizada.
El tiempo de aparición de la infección fue en promedio 1.3 años postrasplante, dos casos se presentaron antes de terminar la profilaxis universal. Dado el diseño del estudio, no se lograron establecer factores asociados con la aparición de infección durante la fase de profilaxis. El diagnóstico en la mayoría de los casos se hizo con carga viral por PCR, que es el estándar de oro, sólo en un caso, el diagnóstico se hizo con antígeno pp65, ya que en ese momento no estaba disponible la PCR. En un caso de enfermedad, con compromiso gastrointestinal, confirmado por colonoscopia (úlcera en ciego) y patología (efectos citopáticos por CMV), la carga viral fue negativa. Recordamos que en casos de enfermedad que afecta tracto gastrointestinal o retina, la carga viral en sangre puede ser negativa y ello no descarta el diagnóstico. Esta es una infección que conlleva mayor morbimortalidad, por ello debe estar dentro de los diagnósticos diferenciales de patologías infecciosas en el paciente inmunosuprimido, la mortalidad en esta cohorte fue 5%.
Este estudio tiene las limitaciones propias de un estudio retrospectivo, corresponde a un solo centro, lo que puede limitar la generalización de los resultados. Dada la baja frecuencia de eventos, no fue posible establecer asociaciones.
Conclusiones
En la cohorte de pacientes trasplantados, la densidad de incidencia de infección-enfermedad por CMV en pacientes trasplantados renales fue de 10.08 casos y 5.88 casos por 1000 pacientes/año, respectivamente. Estas tasas son menores a los reportados en la literatura, el uso de profilaxis universal en todos los pacientes puede contribuir a estos hallazgos.