Introducción
La cardiopatía isquémica continúa siendo la principal causa de muerte en países desarrollados, y ha aumentado su letalidad en los países en vía de desarrollo. Estudios recientes han subrayado un descenso en la mortalidad aguda y a largo plazo después de un infarto agudo de miocardio con elevación del segmento ST (SCACEST), en paralelo con un aumento de la terapia de reperfusión, intervención coronaria percutánea (ICP) primaria, tratamiento antitrombótico moderno y tratamientos de prevención secundaria1-4. A pesar de esto, la mortalidad de los pacientes es elevada, lo que justifica los esfuerzos continuos por mejorar la calidad de la atención, la adherencia a las guías y la investigación1.
En Cuba, las enfermedades isquémicas del corazón alcanzaron una tasa de mortalidad en el año 2020 de 165.8 defunciones por cada 100,000 habitantes. En esta, el infarto de miocardio ocupa un lugar preponderante, con una tasa de mortalidad de 69.7 fallecidos por 100,000 habitantes, superior a las cifras del año precedente4.
En diversos estudios se ha demostrado que tanto el recuento leucocitario como la glucemia, de forma independiente o en conjunto, se relacionan con la génesis y progresión de la enfermedad aterosclerótica, así como con la extensión y las complicaciones del IAMCEST5-10. En años recientes se ha hecho referencia al valor combinado de estos dos elementos, siendo Quiroga et al.11, en 2010, los primeros en proponer el índice leucoglucémico (ILG) como un marcador pronóstico de muerte y complicaciones intrahospitalarias en pacientes con IAMCEST, con un punto de corte en 1 600. La ventaja de este índice radica en la evaluación, en conjunto, del efecto sinérgico de la respuesta inflamatoria e hiperglucémica, lo que aumenta la utilidad práctica y clínica de ambos parámetros complementarios.
Basado en lo anteriormente descrito, se diseñó el presente estudio con los objetivos de identificar la asociación entre el ILG y la aparición de complicaciones intrahospitalarias durante el IMACEST, y determinar si el ILG es un marcador predictivo de complicaciones intrahospitarias.
Materiales y métodos
Tipo de estudio y participantes
Se realizó un estudio analítico, observacional, multicéntrico, longitudinal, de cohorte histórica, con los datos almacenados en la Red Cubana de Infarto de Miocardio Agudo (RECUIMA), proyecto multicéntrico de siete hospitales ubicados en seis provincias cubanas, creado con el objetivo de almacenar, organizar y manipular datos de forma homogénea en unidades coronarias u otras unidades asistenciales del sistema nacional de salud que atienden pacientes ingresados con infarto agudo de miocardio (IAM)12,13. En esta cohorte observacional nacional, se incluyeron, de forma consecutiva, 1,548 pacientes diagnosticados con IAMCEST desde enero de 2018 hasta junio de 2021; se excluyeron 415 pacientes que no cumplían los siguientes criterios de inclusión: 1) diagnóstico de IAMCEST, según los criterios clínicos y electrocardiográficos definidos en la Cuarta Definición Universal del Infarto del Miocardio;14 2) realización de conteo total de leucocitos y glucemia en las primeras 24 horas del ingreso hospitalario, y 3) ausencia de enfermedad inflamatoria sistémica, infecciosa o hematológica conocida en el momento del ingreso. Finalmente, 1,133 pacientes se incluyeron en este análisis.
Se extrajeron de la base de datos distintas variables clínicas y epidemiológicas: edad, sexo, antecedentes personales (diabetes mellitus, hipertensión, dislipidemia, tabaquismo, infarto cardiaco, accidente cerebrovascular e insuficiencia renal crónica), y la clase Killip-Kimball al ingreso. Se consideró tabaquismo al hábito de fumar en el momento del ingreso o haberlo hecho en algún momento de la vida. Se registraron también la terapia de reperfusión empleada (fibrinólisis o intervención coronaria percutánea), las complicaciones intrahospitalarias y el estado al egreso (vivo o fallecido), así como distintos exámenes de laboratorio realizados en las primeras 24 horas del ingreso (creatinina, triglicéridos, glucemia y leucograma).
La investigación se realizó bajo los principios establecidos en la Declaración de Helsinki, y fue aprobada por el Comité de Ética de la investigación del Hospital General Docente “Enrique Cabrera”.
Definición del ILG y desenlace final
El constructo ILG fue calculado como glucemia (mmol/L) x 18 x leucograma (109/L), derivado de estudios previos15-21. El evento primario analizado fue definido como complicaciones ocurridas durante el internamiento hospitalario: mecánicas, arritmias, pericarditis, insuficiencia cardiaca, shock cardiogénico, angina, reinfarto, entre otros, excepto la muerte. Los participantes fueron estratificados en cuatro grupos, de acuerdo con los cuartiles calculados para el ILG.
Análisis estadístico
La información fue procesada por el paquete estadístico IBM® SPSS® (Statistical Product and Service Solutions) versión 19.0.0. Las variables continuas tuvieron una distribución normal de acuerdo con la prueba de Kolmogorov-Smirnov; fueron presentadas como media ± desviación estándar, y las diferencias entre los grupos se analizaron con la prueba de t de Student para muestras independientes; ante eventos que involucraron más de dos grupos de variables cuantitativas y fue necesario efectuar el análisis de varianza (ANOVA de un factor). Las variables categóricas se presentaron como frecuencias y porcentajes. Para su asociación se utilizó el test de chi cuadrado de Pearson o la prueba exacta de Fisher. El nivel de significación estadística utilizado fue de p < 0.05 con un intervalo de confianza del 95%.
Se calculó el ILG con la fórmula presentada anteriormente. El rendimiento se evaluó mediante la discriminación y la calibración. La discriminación del ILG se evaluó con el estadístico C, también denominado área bajo la curva ROC (receiver operating characteristic); se determinó como valor aceptable de discriminación cuando el AROC superó el valor de 0.7. Se utilizó el índice de Youden para obtener el punto de corte óptimo, con lo cual se dividió el universo en dos grupos. La calibración se midió al evaluar la bondad del ajuste a través de la prueba C de Hosmer-Lemeshow. La ausencia de significación (p > 0.05) indicó una buena calibración. El test de correlación de Pearson fue usado para evaluar las correlaciones entre el ILG y los factores de riesgo coronario.
El valor predictivo de las variables para el evento primario fue evaluado a través del análisis de regresión logística univariada y multivariada. Las variables iniciales con buena correlación en el análisis univariado con el desenlace final, fueron incluidas en el modelo multivariado. Se evaluó nuevamente el rendimiento del modelo con la curva ROC.
Se realizó el análisis de supervivencia de Kaplan-Meier para evaluar la incidencia de eventos adversos entre los grupos de acuerdo con el punto de corte óptimo del ILG; las diferencias entre los grupos fueron evaluadas con una prueba de rango logarítmico.
Resultados
Características del universo relacionado con el ILG
La edad media de los pacientes fue de aproximadamente 64 ± 11.9 años. En la tabla 1 se presentan las características clínicas y de laboratorio de los participantes. Los pacientes fueron divididos en cuartiles de acuerdo con el ILG al ingreso; los niveles medio del ILG en cada grupo fueron 755.8 ± 118.8; 1 056.8 ± 81.4; 1 426 ± 149.4 y 1 501.2 ± 1 057.7; respectivamente. Entre los cuatro grupos existieron diferencias significativas al tener en cuenta el antecedente de diabetes mellitus, clase funcional Killip-Kimball ≥ II, creatinina, triglicéridos, glucemia, leucograma, complicaciones intrahospitalarias y estado al egreso (todos con p < 0.001).
Tabla 1 Características basales de cada grupo
| Variable | Cuartil 1 (n = 282) | Cuartil 2 (n = 286) | Cuartil 3 (n = 282) | Cuartil 4 (n = 283) | p |
|---|---|---|---|---|---|
| ILG | 755.8 ± 118.8 | 1056.8 ± 81.4 | 1426.1 ± 149.4 | 1501.2 ± 1057.7 | < 0.001 |
| Edad, años | 64.8 ± 12.2 | 63.8 ± 11.4 | 64.6 ± 11.9 | 64.58 ± 12.0 | 0.752 |
| Sexo masculino | 196 (69.5) | 213 (74.5) | 198 (70.2) | 186 (65.7) | 0.156 |
| Antecedentes personales | |||||
| Hipertensión | 207 (73.4) | 220 (76.9) | 221 (78.4) | 230 (81.3) | 0.158 |
| Diabetes | 32 (11.3) | 43 (15.0) | 54 (19.1) | 143 (50.5) | < 0.001 |
| Fumador | 162 (57.4) | 175 (61.2) | 162 (57.4) | 155 (54.8) | 0.487 |
| Dislipidemia | 12 (4.3) | 11 (3.8) | 17 (6.0) | 19 (6.7) | 0.351 |
| IMA previo | 18 (6.4) | 26 (9.1) | 15 (5.3) | 25 (8.8) | 0.236 |
| IRC previa | 5 (1.8) | 6 (2.1) | 5 (1.8) | 13 (4.6) | 0.096 |
| AVE previo | 9 (3.2) | 11 (3.8) | 10 (3.5) | 12 (4.2) | 0.925 |
| Presentación clínica y exámenes de laboratorio | |||||
| KK II - IV | 49 (17.4) | 37 (12.9) | 70 (24.8) | 90 (31.8) | < 0.001 |
| Creatinina. mmol/L | 96.3 ± 68.3 | 94.8 ± 37.5 | 97.7 ± 36.4 | 112.3 ± 50.1 | < 0.001 |
| TG, mmol/L | 1.28 ± 0.84 | 1.45 ± 0.88 | 1.48 ± 1.01 | 1.75 ± 1.13 | < 0.001 |
| Glucemia, mmol/L | 5.08 ± 0.86 | 6.04 ± 0.99 | 7.06 ± 1.49 | 12.0 ± 5.80 | < 0.001 |
| Leucograma, 109/L | 8.4 ± 1.6 | 9.9 ± 1.8 | 11.6 ± 2.2 | 13.6 ± 6.9 | < 0.001 |
| Terapia de reperfusión y egreso | |||||
| Fibrinólisis | 156 (55.3) | 163 (57.0) | 173 (61.3) | 180 (63.6) | 0.161 |
| ICP | 9 (3.2) | 6 (2.1) | 4 (1.4) | 13 (4.6) | 0.114 |
| Complicación presente | 104 (36.9) | 102 (35.7) | 150 (53.2) | 157 (55.5) | < 0.001 |
| Fallecidos | 8 (2.8) | 9 (3.1) | 14 (5.0) | 43 (15.2) | < 0.001 |
Los valores son presentados como media ± desviación estándar, o número (%). ILC: índice leucoglucémico; HTA: hipertensión arterial; IMA: infarto agudo de miocardio; IRC: insuficiencia renal crónica; AVE: accidente cerebrovascular; KK: clasificación Killip-Kimball; TG: triglicéridos; ICP: intervención coronaria percutánea.
Se calculó la curva ROC del ILG relacionado con las complicaciones intrahospitalarias, obteniéndose un área bajo la curva de 0.609 (95% IC: 0.576-0.642; p < 0.001). A pesar de ser estadísticamente significativa, la capacidad discriminativa del índice se puede clasificar como pobre. A continuación, se calculó el punto de corte con mejor sensibilidad y especificidad, a través del índice de Youden, el cual determinó el ILG de 1,188.4; con una sensibilidad de 61.4% y especificidad de 57.3%. Se dividió el universo de estudio de acuerdo con el punto de corte obtenido, y nuevamente se relacionaron las características basales de los participantes (Tabla 2). En este nuevo análisis, se observaron diferencias significativas entre los dos grupos en las mismas variables del análisis por cuartiles, sumándose esta ocasión el antecedente de HTA.
Table 2 Características basales de acuerdo con punto de corte del índice leucoglucémico
| Variable | ILG < 1 188.4 (n = 553) | ILG ≥ 1 188.4 (n = 580) | p |
|---|---|---|---|
| ILG | 899.6 ± 177.8 | 2074.8 ± 1217.3 | < 0.001 |
| Edad, años | 64.3 ± 11.9 | 64.4 ± 11.9 | 0.741 |
| Sexo masculino | 399 (72.2) | 394 (67.9) | 0.121 |
| Antecedentes personales | |||
| Hipertensión | 414 (74.9) | 464 (80.0) | 0.039 |
| Diabetes | 74 (13.4) | 198 (34.1) | < 0.001 |
| Fumador | 327 (59.1) | 327 (56.4) | 0.348 |
| Dislipidemia | 23 (4.2) | 36 (7.2) | 0.121 |
| IMA previo | 42 (7.6) | 42 (9.1) | 0.820 |
| IRC previa | 10 (1.8) | 19 (3.3) | 0.118 |
| AVE previo | 20 (3.6) | 22 (3.8) | 0.875 |
| Presentación clínica y exámenes de laboratorio | |||
| KK II - IV | 82 (14.8) | 164 (28.3) | < 0.001 |
| Creatinina, mmol/L | 95.5 ± 54.9 | 104.8 ± 44.7 | 0.002 |
| TG, mmol/L | 1.37 ± 0.87 | 1.60 ± 1.07 | < 0.001 |
| Glucemia, mmol/L | 5.56 ± 1.05 | 9.46 ± 4.89 | < 0.001 |
| Leucograma, 109/L | 9.1 ± 1.8 | 12.6 ± 5.2 | < 0.001 |
| Terapia de reperfusión y egreso | |||
| Fibrinólisis | 312 (56.4) | 360 (62.1) | 0.053 |
| ICP | 15 (2.7) | 17 (2.9) | 0.824 |
| Complicación presente | 198 (35.8) | 315 (54.3) | < 0.001 |
| Fallecidos | 16 (2.9) | 58 (10.0) | < 0.001 |
Los valores son presentados como media ± desviación estándar, o número (%). ILC: índice leucoglucémico; HTA: hipertensión arterial; IMA: infarto agudo de miocardio; IRC: insuficiencia renal crónica; AVE: accidente cerebrovascular; KK: clasificación Killip-Kimball; TG: triglicéridos; ICP: intervención coronaria percutánea.
El análisis de correlación de Pearson permitió determinar la correlación entre el ILG y los factores de riesgo coronarios considerados como clásicos. El ILG se correlacionó de forma positiva y significativa con el antecedente de diabetes mellitus, la clasificación funcional Killip-Kimball II-IV al ingreso, y los valores más altos de creatinina y glucemia (Tabla 3).
Table 3 Correlaciones entre el índice leucoglucémico y los factores clásicos de riesgo cardiovascular
| Variable | Coeficiente de correlación de Pearson | p |
|---|---|---|
| Edad | 0.35 | 0.237 |
| HTA | 0.53 | 0.076 |
| Diabetes | 0.316 | < 0.001 |
| Tabaquismo | −0.43 | 0.150 |
| IMA previo | 0.003 | 0.925 |
| KK II – IV | 0.171 | < 0.001 |
| Creatinina | 0.180 | < 0.001 |
| Triglicéridos | 0.114 | < 0.001 |
HTA: hipertensión arterial; IMA: infarto agudo de miocardio; KK: clasificación Killip-Kimball.
Factores de riesgo para complicaciones intrahospitalarias en el IAMCEST
Los resultados de los análisis univariado y multivariado y los predictores de complicaciones intrahospitalarias en el IMACEST se presentan en la tabla 4. El análisis univariado reveló que el ILG, la edad, los antecedentes de HTA, diabetes mellitus, tabaquismo, IAM e IRC previos, clase funcional de Killip-Kimball ≥ II, creatinina, triglicéridos, glucemia, leucograma, la no realización de fibrinólisis y el estado al egreso, eran factores de riesgo de aparición de complicaciones durante el internamiento (todos con p < 0.05).
Table 4 Análisis de regresión univariado y multivariado para predecir complicaciones intrahospitalarias
| Variable | Análisis univariado | Análisis multivariado | ||
|---|---|---|---|---|
| OR (IC 95%) | p | OR (IC 95%) | p | |
| ILG | 2.131 (1.679-2.705) | < 0.001 | 1.675 (1.130-2.482) | 0.010 |
| Edad | 1.044 (1.033-1.055) | < 0.001 | 1.025 (1.011-1.040) | < 0.001 |
| Sexo | 1.108 (0.859-1.430) | 0.430 | ||
| HTA | 1.597 (1.198-2.129) | 0.001 | ||
| Diabetes | 1.622 (1.233-2.134) | 0.001 | ||
| Tabaquismo | 0.572 (0.451-0.726) | < 0.001 | ||
| Dislipidemia | 0.883 (0.520-1.500) | 0.645 | ||
| IMA previo | 1.589 (1.016-2.487) | 0.043 | ||
| IRC previa | 2.754 (1.243-6.102) | 0.013 | ||
| AVE previo | 1.103 (0.595-2.044) | 0.756 | ||
| KK II – IV | 42.495 (23.387-77.212) | < 0.001 | 1.029 (1.016-1.054) | < 0.001 |
| Creatinina | 1.010 (1.007-1.014) | < 0.001 | ||
| Triglicéridos | 0.858 (0.755-0.976) | 0.020 | 0.814 (0.687-0.965) | 0.018 |
| Glucemia | 1.073 (1.039-1.110) | < 0.001 | ||
| Leucograma | 1.080 (1.039-1.123) | < 0.001 | ||
| Fibrinólisis | 0.787 (0.620-0.998) | 0.048 | 1.461 (1.087-1.965) | 0.012 |
| ICP | 1.382 (0.683-2.796) | 0.368 | ||
| Egreso | 50.449 (12.313-206.703) | < 0.001 | ||
ILC. índice leucoglucémico; HTA: hipertensión arterial; IMA. infarto agudo de miocardio; IRC: insuficiencia renal crónica; AVE: accidente cerebrovascular; KK: clasificación Killip-Kimball; ICP: intervención coronaria percutánea; OR: razón de disparidad ratio; IC. intervalo de confianza.
Después de ajustar potenciales factores confusores (como el estado al egreso), el análisis multivariado encontró que el ILG, la edad, la clase funcional Killip-Kimball ≥ II, los triglicéridos y la no realización de fibrinólisis eran predictores independientes de complicaciones intrahospitalarias en el IMACEST. Este modelo tuvo una discriminación evaluada mediante el área bajo la curva ROC de 0.803 (IC 95%: 0.777-0.830; p < 0.001) de predecir complicaciones intrahospitalarias en el IMACEST, lo cual se considera muy bueno, como se muestra en la figura 1.
Análisis de Kaplan-Meier para las complicaciones intrahospitalarias
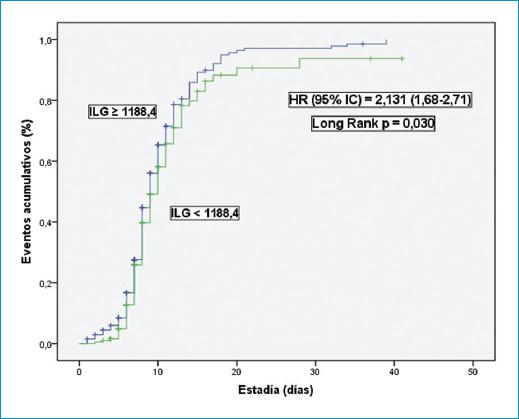
Durante una media de estadía intrahospitalaria de 7.6 ± 3.3 días, se observaron complicaciones en 198 (35.8%) pacientes en el grupo de ILG < 1 188.4 y en 315 (54.3%) pacientes en el grupo con ILG ≥ 1 188.4 (OR no ajustado; IC 95%: 2.131 [1.68-2.71; p < 0.001]). Las principales complicaciones fueron la insuficiencia cardiaca, las arritmias, el shock cardiogénico y la angina posinfarto, con 18.5, 12.9, 9.9 y 8.8%, respectivamente. En la figura 2 se muestra la curva de Kaplan-Meier de acuerdo con las complicaciones intrahospitalarias, separadas por grupos de acuerdo con el punto de corte del ILG; se observaron diferencias significativas según la prueba de rango logarítmico (p = 0.030).
Discusión
En esta investigación, los valores del ILG fueron superiores, con diferencia estadística muy significativa, en los pacientes que tuvieron complicaciones intrahospitalarias, comparado con aquellos que no la presentaron durante su internamiento. Sin embargo, cuando se calculó la curva ROC, su capacidad discriminativa fue pobre, con un punto de corte de 1,188.4.
Quiroga et al.11 relacionaron el leucograma y la glucemia obtenidos al ingreso del paciente y propusieron el ILG como un marcador pronóstico de muerte y complicaciones intrahospitalarias en pacientes con IAMCEST. En este estudio, si bien con una muestra pequeña, se correlacionó el ILG con el desarrollo de muerte, insuficiencia cardiaca y angina posinfarto (p < 0.001). A pesar de que en este estudio solo se incluyeron como complicaciones intrahospitalarias la muerte, la insuficiencia cardiaca y la angina posinfarto, se puede considerar como el primero en el que se propone el ILG como predictor de eventos adversos en los pacientes con síndromes coronarios agudos.
En la investigación desarrollada por Reyes et al.15 los valores de ILG en pacientes con síndrome coronario agudo se relacionaron de forma significativa con un punto final combinado de mortalidad, insuficiencia cardiaca y reinfarto (p = 0.007). El área bajo la curva ROC obtenida fue de 0.63, con un punto de corte de 1 550. Aunque el valor del área bajo la curva es superior al obtenido en esta investigación, se deben tener en cuenta elementos que varían entre los dos estudios, como la no inclusión de otras complicaciones como punto final, y que no solo se incluyeron en el estudio pacientes con IMACEST, sino todos los afectados de síndrome coronario agudo. Al realizar el modelo de regresión logística de Cox, los autores concluyeron que el ILG constituía un predictor independiente de eventos adversos (p = 0.007). En la presente investigación, el ILG también alcanzó una diferencia significativa en el modelo de regresión logística, lo cual reafirma su importancia como factor de riesgo independiente de complicaciones intrahospitalarias. Por último, los autores comparan las curvas de supervivencia de Kaplan-Meier de los grupos de acuerdo con el punto de corte, y encontraron diferencias significativas entre ellos, aunque no especifican su valor. Este resultado es similar al encontrado en la presente investigación.
Hirschson et al.16 analizaron el valor pronóstico del ILG en 405 pacientes con IAMCEST con la información obtenida del Registro Multicéntrico SCAR (Síndromes Coronarios Agudos en Argentina). Para ello dividieron la muestra en cuartiles según el valor del ILG, y los relacionaron con el resto de los factores de riesgo; el punto final del estudio fue la muerte y una escala Killip-Kimball III-IV. Los cuartiles superiores de ILG se correlacionaron significativamente con la localización anterior del IAM y con mayor frecuencia cardíaca, glucemia en ayunas, recuento leucocitario y niveles de CPK total. La incidencia del punto final analizado fue significativamente creciente por cuartiles de ILG: 0, 7.60, 9.30 y 30%, respectivamente (p < 0.001). El área bajo la curva ROC fue de 0.77 (IC 95% 0.71-0.88; p < 0.001). El mejor valor de corte para el punto final fue 1,000. En la presente investigación también se observó que los cuartiles de ILG presentaban diferencias significativas crecientes al tener en cuenta la aparición de complicaciones; sin embargo, se obtuvo un área bajo la curva menor.
El primer estudio realizado en Cuba sobre la capacidad predictiva del ILG fue publicado por León-Aliz et al.18. Los autores evaluaron el ILG como marcador pronóstico en 128 pacientes con IAMCEST que ingresaron entre enero de 2009 y octubre de 2010. Se definieron como complicaciones cardiacas mayores el fallo de bomba con clase Killip mayor o igual que II, arritmias supraventriculares, principalmente fibrilación auricular paroxística; arritmias ventriculares (taquicardia y fibrilación), trastornos de la conducción auriculoventricular de alto grado y reinfarto o angina posinfarto. El área bajo la curva ROC obtenida fue de 0.682 (IC 95%: 0.590-0.775; p = 0.000), con un punto de corte de 1 158; esta área se considera una mala discriminación del estadígrafo C, semejante a lo descrito en la actual investigación, aunque se obtuvo un punto de corte ligeramente superior. Al realizar el análisis multivariado de regresión logística para analizar la posible influencia de otras variables confusoras, se demostró que la edad mayor a 75 años, la TA sistólica inferior a 100 mm Hg y el ILG superior a 1 158 fueron predictores independientes de muerte y complicaciones cardiacas, o ambas. En el estudio que se presenta, se mostró que la edad, una clase de Killip-Kimball ≥ II, los valores de triglicéridos, la estadía y el estado al egreso fueron los predictores independientes de las complicaciones intrahospitalarias.
El ILG tiene una capacidad predictiva de complicaciones tanto en sujetos diabéticos como en no diabéticos. A pesar de que su punto final era la mortalidad intrahospitalaria, Rodríguez et al.21 observaron en 424 pacientes, que las medias de ILG presentaban diferencias significativas si tenían en cuenta el antecedente de diabetes mellitus (p = 0.003). Sin embargo, el área bajo la curva ROC en el grupo de no diabéticos mostraba mejor capacidad discriminativa (C = 0.707 vs. C = 0.673). Los autores utilizaron como punto de corte el percentil 75 del ILG, y al calcular el área bajo la curva con este percentil obtuvieron un estadígrafo C de 0.721 (IC 95%: 0.673-0.770; p < 0.001), con una sensibilidad y especificidad de 34 y 57%, respectivamente. Este es uno de los pocos trabajos que expone estos valores de su curva ROC de ILG, y, en comparación con los datos obtenidos por este autor, los valores de sensibilidad y especificidad en la actual investigación están por encima de los obtenidos por Rodríguez et al.
Los estudios anteriormente descritos presentan diferencias que no hacen posible la comparación con esta investigación. Estas diferencias están relacionadas, fundamentalmente, con muestras heterogéneas en cuanto a su tamaño y composición, con objetivos finales primarios diferentes, en los que se incluyen la muerte como complicación, y en otros no toman en cuenta todas las posibles complicaciones intrahospitalarias después de un IAMCEST; y, por último, y no menos importante, con la ausencia de la sensibilidad y especificidad del área bajo la curva estimada. Sin embargo, en todas estas publicaciones se observa un denominador común, la baja capacidad discriminativa del ILG según el estadígrafo C, lo cual se asemeja a los resultados obtenidos en esta investigación.
Un nuevo elemento introducido en esta investigación es la presentación de la capacidad discriminativa del modelo del análisis multivariado, con lo cual se alcanzó un área bajo la curva de 80.3%, muy superior al de 60.8% cuando solo se analizaba el ILG. Este resultado lleva a concluir que al índice leucoglucémico se deben unir otras variables clínicas con el objetivo de optimizar su capacidad predictiva de complicaciones intrahospitalarias.
Conclusiones
Este estudio demostró que altos niveles de ILG están relacionados de forma significativa con la aparición de complicaciones intrahospitalarias en el IAMCEST; sin embargo, no presenta una buena capacidad predictiva como factor de riesgo independiente. La adición del ILG a un modelo basal de riesgo tiene un fuerte efecto positivo en la predicción de pronósticos adversos en pacientes con diagnóstico de IAMCEST.