INTRODUCCIÓN
Durante las últimas décadas, la contaminación con petróleo y sus derivados ha generado graves problemas ambientales, debido a que las actividades relacionadas con la extracción, almacenamiento y transporte de hidrocarburos generan inevitablemente vertidos o derrames accidentales en suelos y aguas (Pucci et al., 2011). La contaminación en los ecosistemas terrestres y acuáticos afecta severamente a la flora y fauna asociada dada a la toxicidad de estos (Alessandrello etal,. 2017). Además de provocar daños al medio ambiente, la contaminación con hidrocarburos también genera impactos negativos en lo económico y social y en la salud en las zonas cercanas al sitio afectado (Valdivia-Rivera et al., 2018). Existen distintos tipos de tratamientos para remediar los sitios contaminados; estos pueden ser físicos, químicos y biológicos, siendo este último método altamente eficiente, amigable con el medio ambiente y de bajo costo económico (Al-Hawash et al., 2018).
La biorremediación puede llevarse a cabo, entre otras maneras, mediante bioestimulación o por bioaumentación (García-Alcántara et al., 2016; Lizardi-Jiménez et al., 2016). La bioaumentación consiste en la incorporación de microorganismos especializados al sitio contaminado, a fin de acelerar el proceso de biorremediación, mientras que la bioestimulación consiste en estimular los microorganismos del ambiente natural mediante el agregado de nutrientes, principalmente nitrógeno y fósforo (Varjani, 2017). Para que los procesos de biodegradación por parte de los microorganismos puedan realizarse de forma totalmente efectiva, deben tenerse en cuenta una serie de factores en el área a tratar, como el tipo de microorganismos presentes, las condiciones ambientales del sitio contaminado (temperatura, oxígeno, energía, etc.) y la cantidad y toxicidad del contaminante (Alessandrello et al., 2017; Varjani et al., 2017).
Los suelos de la Patagonia se caracterizan por ser pobres en el contenido de nutrientes, en particular en nitrógeno y fósforo (Peri et al., 2019), por lo que las comunidades microbianas autóctonas se encuentran generalmente muy bien adaptadas a este marcado déficit y a las condiciones ambientales en las que habitan (Acuña et al., 2007). Por ello es importante tener en cuenta que la incorporación de altas concentraciones de nutrientes pueden ser sumamente tóxicas para los microorganismos, ya que puede reducir considerablemente el número de bacterias degradadoras o alterar sus actividades metabólicas, y por lo tanto no podrían degradar los contaminantes de forma correcta (Chikere et al., 2017). Por lo tanto es fundamental estudiar las proporciones adecuadas de nutrientes que se necesitan, antes de su aplicación, para obtener resultados satisfactorios (Adams et al., 2015).
La industria automotriz se caracteriza por comercializar vehículos que funcionan a base de combustibles líquidos derivados del petróleo. La gran mayoría de ellos lo hacen a expensas de nafta o gasoil, utilizando diferentes tipos de aceites para lubricación. El despacho de este tipo de combustibles se realiza en las denominadas "estaciones de servicios". Toda estación de servicio, en su playa de abastecimiento de combustibles, posee un sistema de alcantarillas que tiene la finalidad de recoger los derrames de combustibles que puedan ocurrir durante las maniobras de carga de estos. Estos sistemas de alcantarilla confluyen en una pileta de tipo api subterránea donde el hidrocarburo lixiviado, por procesos físicos, es retenido evitando que sea arrastrado con los efluentes del lugar por el agua que entra en el sistema. Dicha agua entra en el sistema de alcantarillas debido a las lluvias ocasionales, o la limpieza de la playa de abastecimiento. Actualmente en la ciudad de Río Gallegos, el hidrocarburo retenido en la pileta tipo api se retira del lugar con camiones de alto vacío, se transporta como un residuo peligroso y recibe finalmente un tratamiento térmico. Este tipo de procedimiento suele ser de un costo muy elevado.
Debido a que los contaminantes que probablemente conformen el lixiviado retenido en la pileta tipo api son nafta y gasoil, y eventualmente los aceites lubricantes que entran en el sistema desde fugas de los vehículos (Mazumber y Mukherjee, 2011; Adish Kumar et al., 2014), es probable su tratamiento por métodos biológicos.
Los lixiviados de las estaciones de servicios en Argentina se encuadran en la categoría de residuos peligrosos, ya que según la Ley nacional N° 24 051 de Residuos Peligrosos, artículo 2 Anexo I, se establece que las corrientes de desecho "Y9 mezclas y emulsiones de desecho de aceite y agua o de hidrocarburos y agua" se consideran peligrosas, debido a que de algún modo pueden dañar directamente o indirectamente a los seres vivos o contaminar el suelo, el agua, la atmosfera o el ambiente en general. La provincia de Santa Cruz se adhiere a la legislación nacional mediante la Ley N° 2567 y el Decreto 712/02, que establecen la necesidad de realizar el tratamiento de los residuos peligrosos o petroleros.
Yasin et al. (2012) estudiaron las características de los efluentes de diferentes estaciones de servicios observando que el principal contaminante que poseen son los hidrocarburos, y proponen que estos deben ser eliminados antes del vuelco del agua en el sistema cloacal, ya que los hidrocarburos generan importantes problemas de toxicidad en agua y suelo (Khan et al., 2018), y además generan problemas en el correcto funcionamiento del sistema cloacal. Por lo anterior, muchos desarrollos científicos se han direccionado a la eliminación de los compuestos de este tipo de efluentes. Es así como existen tecnologías que proporcionan sistemas de tratamientos fisicoquímicos, como los de adsorción con materiales inorgánicos (Hebbar et al., 2013) u orgánicos (Asha et al., 2016; Banchon et al., 2017) o coagulación (Mazumder y Mukherjee, 2011), dentro de los más utilizados. Sin embargo, estos procesos de tratamiento suelen ser de un elevado costo, por lo que se comenzaron a desarrollar alternativas con los tratamientos biológicos de los efluentes contaminados (Mallick y Chakraborty, 2019), con base en el conocimiento de que estos hidrocarburos podrían ser biodegradados por microorganismos (Shadizadeh et al., 2014).
Tanto Álvarez (2015) como Álvaro et al. (2017) demostraron que los suelos de la Patagonia Argentina poseen buenas características para ser utilizados como soporte en sistemas de biodegradación de hidrocarburos. Si a esto se le suma que la posible composición del hidrocarburo que formaría parte del lixiviado de las estaciones de servicio está relacionada con gasoil, nafta o aceite lubricante, se estima que podrán ser biodegradados por los microorganismos presentes en estos suelos.
El objetivo principal del presente estudio fue evaluar la biodegradabilidad de dos residuos provenientes de estaciones de servicio de la ciudad de Río Gallegos, Santa Cruz, Argentina, mediante su incorporación en un suelo de la región.
MATERIALES Y MÉTODOS
Muestra de suelo utilizado como soporte para biorremediación.
Se tomó una muestra de suelo patagónico de aproximadamente 8 kg en las inmediaciones de la ciudad de Río Gallegos, Santa Cruz, Argentina, a una profundidad comprendida entre los 10 y 30 cm. La misma se tamizó con una malla de 2 mm de poro y se almacenó en refrigeración hasta el momento de su estudio. Las principales características físico químicas del suelo fueron: pH 7,66; cloruro 37,4 ppm; sulfato 48,7 ppm; bicarbonato 45,7 ppm; carbonato < 1 ppm; calcio 40,8 ppm; magnesio 12,2 ppm; nitrito 0,52 ppm; nitrato 18,1 ppm; amonio 0,05 ppm; fosfato < 1 ppm; conductividad 84,5 μS.cm-1; humedad 1,07%; materia orgánica 0,98 %; materia inorgánica 99,02 %; densidad aparente 1,31 g.cm3-1; densidad real 2,46 g.cm3-1; porosidad 46 %; hidrocarburos totales < 1 mg.kg-1; bacterias aerobias totales (BAT) 5,30E+05 UFC.g-1; bacterias degradadoras de hidrocarburo (BDH) 8,90E+03 UFC.g-1. Los parámetros mencionados se determinaron de acuerdo a lo propuesto por el Standard Methods (Rice et al., 2017) a partir de un extracto de suelo 1:2,5.
Obtención y caracterización de los residuos de las estaciones de servicio.
La toma de las muestras de lixiviados se realizó en dos estaciones de despacho de combustible de la ciudad de Río Gallegos. Durante un año se realizaron tres muestreos en ambas estaciones de servicios y las muestras se mantuvieron en refrigeración hasta su estudio. La separación física de las muestras de lixiviado consistió en el empleo de ampollas de decantación, con el objeto de separar físicamente la fase acuosa de la líquida no acuosa. Una vez obtenida esta última fase, se procedió a analizar su composición. Para ello, el residuo se diluyó en pentano y la fracción de hidrocarburos n-alcanos de C8 a C40 se estudió por cromatografía gaseosa con detección por espectrometría de masas (GC/MS) según los parámetros de corrida propuestos por la norma EPA 8015. La identificación y cuantificación se realizó utilizando un cromatógrafo de gases Agilent 7890A equipado con una columna capilar (HP5ms) de sílica gel fundida de 30 m por 0,25 mm por 0,25 μιη y un programa de temperatura de 45 °C iniciales por tres minutos, seguido de una rampa de 45 °C a 275 °C a 12 °C.min-1, finalizando con 12 min a 275 °C, con una temperatura del inyector de 200 °C. El volumen de muestra inyectado fue de 1 μL en modo split con una relación 1:10. Como gas acarreador se utilizó helio con un flujo de 1,2 mL.min-1. El detector de masas se utilizó con una temperatura de la fuente de iones y la línea de transferencia de 230 °C y 180 °C respectivamente y una energía de impacto de 70 eV. El escaneo de masas entre 29 y 400 u.m.a. se realizó en modo Scan.
Ensayo de biorremediación asistida.
El presente ensayo se realizó en microcosmos, por triplicado, utilizando 200 g de suelo a los que se los contaminó con cada residuo en estudio en una concentración equivalente a 3 % (P/P). La relación C:N:P utilizada fue 100:2,5:0,25 incorporando KNO3 y KH2PO4 como fuente de nitrógeno y fósforo respectivamente, con una humedad de 10 % (Acuña et al., 2007). Se utilizó un sistema control, el cual se preparó de la misma forma antes mencionada, sin el agregado del residuo como contaminante. La incubación de los microcosmos se realizó a 28 °C por 100 días. El monitoreo se realizó por seguimiento de mineralización y cuantificación de hidrocarburos, conteo de bacterias degradadoras de hidrocarburos (BDH) y cálculo de índices microbiológicos estimados a partir del estudio de los ácidos grasos (FAMEs) microbianos totales del suelo. A tal fin, de cada microcosmo se tomaron muestras de 15 g de suelo a tiempos de cero, 21, 41, 63, 80 y 100 días. Para el análisis de los datos obtenidos, los resultados de todos los parámetros del sistema control se restaron a los obtenidos en los sistemas diseñados para estudiar la biodegradabilidad de los residuos.
Mineralización de hidrocarburos.
Se determinó midiendo el CO2 producido como resultado de la utilización de la fuente carbonada. En principio, el CO2 liberado del sistema productor se fija en NaOH y el carbonato formado se titula con HCl de concentración conocida. A tal efecto, se colocó dentro de cada sistema un frasco colector con 3 mL de NaOH 3 N (Dibble y Batha, 1979). Las determinaciones se realizaron en forma semanal y la producción de CO2 se calculó según la siguiente fórmula:
donde V1 es el volumen de NaOH tomado del frasco colector dentro del sistema, VHCl es el volumen de HCl utilizado hasta el viraje de la heliantina, NHCl es la normalidad del HCl utilizado, V2 es el volumen de NaOH colocado en el frasco colector dentro del sistema y Psuelo representa la masa de suelo colocada dentro del sistema expresada en kilogramos.
Cuantificación de hidrocarburos.
Para la evaluación de los hidrocarburos se siguieron los lineamientos propuestos por la norma TNRCC 1005. A tal efecto, se colocaron 10 g de suelo en un vial de 20 mL y se agregaron 10 mL de pentano. Los viales se agitaron en agitador horizontal a 120 oscilaciones/min por una hora. Los extractos se dejaron decantar toda la noche para finalmente separar la fase orgánica. Para la identificación y cuantificación se utilizó un cromatógrafo de gases marca Agilent, modelo 7890B con detector tipo FID, según TNRCC 1005. Por otro lado, se determinaron los índices C17/pristano y C18/fitano que permiten establecer si la disminución de hidrocarburos en los sistemas en estudio se debe a un proceso de biodegradación (Minai Tehrani et al., 2015). De esta manera se calculan los mencionados índices que comparan un hidrocarburo altamente biodegradable como el n-alcano heptadecano (C17) o el octadecano (C18) con los isoprenoides muy poco biodegradables como el pristano o el fitano. La observación de la disminución de estos índices demuestra que C17 o C18 disminuyen en mayor magnitud que pristano o fitano, relacionándose esto con un proceso de biodegradación llevado a cabo por microorganismos. Con los resultados obtenidos se calculó el porcentaje de biodegradación de hidrocarburos según la siguiente fórmula:
donde HC es la concentración de hidrocarburos inicial y HCf la concentración de hidrocarburos final en el período de tiempo en el cual se calcula.
Conteo de bacterias degradadoras de hidrocarburos.
El recuento de BDH se realizó por el método de diseminación en superficie. Para ello se realizó una suspensión de 1 g de muestra en 9 mL de solución fisiológica estéril y se homogeneizó en un agitador orbital por 30 min a 80 r.p.m. El medio de cultivo utilizado fue BDH (en g/L): NaCl 5; K2HPO4 0,5; NH4H2PO4 0,5; (NH4)2SO4 1; MgSO4 0,2; KNO3 3; FeSO4 0,05; SL 10 B ((HCl 25 %) 7,7 mL; FeSO4.7H2O 1,5; ZnCl2 0,07; MnCl2.4H2O 0,1; H3BO3 0,3; CoCl2.6H2O 0,19; CuCl2.2H2O 0,002; NiCl2.6H2O 0,024; Na2MoO4.2H2O 0,036; agua destilada csp 1000 mL) 10 mL, agar 15, agua destilada csp 1000 mL, al que se adicionaron 30 μL de una mezcla de petróleo y gasoil 1:1 (Acuña et al., 2009). La incubación de las placas de recuento se realizó a 28 °C por 20 días.
Análisis de los ácidos grasos microbianos.
La extracción de ácidos grasos totales se realizó por duplicado utilizando el método modificado propuesto por Ritchie et al. (2000). Se tomaron 3 g de suelo a los que se les adicionó 15 mL de una solución 0,2 M de KOH en CH3OH y se incubó una hora a 37 °C. Luego se añadieron 3 mL de CH3COOH 1 M para neutralizar el pH y finalmente se agregaron 10 mL de hexano. Seguidamente se agitó durante 20 min en agitador horizontal a 100 oscilaciones por minutos para finalmente separar la fase orgánica. Esta fase se evaporó bajo corriente de nitrógeno hasta sequedad para luego resuspender los FAMEs en 200 μL de hexano, que finalmente se transfirieron a un vial de GC. Los ácidos grasos se determinaron como metil esteres por GC/MS mediante la utilización de una columna capilar (HP5ms) de silicagel fundida de 30 m por 0,25 mm por 0,25 μη-ι. Los análisis se llevaron a cabo con un cromatógrafo de gases Agilen 7890A (inyección splitless; presión inicial 10 psi; programa de temperatura: 170-288 °C a 28 °C.min-1, 288-310 °C a 60 °C.min-1, 1,5 min de permanencia a 310 °C) con detector por espectrometría de masas Agilent 5975C con una temperatura de la fuente de iones y la línea de transferencia de 230 °C y 180 °C respectivamente y una energía de impacto de 70 eV. La identificación de los ácidos grasos como metil ésteres se realizó con los estándares propuestos por el sistema MIDI y la biblioteca NIST 08. La composición de los ácidos grasos se calculó como porcentaje del área del pico.
Con los datos obtenidos del estudio de ácidos grasos microbianos del suelo, se procedió a estimar la evolución en el tiempo de los índices microbianos correspondientes a bacterias Gram positivas, de acuerdo a la fórmula Σ (15:0 + a15:0 + i15:0 + 16:0 + a17:0 + i17:0) (Song et al., 2008), a bacterias Gram negativas según Σ (cy17:0 + 18:1a>7c) (Song et al., 2008), a actinomices según Σ (18:0 10Me + 19:0 10Me) (Zheng et al., 2013) y a hongos por el monitoreo del ácido graso 18:2 a>6c (Mummey et al., 2002). Por otro lado, también se calculó el índice de biodiversidad de Shannon para cada sistema en los diferentes tiempos.
Análisis de resultados.
Los resultados obtenidos se analizaron por análisis de la varianza (ANOVA). Para los análisis de biodiversidad de Shannon se utilizó el programa PAST (Hammer et al., 2001).
RESULTADOS
A partir de los estudios realizados por GC/MS, se logró identificar la composición de hidrocarburos presentes en los residuos obtenidos de ambas estaciones de servicio donde se tomaron las muestras. Asimismo, se pudo establecer el perfil de carbono equivalente presente en los mismos.
Como resultado, se determinó que la composición de hidrocarburos correspondió mayormente a la fracción de carbono equivalente comprendida entre C12/13 a C24/25 (Tabla 1 y Fig. 1a), siendo los hidrocarburos mayoritarios identificados los n-alcanos comprendidos entre dodecano y pentacosano. Debido a la uniformidad observada en la composición de hidrocarburos encontrada en todos los residuos estudiados, se procedió a mezclar los mismos para formar un único residuo al que se denominó "Residuo 1". En una sola oportunidad, se encontró un residuo de composición particularmente distinta a la del Residuo 1 que presentó una composición de hidrocarburos que se correspondió mayormente a la fracción de carbono equivalente comprendida entre C10 a C16 (Tabla 2 y Fig. 1b). Dicha fracción se correspondería a la nafta con un alto contenido de hidrocarburos aromáticos policíclicos del grupo de los alquil naftalenos, por lo cual este residuo particular se denominó "Residuo 2" y se estudió de forma separada. El Residuo 2 también mostró la presencia de un perfil rico en compuestos n-alcanos comprendidos dentro de la fracción de carbono equivalente en C16 y C24. Los dos residuos presentaron perfiles de hidrocarburos diferentes (Fig. 1). La composición de hidrocarburos que mostró el Residuo 2 fue más rico en hidrocarburos livianos menores a 14 átomos de carbono, en comparación con el Residuo 1. Esto impactó significativamente (p < 0,05) sobre los valores de mineralización (Fig. 2) y disminución de los hidrocarburos en la muestra de suelo (Tabla 1 y 2).
Tabla 1: Análisis de hidrocarburos (mgHC.kgsuelo -1) realizados en el sistema utilizado para estudiar la biodegradabilidad del Residuo 1. Los resultados obtenidos mostraron un porcentaje de biodegradación de hidrocarburos totales cercano al 80 % en los primeros 63 días. La disminución de los índices C17/Pri y C18/Fit son indicativos de que el proceso de remediación de hidrocarburos es de origen biológico. Pri: Pristano, Fit: Fitano.
| Hidrocarburo | Tiempo (días) | |||||
|---|---|---|---|---|---|---|
| 0 | 21 | 41 | 63 | 80 | 100 | |
| < 8 | 70,81 | 51,87 | 25,26 | 0,00 | 0,00 | 0,00 |
| 8 a < 10 | 75,00 | 138,06 | 2,60 | 0,00 | 0,00 | 0,00 |
| 10 a < 12 | 574,69 | 268,31 | 166,93 | 156,36 | 131,70 | 118,53 |
| 12 a < 14 | 4085,55 | 1736,52 | 1179,15 | 1214,53 | 1158,59 | 1042,73 |
| 14 a < 16 | 6140,07 | 2549,40 | 1823,43 | 1750,00 | 1235,20 | 1111,68 |
| 16 a < 18 | 6217,59 | 2590,95 | 1861,00 | 1722,75 | 1291,94 | 1162,75 |
| 18 a < 20 | 4854,62 | 1927,80 | 1472,01 | 1272,98 | 1297,94 | 1168,15 |
| 20 a < 22 | 3893,59 | 1166,63 | 948,50 | 764,45 | 791,15 | 712,04 |
| 22 a < 24 | 1601,98 | 552,61 | 482,18 | 475,18 | 461,26 | 415,14 |
| 24 a < 26 | 608,28 | 128,87 | 93,46 | 90,57 | 85,37 | 76,84 |
| 26 a < 28 | 239,60 | 77,89 | 44,10 | 46,50 | 43,10 | 38,79 |
| 28 a < 30 | 208,51 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| 30 a < 32 | 199,90 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| > 32 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| C17/Pri | 2,74 | 0,40 | 0,50 | 0,14 | 0,05 | 0,05 |
| C18/Fit | 2,50 | 0,50 | 0,61 | 0,28 | 0,08 | 0,08 |
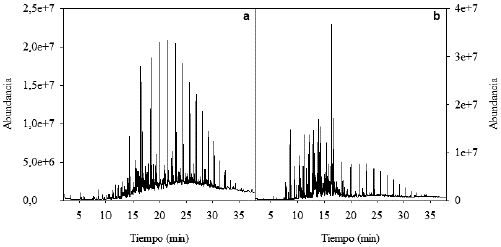
Figura 1 Perfil cromatográfico de los residuos estudiados. El perfil de hidrocarburos del Residuo 1 correspondió a hidrocarburos de tipo n-alcanos comprendidos entre C12 y C25, mientras que el perfil del Residuo 2 se caracterizó por ser rico en hidrocarburos poliaromáticos comprendidos entre C10 y C16. a: perfil del Residuo 1, a: perfil del Residuo 2.
Tabla 2 Análisis de hidrocarburos (mgHC.kgsuelo -1) realizados en el sistema utilizado para estudiar la biodegradabilidad del Residuo 2. Los datos presentados muestran una tasa de degradación de las fracciones de hidrocarburos comprendidas entre C10 y C14 despreciable, pero con más del 50 % de biodegradación de las fracciones comprendidas entre C14 y C26 luego del día 63. La disminución de los índices C17/Pri y C18/Fit son indicativos de que el proceso de remediación de hidrocarburos es de origen biológico. Pri: Pristano, Fit: Fitano.
| Hidrocarburo | Tiempo (días) | |||||
|---|---|---|---|---|---|---|
| 0 | 21 | 41 | 63 | 80 | 100 | |
| < 8 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| 8 a < 10 | 675,88 | 242,63 | 125,42 | 23,54 | 0,00 | 0,00 |
| 10 a < 12 | 8284,88 | 7935,48 | 7225,48 | 7745,75 | 7651,61 | 7498,58 |
| 12 a < 14 | 8738,36 | 8601,73 | 8486,75 | 8338,58 | 8403,94 | 8235,86 |
| 14 a < 16 | 2436,69 | 2394,56 | 1413,49 | 889,89 | 882,24 | 864,60 |
| 16 a < 18 | 1912,55 | 1853,30 | 1129,48 | 681,79 | 680,26 | 666,66 |
| 18 a < 20 | 1655,20 | 1588,53 | 999,24 | 557,03 | 553,50 | 542,43 |
| 20 a < 22 | 1291,61 | 344,23 | 321,76 | 246,29 | 243,10 | 238,24 |
| 22 a < 24 | 305,34 | 298,01 | 247,17 | 137,59 | 140,10 | 137,30 |
| 24 a < 26 | 179,81 | 175,56 | 153,00 | 69,08 | 52,39 | 51,35 |
| 26 a < 28 | 170,01 | 151,47 | 144,85 | 0,00 | 0,00 | 0,00 |
| 28 a < 30 | 114,47 | 118,37 | 0,00 | 0,00 | 0,00 | 0,00 |
| 30 a < 32 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| > 32 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 | 0,00 |
| C17/Pri | 3,10 | 1,96 | 1,04 | 0,12 | 0,12 | 0,12 |
| C18/Fit | 3,12 | 1,80 | 1,30 | 0,34 | 0,33 | 0,33 |
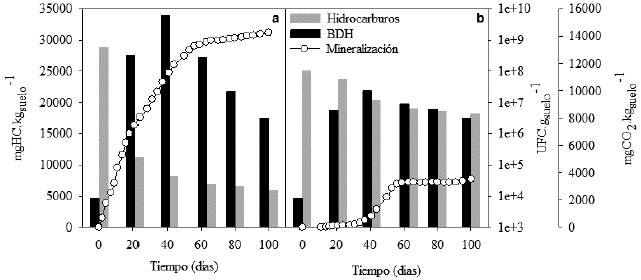
Figura 2 Diferentes parámetros de monitoreo de los microcosmos estudiados. Los datos demuestran las diferencias en las posibilidades de biorremediación que presentan ambos residuos; se observa que todos los parámetros siguieron tendencias favorables durante el monitoreo del sistema de biodegradación del Residuo 1. a: monitoreo del sistema correspondiente al Residuo 1, b: monitoreo del sistema correspondiente al Residuo 2. BDH: bacterias degradadoras de hidrocarburos.
En relación al Residuo 1, se observó que los sistemas presentaron tasas de mineralización elevadas en los primeros 20 días de la experiencia, con valores de éste parámetro comprendidos entre 300 y 600 mgCO2.kg-1 suelo. día-1, lo que evidenció una producción de CO2 total de aproximadamente 14.000 mgCO2.kg-1 suelo (Fig. 2a), con un porcentaje de degradación de 79,68 %. La composición química de este residuo fue similar al gasoil (C10-C22), como se puede observar a partir de los datos expuestos en la Tabla 1, por lo cual en los ensayos se evidenció una degradación satisfactoria. Las fracciones más livianas de carbonos desaparecieron en su mayoría durante los primeros 41 días de la experiencia, mientras que las fracciones restantes se redujeron en un 70 y 80 % en el mismo periodo de tiempo.
El Residuo 2 presentó una fase de latencia en donde no se observaron mediciones de CO2 durante los primeros 40 días de la experiencia. Al cabo del primer mes, se comenzó a evidenciar un aumento en la tasa de producción de CO2 (Fig. 2b), que posteriormente aumentó muy lentamente hasta el día 50, y que luego llegó a fase estacionaria rápidamente. El valor máximo de producción de CO2 que se registró durante la experiencia fue de aproximadamente 3500 mgCO2.kg-1 suelo, observándose un porcentaje de degradación de 29,23 %. De acuerdo a la composición química particular del Residuo 2, que fue muy similar a la nafta, en los ensayos se evidenció una degradación significativamente menor a lo observado para el Residuo 1 (p < 0,05). Las fracciones más livianas de carbonos (< C10) de este Residuo 2, lograron desaparecer completamente a los 63 días. Por otro lado, las fracciones de carbonos correspondientes al rango de C10-14 casi no evidenciaron degradación, mientras que la fracción de C14-26 sufrieron una reducción de un poco más de la mitad a los 63 días, manteniéndose casi sin variaciones hasta final de la experiencia (Tabla 2). Caso contrario se dio en la fracción de C20-C22, que exhibió una buena degradación de alrededor de un 80 % a los 63 días, mientras que las fracciones más pesadas (C26-C30) fueron eliminadas en su mayor parte durante el mismo periodo de tiempo.
Las relaciones n-C17/Pristano y n-C18/Fitano disminuyeron significativamente (p < 0,05) con el tiempo al utilizar los Residuos 1 y 2 como fuente de carbono, lo que indica un proceso de biodegradación en el que los n-alcanos se degradaron más rápidamente que los isoprenoides (Tabla 1 y 2).
Con respecto al impacto de la composición del residuo sobre la comunidad bacteriana, el Residuo 2 generó una respuesta negativa sobre los índices microbianos estudiados (p < 0,05), con una baja considerable del índice de Shannon (Fig. 3b). El impacto fue menor con el Residuo 1 con respecto de los índices microbianos para el estudio de hongos, actinomices y bacterias Gram negativas, mostrando una tendencia de aumento de las bacterias Gram positivas (Fig. 3a). Finalmente, el índice de Shannon calculado para los sistemas con Residuo 1 como contaminante, se mostró casi constante durante los 100 días de experiencia.

Figura 3 Diferentes índices microbianos y de biodiversidad utilizados para el seguimiento de la comunidad microbiana en los microcosmos estudiados. Los datos muestran que, independientemente del residuo estudiado, existe una marcada tendencia a que el proceso de biodegradación sea llevado adelante por microorganismos Gram positivos. Claramente se observa cómo el Residuo 2 produce un importante disturbio en la comunidad bacteriana del suelo, ya que el índice de Shannon desciende significativamente luego de su incorporación al sistema. a: monitoreo del sistema correspondiente al Residuo 1, b: monitoreo del sistema correspondiente al Residuo 2.
DISCUSIÓN
En la totalidad de los muestreos realizados en las estaciones de servicios, la fase líquida no acuosa extraída presentó una composición de hidrocarburos rica en n-alcanos comprendida entre C12 y C25, la cual se corresponde con la composición de gasoil, siendo está altamente biodegrada ble (Nozari et al., 2018). Una excepción fue un muestreo en el cual se obtuvo el Residuo 2, que al ser rico en hidrocarburos policíclicos del tipo alquil naftalenos posee un perfil químico semejante al de nafta altamente evaporada (Cheenmatchaya y Kungwankunakorn, 2017).
La utilización de la comunidad bacteriana autóctona para la degradación de hidrocarburos mediante bioestimulación, agregado de nutrientes y humedad, es una de las tecnologías más frecuentemente utilizada para la eliminación de hidrocarburos (Al-Hawash et al., 2018; Pucci et al., 2011). Esto es porque utiliza el potencial de la comunidad principalmente bacteriana, que ya posee una adaptación al medio ambiente, el cual en las zonas del sur de Argentina suele ser de condiciones extremas (Lewin et al., 2013; Pucci et al., 2013). En el caso del Residuo 1, la bioestimulación aplicada al suelo mostró aceptables resultados en todos los parámetros estudiados durante su biorremediación. Se pudo observar una eliminación de aproximadamente 80 % de los hidrocarburos presentes, con tasas significativas de mineralización y un número alto de microorganismos degradadores de hidrocarburos. Adish Kumar et al. (2014) estudiaron la posibilidad de biodegradar los hidrocarburos de este tipo de residuos; trabajaron con un reactor en medio líquido y lograron un porcentaje de remediación superior al 90 % mediante la inoculación de una cepa de Pseudomonas aeruginosa y el agregado de glicerol y un surfactante.
Los índices de Shannon calculados durante la experiencia con el Residuo 1, demostraron que la biodiversidad de la comunidad bacteriana estudiada no se modificó durante el proceso de biodegradación; el principal grupo de microorganismos presente resultaron ser bacterias Gram positivas. Adams et al. (2014) estudiaron el proceso de biorremediación en un suelo contaminado con hidrocarburos provenientes de residuos de estaciones de servicios y lograron determinar que la biorremediación fue posible y que los géneros bacterianos identificados en mayor proporción fueron Bacillus, Staphylococcus y Arthobacter, todos Gram positivos. En suelos patagónicos, Acuña et al. (2018) observaron que los microorganismos responsables de biodegradar los hidrocarburos contaminantes fueron principalmente del tipo Gram positivos, con participación de los géneros bacterianos Bacillus, Rhodococcus y Paenibacillus, tendencia que concuerda con lo observado en el presente estudio. El hecho de que la mayor eliminación de hidrocarburos en el Residuo 1 se haya evidenciado en los primeros 20 días, con la carencia de fase de latencia, hace pensar en la alta biodegradabilidad de estas sustancias. Anyasi y Atagana (2011) reportaron que la biodegradación en suelos es más eficiente en las primeras semanas independientemente de la cantidad de microorganismos presentes, cuando los contaminantes son altamente biodegradables.
La utilización de las relaciones n-C17/pristano y n-C18/ fitano como un método para comparar los potenciales de biodegradación es de aceptación. En este caso se observó la disminución de los valores de ambas relaciones durante los 100 días de experiencia, con lo cual la degradación observada con los dos residuos estudiados fue biológica (Minai Tehrani et al., 2015). Sin embargo, los perfiles cromatográficos de los Residuos 1 y 2 mostraron que las fracciones volátiles de hidrocarburos (< n-C10) no se detectaron a partir del día 63, probablemente debido a que esta eliminación no fue biológica, sino por volatilización de los hidrocarburos desde los sistemas cuando se ventilaron para su aireación.
A pesar de que se utilizó el mismo suelo para todas las experiencias de degradación, la composición inicial del residuo produjo un impacto diferente en la microbiota edáfica. De esta forma, con el Residuo 2 como contaminante se observó una fase de latencia de aproximadamente 40 días, una disminución del índice de Shannon y un aumento menor de bacterias degradadoras de hidrocarburos con respecto a lo observado en el Residuo 1. Esto pone en evidencia que la composición del Residuo 2 resulta tóxica para los microorganismos del suelo debido a su composición rica en compuestos poliaromáticos (Singh et al., 2014), característicos de nafta altamente evaporada. Muchos son los reportes que indican que los hidrocarburos poliaromáticos producen una marcada disminución de la biomasa del suelo y una inhibición de la actividad enzimática microbiana (Sakshi et al., 2019), lo que redunda en una disminución en la diversidad bacteriana (Khomarbaghi et al., 2019). Se ha demostrado que concentraciones de mezclas de estos contaminantes de 30 mg.kg-1 en suelos no generan estos efectos, pero con concentraciones de 300 mg.kg-1 o superiores se comienzan a ver efectos de disturbio de la comunidad bacteriana y de inhibición de la actividad enzimática, principalmente de los complejos enzimáticos deshidrogenasa y ureasa (Verrhiest et al., 2002; Klamerus-Iwan et al., 2015). Tal situación pudo ocurrir en el suelo del presente estudio al utilizar el Residuo 2 como contaminante, ya que las fracciones de carbono equivalente de C10 a C14 y ricas en hidrocarburos poliaromáticos fueron superiores a estos valores. Angeles et al. (2017) demostraron que los hidrocarburos presentes en un sistema de biorremediación son incorporados por los microorganismos por contacto directo, situación que muchas veces es responsable de explicar los efectos tóxicos de los hidrocarburos poliarómaticos cuando forman parte de sistemas contaminados. En suelos, los microrganismos utilizan el contacto directo para incorporar este tipo de contaminantes (Denis et al., 2017) y así utilizarlos como fuente de carbono y energía. Sin embargo, una vez finalizada esta fase de latencia, se pudo observar una recuperación de la comunidad bacteriana que se reflejó en el paulatino aumento del índice de biodiversidad, así como también de las bacterias Gram positivas; de esta manera, se produjo cerca de un 70 % de biodegradación de la fracción rica en n-alcanos comprendida entre C16 y C24. En general, los alcanos normales no volátiles son degradados fácilmente por las bacterias (Minai Tehrani et al., 2015). El día 63 marcó el inicio en ambos sistemas de la fase estacionaria; a partir de ese momento todos los parámetros estudiados no presentaron cambios significativos, pudiendo esto deberse a un agotamiento de los nutrientes en los sistemas de estudio (Acuña et al., 2007; Pucci et al., 2011).
Carrizo et al. (2015) demostraron que en suelos de la región norte de la provincia de Santa Cruz es posible la biodegradación de mezclas complejas de hidrocarburos a escala de campo mediante la utilización de biopilas. Encontraron un porcentaje de biodegradación de estos compuestos cercano al 50 % con la realización de una adecuada bioestimulación. Por otro lado, Alvaro et al. (2017) demostraron que los suelos de la Patagonia poseen comunidades bacterianas capaces de incrementar su capacidad de biodegradar los hidrocarburos poliaromáticos, como los presentes en el Residuo 2, cuando el suelo es suplementado con materia orgánica, para así estimular el co-metabolismo de este tipo de compuestos. Si bien en el presente trabajo no se planteó un estudio de mezclas de los dos residuos obtenidos, sería interesante su caracterización en futuras experiencias para evaluar si esta situación estimula el co-metabolismo de los hidrocarburos poliaromáticos que forman parte del Residuo 2. El hecho que este tipo de residuos puedan ser biodegradados por los microorganismos del suelo es alentador, ya que permite pensar en una forma de tratarlos menos perjudicial para el ambiente (Álvarez, 2015). Actualmente, para la incineración de los residuos producidos en las estaciones de servicio estos deben transportarse grandes distancias, lo que en algún momento podría fomentar su descarga clandestina o accidental en sitios no adecuados. No obstante, este último punto no puede ser eludido en un posible tratamiento biológico con biopilas, ya que igualmente el contaminante debería ser transportado, pero sí se evitaría su incineración, siendo esto muy positivo para la conservación del ambiente. Una alternativa de biotratamiento que evitaría el transporte de los contaminantes sería diseñar un reactor a base de suelo, en el cual se realice la biorremediación in-situ, lo que obviaría tanto la incineración como el transporte y permitiría una mejora significativa en el tratamiento y disposición final de este tipo de residuos.
CONCLUSIONES
Los resultados obtenidos son alentadores con respecto a la posibilidad de biodegradar la fase libre no acuosa que forma parte de los efluentes de estaciones de servicios de automóviles de la ciudad de Río Gallegos, en sistemas de biorremediación a base de suelo. Esto implicaría que este residuo podría incorporse en los sistemas de tratamiento actualmente desarrollados en la región, biopilas o landfarming, los cuales se aplican de rutina en la remediación de suelos contaminados con hidrocarburos proveniente de la gran actividad de la industria responsable de la extracción y transporte de hidrocarburos. Sin embargo, es de fundamental importancia caracterizar la naturaleza química del contaminante antes de su incorporación en los sistemas de tratamiento, ya que, en caso de poseer una alta proporción de hidrocarburos tóxicos para los microorganismos, como el caso del Residuo 2, podría causar un estancamiento del proceso. Sin embargo, de acuerdo con los resultados obtenidos en este trabajo, una vez que la comunidad bacteria del suelo se adapta a la presencia de estos compuestos, puede recuperarse y continuar con la biodegradación de los compuestos con mayor tendencia a ser biodegradados.















