INTRODUCCIÓN
En las sustancias húmicas, se encuentra una fracción denominada ácidos húmicos, que poseen anillos aromáticos y estructuras poliaromáticas, enlazados por medio de cadenas alifáticas. Los grupos carboxílicos presentes en la estructura de estos ácidos son los responsables del intercambio iónico con los minerales presentes en el suelo, estimulando el crecimiento de la planta (Peña et al. 2005; Canellas & Olivares, 2014; Pantoja Guerra et al. 2016). Constituyen uno de los componentes principales de algunos suelos, turbas y carbones. Éstas, se clasifican en ácidos húmicos (AH), ácidos fúlvicos (AF) y huminas (Canellas & Olivares, 2014). Los ácidos húmicos son la fracción de las sustancias húmicas insolubles en soluciones acuosas bajo condiciones acidas (pH<2), pero sí solubles a valores mayores de pH. La base de su estructura es altamente compleja, formada por un grupo de estructuras aromáticas y cadenas alifáticas. Poseen varios grupos funcionales, dentro de las cuales, están los hidroxilos, carboxilos, fenólicos, entre otros (Gomes de Melo et al. 2016; Fischer, 2017).
Los ácidos húmicos tienen efectos físicos, químicos y biológicos sobre el suelo, por ello, en la actualidad, su uso principal es en la agricultura, como fertilizante orgánico, por las grandes ventajas que brinda, tanto al suelo como a las plantas (Pédrot et al. 2010). Otros usos, no menos importantes, se basan en su poder para transportar compuestos orgánicos no iónicos, como pesticidas y contaminantes, pudiéndolos eliminar de soluciones acuosas (Nardi et al. 2016). Además, en la industria del cemento, se pueden usar como agentes licuantes del concreto u hormigón, pues mejora sus propiedades fisco-químicas. En la industria del papel es usado para colorear el papel y mejorar el grosor. En el tratamiento de aguas residuales, se emplea para eliminar metales tóxicos (como el plomo, mercurio, níquel, zinc y cromo), grasas, aceites y materia suspendida (Lipczynska-Kochany, 2018).
La fuente, tradicionalmente usada para el aislamiento de sustancias húmicas es el suelo; sin embargo, hay otra cantidad de materiales que pueden ser usados como materia prima, donde se destacan los carbones, las turbas y el compost (Manzak et al. 2017; De Souza & Bragança, 2017). Los modelos estructurales de los carbones bituminosos de alto rango (Barrera et al. 2014) son similares a las estructuras de los ácidos húmicos, haciendo estos minerales propicios para la extracción de sustancias húmicas. Se pueden someter a reacciones de oxidación, para incrementar los grupos oxigenados en la matriz carbonacea y, por ende, el de ácidos húmicos y, así, mayor eficiencia en la extracción de estas sustancias (Kodama et al. 2018).
En esta investigación, se evalúa la influencia de tamaño de partícula, la concentración de agente oxidante y el tiempo en la extracción de ácidos húmicos, a partir de carbón bituminoso, procedente de una mina de la región del Cerrejón, en el departamento de La Guajira (Colombia).
MATERIALES Y MÉTODOS
Diseño experimental: Se utiliza un diseño experimental de tipo factorial, con arreglo 22X3, ensayando dos niveles de tiempo (3h y 6h), tres niveles de concentración de 30, 40 y 50% de agente oxidante (H2O2) y dos niveles de tamaño de partícula, de 0,25mm (malla 60) y 0,125mm (malla 120).
Preparación de la muestra: El carbón procedente de la mina del Cerrejón, ubicada en el departamento de La Guajira (Colombia), fue triturada en un molino de bola marca Pulvex y tamizada a dos tamaños de partícula, utilizando tamices con número de malla 60 y 120. La desmineralización y la remoción del solvente, se realizó de acuerdo con el procedimiento sugerido por Anillo-Correa et al. (2013).
Oxidación Acuosa: Se realizó según la metodología de Anillo-Correa et al. (2013).
Caracterización de los materiales: Las muestras del carbón y el ácido húmico fueron caracterizadas por espectrometría infrarroja (FTIR). Los estudios próximales, acorde con las normas ASTM (2012), para determinar el porcentaje de humedad, de materia volátil (%MV), de ceniza, porcentaje de carbono fijo (%CF) y la relación %CF/MV (Anillo-Correa et al. 2013; Colpas Castillo et al. 2017).
Análisis termogravimétrico: El análisis termogravimétrico (TGA), se efectuó en un equipo de termografía TGA Q-500, con acople de horno estándar, utilizando un flujo de nitrógeno de 50mL min-1 (Manals-Cutiño et al. 2011).
Mediante la ecuación 1, se determina la cantidad de ácidos húmicos.
Análisis estadístico: Los resultados encontrados fueron analizados estadísticamente mediante un ANOVA, utilizando el software SPSS (versión 17.0). Todos los ensayos fueron realizados por triplicado.
RESULTADOS Y DISCUSIÓN
El análisis próximal de la muestra de carbón arrojó los siguientes resultados: humedad = 5.99±0.09; materia volátil (MV) = 22,25±0,43; cenizas = 2,714±0,076; carbono fijo (CF) = 69,05±0,58 y relación CF/MV = 2,83±0,03. De acuerdo con estos resultados, se puede afirmar, que corresponde a un carbón bituminoso clase B (Anillo-Correa et al. 2013).
En la figura 1, se observa la curva del termograma (TGA) de la muestra de carbón. En el intervalo comprendido entre 100 y 200°C, se evidencia el inicio de la descomposición térmica, con pérdidas de humedad del 5,99±0,09%. A una temperatura cercana a los 200°C, se presenta una pérdida elevada de sustancias volátiles, comportamiento que se mantiene hasta alcanzar un valor próximo a los 550°C; a partir de esta temperatura, se puede afirmar, que comienza la principal pérdida de masa. Posteriormente, se observa un descenso regular en la pérdida de masa, que dura hasta los 630°C, temperatura donde se inicia la formación de cenizas (De Souza & Bragança, 2017).
En la figura 2 aparecen los espectros FTIR de la muestra de carbón antes de la oxidación. Se observa una banda ancha centrada a los 3400cm-1, correspondiente a grupos OH superficiales o fenólicos de la matriz carbonácea. Las bandas analizadas en el intervalo entre 2915-2800cm-1 son productos de los estiramientos CH de cadenas alifáticas presentes en la estructura del carbón; estas cadenas alifáticas, se confirman por la banda a 1380-1436cm-1, las cuales, se atribuyen a deformaciones del ángulo del enlace CH.
La estructura policondensada aromática de los carbones en estudio originó, de igual manera, una banda a los 1600cm-1, ocasionada por estiramientos C=C del tipo aromático y por las bandas entre 800-750cm-1, que se deben a deformaciones CH fuera del plano (Wang et al. 2017).
La materia inorgánica presente en esta muestra genera la aparición de bandas a 1178-679-811cm-1, correspondientes al enlace Si-O o Si-O-Al, mientras que las bandas a 537-465cm-1, se atribuyen a enlaces Fe-O y Zn-O, respectivamente.
En la tabla 1, se encuentran tabulados la cantidad (%) de ácidos húmicos extraído a diferente tamaño de partícula y concentración de agente oxidante. La mayor cantidad de AH extraídos (76,8±3,5%) de las muestras oxidadas con H2O2, se obtiene al utilizar un tamaño de partícula correspondiente a un tamiz malla 120 en la matriz carbonácea, a una concentración de 50% de H2O2 y un tiempo de contacto con el agente oxidante de tres (6) horas. Debido al tratamiento realizado, se logra que los grupos funcionales oxigenados del peróxido de hidrógeno (H2O2) sufran una descomposición, que se ve favorecida por la existencia de algunas estructuras, que son similares a los ácidos húmicos, como son los ácidos fúlvicos, entre otros (Manzak et al. 2017). En la tabla 1, se observa que una oxidación durante 6 horas provoca que la cantidad (%) de ácidos húmicos se incremente en la estructura de los carbones a las diferentes concentraciones del agente oxidante. Este porcentaje de extracción estuvo por encima del 40%, en la mayoría de los casos.
Tabla 1 Porcentajes de extracción de ácidos húmicos, utilizando diferentes concentraciones de agente oxidante, tiempos de extracción y tamaño de partículas de carbón bituminoso.
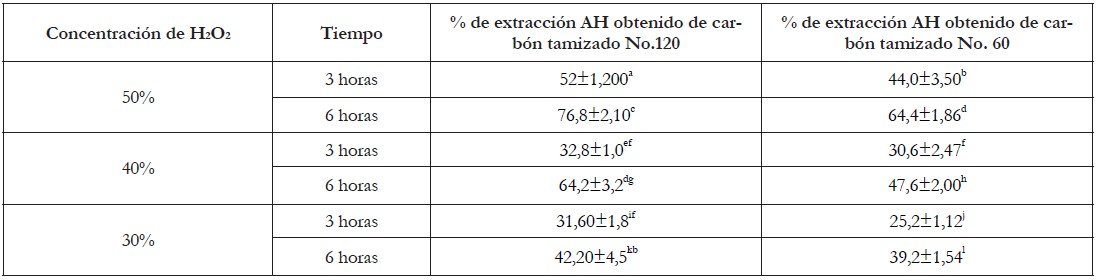
Valores con letras diferentes en la misma fila y en la misma columna, difieren estadísticamente (p<0,05). Los valores de las medidas representan la media ± de tres determinaciones (N=3).
El mayor porcentaje de extracción, se obtuvo a partir del carbón tamizado No. 120, utilizando una concentración de H2O2 del 50%. El contenido de ácidos húmicos en las muestras sometidas a oxidación con H2O2 durante 3h fue menor a los oxidados durante 6h, pero se observó que el porcentaje de la cantidad extraída fue superior al 25%, en todos los casos.
Todos valores en los porcentajes de extracción de AH, utilizando una concentración de 50% de agente oxidante y un tamaño de partículas a malla No. 120, presentan diferencias estadísticamente significativas (P<0,05), al compararlas con los valores obtenidos para una concentración de agente oxidante de 40 y 30%, respetivamente.
El tiempo de extracción influye en la cantidad de ácido húmico que se puede extraer, aunque para una concentración de 40% de agente oxidante, no se encontraron diferencias estadísticamente significativas (P> 0,05), para tiempos de 3h, pero sí para un tamaño de partículas a malla No. 120.
Los porcentajes de extracción de AH aumentaron al disminuir la concentración de peróxido de hidrógeno (H2O2) y al aumentar la superficie de contacto, que se consigue al disminuir el tamaño de partícula a tamaño (tamizado a malla No. 60); en todos los casos, se encontraron diferencias estadísticamente significativas (P<0,05), incluso, al utilizar la misma concentración de agente oxidante, pero diferente tamaño de partícula y diferentes tiempos de extracción (Anillo-Correa et al. 2013) (Tabla 1).
Los espectros FTIR de los ácidos húmicos que se obtuvieron después de realizar la oxidación con H2O2, a una concentración de 50%, muestran entre 3500-3200cm-1 una absorción de tensión OH ancha y fuerte características de los grupos carboxílicos (Figura 3).

Figura 3 Espectros FTIR de ácidos húmicos extraídos con H2O2 al 50%, tiempos de extracción de 3 y 6 horas y tamaños de partículas a malla No. 120 y No. 60. a. Carbón tamizado No.120 oxidado en 3h; b. Carbón tamizado No. 60 oxidado en 3h; c. Carbón tamizado No. 120 oxidado en 6h; d. Carbón tamizado No. 60 oxidado en 6h.
Esta banda es más ancha que la registrada por la muestra de carbón sin oxidar, lo que da indicio del aumento del número de grupos carboxílicos. Esta banda también aparece en los espectros obtenidos al utilizar concentraciones de agente oxidante de 40 y 30%, diferentes tamaños de partículas y tiempos de extracción (Figuras 4 y 5). Un incremento de las bandas estrechas entre 3000 y 2800cm-1 son producto de la tensión C-H en las estructuras alifáticas, lo que explica que la oxidación con H2O2 produjo un rompimiento en los enlaces de las macroestructuras, que originaron la presencia de estos grupos alifáticos, que se pueden presentar como sustituyentes en las estructuras aromáticas o también pueden actuar como puentes (Quintero & Bonillas, 1991).

Figura 4 Espectros FTIR de ácidos húmicos extraídos con H2O2 al 40%, tiempos de extracción de 3 y 6 horas y tamaños de partículas a malla No. 120 y No. 60. a. Carbón tamizado No. 120 oxidado en 3h; b. Carbón tamizado No. 60 oxidado en 3h; c. Carbón tamizado No. 120 oxidado en 6h; d. Carbón tamizado No. 60 oxidado en 6h.
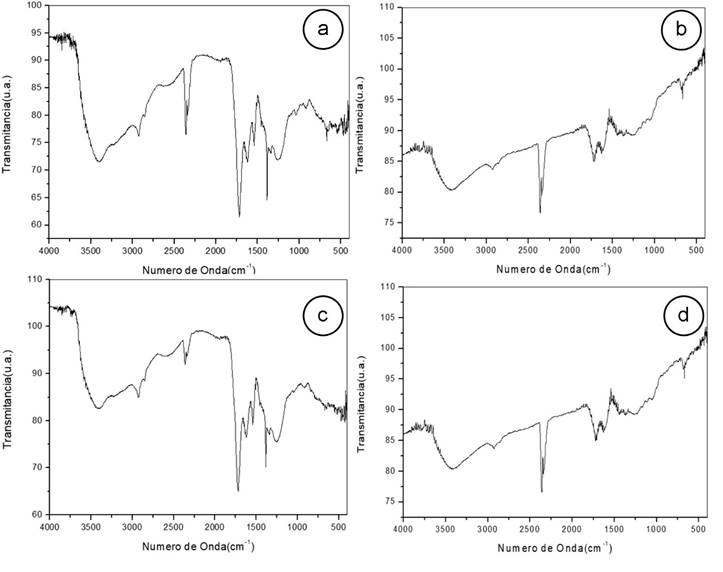
Figura 5 Espectros FTIR de ácidos húmicos extraídos con H2O2 al 30%, tiempos de extracción de 3 y 6 horas y tamaños de partículas a malla No. 120 y No. 60. a. Carbón tamizado No. 120 oxidado en 3h; b. Carbón tamizado No. 60 oxidado en 3h; c. Carbón tamizado No. 120 oxidado en 6h; d. Carbón tamizado No. 60 oxidado en 6h.
Entre los 1800-1600cm-1, se pueden observar las generadas por las tensiones C=O, centradas en 1270cm-1, por la presencia de C=C o Ar-O-R y en el intervalo de 1300-1000cm-1, por los enlaces C-O-C. Estos resultados corresponden con la estructura molecular de los ácidos húmicos, reportados en la literatura (López et al. 2014; Izquierdo et al. 2004).
Las aguas residuales que se originan en el proceso de extracción son ricas en sustancias altamente contaminantes, como el hidróxido de sodio y el peróxido de hidrógeno. A nivel industrial, estos efluentes causarían un impacto ambiental negativo, que se hace necesario resolver, a través de la implementación de un proceso de tratamiento. Una alternativa para mitigar este tipo de daño ambiental sería conducir el efluente, mediante sistema de bombeo a un tanque de almacenamiento, para controlar el pH, posteriormente, someterlo a un proceso de evaporación, por medio de evaporadores de llama directa, hasta llevarlo a concentraciones determinadas, para la recuperación del hidróxido de sodio y ser recirculado nuevamente al proceso.
En el caso del peróxido de hidrógeno, por su gran inestabilidad, se puede descomponer de una manera muy rápida a oxígeno y agua, con posterior liberación de energía.
Los resultados obtenidos, se soportan con los reportados en la literatura científica (De Souza & Bragança, 2017; Anillo-Correa et al. 2013).
Un gran porcentaje de los ácidos húmicos fueron extraídos del carbón tamizado a malla No. 120, a una concentración de 50% y durante 6 horas. Los espectros FTIR de los ácidos húmicos que se obtienen, al oxidar con peróxido de hidrógeno, a concentraciones de 50, 40 y 30%, confirman que el material obtenido en las oxidaciones son ácidos húmicos, acordes con la estructura macromolecular definida para este tipo de sustancia. El tiempo de extracción y la concentración de agente oxidante utilizado influyen en la cantidad de AH, que puede ser extraído de la muestra carbonácea. El carbón procedente de la mina del cerrejón (Colombia) puede ser un candidato potencial para obtener ácidos húmicos, útiles en la industria agrícola.

















