INTRODUCCIÓN
Los cambios en el uso del suelo y las actividades antrópicas alteran la calidad del agua en los sistemas lóticos, afectando las comunidades biológicas que se encuentran aguas abajo de las áreas intervenidas (González-Agudelo et al., 2012; Rivera Usme et al., 2013; Ruiz et al., 2016), principalmente por el aumento de nutrientes, pérdida de cobertura vegetal, presencia de contaminantes inorgánicos y orgánicos, y por la canalización y perdida de continuidad de los sistemas lóticos (Ramírez y San Martin, 2006; Cuellar, 2016).
Al respecto, la construcción y posterior funcionamiento de un embalse produce consecuencias negativas en la bio-diversidad (Rosenberg et al., 2000), donde el bloqueo y la reducción de caudal en una quebrada o río conlleva una serie de alteraciones físicas, químicas y geológicas (López-Pujol, 2011; Reinoso-Aguirre, 2016; Meza-Rodríguez et al., 2017).
Para establecer un diagnóstico de los impactos negativos que genera un embalse, es necesario elaborar planes de gestión ambiental para mejorar las condiciones de las comunidades biológicas acuáticas afectadas por la intervención humana (Medina-Tafur et al, 2013; Gil-Gómez, 2014).
Esta investigación pretende evaluar el impacto que puede ocasionar un embalse sobre las comunidades acuáticas bentónicas, a través del análisis de la distribución espacio-temporal de los grupos funcionales alimenticios. Con este propósito, realizamos el análisis de variables bióticas, que incluyen la identificación de la estructura y composición de los macroinvertebrados acuáticos en los biotopos disponibles en la quebrada La Nitrera, como son la hojarasca y el sustrato rocoso (Aguirre et al., 2004; Greathouse y Pringle, 2006; Montoya et al., 2011; Aguirre y Caicedo, 2013; Murillo et al. 2016; Ruiz et al., 2016).
La red trófica se estableció a partir de los grupos funcionales alimenticios como son los fragmentadores, filtradores, colectores, raspadores y depredadores, siguiendo la guía de diversos autores (Gutiérrez, 2006; Chará-Serna et al., 2010; Ramírez y Gutiérrez-Fonseca, 2014). Con base en lo anterior, se pueden obtener modelos ecológicos que permiten desarrollar mejores modelos conceptuales sobre la estructura y funcionamiento de los macroinvertebrados acuáticos asociados a las corrientes tropicales (Tomanova et al., 2006).
De acuerdo con Sánchez et al. (2013), la estimación de la tasa energética o contenido calórico se puede emplear para conocer la cantidad de energía disponible que aporta la biomasa de los macroinvertebrados acuáticos a la cadena trófica, respecto a un orden trófico superior. Para ello, se emplean modelos bioenergéticos expresados como gramos de alimento en un porcentaje de peso corporal individual a partir de la calorimetría o TGA (Encina et al., 1999).
Schmidt-Kloiber y Hering (2012), evaluaron el equilibrio a largo plazo de la biomasa de los macroinvertebrados acuáticos para determinar la coexistencia estable de cada taxón. Según Schuwirth y Reichert (2013), esto permite incluir conocimientos en modelos mecanicistas y se puede modelar la composición comunitaria de los macroinvertebrados acuáticos en corrientes. Recientemente, fueron integrados en el modelo "Streambugs" los conceptos de modelado teórico de la red alimenticia, la teoría metabólica de la ecología y la estequiometria ecológica, usando además bases de datos de rasgos funcionales (Schuwirth et al., 2015).
Blanco (2013) y Rodríguez (2011) describen un grado de complejidad respecto a un modelo ecológico en función de los macroinvertebrados acuáticos, el cual depende de algunos objetivos específicos: 1) representar variables y tasas de cambio; 2) describir la estructura de un ecosistema y los patrones temporales y espaciales de procesos ecosistémicos individuales; 3) reconstruir el pasado o predecir el comportamiento futuro del ecosistema estudiado; 4) generar y probar teorías e hipótesis ecológicas sobre la organización y funcionamiento de los ecosistemas; 5) mostrar, codificar, transferir, evaluar e interpretar el conocimiento ecológico; 6) guiar el desarrollo y evaluación de políticas ambientales.
La pregunta de investigación de este trabajo es: ¿Cómo es el impacto del embalse en la distribución espacio-temporal de los macroinvertebrados acuáticos en la quebrada La Nitrera? Para ello se planteó como hipótesis, que la variación espacio-temporal de los macroinvertebrados acuáticos en la quebrada La Nitrera está influenciada por características ambientales como el caudal y la morfología de la quebrada, y se refleja en la distribución energética y biomasa de los organismos. De acuerdo con lo anterior, se planteó en la hipótesis que aguas arriba del embalse la quebrada exhibe una alta capacidad calórica en relación a la biomasa, debido al aporte de la vegetación ribereña, mientras que aguas abajo se reduce la disponibilidad de energía y materia por la alteración del ecosistema. Al probar esta hipótesis y evidenciar los cambios ocasionados en el ensamblaje de los macroinvertebrados acuáticos, se pretende demostrar que el embalse genera un impacto negativo en las condiciones ambientales y en el funcionamiento de la red trófica de las comunidades bentónicas.
MATERIALES Y MÉTODOS
Área de estudio
La quebrada La Nitrera nace en la reserva natural que lleva el mismo nombre y se localiza al suroeste del departamento de Antioquia en el municipio de Concordia. Su nacimiento se encuentra a 2190 metros sobre el nivel del mar (m.s.n.m), y su caudal promedio es de 37 1/s (Fig. 1.). Se realizaron cinco muestreos durante un ciclo hidrológico, ubicando en la quebrada cuatro estaciones de muestreo. Las estaciones se escogieron de acuerdo con condiciones que permiten conocer la distribución funcional alimenticia, abundancia, riqueza y biomasa de los macroinvertebrados acuáticos bentónicos. La primera estación (E1) se ubicó aproximadamente a 3 km aguas arriba del embalse (6°2,129' N, 75°56,026' W), a 2171 m.s.n.m. La segunda estación (E2) se estableció aproximadamente a 1 km aguas abajo de E1 (6°2,139' N, 75°55,669' W), a 2156 m.s.n.m. La tercera estación (E3) se localizó donde la quebrada vierte sus aguas en el embalse (6°2,119' N, 75°55,951' W) a 2149 m.s.n.m, que corresponde a una transicional de un sistema lótico a uno léntico. Por último, la cuarta estación (E4) se ubicó a una distancia aproximada de 400 m aguas abajo del embalse (6°1,969' N, 75°55,769' W), a 2130 m.s.n.m.
Macroinvertebrados acuáticos
Los macroinvertebrados acuáticos fueron recolectados mediante una red Surber con un área de 33 cm*33 cm = 0,11 m2, colocada estratégicamente en los sustratos de hojarasca y roca. Así mismo, se realizó una recolección con la red tipo D en cada sustrato en un tramo de 10 m lineales en cada estación. Las muestras fueron depositadas en bandejas plásticas donde se separó el material biológico, y luego se preservaron en recipientes con alcohol al 70 %. Para la identificación de los macroinvertebrados acuáticos en el laboratorio, se empleó un estereomicroscopio marca Karl Zeiss® y claves taxonómicas descritas por Fernández y Domínguez, (2001), Roldán (2003); Posada-García y Roldán-Pérez (2003), Domínguez y Fernández (2009). Para la asignación del rol trófico se utilizó la guía de grupos de alimentación funcional por familias de insectos acuáticos en América Latina de Ramírez y Gutiérrez-Fonseca (2014).
TGA
El análisis TGA se realizó en el laboratorio del Grupo Procesos Químicos Industriales-PQI- de la Universidad de Antioquia, bajo las condiciones siguientes: atmósfera de nitrógeno con una pendiente de calentamiento de 20 oC/ min hasta una temperatura 500 oC/min, con cambio a una atmósfera oxidante de 500 a 900 oC. El equipo Analizador Térmico Simultáneo (STQ Q600®, de TA Instruments) se utilizó para una biomasa de macroinvertebrados acuáticos entre 5 a 10 mg, con el fin de determinar su contenido de materia orgánica, inorgánica y de material sintético, estableciendo el porcentaje de humedad (%w), ceniza (%cz), sólidos volátiles (%SV) y carbono fijo (%CF) de manera simultánea. Este equipo permitió por gravimetría observar pérdidas de peso en función de la temperatura en una atmósfera de gases controlada. Las técnicas utilizadas por este equipo cumplen con las normas ASTM -ASTM D 3174-02, 2002, ASTM D 5142-02a, 2003 y ASTM D7582, 2012 (ASTM International, 2002; 2003; 2012) y se encuentran aprobadas por la AOAC International y la AACC International (Golato, 2014).
Modelo general de energía
Para la modelación de la biomasa de los macroinvertebrados acuáticos en función del grupo funcional alimenticio, se empleó el programa Gephi 0.9.1®; este software fue empleado inicialmente para agrupar y asociar redes sociales pero paulatinamente ha sido aplicado a sistemas biológicos generando diseños de grafos de fácil visualización, información y estructuración (Bastian et al., 2009; Wang et al., 2015). Para el desarrollo del modelo se usó la siguiente ecuación del programa:
Donde ∆Q es la modularidad y representa cada nodo, Σin es la suma de los pesos de los enlaces dentro de la comunidad, Σtot es la suma de los pesos de los enlaces incidentes a los nodos en la comunidad, Ki es la suma de los pesos de los enlaces incidentales al nodo, k i,in es la suma de los pesos de los enlaces de a los nodos en la comunidad ym es la suma de los pesos de todos los enlaces de la red. Modularidad ∆Q: esta permite visualizar los comportamientos y cambios locales de las comunidades para construir una nueva red (Blondel et al., 2008).
RESULTADOS
Variables bióticas
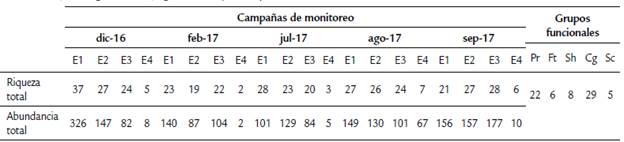
Los resultados de riqueza y abundancia taxonómica y la clasificación en los grupos funcionales alimenticios (Ramírez y Gutiérrez-Fonseca, 2014) de los macroinvertebrados bentónicos obtenidos en los muestreos realizados en los meses de diciembre de 2016, febrero, julio, agosto y septiembre del 2017 se observan en la Tabla 1.
TGA
Para este análisis se tuvieron en cuenta los meses de julio, agosto y septiembre de 2017. El estudio termogravimétrico mostró que entre las estaciones se presentaron tres rangos térmicos similares (Fig. 2), el primero entre 25 y 230 oC, el segundo entre 231 y 700 oC y el último entre 701 y 900 oC.
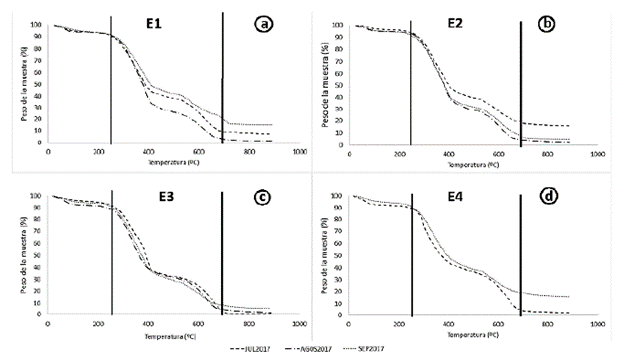
Figura 2 Análisis termogravimétrico para los periodos de julio, agosto y septiembre del 2017 en las cuatro estaciones de muestreo. (a) E1, (b) E2, (c) E3 y (d) E4
En la figura 2a (E1), se observa en el primer rango térmico la variación del porcentaje del peso de la muestra en función del gradiente de temperatura. También se aprecia una pérdida del 10 % correspondiente a la humedad analizada. En el segundo rango térmico se observaron cambios entre los meses monitoreados, siendo septiembre el mes con menor pérdida de biomasa (con un porcentaje del 70 %), seguida por los meses de julio y agosto con 80 y 88 % respectivamente. Finalmente, en el último intervalo se observó que en los diferentes meses no hubo pérdidas apreciables de biomasa.
En la figura 2b (E2), se evidenció que el primer rango térmico se comportó de manera similar al de la estación 1. El segundo rango mostró diferencias entre los meses de monitoreo, siendo julio el mes con menor pérdida de biomasa (con un porcentaje del 70 %), seguida de los meses de agosto y septiembre con pérdidas muy similares (85 % aproximadamente). En el tercer rango no hubo pérdidas apreciables.
En la figura 2c (E3) se evidenció que el primer intervalo tuvo un comportamiento similar a las estaciones anteriores.
En el segundo intervalo, los 3 meses tuvieron pérdidas semejantes (entre el 80 % y el 90 %) y en el último intervalo se observó la misma tendencia de las estaciones anteriores.
En la figura 2d (E4) se evidencia una similitud en el primer y tercer rango térmico de las estaciones 1, 2 y 3. No obstante, se presentan diferencias en el segundo rango entre los meses de julio y septiembre con una pérdida de biomasa del 20 % aproximadamente. Es de señalar que en la campaña de agosto no se reportaron resultados ya que la biomasa disponible no fue suficiente para el TGA.
Modelo
En la tabla 2 se muestran los resultados obtenidos de la modularidad. Las estaciones 1, 2 y 3 presentan conexiones sólidas (modularidad alta) entre los nodos (taxonomía) en relación a cada módulo (grupo funcional alimenticio). Caso contrario ocurre con E4 donde hay poca conectividad entre los nodos en relación con el módulo (modularidad baja).
El modelo de la red trófica para E1 (Fig. 3a) demostró que el 37,14 % de las familias identificadas correspondieron al grupo de depredadores (Pr) (Naucoridae, Vellidae, Polythoridae, Gomphidae, Calopterygidae, Libellulidae, Staphylinidae, Hydrophilidae, Gyrinidae, Hydrobiosidae, Corydalidae y Arachnoidea), el 25,71 % al grupo de los colectores (Cg) (Leptophlebiidae, Baetidae, Tricorythidae, Elmidae, Leptoceridae, Chironomidae, Planariidae, Gamaridae y Collembola), el 14,28 % al grupo de los fragmentadores (Sh) (Ptilodactylinidae, Calamoceratidae, Odontoceridae, Tipulidae y Limonea) y por último los grupos de los filtradores (Ft) y raspadores (Sc) representaron un 11,42 % cada uno (Simuliidae, Philopotomidae, Hydropsychidae, Polycentropodidae, Psephenidae, Scirtidae, Glossosomatidae e Hydroptilidae).

Figura 3 Modelo de la cadena trófica de los macroinvertebrados acuáticos en las diferentes estaciones de muestreo durante todas las campañas monitoreadas; Pr= Depredadores, Cg= Colectores, Sh= Fragmentadores, Ft= Filtradores y Sc= Raspadores; (a) E1, (b) E2, (c) E3 y (d) E4
Los modelos de la red trófica para E2 y E3 (Figs. 3b y 3c) demostraron semejanzas con los resultados del modelo E1.
Para E4 (Fig. 3d), el modelo de la red trófica demostró que el 41,66 % de las familias observadas correspondieron al grupo funcional de depredadores (Hebridae, Vellidae, Calopterygidae, Hydrobiosidae y Libellulidae), el 41,66 % al grupo de los colectores (Chironomidae, Leptoceridae, Elmidae, Physidae y Baetidae) y por último, los grupos de los filtradores (Simullidae) y raspadores (Haplotaxidae) tuvieron un 8,33 % para cada uno.
Para el grupo de depredadores la familia predominante es Perlidae, para el grupo de colectores Elmidae, para los fragmentadores Calamoceratidae, para los filtradores Hydropsychidae y para el grupo de los raspadores Psephenidae. Esto significa que estas familias son las mayores aportantes de biomasa y por ende de energía calórica en la cadena trófica.
DISCUSIÓN
En el TGA se presentaron tres eventos térmicos por estación. El primer evento térmico corresponde a la pérdida de humedad de la biomasa analizada (10 % aproximadamente), coincidiendo con la información reportada por diferentes autores como Kaya et al. (2014) y Torres Hernández y Altamirano Torres (2015); el segundo evento térmico corresponde a la pérdida de quitina y de proteínas que aportan la energía calórica a los consumidores de mayor orden (Liu et al., 2012; Sotelo-Boyás et al., 2015); y el tercer evento térmico corresponde a la materia inorgánica (principalmente carbonato de calcio) que es la parte no aprovechable por otros consumidores (Sotelo-Boyás et al., 2015; Ramírez y Roció, 2018).
De las pérdidas de peso entre cada campaña en el análisis del TGA se infiere que el aporte de energía calórica en cada periodo de tiempo varía, lo cual sugiere la ocurrencia de cambios importantes en el comportamiento de la cadena trófica en cada microhábitat o estación monitoreada.
La modularidad brinda información sobre la dinámica y distribución del ensamblaje de las comunidades de los macroinvertebrados acuáticos; los valores altos indican comunidades con estructuras y conexiones sólidas y los valores bajos reflejan conexiones débiles y pocas estructuras (Buitrago, 2016; Motta y Tostes, 2016; Losavio y Ordaz, 2017).
Todas las estaciones de monitoreo antes del embalse presentaron valores altos de modularidad, mientras que sucedió lo contrario con la estación ubicada después del embalse. Estas diferencias exhiben el empobrecimiento de la red de las comunidades y la disminución de las conexiones entre los grupos funcionales alimenticios por la presencia del embalse, sugiriendo además alteraciones en las comunidades hidrobiológicas que podrían ser permanentes.
El software Gephi® se puede emplear como herramienta para modelar los cambios de los grupos funcionales alimenticios de los macroinvertebrados acuáticos mediante el índice de modularidad, algoritmo que permite analizar de qué modo el sistema-red se estructura y se agrupa en distintas comunidades y así establecer los posibles impactos sobre el recurso hídrico.
CONCLUSIONES
A partir del análisis del índice de modularidad y de grafos, se pudo constatar que las estaciones E1, E2 y E3 presentaron similitudes en cuanto al agrupamiento de la red trófica de los grupos funcionales alimenticios.
Las estaciones E1, E2 y E3 (antes del embalse) presentaron modularidades altas y por lo tanto comunidades estructuradas y fuertemente conectadas.
La estación E4 (posterior al embalse) demostró modularidad baja, es decir, comunidades poco estructuradas y con conexiones débiles. Con lo que se puede afirmar que el embalse genera una alteración en la cadena trófica de las comunidades de macroinvertebrados acuáticos.
Los grupos funcionales alimenticios podrían ser un criterio óptimo en la valoración de la calidad ecológica y del agua utilizando el TGA y el modelo Ghepi.
Con el fin de mantener la estabilidad ecológica después del embalse y evitar alteraciones permanentes en la cadena trófica, es necesario mantener un caudal mínimo y un mantenimiento del lecho aguas abajo del embalse que permita la colonización de estas comunidades acuáticas.