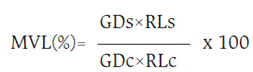Introducción
La producción de coco es una de las actividades económicas más importante de las comunidades afrodescendientes y campesinas asentadas en las zonas costeras de Colombia. Según cifras del Ministerio de Agricultura y Desarrollo Rural, en el año 2019, la producción de coco se incrementó en un 10.95 %, respecto a las 129 633 toneladas reportadas en el año 2014 (Agronet, 2014), aumentando las áreas cultivadas a 22 865 hectáreas (Agronet, 2020), donde el Cauca es el tercer productor en el país, concentrando su cultivo en los municipios de Timbiquí y López de Micay, quienes representan el 12.5 % de la producción nacional de coco (Agronet, 2014); no obstante, su cosecha genera grandes volúmenes de subproducto poco aprovechable (mesocarpio, que localmente se denomina estopa), el cual se acumula al borde de las carreteras y terrenos baldíos (Anuradha Jabasingh, 2011; Karmegam et al., 2021) e, inclusive, es vertido sobre los ríos y las zonas de manglares, generando problemas ambientales y contaminación del suelo, el agua y el aire (Granados y López, 2002; Islas y Tzec, 2021).
El mesocarpio de coco se considera un residuo agrícola que expone dos componentes importantes: la fibra de coco, que ha tenido una buena aplicación en el desarrollo de industrias destinadas a la obtención de fibras (Etim et al., 2016; Jayakumar et al., 2022), y la médula de coco, que es un material particulado con el cual se han venido desarrollado procesos industriales importantes (Etim et al., 2016), convirtiéndose en una alternativa de bajo costo con potencialidades de aprovechamiento en diferentes campos de la agroindustria, como precursor en la síntesis de biocompuestos (Ma et al., 2022; Rejani y Radhakrishnan, 2022) y enzimas (Anuradha Jabasingh, 2011; Muniswaran y Charyulu, 1994; Prabaningtyas et al., 2018), material adsorbente en el tratamiento de aguas (Etim et al., 2016; Ewecharoen et al., 2008; Namasivayam et al., 2001), maderas plásticas (Pratheep et al., 2021), cultivos agrícolas (Agarwal et al., 2021; Carlile et al., 2015; Guerrero et al., 2021; Karmegam et al., 2021; Jayakumar et al., 2022; Nattudurai, 2014; Noguera et al., 2011), entre otros.
La médula de coco, como material lignocelulósico esponjoso de color marrón (Karmegam et al., 2021), está compuesto por celulosa, ligninas, taninos, pentosano y furfural, y representa el 70 % del peso del mesocarpio (Etim et al., 2016), es decir, por cada kilogramo de fibra de coco, se obtienen 2 kg de médula (Anuradha, 2011). De igual forma, por la complejidad de las estructuras que constituyen la médula de coco, su descomposición en el ambiente es muy lenta (Nattudurai et al., 2014), razón por la cual, este material posee una alta estabilidad y un alto potencial para ser utilizado en diversos campos de la industria, así como en procesos agrícolas, tales como la elaboración de sustratos de cultivo (Agarwal et al., 2021; Carlile et al., 2015; Jayakumar et al., 2022; Karmegam et al., 2021), esto le es conferido por sus características físicas (elevada capacidad de aireación) y químicas (buena capacidad de intercambio catiónico), relacionadas con la granulometría del material (Vargas et al., 2008); sin embargo, al poseer un alto contenido de sales (Na, Cl, K), debe ser lavado para evitar afectaciones en las plantas durante el cultivo (Agarwal et al., 2021; Carlile et al., 2015; Ma y Nichols, 2006), influenciado por el tipo de molienda y el origen del material (Vargas et al., 2008); no obstante, esto no impide que sea una posible alternativa de aprovechamiento y de agregar valor a un material que en la Costa Pacífica Caucana se considera como un desperdicio que genera afectaciones sobre el entorno y las comunidades.
Por lo anterior, el presente estudio tiene como objetivo realizar una caracterización morfológica, física y de fitotoxicidad de la médula de coco proveniente de la Costa Pacífica Caucana, puesto que no existen reportes previos que caractericen o que propongan un uso potencial para este material.
Materiales y métodos
Localización
En el laboratorio de Análisis de Reología y Bioempaques de la Facultad de Ciencias Agrarias de la Universidad del Cauca se evaluaron 76 muestras de coco maduro provenientes de los municipios de Timbiquí, López de Micay y Guapi, ubicados en la Costa Pacífica Caucana.
Caracterización morfológica
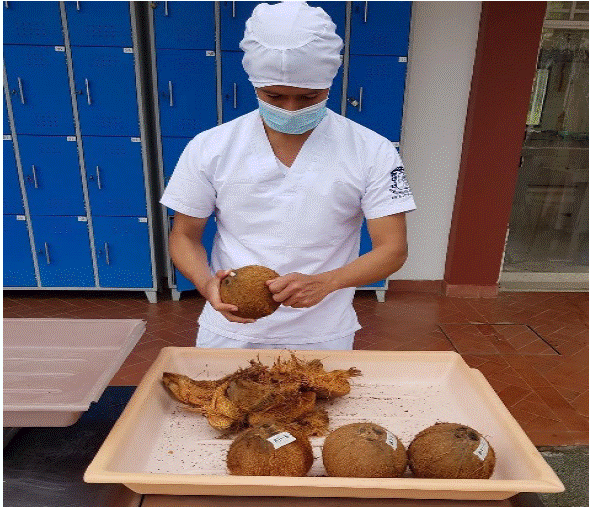
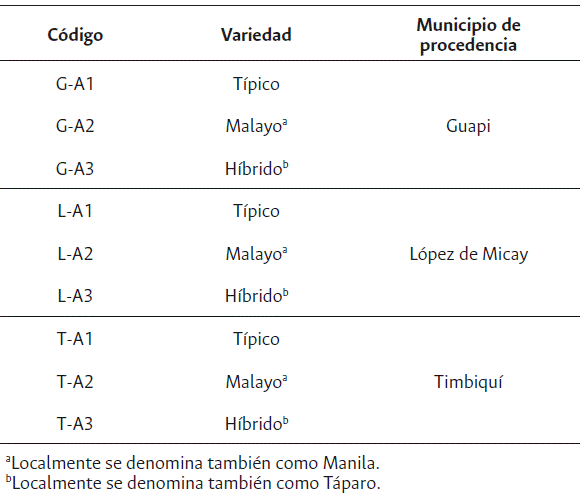
Se realizó la separación del mesocarpio y la nuez del coco; del mesocarpio, a través de una remoción manual y en seco, se hizo la extracción de la médula de coco y la separación de la fibra. Posteriormente, se obtuvieron los rendimientos y se analizaron las muestras de coco por variedad y procedencia (Figura 1 y Tabla 1), y en combinación de todas las muestras. Las evaluaciones con la médula de coco se realizaron con el material crudo, es decir, sin ningún tipo de tratamiento posterior a la extracción.
Caracterización física
Se realizaron diferentes pruebas de caracterización, donde la distribución del tamaño de partículas se analizó mediante el método propuesto por Martínez y Abad (1993), usando cribas con distintos tamaños de partícula, según especificación ASTM de los tamices N10, N12, N16, N20, N25, N30 y N40, colocadas sobre un agitador electromagnético de vaivén Fritsth Analysette 3 pro; la densidad real (Dr), la densidad aparente (Da) y la capacidad de retención de agua, se evaluaron mediante el método descrito por Ansorena (1994); el pH se determinó mediante un titulador Metrohm 848 Titrino plus; y la conductividad eléctrica (CE) se midió con un conductímetro Hanna HI 9033 en extracto acuoso de la muestra de médula de coco (1:10). Para la valoración de estos parámetros las muestras se analizaron por triplicado.
Determinación de fitotoxicidad
Se realizó un ensayo de germinación siguiendo la norma UNE EN 16086-2, tal y como lo describe Flórez et al. (2021), para ello se utilizaron cuatro diluciones de la médula de coco en agua destilada: 1.0 g/L; 0.1 g/L; 0.01 g/L; 0.001 g/L y 0 g/L como control. Para cada tratamiento se prepararon tres cajas Petri con perlita. Sobre ellos se colocó una hoja de papel filtro y se humedeció uniformemente con 50 mL de la solución respectiva. Se colocaron diez semillas de berro (Lepidium sativum) sobre el papel filtro y se incubaron en oscuridad a 25 ± 5 °C durante 72 h. Después de este tiempo se determinaron los siguientes parámetros:
RL: longitud promedio de raíz por planta (mm) SL: longitud media de los brotes por planta (mm) R/S: relación raíz:brote
GD (%): grado de germinación de cada tratamiento (% respecto al total de semillas)
RI (%): índice de raíces, desarrollo de raíces en comparación con el control
El índice de vitalidad de Munoo-Liisa (MLV), que compara el producto del grado de germinación (GD) por la longitud promedio de la raíz (RL) en las muestras con el control, se calculó de acuerdo con la ecuación (1).
Donde:
GDs es el grado de germinación de cada réplica de un tratamiento.
GDc es el grado de germinación promedio del control.
RLs es la duración promedio de cada réplica de un tratamiento.
RLc es la duración promedio de las tres réplicas del tratamiento de control.
Análisis estadístico
El análisis de los datos fue realizado mediante el software IBM® SPSS® Statistics Versión 23.0.0.0, realizando Tukey α>0.05.
Resultados y discusión
Caracterización morfológica
Las muestras de coco evaluadas, donde las variedades morfológicamente son diferentes (A1, típica de porte alto y frutos grandes; A2, malayo de porte bajo y frutos pequeños, y A3, variedad híbrida que combina características fisiológicas de las variedades A1 y A2) (Granados y López, 2002), presentan una proporción del mesocarpio similar, comparada a la masa total del fruto (Tabla 2), que oscila entre el 35.27 % y el 48.48 %; es decir, de la producción de nuez de coco, cerca de la mitad del fruto es un subproducto que no difiere de las características morfológicas de la planta (Granados y López 2002). Sin embargo, estos valores son cercanos a lo reportado por Maruchis et al. (2007), donde de los frutos se puede separar un 37.77 % como mesocarpio; mientras que Zhang et al. (2021) se enfocaron en analizar únicamente la proporción comestible del fruto (agua y pulpa de coco), obteniendo valores que varían desde los 25.39 % a los 53.18 %, siendo los componentes restantes el mesocarpio y pericarpio (concha).
Tabla 2 Porcentaje de mesocarpio, médula y fibra extraídas de muestras de coco de la Costa Pacífica Caucana
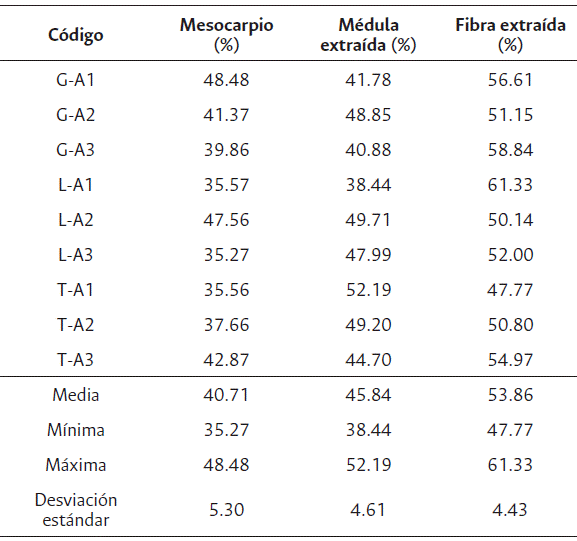
Por otra parte, en cuanto a la cantidad de fibra y médula que se puede extraer del mesocarpio, el contenido de fibra reporta los valores más altos (61.33 % en L-A1) como consecuencia de la característica esponjosa de la médula (Karmegam et al., 2021); no obstante, los estudios no se enfocan directamente en establecer las proporciones de los componentes de la estopa de coco, puesto que se prioriza la productividad para la comercialización y el consumo de productos hacia la industria alimentaria (Granados y López, 2002; Islas y Tzec, 2021; Maruchis et al., 2007), a pesar de que estos subproductos también pueden ser una fuente rentable de ingresos (Islas y Tzec, 2021).
Distribución de tamaño partícula
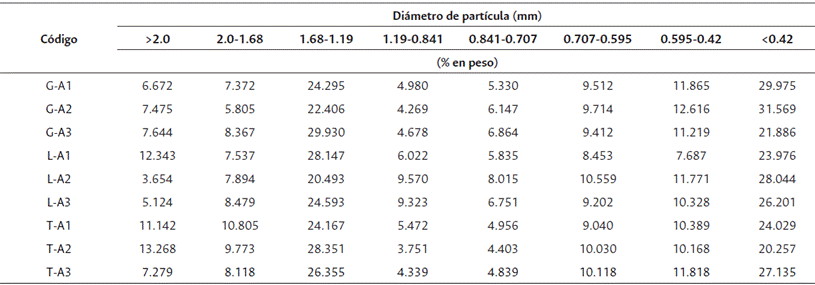
El análisis granulométrico (Tabla 3) indicó que la distribución de partícula en todas las muestras posee una variación similar en todas las fracciones, obteniendo gránulos de médula de coco mayores a 2.0 mm en T-A2, mientras que en G-A2 se alcanzó la mayor cantidad de partículas con un diámetro menor a 0.42 mm; no obstante, Vargas et al. (2008) reportaron un alto porcentaje de partículas mayores a 2.0 mm variando desde un 15.3 % hasta un 39.0 %, al igual que el contenido de partículas finas menores a 0.42 mm es superior, ya que el material particulado menor a 0.50 mm oscila entre un 49.1 % a un 8.5 %; por su parte, Guerrero et al. (2021) obtuvieron una distribución de partícula donde en el tamiz de 2.0 mm se retuvo un 13.69 % del material, semejante a T-A2, y el gránulo más fino menor a 0.50 mm tuvo una proporción de 35.8 %.
También, al no tener un porcentaje alto con partículas muy finas (<0.25 mm) puede favorecer el proceso de formulación para la elaboración de un sustrato de cultivo y su aplicación en campo, puesto que en el proceso productivo se puede generar compactación del sustrato, mayor retención de agua, menor aireación sobre las raíces de las plantas, afectando el rendimiento del cultivo sobre el cual se utiliza (Ansorena, 1994; Guerrero et al., 2021; Noguera et al., 2003).
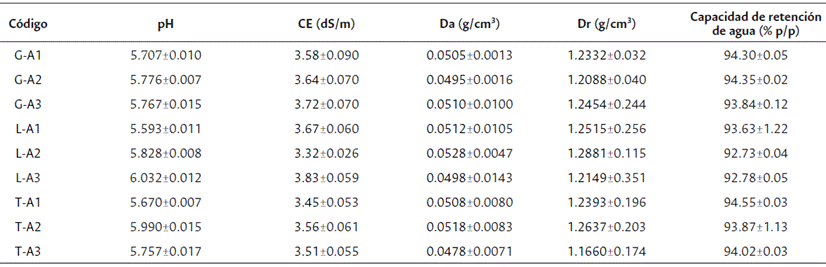
Capacidad de retención de agua
La capacidad de retención de agua en todas las muestras se mantuvo sobre un margen similar (Tabla 4), oscilando entre 92.73 ± 0.04 a 94.55 ± 0.03 % p/p, ya que como lo menciona Guerrero et al. (2021), la médula de coco posee un alto número de poros entre sus partículas que, además de permitir almacenar humedad, facilita el proceso de drenaje; no obstante, durante el cultivo, el flujo constante de agua puede generar un cierto grado de compactación a causa del tamaño de la partícula, provocando una mayor retención de agua (Ansorena, 1994; Vargas et al., 2008); por tanto, es recomendable tener un tamaño de partícula variable que aumente la aireación del sustrato y, a su vez, disminuya la retención de humedad (Noguera et al., 2003).
Densidad aparente
La densidad aparente (Da) de las muestras (Tabla 4) se encuentra dentro del rango de 0.0478 a 0.0528 g/cm3, similar a reportada por (Noguera et al., 2003), quienes obtuvieron una variación de 0.122 a 0.041 g/cm3, influenciada por diferentes tamaños de partícula del material; mientras Guerrero et al. (2021), registraron un valor de 0.14 g/ cm3, además Guerrero et al. (2021), al citar a Quintero et al. (2006), menciona que la densidad aparente para este tipo de material oscila entre 0.05 g/cm3 y 0.4 g/cm3; sin embargo, se atribuye este margen de variación alto al efecto del contenido de humedad cuando se hidrata la médula de coco. La densidad real (Dr) fue muy similar a lo reportado por Guerrero et al. (2021), quien obtuvo una densidad de 1.00 g cm3; además, Guerrero et al. (2021), citando a Quintero et al. (2006), menciona que valores altos (mayores a 1.6 g/cm3) pueden estar influenciados por el método de extracción.
pH
El pH en todas las muestras (Tabla 4) se mantuvo en un rango ligeramente ácido (de 5.593 a 6.032), ubicándose dentro del rango de los valores de 5.04 a 5.6, obtenidos por Vargas et al. (2008), Noguera et al. (2003) y Seob et al. (2021); también coincide con los 5.7 reportados por Crespo et al. (2018); y con los 5.9 encontrados por Guerrero et al. (2021); pero, con valor menor de 6.3 a 6.7, mencionado por Monsalve et al. (2021) y Agarwal et al. (2021) sugieren que el pH óptimo para la médula de coco debe estar entre 5.5 a 6.8, que favorece el crecimiento de la mayoría de las plantas; sin embargo, Karmegam et al. (2021) indican que si la médula de coco se combina con otros materiales, como por ejemplo estiércol de vaca precompostado (1:1), se puede presentar un aumento del pH a 6.84 ± 0.08.
Conductividad eléctrica
En cuanto a los valores de conductividad eléctrica (CE), se determinó que los valores variaron entre 3.51 y 3.83 dS/m (Tabla 4), resultados que fueron menores en comparación con otras referencias como Noguera et al. (2003), quienes reportaron una conductividad entre 3.96 a 7.48 dS/m, la cual estaba influenciada por el tamaño de partícula del material; Seob et al. (2021), encontraron que en muestras de médula de coco fresco presentaban una conductividad de 9.19 dS/m, pero al analizarse durante un periodo de evaluación en campo, este parámetro descendió a 1.8 dS/m en la cuarta semana; es decir, la conductividad eléctrica, al estar asociada al potencial hídrico de la solución del suelo, expresa disminución en el crecimiento de las plantas, al generar inhibición en la absorción del agua cuando la conductividad es alta (Marschner, 2012), superior a 5 dS/m (Guerrero et al., 2021).
Análisis de fitotoxicidad
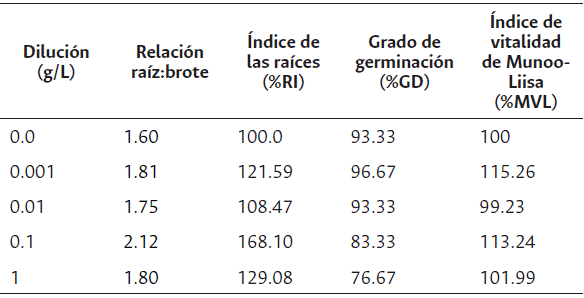
La Tabla 5 permitió determinar que existe diferencia significativa entre los tratamientos, no obstante, no se aprecia efectos de fitotoxicidad de la médula cruda de coco sobre la germinación de semillas de berro (Lepidium sativum), puesto que el índice de vitalidad de Munoo-Liisa (MVL) en los tratamientos son superiores al control, a excepción del 99.23 % de la dilución 0.01 g/L; con un grado de germinación que es proporcionalmente inverso a la concentración de la dilución de médula, donde la dilución 1.0 g/L muestra una leve inhibición, Cesaro et al. (2015) expresan que un índice de germinación menor al 80 % empieza a mostrar señales inhibitorias sobre el crecimiento de las plantas, pero no debe ser menor al 50 % para considerarse fitotóxico (Gavilanes et al. 2016; Vargas et al., 2008).
Por otra parte, la relación raíz:brote muestra que los resultados de los tratamientos son superiores al tratamiento control, y un índice alto de raíz:brote permite que las plantas sean más efectivas en la extracción de nutrientes de las capas más profundas del suelo e influye en la madurez del cultivo como un todo (Flórez et al., 2021); sin embargo, (Ma y Nichols, 2004), al analizar el efecto de fitotoxicidad en lechuga, encontraron que la médula de coco fresca con un tamaño de partícula entre 0.25 y 1.0 mm, genera una afectación en el crecimiento de las raíces, comparada con el tratamiento control, así como se pueden desencadenar desequilibrios nutricionales durante este periodo (Noguera et al., 2003). Sin embargo, en aplicación en campo, la médula sin tratamiento es capaz de disminuir el efecto de fitotoxicidad sobre el crecimiento radicular de las plantas, revirtiendo este efecto a través de tratamientos preliminares de vermicompostaje (Karmegam et al., 2021) o con la adición de carbonato de calcio (Ma y Nichols, 2004), aplicando un lavado con agua limpia que remueva la concentración de sales (Na, Cl, K) y realizando después un tamponado con nitrato de calcio (Ca(NO)3) (Agarwal et al., 2021; Carlile et al., 2015; Seob et al., 2021) o simplemente por la lixiviación de las sales a través del proceso productivo (Vargas et al., 2008).
A pesar de que los resultados de fitotoxicidad pueden parecer contradictorios frente a otras investigaciones, donde estudios previos han demostrado que la médula de coco cruda posee un alto contenido de K, Na y Cl, y esta alta concentración de sal inorgánica también puede contribuir a la inhibición en el crecimiento de las plantas (Gavilanes et al. 2016; Seob et al., 2021), los resultados del presente estudio mostraron que la conductividad eléctrica de las muestras variaba entre 3.51 y 3.83 dS/m, valores que se mantienen dentro de los límites recomendados (<4.0 dS/m) (Guerrero et al., 2021; Karmegam et al., 2021) y, además, disminuye el riesgo inhibidor de crecimiento en las plantas. No obstante, es pertinente corroborar la existencia o no del efecto inhibidor de la médula de coco cruda, a través del envejecimiento en campo y en la aplicación hacia un proceso productivo (Ma y Nichols, 2004; Noguera et al., 2003; Seob et al., 2021).
Conclusiones
La caracterización de la médula de coco de muestras provenientes de la Costa Pacífica Caucana mostró que la proporción de mesocarpio de las variedades analizadas se mantuvo en un rango muy similar a reportes de estudios previos, al igual que las demás propiedades físicas analizadas. Por otra parte, el análisis de fitotoxicidad arrojó que la médula de coco cruda genera un efecto leve de fitotoxicidad en el grado de germinación de la muestra de concentración 1.0 g/L, mientras que el índice de vitalidad de Munoo-Liisa es similar o superior al control, lo que le permite ser un material con un alto potencial de aprovechamiento para la elaboración de sustratos de cultivo.