INTRODUCCIÓN
En el paradigma interpretativo del modelo de Henderson-Hasselbalch (H-H), la alcalosis metabólica en humanos y animales se caracteriza por un aumento en el pH plasmático, con aumento en las concentraciones de bicarbonato. Este modelo ha identificado dos fases de la alcalosis metabólica: la de generación y la de mantenimiento (1-5). La generación requiere que ocurra la pérdida de H+ o la ganancia de HCO3 (6,7). En rumiantes la pérdida de ácido ocurre comúnmente en desplazamiento o vólvulo abomasal, indigestión vagal u obstrucciones intestinales proximales; mientras la ganancia de HCO3 es poco común y se presenta cuando se adiciona bicarbonato o hidróxido de magnesio a las dietas como tratamiento (8,9).
El mantenimiento de la alcalosis metabólica se da como consecuencia de la incapacidad renal para excretar el exceso de HCO3-filtrado (4,5,10-13). En rumiantes se ha identificado que los mecanismos que mantienen la alcalosis metabólica son la disminución en las concentraciones de K+ y Cl- plasmático y la reducción en el volumen circulante (9,12,14-16). También se ha encontrado que la reducción en la concentración de K+ que acompaña a la alcalosis metabólica puede ser una causa o consecuencia del mantenimiento de este desorden (4). La disminución en la concentración de K+ puede generar alcalosis metabólica por la reducción en la tasa de filtración glomerular o la generación de acidosis intracelular (4,9,17-19).
La excreción renal es un factor importante en el control del estado ácido base en pacientes con alcalosis metabólica, en la cual la regulación de la concentración de H+ a través del mantenimiento de la concentración de los diferentes electrolitos es fundamental. Cuando un catión o un anión es excretado en mayor medida con respecto al otro, este es acompañado por la excreción de bicarbonato o de hidrogenión. Estos procesos fisiológicos dentro de los túbulos renales son los que determinan la excreción de H+ (5,9,20-23).
En relación con el paradigma físico-químico de la interpretación de los desórdenes ácido base, no hay hasta el momento estudios que muestren la aplicación de esta aproximación en la orina de pacientes con alcalosis metabólica hipoclorémica. Sin embargo, Constable y colaboradores, en 2009 (9), registraron la aplicación de la aproximación físico-química en la orina de bovinos y la relación de la diferencia de iones fuertes (SID) con el pH. Según esta aproximación, la ecuación general para la electroneutralidad en la orina está determinada de la siguiente manera (20):
-(SID - k) = AT + [NH4] - [HCO3 -]
Donde el SID corresponde a la diferencia entre la suma de los cationes y los aniones completamente disociados en la orina, bajo condiciones de pH entre 4,7 y 8,7; y k corresponde al SID actual, cuando el pH es de 7,4 y AT a la acidez titulable de la orina (20).
Bajo un rango más estrecho de pH, entre 5,0 y 8,0, se puede derivar la ecuación que expresa la relación del pH con las siguientes variables independientes SID, [NH4], [PO4] y PCO2; y tres constantes: la constante de disociación de H2CO3 (K1'), la de disociación del H2PO4 (Ka2) y la solubilidad del CO2 en la orina (S). De esta manera se obtiene la siguiente ecuación para el pH (20):
Como en rumiantes, las concentraciones de fosfatos en la orina son menores a las de aniones fuertes, cationes fuertes y amonio. De hecho, son cercanas a 0 cuando se maneja un rango de pH entre 5,0 y 8,0. La ecuación anteriormente mencionada se puede simplificar de la siguiente manera (20):
Donde el SID corresponde a:
SID = [K+] + [Na+] + [Mg+] + [Ca+] - [Cl-] - [SO4 2-].
La ecuación descrita anteriormente solo será válida si la orina se mantiene dentro del rango de pH mencionado. Además de ello, esta ecuación indica que la concentración de bicarbonato urinario no afecta directamente el pH, lo cual revela que esta es una variable dependiente en la orina al igual que en el plasma (20). La principal limitación de la aproximación físico-química en la orina es obtener valores exactos del SID, ya que la medición de cada anión y catión por separado trae consigo un error propio en su medición (20). Teniendo en cuenta esta limitación, se estableció que la titulación de la orina proporciona un método acertado para la medición del SID, y así en el caso de bovinos puede ser calculado de la siguiente manera (20):
SID = excreción neta de base (ENB) + 2,6 = -excreción neta de ácido (ENA) + 2,6
Este modelo, desarrollado por Constable y colaboradores (9), predice que los valores de (SID - k) en la orina son equivalentes a la ENB o -ENA (20).
Con base en este modelo (20), el objetivo del presente estudio fue determinar la relación entre el pH urinario y el SID en ovinos con alcalosis metabólica hipoclorémica mediante el cálculo del SID a través de la ENA, en un modelo experimental de pérdida masiva de flujo abomasal por medio de una cánula duodenal.
MATERIALES Y MÉTODOS
Sujetos experimentales
Un total de 8 ovinos, de raza criolla, hembras no preñadas, con edades entre 2 y 6 años, pesos entre 25 y 45 kg, fueron usados en el experimento. Los animales fueron mantenidos en la Clínica de Grandes Animales de la Universidad Nacional de Colombia, donde recibieron supervisión veterinaria continua. Fueron alimentados con pasto kikuyo (Pennisetum clandestinum) y agua a voluntad, junto con suplementación de 40 g por animal de sal mineralizada para ovinos (Ganasal Ovi-Caprinos®).
Cada uno de los sujetos experimentales fue sometido a la implantación de una cánula duodenal en forma de T construida a base de nylon quirúrgico (figura 1), la cual consta de dos tapones, uno de los cuales permite el paso normal del flujo abomasal, y el otro genera bloqueo completo del flujo para la inducción de la alcalosis metabólica hipoclorémica. La cánula fue colocada por medio de laparotomía exploratoria por flanco derecho en el duodeno proximal, y adicionalmente se realizó la exteriorización de la arteria carótida en cada sujeto experimental (2,19,23,24).

Figura 1 Cánula duodenal en forma de T, en la que se observa el tapón que bloquea completamente el paso de contenido abomasal y permite el drenaje hacia el exterior del animal, para la generación de la alcalosis metabólica hipoclorémica
Los animales fueron mantenidos en el estudio bajo monitoreo médico veterinario las 24 h, con el fin de identificar alteraciones patológicas durante la recuperación de la cirugía (14 días), más un periodo de adaptación (7 días), durante el proceso experimental, hasta que la condición de aciduria paradójica se reprodujera, o cuando las condiciones fisiológicas de cada uno de los sujetos se deterioraran (figura 2). En ese momento se decidió la realización de la eutanasia, la cual efectuó un médico veterinario con pentobarbital sódico vía endovenosa, previa tranquilización con xilazine.
Periodo experimental
Se suspendió la administración de sal mineralizada una semana antes del inicio de la fase experimental. El periodo experimental se dividió en dos etapas (figura 2). La primera correspondió al control y se realizó por 48 h; durante este periodo se hizo la toma de muestras cada 24 h para las variables en la orina. La segunda correspondió a la apertura de la cánula y la inducción de la alcalosis metabólica hipoclorémica; durante esta etapa se tomaron muestras para las variables urinarias cada 24 h. La toma de muestras fue suspendida cuando el sujeto experimental desarrolló aciduria, o cuando la condición física se deterioró.
Toma de muestras
Las muestras de orina fueron tomadas a las 2:00 p. m. todos los días cada día, momento durante el cual, según lo evidenciado por los resultados de ENA, son más confiables (9). Las muestras fueron tomadas por micción natural, y cuando esta no fue posible, se utilizó una sonda urinaria calibre 8. Se recolectaron en beaker de plástico con tapa, y fueron procesadas durante las siguientes 4 h. El restante se almacenó en tubos de criopreservación de 2 ml y se congelaron a menos -70 °C para su posterior medición (9).
Procesamiento de muestras
La determinación de la ENA ha sido registrada por diferentes autores (3,4,21,25), pero para el presente estudio la acidez titulable y el amonio se calcularon con el método utilizado por Jorgensen y colaboradores (21), en el que se titula la orina manualmente. El pH se midió por medio de un potenciómetro (Schott Lab 850®, con electrodo Schott pH electrode Blue Line®). El SID se calculó con base en la ENA (SID = ENB + 2,6 = -ENA + 2,6) de acuerdo con lo evidenciado por Constable y colaboradores (9). Para el cálculo del pH urinario se usó la fórmula también utilizada por Constable y colaboradores (9), para pH urinario con rango entre 5 y 8 (3,4,9,21,25).
Análisis estadístico
Para el presente estudio se realizó inicialmente un análisis de tipo descriptivo, usando promedios y medias para evaluar el comportamiento del pH durante la fase experimental, y luego análisis de correlación entre el pH medido y el pH calculado, basados en el SID calculado con la ENA, el SID calculado y el pH calculado y el SID calculado y el pH medido. Para esto se hizo una prueba de Friedman, con el objetivo de determinar si existieron o no diferencias significativas. Esta prueba se implementó por separado para los tiempos de control e inducción de la alcalosis metabólica con una p <= 0,05. También se realizó la prueba de correlación de Pearson entre los siguientes pares de variables: el pH calculado y el medido, el SID calculado y el pH calculado y, finalmente, entre el SID calculado y el pH medido, usando una p <= 0,01.
El presente estudio experimental se llevó a cabo estrictamente según las normas estipuladas en la Ley 84 de 1989 y la Resolución 8430 de 1993 de la República de Colombia. Además, fue aprobado por el Comité de Ética de la Facultad de Medicina de la Universidad Nacional de Colombia, de acuerdo con el Acta de Evaluación 83 del 21 de junio de 2012.
RESULTADOS
De los 8 sujetos experimentales, solo 7 fueron utilizados en el experimento, debido a que uno de ellos desarrolló peritonitis durante los 14 días de la fase de recuperación de la cirugía. Los registros obtenidos durante la fase tanto experimental de control como de inducción de la alcalosis metabólica fueron 56 lecturas, de la cuales 22 ocurrieron durante el periodo de control, y 34, durante el de inducción. Sin embargo, 3 de los sujetos experimentales presentaron dificultades en la apertura adecuada de la cánula al momento de la inducción, por lo que no se produjo pérdida de contenido abomasal y los datos de estas lecturas, que fueron 14, se consideraron como parte del periodo de control, ya que no mostraron ningún tipo de alteración en ENB ni en AT ni en el equilibrio ácido base. Esto hizo que en tales sujetos experimentales el periodo de control durara 5.
El periodo de inducción varió entre los sujetos experimentales. Se encontraron duraciones de 2 d para un sujeto; 4 para 2; 5 para 1; 6 para 2, y 7 para 1. De estos animales, solo 2 desarrollaron un pH ácido en la orina (aciduria paradójica) durante la fase de inducción. Se observó que aquellos animales en los cuales el tiempo de inducción tomó entre 6 y 7 días fueron los únicos que desarrollaron este fenómeno de aciduria paradójica.
Los sujetos experimentales mantuvieron un rango promedio de pH medido entre 8,313 (DE 0,089) y 8,403 (DE 0,040), mientras el rango promedio del pH calculado tuvo un rango entre 8,166 (DE 0,372) y 8,420 (DE 0,095) en el periodo de control. En la fase de inducción de la alcalosis metabólica previa al desarrollo del fenómeno de aciduria paradójica, el promedio de pH medido se mantuvo entre 8,200 (DE 0,123) y 8,459 (DE 0,076), mientras que el promedio calculado estuvo entre 8,317 (DE 0,105) y 8,423 (DE 0,155). Finalmente, durante el desarrollo del fenómeno de aciduria, el rango promedio del pH medido bajó y se mantuvo entre 6,150 (DE 0) y 7,363 (DE 1,475), mientras el calculado fluctuó entre 7,041 (DE 0) y 7,645 (DE 1,145).
En la tabla 1 se ilustra el promedio de pH calculado y medido durante los días de control e inducción de la alcalosis metabólica durante el estudio, así como la diferencia que existe entre el pH calculado y el medido. Aquí las variaciones entre la diferencia absoluta mínima entre el pH calculado y el medido solo fueron de 0,25, mientras que la diferencia máxima fue de 0,891 en las dos fases del estudio.

Tabla 1 Promedios de pH urinario durante la fase experimental de control correspondiente a 5 días y la fase de inducción de la alcalosis metabólica hipoclorémica correspondiente a 7 días
Adicionalmente, en la figura 3 se muestran las tendencias de los promedios tanto de pH calculado como medido a través del tiempo. Aquí se puede observar una clara orientación creciente en la diferencia absoluta por cada día que transcurre específicamente en el tiempo de inducción; es decir, a mayor tiempo durante la fase de inducción, el pH calculado se distancia del medido, como también se evidencia en la tabla 1, con los valores absolutos, mientras que para los días de control las diferencias no muestran ninguna tendencia.

Figura 3 Barras del comportamiento del pH urinario durante las fases de control e inducción de la alcalosis metabólica hipoclorémica, en las que se puede apreciar la disminución marcada en el pH en las últimas 48 h de la fase de inducción, lo cual muestra el desarrollo del fenómeno de aciduria paradójica
Los resultados de la prueba de Friedman (p <= 0,05) sobre diferencias significativas entre el pH urinario calculado y medido durante las fases de control e inducción de la alcalosis metabólica indican que durante el periodo de control (0,201) no existe diferencia entre las dos variables, pero durante la inducción (0,0) sí se evidencian diferencias. A pesar de estas diferencias, la correlación de Pearson mostró un valor de r = 0,874 (p <= 0,01), lo cual indica una alta correlación entre el pH calculado y el pH medido, lo que se puede apreciar en el gráfico de dispersión de la figura 4, que confirma la aplicación de la teoría de iones fuertes en ovinos con alcalosis metabólica hipoclorémica.
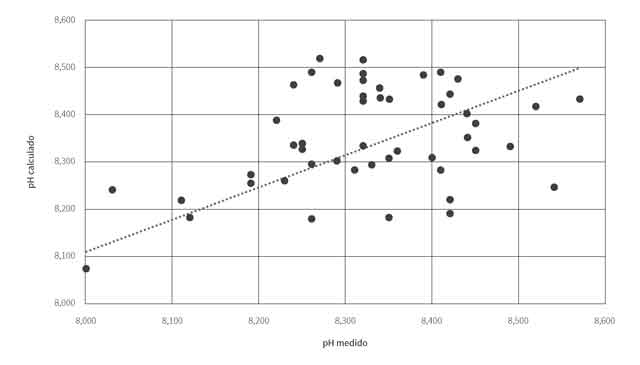
Figura 4 Dispersión de datos según el coeficiente de correlación de Pearson, que muestra la concentración de datos y confirma la asociación entre el pH medido y el calculado con la aplicación de la teoría de iones fuertes en la orina
Cuando se calculó el SID urinario con la ENB, se encontró que mientras se mantuvo un pH urinario alcalino, este mostró valores entre 208,779 (DE 54,943) y 133,671 (DE 63,568) mmol/L. Sin embargo, el valor bajó drásticamente cuando se presentó el fenómeno de aciduria, con promedios entre -7,900 (DE 1,061) y 98,433 (DE 91,73) mmol/L. Este comportamiento también mostró la ENB, pero en sentido inverso, mientras se mantuvo el pH alcalino. De esta manera, el promedio mínimo observado fue de -131,071 (DE 69,481)- -206,179 (DE 59,700) mmol/L.

Figura 5 Dispersión de datos según el coeficiente de correlación de Pearson que muestra la concentración de datos y confirma la asociación entre el SID calculado con la ENA y el pH calculado, lo cual evidencia la asociación entre estas variables y la importancia del SID como determinante del pH urinario en ovinos con alcalosis metabólica hipoclorémica
El valor de la correlación de Pearson entre el SID calculado y el pH calculado fue de p = 0,838, mientras la correlación de Pearson entre el SID y el pH medido presentó un valor de p = 0,588. Esto muestra una fuerte correlación entre el SID calculado y el pH calculado, pero una media correlación entre el SID calculado y el pH medido. Los valores mencionados se pueden apreciar en el gráfico de dispersión, en el caso del SID y el pH calculado. En la figura 5 se observa una clara tendencia, pero esta no se aprecia de la misma manera en el SID y el pH medido en la figura 6.

Figura 6 Dispersión de datos según el coeficiente de correlación de Pearson, que muestra la concentración de datos y confirma la asociación entre el SID calculado con la ENA y el pH medido, lo cual evidencia la asociación entre estas variables y la importancia del SID como determinante del pH urinario en ovinos con alcalosis metabólica hipoclorémica
En el caso del amonio, se evidenció un claro aumento en las concentraciones de este metabolito cuando la orina mostró el fenómeno de aciduria. Se encontraron concentraciones promedio entre 4,667 (DE 3,166) y 16,250 (DE 0) mmol/L. Dicho comportamiento de aumento en las concentraciones mientras se desarrolla la aciduria es evidente también con la acidez titulable -100,500 (DE 88,556) - -5,750 (DE 0) mmol/L.
En la tabla 2 se muestran los promedios de la acidez titulable, la concentración de amonio, la ENB y la diferencia de iones fuertes para la orina de los sujetos experimentales durante las fases de control y de inducción de la alcalosis metabólica. Cabe resaltar que aquellos sujetos experimentales que desarrollaron aciduria durante el experimento muestran una disminución marcada en el SID, como se muestra en la figura 7, y aumento en los valores de amonio, acidez titulable y ENB.

Tabla 2 Promedios de AT, NH4, ENA y diferencia de iones fuertes (SID) urinario durante la fase experimental de control correspondiente a 5 días y la fase de inducción de la alcalosis metabólica hipoclorémica correspondiente a 7 días

Figura 7 Comportamiento del SID durante las fases de control e inducción de la alcalosis metabólica hipoclorémica, en el que se puede apreciar el descenso marcado en los valores de esta variable determinante del pH al momento de la generación de la aciduria paradójica y que explica el porqué del descenso en el pH urinario
DISCUSIÓN
El hecho de que se haya extendido la fase de control en tres de los sujetos experimentales se pudo deber al tipo de cánula que se implementó en el desarrollo del estudio, ya que las cánulas en forma de T, como la usada en el presente modelo experimental, se encuentran diseñadas para evaluación de componentes nutricionales en la dieta de rumiantes (19,20). Los trabajos realizados en el análisis metabólico de estado ácido base usan modelos con cánulas de reentrada, y obstruyen el paso del contenido al intestino delgado. Estos modelos garantizan una completa pérdida de contenido o bloqueo en el paso de este, al momento deseado; mientras que con las cánulas en forma de T se presenta taponamiento por el contenido alimenticio, debido al diámetro de estas, evento que dificulta el adecuado manejo de la condición deseada. Sin embargo, la liberación de contenido abomasal es abundante mientras se garantice que exista un flujo adecuado y continuo (20,26-28).
Por otra parte, las cánulas en forma de T permiten el paso de contenido alimenticio por sus bordes externos, hecho que posiblemente extiende los tiempos en el desarrollo de la alcalosis metabólica hipoclorémica, y desde luego hacen más lenta la compensación renal. Esto explica el hecho de que en el actual modelo experimental el desarrollo de la aciduria se tomara entre 6 y 7 días, mientras en otros modelos tan solo se demora entre 2,5 a 4 días. Es posiblemente por este mismo evento que no todos los sujetos experimentales desarrollaron dicha alteración antes de su deterioro físico y la realización de la eutanasia (24,26,27).
A pesar de lo mencionado, se decide realizar el presente estudio con las cánulas en forma de T, ya que en el país no se cuenta con cánulas de reentrada y no fue posible su consecución para el estudio por motivos de presupuesto; además, no sería posible la obstrucción completa del contenido intestinal por conflictos éticos.
El comportamiento del pH en la orina se mantuvo alcalino durante casi toda la fase experimental, como se encuentra registrado en diferentes estudios sobre la alcalosis metabólica hipoclorémica, y solo descendió a concentraciones ácidas en la últimas 48 h del experimento, seguramente como consecuencia del desorden electrolítico y la compensación frente a dichos estados. Sin embargo, en el presente estudio, aunque se midieron los electrolitos, y se tuvieron en cuenta los resultados obtenidos con los equipos con que se contaba, las mediciones no fueron confiables, y los resultados fueron descartados; por lo tanto, no se pudieron medir las alteraciones electrolíticas que explicarían acertadamente el fenómeno que se presenta cuando el pH desciende. Por tal razón, solo se podría especular sobre las causas de dicho descenso (26,28,29). No obstante, se determinó el SID de manera indirecta, utilizando la fórmula sugerida por Constable y colaboradores en 2009 (9), que incluye la ENA y que a su vez representa la diferencia electrolítica.
A pesar de observarse una diferencia aparentemente amplia entre los valores absolutos medidos y calculados del pH, la prueba de Friedman confirmó que durante el control no existieron diferencias significativas (p <= 0,05) entre el pH medido y el calculado. Sin embargo, esta diferencia fue apreciable durante el periodo de inducción de la alcalosis metabólica, muy seguramente debido a los desórdenes electrolíticos que se presentan durante este periodo experimental. Pero el análisis de correlación de Pearson (p = 0,874 [p <= 0,01]) evidencia una alta correlación entre los valores calculados y los medidos. Ello sugiere que a pesar de encontrarse una aparente diferencia entre estos valores, sobre todo durante la fase final de inducción de la alcalosis metabólica, dicha diferencia no altera la predicción del pH, y seguramente se da como consecuencia del desorden electrolítico que se está presentando en el plasma y su efecto en la zona renal (9).
Por otra parte, la correlación de Pearson confirma los hallazgos de Constable y colaboradores (9), quienes sustentan que el pH urinario de los bovinos es determinado por el SID urinario, la concentración de amonio y la PCO2, lo que obtuvieron aplicando la ecuación descrita por para pH urinario entre 5 y 8. En el presente estudio dicha ecuación fue igualmente valedera para ovinos que manejan el pH urinario dentro de estos rangos, y se aplican las mismas variables independientes. Por lo tanto, en el caso de ovinos se confirma, de esta manera, que la concentración de bicarbonato no afecta directamente el pH, y por ello es considerada una variable dependiente de las ya descritas variables independientes (9).
El hecho de que exista una correlación mayor entre el SID y el pH calculado que para el medido puede deberse a que el pH calculado es tomado a partir de diferentes variables que desde el punto de vista teórico son las generadoras del valor real. Sin embargo, siempre existirá cierto grado de error al momento de los cálculos, lo cual no permite obtener un valor idéntico sino más bien muy cercano al esperado, que es lo que finalmente se encontró con la alta correlación entre el pH calculado y medido. Además de esto, solo se está correlacionando una variable, y, como ya se sabe, según la teoría de diferencia de iones fuertes en la orina, son el SID y los ácidos débiles no volátiles los que mayormente afectan este valor. Por lo tanto, esta correlación muestra que otros factores contribuyen al mantenimiento del pH en los valores medidos, siendo el SID uno de los más importantes (9).
En este estudio no fue posible la determinación directa del SID, debido a la no confiabilidad de las mediciones de los electrolitos. Sin embargo, el SID se obtuvo utilizando la fórmula matemática descrita por Constable y colaboradores en 2009 (9), en la cual el SID es igual a (SID = ENB + 2,6 = -ENA + 2,6), donde la ENA se obtuvo por la titulación de la orina. Los valores del pH calculado se obtuvieron usando los valores de este SID. Los resultados muestran un grado importante de confiabilidad gracias a la alta correlación entre el pH urinario medido y el pH urinario calculado (p ≤ 0,01). Esta fórmula es aplicable para rangos de pH entre 5 y 8, lo cual permite determinar el pH urinario cuando no se cuenta con los equipos necesarios para la medición de electrolitos, y se aplica la teoría de iones fuertes en la orina de ovinos (9). Esto, desde el punto de vista tanto investigativo como clínico, facilita la interpretación del estado ácido base sin necesidad de realizar la medición de cada uno de los electrolitos implicados.
Cuando se aplicó la anterior fórmula matemática para el cálculo del valor del SID, se encontró que en el momento en que se presentaba el fenómeno de aciduria en la orina de pacientes con alcalosis metabólica hipoclorémica descendían drásticamente los valores de SID; según la teoría de iones fuertes o el análisis físico-químico, en condiciones alcalinas los valores de este parámetro son altos, mientras que en condiciones ácidas estos valores descienden. Por lo tanto, el comportamiento del SID durante el experimento es concordante con lo estipulado en esta teoría. Adicionalmente, no se cuenta con parámetros de referencia de estos valores de SID, con los cuales comparar los actuales resultados, pero su comportamiento, como ya se comprobó, corresponde al esperado (5,6,9,22,30,31). La aplicación de esta fórmula permitirá realizar de manera económica y práctica el cálculo del SID, lo cual es importante en diferentes investigaciones que implican el uso de este modelo y la medición de esta variable, como en el cálculo de las dietas catiónicas para la prevención de enfermedades metabólicas en rumiantes.
Existen diferentes estudios sobre el efecto directo del escape del CO2 en la medición del pH. Algunos autores sugieren que este puede afectar incrementando 0,5 unidades sobre el pH real. Sin embargo, otros estudios exponen que este solo incrementa el pH urinario en 0,06 unidades. En el presente estudio se decidió asumir que la PCO2 era constante, y por lo tanto no afectaba ni la medición ni el cálculo del pH (9); y como se evidenció, existe una alta correlación entre el pH calculado y el medido, lo que permite sustentar que la asunción de una presión de CO2 constante es valedera para la realización de los cálculos del pH, y que el CO2 no afecta de manera significativa dichos cálculos. Lo anterior, por ende, permite inferir que posiblemente los grandes involucrados en la determinación del pH son el SID y la concentración de amonio (9).
Cuando el pH urinario se encuentra alcalino, la excreción de amonio es casi cercana a 0, como se evidencia en diferentes estudios (25,32). Esto explica por qué los valores encontrados en la concentración de amonio antes de la presentación del fenómeno de aciduria fueron bajos. En el presente estudio, los valores de amonio se incrementaron significativamente durante la aciduria en los sujetos experimentales; este aumento ha sido relacionado con la disminución en la concentración de K+, disminución que ocurre posiblemente por un estímulo de la reabsorción de K+, lo cual generaría, desde el punto de vista físico-químico, una disminución en el valor del SID, y de esta manera una disminución del pH urinario, lo que estimularía la producción de amonio en túbulos renales. Esta hipótesis no se pudo comprobar, ya que no fue posible la medición de electrolitos y el cálculo directo del SID. Sin embargo, esta inferencia es la presunción más cercana a la explicación de este comportamiento en las concentraciones de amonio (9,26,32-34).
Cabe resaltar, en este punto, que Constable y colaboradores (9) proponen que las concentraciones de K+ tienen un efecto marcado en el pH urinario en bovinos. Proponen, además, que cuando existe una excreción alta de K+ en la orina, el pH se torna alcalino, y que cuando estas bajan, el pH urinario es ácido, basado en la ecuación para predecir el pH en rangos entre 5 y 8. Teniendo en cuenta que la concentración de K+ es dependiente del consumo y del estado ácido base, en el presente estudio, en el cual los sujetos experimentaron la alcalosis metabólica y desarrollaron anorexia, se podría explicar la presencia de aciduria por las concentraciones bajas de K+ en la orina. Sin embargo, dicha hipótesis no pudo ser comprobada debido a la no determinación de las concentraciones electrolíticas de K+ en la orina (9,33,34).
Finalmente, se puede concluir del presente estudio que el pH calculado urinario, según el aboramiento físicoquímico, es muy similar al pH medido en la orina de ovinos con alcalosis metabólica hipoclorémica. Por otra parte, también se puede señalar la importancia del SID como determinante del pH, dada la alta correlación entre esta variable y el valor del pH.

















