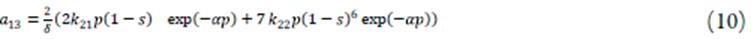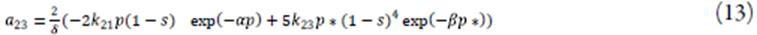INTRODUÇÃO
Perilartina (figura 1 à esquerda, (S)-4-(prop-1-en-2-ilo)ciclohex-1-enaldoxima, M=165 g/mol, número CAS: 30950-27-7, número PubChem: 5366782), isto é anti-aldoxima de perilaldeído, é um adoçante natural, extraído das folhas da perila japonesa (planta shiso) [1-4]. Ela é considerada duas vezes mais doce que a sucralose, 4 vezes mais doce que a sacarina e 2000 vezes mais doce que o açúcar comum.
Além da própria perilartina, o seu derivado etérico (figura 1, à direita) também é usado, apesar de ser muito menos doce. Ele possui o dulçor bastante próximo do de aspártamo.
A oxima é biodegradável e bioacessível, ao contrário dos adoçantes sintéticos como aspártamo, sacarina e sucralose. Outrossim, ela não é considerada tóxica ou perigosa para o ambiente.
No Japão a perilartina é amplamente usada na indústria farmacêutica como corretor de sabor e componente de alimentação especial. Também, ela é componente da receita original do molho de soja (shoyu).
Posto que a perilartina se considere segura, ela pode ser alérgica para pessoas alérgicas para produtos da perila japonesa [5, 6]. Outrossim, a hidroxilamina e seus derivados tóxicos podem aparecer durante o seu metabolismo em algumas pessoas. Vale a pena mencionar que a perilartina e derivados muito pouco se usam pela indústria alimentar e farmacêutica fora do Japão, o que pode ser usado para verificar se o produto alegadamente produzido no Japão é realmente japonês. Destarte, o desenvolvimento de um método rápido e eficiente da detecção da perilartina é realmente natural, e os métodos eletroanalíticos podem providenciar-lhe bom serviço [7-15].
Por ora, nenhum método eletroanalítico para a detecção da perilartina há sido desenvolvido. Entretanto, aldoxima pode ser eletroquimicamente ativa, podendo ser tanto reduzida como oxidada. Em ambas as opções, é preferível usar elétrodos quimicamente modificados, que diminuem a sobretensão e aumentam a sensibilidade do elétrodo e a sua afinidade ao análito [16-30].
Tanto processos catódicos como anódicos podem ser aplicados à perilartina. No último caso, é preferível usar oxidantes fortes e específicos, haja vista que o grupo funcional da oxima é um aceptador de elétrons, o que aumenta o potencial da oxidação do analito e sobrevoltagem.
Um desses oxidantes é o dióxido de cobalto. É um oxidante bastante forte, já que o estado de oxidação +4 é bastante instável para cobalto. Assim, vista a instabilidade do dióxido de cobalto, é preferível usar como modificador de elétrodo um composto bem mais estável, o oxihidróxido de cobalto trivalente, já amplamente usado em sistemas eletrocatalíticos e eletroanalíticos [31-38]. Na etapa electroquímica, o oxihidróxido é oxidado, rendendo o dióxido de cobalto (1):
Depois, o dióxido oxida a perilartina, conforme o exposto abaixo.
Para aumentar o desempenho funcional do oxihidróxido e do dióxido de cobalto, é preferível usá-lo como componente de um compósito híbrido, cuja fase orgânica seria um polímero condutor [39-42] ou composto afim (exemplo, corante esquárico) [43-46]. A fase orgânica desempenha funções de matriz estabilizadora para fase inorgânica, além da função de mediação da transferência de elétron, providenciando a aparição e interpretação do sinal analítico.
No entretanto, o seu uso poderia acarretar uma influência comportamental, nociva à estabilidade do sistema e à sua eficiência eletroanalítica [47-53]. Destarte, o uso prático deste sistema eletroanalítico não pode ser realizado sem uma descrição teórica prévia do comportamento do sistema, o que se faz neste trabalho.
Assim, neste trabalho, pela primeira vez, faz-se uma análise comportamental do sistema eletroanalítico da detecção eletroquímica da perilartina sobre o oxihidróxido de cobalto, emparelhado com o dióxido de cobalto (IV), estabilizado pelo corante esquaraínico. A análise comportamental do sistema eletroanalítico faz-se mediante o desenvolvimento e a análise do modelo correspondente. Com isto também se faz a comparação do comportamento do sistema eletroanalítico com o dos semelhantes [54-56].
O SISTEMA E O SEU MODELO
Neste caso, a oxidação da perilartina se realiza no meio ligeira ou moderadamente básico. Nele, o oxihidróxido de cobalto é oxidado conforme a reação (1). Já a perilartina pode ser oxidada por dois mecanismos:
Os fragmentos alcénicos são oxidados conforme o mecanismo da reação de Wagner, rendendo os polióis correspondentes. O fragmento glicólico, por sua vez, é imediatamente oxidado, rendendo uma dicetona;
O grupo funcional da oxima é oxidado para render o íon do "pseudoácido". O "pseudoácido" é uma das formas do nitrocomposto, existente no meio básico (figura 2).
Como o pseudoácido é ionizado, a formação do seu íon aumenta a condutividade e a força iónica da dupla camada elétrica (DCE), o que pode contribuir para a formação da positiva conexão de retorno no sistema eletroanalítico.
Esquematicamente, o processo eletroanalítico pode ser exposto na figura 3:
Havendo vista o supracitado, para descrever o comportamento do sistema eletroanalítico em questão, usar-se-á o conjunto de três equações diferencias de balanço com as variáveis:
p: concentração da perilartina na camada pré-superficial;
p*: concentração do íon do pseudoácido na camada pré-superficial;
c: o grau do recobrimento da superfície pelo oxihidróxido de cobalto.
Para simplificar a modelagem, supomos que o reator esteja sob agitação intensa (destarte, podemos menosprezar o fluxo de convecção), que o eletrólito de suporte esteja em excesso (destarte, podemos menosprezar o fluxo de migração). Outrossim, supomos que o perfil concentracional das substâncias na camada pré-superficial seja lineal, e a sua espessura, constante, igual a δ.
Diante do exposto, o comportamento do sistema será descrito por um conjunto de equações diferenciais (2), conforme:
Aqui, p é coeficiente de difusão do edulcorante, p0 é a sua concentração no interior da solução, c é a concentração superficial máxima do oxihidróxido de cobalto, e os parâmetros r são correspondentes velocidades de reações, calculadas conforme:
Sendo os parâmetros k constantes das velocidades das reações, α e β descrevem as influências da formação dos compostos iónicos na dupla camada eléctrica, F é o número de Faraday, ϕ0 é salto do potencial, relativo ao potencial da carga zero, R é a constante universal de gases e T é a temperatura absoluta.
Como a formação do íon do pseudoácido contribui para a condutividade e a força iónica da dupla camada eléctrica, isso gera a oposição entre aumento da condutividade e capacitância da capa e diminuição da atividade da forma inicial da perilartina. Isto pode ser responsável pelo comportamento oscilatório. Apesar disto, o compósito CoO(OH) (corante esquárico) pode ser um modificador eficiente do elétrodo, conforme exposto abaixo.
RESULTADOS E DISCUSSÃO
Para investigar o comportamento do sistema com a determinação da perilartina, assistida pelo compósito CoO(OH) (corante esquárico) analisamos o conjunto de equações diferenciais (2) mediante a teoria de estabilidade linear. Os elementos estacionários da matriz Jacobiana podem ser representados como:
Em que
Para investigar a estabilidade do estado estacionário, aplicamos ao conjunto de equações diferenciais (2) o critério de Routh-Hurwitz. Evitamos as operações com expressões grandes, introduzindo as novas variáveis e expondo o Jacobiano conforme:
Abrindo os parênteses e aplicando o requisito Det J<0, saliente do critério, nós obtemos a condição de estabilidade do estado estacionário, apresentada como (18):
Este sistema é bastante parecido com os outros sistemas, envolvendo o cobalto tetravalente e com a determinação da hidrazina sobre o cobre trivalente simultaneamente [56]. Como anteriormente, o processo eletroanalítico é controlado tanto pela difusão como pela cinética do processo. Entretanto, o fator cinético tende a ser mais importante, haja vista a formação do íon do pseudoácido, cujo sal é um eletrólito mais conductor que a própria perilartina.
Como não há reações laterais, capazes de comprometer a estabilidade do analito ou do modificador, a estabilidade do estado estacionário será eletroanaliticamente eficiente. A dependência linear entre o parâmetro eletroquímico e a concentração manter-se-á numa região vasta de parâmetros do sistema, e o limite de detecção será relativamente baixo.
Este limite é descrito pela instabilidade monotônica, descrevendo a margem entre os estados estacionários estáveis e instáveis. A sua realização é condicionada ao requisito de Det J=0, ou:
O comportamento oscilatório neste sistema é passível de observer, já que os elementos da diagonal principal do Jacobiano possuem elementos, que podem ter valores positivos. A sua positividade descreve a já mencionada positive conexão de retorno.
Neste caso, o comportamento oscilatório pode ser causado pelos dois fatores. Além do elemento jk
1
exp  > ose j<0, descrevendo os câmbios na condutividade da DCE e da superfície durante a reação eletroquímica, os elementose αK
21
P(1-S)2
EX-P(-αP)>0eaK
22
p(1-S)
7
exp(-αp)>0 if α>0eβk
23
p*(1-s)5exp(-βp*)>0eβ0 ese, também descrevem o comportamento oscilatório. Este comportamento, assim, será causado pelas influências da reação química, cujo produto é o íon do pseudoácido, que, posteriormente, também sofre alterações, na força iónica, estrutura e actividade de cada íon na dupla camada. Isto é responsável pelos câmbios cíclicos na condutividade e capacitância da camada.
> ose j<0, descrevendo os câmbios na condutividade da DCE e da superfície durante a reação eletroquímica, os elementose αK
21
P(1-S)2
EX-P(-αP)>0eaK
22
p(1-S)
7
exp(-αp)>0 if α>0eβk
23
p*(1-s)5exp(-βp*)>0eβ0 ese, também descrevem o comportamento oscilatório. Este comportamento, assim, será causado pelas influências da reação química, cujo produto é o íon do pseudoácido, que, posteriormente, também sofre alterações, na força iónica, estrutura e actividade de cada íon na dupla camada. Isto é responsável pelos câmbios cíclicos na condutividade e capacitância da camada.
As oscilações são semelhantes às já descritas experimentalmente [49-53] e teoricamente [54-56].
O mesmo modelo pode também descrever o processo eletroanalítico análogo, mas que emprega o polímero condutor o material de carbono em vez do corante. Outros oxidantes, capaz de assistir a detecção eletroquímica da perilartina são os compostos de bismuto no estado de oxidação +5, cério tetravalente, os ferratos. O seu comportamento com a perilartina pode ser efetivamente descrito por este modelo.
CONCLUSÔES
A análise teórica do processo eletroanalítico da detecção da perilartina, assistida pelo par CoO(OH) - CoO2, estabilizado por um corante esquaraínico, deixou concluir que:
Se trata de um processo eletroanalítico eficiente, em que o composto de cobalto funciona como substância ativa, e o corante desempenha o papel de mediador;
O processo eletroanalítico é controlado pelo tanto pela difusão do analito, como pelos factores cinéticos;
A realização do comportamento oscilatório é mais provável que no caso mais simples e comum, haja vista os câmbios cíclicos da força iónica da dupla camada elétrica, causados pela formação do íon do "pseudoácido".