Introducción
El ibuprofeno es un compuesto farmacéutico que actúa como antiinflamatorio no esteroideo y es una de las drogas más empleadas para tratar la inflamación, el dolor y la fiebre. Tiene propiedades analgésicas y antiinflamatorias y se usa para el dolor medio y moderado, como dolor de cabeza, dismenorrea, dolor dental, dolor postoperatorio y desórdenes musculoesqueléticos de las articulaciones como osteoartritis y artritis reumatoidea [1]. El diclofenaco sódico es otro de los farmacéuticos pertenecientes al grupo de los antiinflamatorios no esteroideos (AINEs) más utilizados. Al igual que el ibuprofeno, tiene efecto analgésico, antipirético y antiinflamatorio y se usa para el tratamiento de la artritis reumatoidea, osteoartritis y lesiones musculoesqueléticas. Ambos compuestos farmacéuticos tienen baja solubilidad en agua, pero se absorben rápidamente en el tracto gastrointestinal [1,2]. Se estima que el consumo anual de compuestos farmacéuticos es de aproximadamente 100 000 toneladas, entre ellos los AINEs como el diclofenaco y el ibuprofeno quienes están entre los 12 compuestos farmacéuticos genéricos de mayor consumo en el mundo, ya que pueden ser adquiridos por los pacientes sin prescripción médica. Posterior a su ingestión, aproximadamente el 65 % de la dosis oral de dichos fármacos, se excreta sin modificación a través de la orina y las heces fecales, llegando así a las plantas de tratamiento de aguas residuales y a fuentes de aguas superficiales por medio de redes de alcantarillado de aguas domésticas. En la actualidad, estos productos farmacéuticos están generando una gran preocupación a numerosos investigadores, debido a que son sustancias de difícil degradación mediante los tratamientos convencionales [3], como los primarios (sedimentación, precipitación, adsorción, filtración, intercambio iónico), secundarios o de transformación biológica (lodos activados, reactores biológicos, filtración aireada, sedimentación, entre otros) y terciarios o de eliminación química (cloración, ozonización, radiación ultravioleta), considerándose tratamientos ineficientes [4], debido a que son sustancias persistentes, bioacumulables, y cuya estructura química y/o metabolitos no sufre transformaciones significativas frente a dichos tratamientos convencionales [5] por lo cual, tanto el diclofenaco como el ibuprofeno, se le denominan contaminantes emergentes. Este tipo de contaminantes emergentes farmacéuticos, si bien son compuestos complejos ampliamente utilizados por sus propiedades fisicoquímicas, una vez que llegan al medio ambiente pueden ser transportadas y distribuidas en el agua, aire, suelo o sedimentos, afectando el ecosistema y a los humanos a través de la cadena trófica. Es de resaltar que este tipo de contaminantes emergentes pueden sufrir transformaciones en el medio ambiente dando lugar a subproductos que pueden llegar a ser incluso más peligrosos. Además, pueden provocar en animales y humanos, por reactividad bioquímica, efectos como: aumento en el riesgo de cáncer de mama en humanos, efecto adverso para el sistema inmunitario, daño al cerebro o al sistema nervioso periférico y modificación de la homeostasis hormonal, entre otras [5]. De acuerdo con lo anterior, se hace necesaria la aplicación de métodos analíticos que permitan la detección y cuantificación de ambos contaminantes emergentes en aguas residuales o superficiales, ya que actualmente no existe un control y regulación directa de los mismos en afluentes domésticos e industriales [6]. En este contexto, la mayoría de los estudios realizados hasta el momento reportan sus resultados basados únicamente en curvas de calibración de los fármacos sin tener en cuenta el desarrollo, validación y verificación del método analítico. Siempre que esto suceda se exige como parte integral del estudio la verificación del método en cuestión, ya que, esto proporciona un alto grado de confianza y seguridad, así como también en la calidad de los resultados que se reportan. Dentro de los retos asociados con el análisis de contaminantes emergentes farmacéuticos como el diclofenaco y el ibuprofeno se encuentran la extracción de los mesurados de la muestra, así como la existencia de métodos analíticos con sensibilidad insuficiente. Para solucionar los problemas de cuantificación con un alto nivel de sensibilidad, se plantea el uso de cromatografía líquida de alta resolución (HPLC). Si bien, se han reportado varios métodos analíticos para la detección y cuantificación de diclofenaco e ibuprofeno en diferentes matrices, el uso de cromatografía líquida de alta resolución (HPLC) como técnica instrumental, es muy común, confiable, reproducible y con un alto nivel de exactitud y precisión [2]. Por otra parte, el desarrollo y verificación de técnicas analíticas se hace una práctica necesaria para toda la industria en diferentes aspectos, que obedece a controles de calidad en aras de entregar resultados confiables, cantidades verdaderas de analitos en las muestras que se desean analizar.
El presente estudio reporta los resultados del desarrollo y validación de un método analítico por HPLC con detector de diodos para la detección y cuantificación de diclofenaco e ibuprofeno de forma conjunta en una matriz de agua basado en los métodos establecidos en las monografías de la United States Pharmacopeia - NF (USP) versión 38 [7,8] para los analitos de interés. Para ello, se determinaron parámetros de desempeño como la linealidad, límites de detección y de cuantificación, exactitud y presión, ya que con estos parámetros se logra un seguimiento estricto de la concentración de ambos contaminantes de manera precisa, exacta y confiable antes, durante y después de los procesos de degradación y mineralización de dichos contaminantes presentes en diferentes tipos de aguas, lo cual también se comprobó haciendo análisis de dichos fármacos en muestras de aguas ideales.
Metodología experimental
Materiales e instrumentos
Se utilizaron estándares de referencia de diclofenaco sódico e Ibuprofeno con una pureza del 99,75 % y 100 % respectivamente, siendo el primero un patrón secundario y el segundo un patrón primario. Todos los demás reactivos son calidad analítica, específicamente grado HPLC (acetonitrilo y ácido fosfórico 85 %), marca Merck Millipore. Se empleó agua purificada grado Milli-Q, previamente filtrada. Así mismo para el proceso de filtración de la fase móvil se usó papel filtro de Nylon de 0,22 um de tamaño de poro y 47 mm de diámetro, Marca Quality Laboratory Supplies, y un equipo de filtración de Polisulfona, Marca Advantec KP-47S. Para la medición del pH del agua acidulada se usó un pH-metro Hanna Instruments, Modelo HI 2221 [7,8], verificado diariamente con soluciones tampón certificadas de pH 4,0, 7,0 y 10,0.
Para la separación cromatográfica y cuantificación de los analitos de interés, se empleó un Cromatógrafo Líquido de Alta Resolución Modular - Modelo Nexera XR, Marca Shimadzu, específicamente UHPLC, con bomba cuaternaria de dos pistones de zafiro ubicados en paralelo en cámara separadas de acero inoxidable. Dicho equipo cuenta con un sistema de inyección automática, con un automuestreador con una capacidad de hasta 100 viales de 1,5 mL. El detector empleado fue de arreglo de diodos para longitudes de onda entre los 190 nm - 800 nm (Tabla 1).
Tabla 1 Parámetros variados en la optimización de las condiciones cromatográficas.
| Parámetro | Variable 1 | Variable 2 |
|---|---|---|
| Columna | ZORBAX Eclipse XDB- C18 (50 mm x 1,8 μm y un tamaño de poro de 95Å). | Agilent, Eclipse Plus C18 (100 mm x 2,1 mm, tamaño de partícula de 1,8 μm). |
| Volumen de flujo (mL/min) | 0,8 | 1,0 |
| Volumen de inyección (μL) | 10 | 50 |
| Temperatura (°C) | 25 | 40 |
Optimización de las condiciones cromatografías
Para la optimización de las condiciones cromatográficas, se partió inicialmente de las condiciones establecidas en la USP 38 para el análisis por separado del ibuprofeno y el diclofenaco sódico [7,8]. Posteriormente, se realizaron algunas variaciones en parámetros como la columna, el volumen de inyección y la temperatura (Tabla 1).
Determinación de los parámetros de desempeño del método analítico
El método analítico se validó en términos de límite de detección, límite de cuantificación, linealidad, exactitud y precisión en términos de repetibilidad y reproducibilidad intermedia, de acuerdo a la guía Directrices Armonizadas de la ICH (Consejo Internacional de armonización de los requisitos técnicos para el registro de medicamentos de uso humano) [9]. En todos los casos los análisis estadísticos se realizaron con un nivel de confianza del 95 % y nivel de significancia del 0,05.
Linealidad: se determinó preparando 9 estándares en donde cada uno contenía los dos fármacos, siendo para el diclofenaco (300, 350, 400, 450, 500, 550, 600, 700, 750 µg/L) y para el ibuprofeno (600, 700, 800, 900, 1000, 1100, 1200, 1400, 1500 µg/L). Las concentraciones se establecieron con base a los valores encontrados en la literatura para estos dos contaminantes emergentes en aguas superficiales y residuales hospitalarias [10 - 16]. Cada estándar fue preparado y analizado por triplicado teniendo así un total de 27 lecturas para obtener las curvas de calibración. En la Tabla 2, se describen los criterios de aceptación definidos para cada parámetro estadístico para comprobar la linealidad. Para lo cual, además de los parámetros estadísticos tradicionales, también, se realizó un análisis de varianza o ANDEVA (ANOVA, por sus siglas en inglés, Analysis of Variance) de la regresión lineal.
Tabla 2 Criterios de aceptación para cada parámetro de desempeño del método.
| Parámetro de desempeño | Parámetro estadístico | Criterio de aceptación |
|---|---|---|
| Linealidad | Coeficiente de determinación | r2 ≥ 0,98. |
| Coeficiente de variación | %CV ≤ 2 %. | |
| Intervalo de confianza | IC = 98-102 % | |
| Ha: el modelo lineal es el adecuado. | ||
| Ho: el modelo lineal no es el adecuado. | ||
| Análisis de varianza de la regresión lineal | Modelo Fisher de una cola | |
| Si Fcal ≤ Ftab se acepta Ho y se rechaza Ha. | ||
| Si Fcal ≥ Ftab se rechaza Ho y se acepta Ha. | ||
| Ha: el intercepto es diferente de cero (b ≠ 0) | ||
| Ho: el intercepto es igual a cero (b = 0). | ||
| Prueba del intercepto | Prueba T-student de dos colas | |
| Si Tcal ≤ Ttab se acepta Ho y se rechaza Ha. | ||
| Si Tcal ≥ Ttab se rechaza Ho y se acepta Ha. | ||
| Ha: la pendiente es diferente de cero (a ≠ 0) | ||
| Ho: la pendiente es igual a cero (a = 0). | ||
| Prueba de la pendiente | Prueba T-student de dos colas | |
| Si Tcal ≤ Ttab se acepta Ho y se rechaza Ha. | ||
| Si Tcal ≥ Ttab se rechaza Ho y se acepta Ha. | ||
| Exactitud | Coeficiente de variación | %CV ≤ 2 %. |
| Intervalo de confianza | IC = 98-102 % | |
| Precisión | Coeficiente de variación | %CV ≤ 2 %. |
| Intervalo de confianza | IC = 98-102 % | |
| Análisis de varianza con tres criterios de clasificación | Si Fcal ≤ F tablas, se acepta Ho y se rechaza Ha | |
| Si Fcal ≥ F tablas, se rechaza Ho y se acepta Ha | ||
| Ver hipótesis establecidas en la Tabla 4. |
Límite de detección y de cuantificación: para la determinación de los límites se utilizó un valor cercano del parámetro relación Señal/Ruido (S/R) de 3 y 10, para el límite de detección (LD) y de cuantificación (LC), respectivamente. De esta manera, se preparó una solución que contenía una concentración de diclofenaco e ibuprofeno igual al primer nivel de concentración. Dicha solución se diluyó sucesivamente y se analizó por triplicado hasta encontrar una concentración correspondiente a los valores definidos para la relación S/R. Adicionalmente, una vez encontradas estas concentraciones correspondientes, se procedió a realizar pruebas para demostrar la existencia de exactitud y precisión para este valor.
Exactitud: para la determinación de la exactitud se empleó el método de adición/recuperación con el porcentaje de recuperación. Así, se prepararon dos (2) soluciones distintas, cada una a un nivel de concentración conocida y diferente de ambos analitos (300 ppb de diclofenaco y 600 ppb de ibuprofeno para la solución 1 y 550 ppb de diclofenaco y 1100 ppb de ibuprofeno para la solución 2) y se inyectaron por sextuplicado en el menor tiempo posible. Se calculó el porcentaje de recuperación de las muestras con base a la concentración preparada el promedio, la desviación estándar (SD), la desviación relativa (RSD), el coeficiente de variación (% CV) y el intervalo de confianza (IC). En la Tabla 2 se indican los criterios de aceptación definidos para comprobar la exactitud del método.
Precisión en términos de repetibilidad y precisión intermedia: se realizaron varias pruebas con el objetivo de determinar la precisión del método, para lo cual se prepararon dos (2) soluciones distintas cada una a un nivel de concentración diferente de ambos fármacos (Tabla 3), las cuales fueron analizadas por diferentes analistas en distintos días y se inyectaron por sextuplicado. Se calculó el porcentaje de recuperación de los analitos con base a la concentración preparada, el promedio, la desviación estándar (SD), la desviación estándar relativa (RSD), el coeficiente de variación (% CV) y el intervalo de confianza (IC). Además, se utilizaron como criterios de aceptación un IC = 98 - 102 % y un % CV ≤ 2 %.
Tabla 3 Factores y niveles definidos para determinar la precisión intermedia del método para el análisis ibuprofeno y diclofenaco.
Adicionalmente, se aplicó un análisis de varianza o ANDEVA (ANOVA, por sus siglas en inglés, Analysis of Variance) con los factores mencionadas anteriormente para determinar si existe una varianza significativa con respecto al porcentaje de recuperación. Los factores con sus correspondientes niveles se presentan en Tabla 3. Se utilizó un valor de nivel de significancia igual a 0,05, y en las Tablas 2 y 4 se describen las pruebas de hipótesis establecidas y los criterios de aceptabilidad. El respectivo análisis de varianza (ANOVA) se realizó usando el software StatGraphics 15,1.
Tabla 4 Hipótesis establecidas y criterios de aceptación para determinar la precisión intermedia del método.
| Hipótesis nula Ha | Hipótesis alternativa Ho |
|---|---|
| Si existe una varianza significativa en el porcentaje de recuperación al variar el analista. | No existe una varianza significativa en el porcentaje de recuperación al variar el analista. |
| Si existe una varianza significativa en el porcentaje de recuperación al variar la concentración del fármaco. | No existe una varianza significativa en el porcentaje de recuperación al variar la concentración del fármaco. |
| Si existe una varianza significativa en el porcentaje de recuperación al variar el día del análisis. | No existe una varianza significativa en el porcentaje de recuperación al variar el día del análisis. |
| Si existe una varianza significativa en el porcentaje de recuperación al variar el analista y la concentración del fármaco. | No existe una varianza significativa en el porcentaje de recuperación al variar el analista y la concentración del fármaco. |
| Si existe una varianza significativa en el porcentaje de recuperación al variar el día del análisis y el analista. | No existe una varianza significativa en el porcentaje de recuperación al variar el día del análisis y el analista. |
| Si existe una varianza significativa en el porcentaje de recuperación al variar el día del análisis y la concentración del fármaco. | No existe una varianza significativa en el porcentaje de recuperación al variar el día del análisis y la concentración del fármaco. |
| Si existe una varianza significativa en el porcentaje de recuperación al variar el día de análisis, el analista y la concentración del fármaco. | No existe una varianza significativa en el porcentaje de recuperación al variar el día de análisis, el analista y la concentración del fármaco. |
Resultados
Optimización de condiciones cromatográficas
Para la optimización de las condiciones cromatográficas requeridas para la separación y cuantificación del diclofenaco e ibuprofeno, se evaluaron numerosos parámetros, como: la columna cromatográfica empleada, la longitud de onda de detección, las velocidades de flujo del sistema, el volumen de inyección, la temperatura de la columna y el tiempo de corrida, como se muestra en la Tabla 1. La columna empleada y otros parámetros se seleccionaron con base a los resultados de separación, forma del pico y tiempo de retención, donde se logró identificar que la columna Eclipse Plus C18 (100 mm x 2,1 mm, tamaño de partícula de 1,8 um de Agilent) proporcionó la mejor selectividad. Para detectar el diclofenaco sódico e ibuprofeno en conjunto se realizó un barrido de longitud de onda entre los 190 nm y los 800 nm con un Detector DAD. La Longitud de onda de detección seleccionada fue 214 nm, ya que ambos compuestos tienen una absorción o fuerza de UV similar o comparable. Se observó que el flujo entre 0,8 mL/min y 1.0 mL/min no fue un factor crítico que afecto la separación, por ello se estableció un flujo Anal de 1.0 mL/min, ya que esto permitía un menor tiempo de corrida disminuyera. El desempeño de la temperatura de columna se evaluó en 25 °C y 40 °C, donde la temperatura con mejores resultados fue la de 40 °C, debido a que a temperaturas inferiores las señales se solapaban y tenían una menor resolución. Finalmente se evaluó el volumen de inyección con el valor mínimo y máximo que permitía el sistema de inyección del equipo (10 µL - 50 µL) respectivamente; se eligió el máximo valor ya que se obtenían picos más resueltos y simétricos. En la Figura 1 se observa el cromatograma obtenido al emplear las condiciones cromatográficas optimizadas y descritas al pie de la figura. En el cromatograma se visualizan picos simétricos que comenzaron y Analizaron en una línea base estable y con una buena resolución.
Determinación de parámetros de desempeño
Linealidad y rango
En la Figura 2 se muestran las curvas de calibración obtenidas para ambos analitos, se observa la existencia de una relación lineal entre la concentración de cada fármaco y la respuesta analítica (área) en el intervalo de concentración comprendido entre 300 y 750 ppb para el diclofenaco y 600 y 1500 ppb para el ibuprofeno. Adicionalmente, en la Tabla 5 se puede observar que los valores calculados para los parámetros estadísticos establecidos satisfacen los criterios de aceptación definidos para la linealidad del método analítico, ya que para todos los catos el r2 ≥ 0,98, el % CV ≤ 2 % y el IC se encuentra entre 98 - 102 %, lo que indica una correspondencia entre los valores obtenidos con la recta de ajuste y los obtenidos experimentalmente.

Figura 1 Cromatograma del diclofenaco sódico e ibuprofeno. Condiciones optimizadas: columna: Eclipse Plus C18 (100 mm x 2,1 mm, tamaño de partícula de 1,8 µm de la Marca Agilent). Fase móvil: solución buffer de agua acidulada con ácido fosfórico 85 % a un valor de pH de 2,5 y acetonitrilo en una proporción de 2:1. Velocidad de flujo: 1,0 mL/min en modo isocrático. Temperatura del horno: 40°C Tiempo de corrida: 20 min. Volumen de inyección: 50 µL. Longitud de onda: 214 nm.
Tabla 5 Parámetros estadísticos generales para determinar la linealidad del método para el diclofenaco e ibuprofeno.
Adicionalmente, de acuerdo con los resultados del análisis de varianza para la regresión lineal (Tabla 6) y la comparación entre el F calculado y el F de tablas (Tabla 7), se encontró que tanto para el diclofenaco como para el ibuprofeno el Fcal ≥ Ftab, por tanto, se acepta la hipótesis alterna, de esta manera se confirma una vez más que el modelo lineal para ambos fármacos es adecuado. Finalmente, se puede afirmar que el sistema lineal es adecuado en su totalidad, ya que al hacer las pruebas del intercepto y la pendiente se puede identificar que todo es matemáticamente correcto y aceptable estadísticamente con un nivel de confianza del 95 % y nivel de significancia del 0,05.
Tabla 6 Valores para los parámetros estadísticos del análisis ANOVA de la regresión lineal para el diclofenaco e ibuprofeno.
| Fuente de variación | Diclofenaco | Ibuprofeno | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Suma de cuadrados | G.L. | Cuadrados medios | Relación | Valor P | Suma de cuadrados | G.L. | Cuadrados medios | Relación | Valor P | |
| F | F | |||||||||
| Modelo | 9,03E+10 | 1 | 9,03E+10 | 2387,92 | 0,0000 | 1,02E+11 | 1 | 1,02E+11 | 3747,16 | 0,0000 |
| residual | 9,45E+08 | 25 | 3,78E+07 | 6,83E+08 | 25 | 2,73E+07 | ||||
| Total (corregido) | 9,12E+10 | 26 | 1,03E+11 | 26 | ||||||
Tabla 7 Comparación entre el F calculado y el F de tablas del análisis ANOVA de la regresión lineal para el diclofenaco e ibuprofeno.
| Parámetro estadístico | Ibuprofeno | Diclofenaco | |
|---|---|---|---|
| ANOVA | Fcal Ftablas | 3747,16 4,23 | 2387,92 4,23 |
| INTERCEPTO | Tcal T tablas | 7,99895 0,96 | 7,99895 0,96 |
| PENDIENTE | Tcal T tablas | 61,2141 0,96 | 61,2141 0,96 |
Los resultados reportados en la literatura también muestran la linealidad tanto para el diclofenaco como el ibuprofeno. Esto se observa con los coeficientes de determinación, los cuales son mayores a 0,9900 en rangos de concentración que van desde 50 µg/L hasta 200 000 µg/L para el diclofenaco [17 - 21] y para el ibuprofeno se reportan coeficientes de determinación mayores 0,9979, en rangos de concentración que van desde 50 µg/L hasta 100 000 µg/L para el ibuprofeno [18,22 - 24].
Límite de detección (LD) y cuantificación (LC)
En la Tabla 8, se indican los parámetros estadísticos obtenidos en el cálculo de los límites de detección y cuantificación para ambos fármacos con base al porcentaje de recuperación. Se puede observar que, aunque en todos los casos los valores obtenidos para dichos parámetros son aceptables, los valores para el límite de detección son mayores a los obtenidos para el límite de cuantificación, lo cual se debe a la misma naturaleza del parámetro de desempeño, indicando que concentraciones cercanas a este valor pueden variar significativamente y por lo tanto, no se podría calcular con alta confiabilidad.

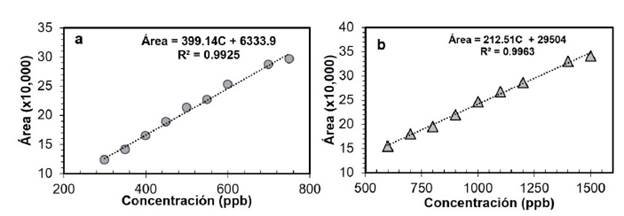
Figura 3 Correspondencia ente la concentración adiciona y la encontrada con la curva de calibración para el diclofenaco (a) y el Ibuprofeno (b).
Tabla 8 Parámetros estadísticos determinados en el cálculo del límite de detección y de cuantificación para el diclofenaco e ibuprofeno.
Para el diclofenaco, el límite de detección obtenido fue 200 ppb y el límite de cuantificación de 300 ppb con % CV de 0,89 % y 0,46 % respectivamente. En el caso de LD, este coincide con los resultados descritos en la literatura, donde se reportan valores entre 200 - 4000 µg/L [17 - 19,25]. De igual forma, el LC se ha establecido entre 200 µg/L hasta valores de 4000 µg/L [17,25]. Con respecto a los límites de detección y cuantificación para el ibuprofeno se obtuvo 400 µg/L y 600 µg/L respectivamente. El límite de detección obtenido experimentalmente se encuentra dentro de los rangos reportados en la literatura, los cuales están en valores que van desde los 30 µg/L hasta 700 µg/L [18,23 - 25]. De igual manera, los límites de cuantificación reportados van desde 90 - 1560 µg/L con valores inferiores a los encontrados en la verificación del método [22,23].
Actualmente existen técnicas más sensibles, que permiten el uso de límites de detección más bajos, o niveles traza, al igual que límites de cuantificación. Tal es el caso de uso de HPLC en fase reversa con elución en gradiente, acoplada a espectrometría de masas ICP en el análisis de diclofenaco [20], donde se obtuvieron límites de cuantificación en 30 - 50 µg/L. También ha sido empleada la técnica de HPLC acoplada a detección de fluorescencia, donde para el Ibuprofeno se han adquirido LD de 33,3 µg/L, es decir valores similares a los obtenidos por HPLC - DAD [24]. Finalmente se han empleado otras técnicas como GC - MS, o UPLC - MS/MS que han permitido cuantificar el ibuprofeno en cantidades traza de 1 µg/L. [24]. A continuación, se muestra las Tabla 8, donde se describen los datos empleados para la determinación del LD y LC del presente estudio.
Exactitud
En la Tabla 9 se detallan los parámetros estadísticos determinados para definir la exactitud del método para el diclofenaco e ibuprofeno. En general se obtuvieron muy altos porcentajes de recuperación, lo cual se ve reflejado en los intervalos de confianza calculados para cada caso, los se encuentran en el rango establecido en los criterios de aceptación. Además, el % CV calculado para las dos soluciones y ambos fármacos es todos los casos es ≤2 %, cumpliendo también con este con el criterio de aceptación, por tanto, se evidencia que el método cromatográflco es exacto.
Precisión en términos de repetibilidad y precisión intermedia
En cuanto a los estadísticos generales determinados para la precisión en términos de repetibilidad y precisión intermedia para ambos fármacos (Tablas 10 y 11) bajos las diferentes condiciones de variabilidad estudiadas, se encontró que, tanto la desviación estándar, la desviación estándar relativa como el coeficiente de variación están por debajo de los criterios de aceptación establecidos, indicando poca variabilidad en los datos y las réplicas y por tanto una alta confiabilidad y confianza en los resultados. En cuanto a la precisión intermedia, los resultados de porcentaje de recuperación no se presentan diferencias estadísticamente significativas, en razón a que se realizó el análisis en días diferentes o con analistas diferentes.
Tabla 10 Parámetros estadísticos calculados para definir la precisión en términos repetibilidad y precisión intermedia del método para la determinación simultánea del ibuprofeno.
| Ibuprofeno | |||||
|---|---|---|---|---|---|
| Nivel de concentración | Parámetro estadístico | Día 1 | Día 2 | ||
| Analista A | Analista B | Analista A | Analista B | ||
| 600 | Promedio | 98,39 | 98,72 | 98,37 | 98,60 |
| SD | 0,88 | 0,80 | 0,88 | 0,83 | |
| SDR | 0,78 | 0,64 | 0,77 | 0,69 | |
| %CV | 0,90 | 0,81 | 0,89 | 0,84 | |
| 1100 | Promedio | 100,54 | 99,57 | 99,81 | 99,78 |
| SD SDR | 0,28 0,08 | 0,23 0,05 | 0,56 0,31 | 0,32 0,10 | |
| %CV | 0,28 | 0,23 | 0,56 | 0,32 | |
Adicionalmente, de acuerdo con los resultados del análisis de varianza (Tablas 12y13), y la comparación entre el F calculado y el F de tablas (Tabla 13), se encontró que tanto para el diclofenaco como para el ibuprofeno en todos los casos el Fcal ≥ Ftab, excepto para la concentración del analito, por tanto, se acepta la hipótesis nula, indicando que no existe una varianza significativa en el porcentaje de recuperación al variar el día de análisis, el analista y la concentración del fármaco. Sin embargo, como se puede observar para la variable concentración del fármaco Fcal ≤ Ft tablas, lo cual es claramente coherente, ya que la sensibilidad del método puede variar al cambiar la concentración de cada analito.
Tabla 11 Parámetros estadísticos calculados para definir la precisión en términos repetibilidad y precisión intermedia del método para la determinación simultánea del diclofenaco.
Tabla 12 Valores para los parámetros estadísticos del análisis ANOVA con tres criterios de clasificación para el diclofenaco e ibuprofeno.
| Fuente de variación | Diclofenaco | Ibuprofeno | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Suma de cuadrados | G.L. | Cuadrados medios | Relación F | Valor P | Suma de cuadrados | G.L. | Cuadrados medios | Relación F | Valor P | |
| Efectos principales | ||||||||||
| Analista (α) | 5,97841 | 1 | 5,97841 | 1,38 | 0,2465 | 0,154133 | 1 | 0,154133 | 0,36 | 0,5515 |
| Concentración (β) | 62,8834 | 1 | 62,8834 | 14,55 | 0,0005 | 23,6883 | 1 | 23,6883 | 55,44 | 0,0000 |
| Día (γ) | 6,96163 | 1 | 6,96163 | 1,61 | 0,2118 | 0,313633 | 1 | 0,313633 | 0,73 | 0,3967 |
| Interacciones | ||||||||||
| αβ | 0,418133 | 1 | 0,418133 | 0,10 | 0,7574 | 1,83301 | 1 | 1,83301 | 4,29 | 0,0448 |
| αγ | 11,427 | 1 | 11,427 | 2,64 | 0,1118 | 0,541875 | 1 | 0,541875 | 1,27 | 0,2668 |
| βγ | 18,6751 | 1 | 18,6751 | 4,32 | 0,0441 | 0,114075 | 1 | 0,114075 | 0,27 | 0,6082 |
| αβγ | 8,67 | 1 | 8,67 | 2,01 | 0,1644 | 0,8112 | 1 | 0,8112 | 1,90 | 0,1759 |
| Residual | 172,907 | 40 | 4,32267 | 17,0916 | 40 | 0,427289 | ||||
| Total (Corregido) | 287,92 | 47 | 44,5478 | 47 | ||||||
Tabla 13 Comparación entre el F calculado y el F de tablas del análisis ANOVA con tres criterios de clasificación de para el diclofenaco e ibuprofeno.
| Efectos | Diclofenaco | Ibuprofeno | ||||
|---|---|---|---|---|---|---|
| principales | F calculado | F tablas | F calculado | F tablas | ||
| Analista (α) | 1,38 | ≤ | 0,36 | ≤ | ||
| Concentración (β) | 14,55 | ≥ | 55,44 | ≥ | ||
| Día (γ) | 1,61 | ≤ | 0,73 | ≤ | ||
| αβ | 0,10 | ≤ | 4,04 | 4,02 | ≤ | 4,04 |
| αγ | 2,64 | ≤ | 1,27 | ≤ | ||
| βγ | 4,02 | ≤ | 0,27 | ≤ | ||
| αβγ | 2,01 | ≤ | 1,90 | ≤ | ||
Es importante puntualizar que, de acuerdo con la revisión bibliográfica realizada, no hay estudios en la literatura en la cual se determinen y analicen a profundidad parámetros de desempeño como precisión en términos de repetibilidad y precisión intermedia, para el análisis de diclofenaco e ibuprofeno de manera aislada o simultánea por cromatografía de líquidos de alta resolución, ya que comúnmente se utilizan, solamente el porcentaje de recuperación, la desviación estándar y/o el coeficiente de variación, en cuyo caso nuestros resultados son muy similares a los encontrados por otros investigadores [17,19 - 21,26].
Determinación de diclofenaco e ibuprofeno en muestras ideales de agua
Con el fin de verificar la efectividad del método, se prepararon 4 muestras de aguas ideales con concentraciones diferentes de diclofenaco e ibuprofeno, las cuales fueron sometidas a varios procesos de adsorción usando TiO2, y se determinó la concentración de ambos fármacos tanto al inicio como una vez Analizados los procesos. Estos procesos se realizaron por duplicado y se analizaron por triplicado. En Tabla 14 se muestran los resultados del promedio, la desviación estándar, la desviación estándar relativa y el coeficiente de variación en términos del porcentaje de remoción de cada fármaco. Sin embargo, no se especifican ninguna de las condiciones experimentales y el análisis de los resultados obtenidos en términos de la adsorción los estudios realizados, ya que esto hace parte de otra investigación que se publicará próximamente.
Tabla 14 Parámetros estadísticos determinados para diferentes muestras de aguas ideales con diclofenaco e ibuprofeno.
Los valores encontrados para los parámetros estadísticos para las diferentes demuestran que es posible determinar en la práctica cotidiana los laboratorios ambientales en muestras de aguas por cromatografía líquida de alta resolución, concentraciones de diclofenaco e ibuprofeno de manera simultánea en un intervalo de 300 ppb a 750 ppb para el diclofenaco y 600 ppb a 1500 ppb para el ibuprofeno. Manteniendo de forma estable los niveles de desempeño mediante procedimientos de control de calidad de los resultados con un nivel de confianza del 95 % y nivel de significancia del 0,05
Conclusiones
La validación del método cromatográfico HPLC para cuantificar diclofenaco e ibuprofeno de manera simultánea en aguas fue desarrollada con éxito mediante la optimización cromatográfica de los parámetros (columna, temperatura de la columna, velocidad de flujo, longitud de onda de detección y volumen de inyección). El método analítico desarrollado presenta un comportamiento lineal en el intervalo de concentración de 300 ppb a 750 ppb para el diclofenaco y de 600 ppb a 1500 ppb para el ibuprofeno, con un coeficiente de determinación de 0,9925 para el diclofenaco y 0,9963 para el ibuprofeno. Los resultados del estudio muestran que el método de separación y cuantificación permite analizar muestras de manera específica, ya que permite identificar la presencia de diclofenaco e Ibuprofeno de manera confiable con parámetros de desempeño que cumple los criterios de aceptación definidos como porcentaje de recuperación, el promedio, la desviación estándar, la desviación estándar relativa, el coeficiente de variación y el intervalo de confianza. Los estudios se pueden extender a la determinación y cuantificación de los fármacos . en aguas reales para de esta manera comprobar la confiabilidad del método.