Introducción
En los últimos años, la colocación de válvulas por vía percutánea ha avanzado de forma permanente, hasta lograr, en la actualidad, realizar intervenciones menos invasivas y menos mórbidas en comparación con los procedimientos quirúrgicos1. En pacientes con cardiopatía congénita, el implante percutáneo de válvula pulmonar es el tratamiento de elección en casos de un tracto de salida del ventrículo derecho (TSVD) disfuncional2. Existen varias válvulas pulmonares percutáneas expandibles con balón, disponibles para la implantación en conductos, tractos nativos y prótesis valvulares. Las válvulas disponibles (Melody, Edwards o Sapiens) se recomiendan para ser implantadas únicamente en TSVD formados con homoinjertos o conductos3,4. Sin embargo, la mayoría de los pacientes con tetralogía de Fallot, se someten a una reparación con técnica de parche transanular que conlleva tractos de salida muy pulsátiles y con dimensiones mayores al tamaño de las válvulas expandibles con balón actualmente disponibles (22 mm para Melody, 29 mm para Edwards)3,5.
Por lo anterior, se generó la necesidad de una válvula que pueda implantarse en un TSVD nativo y que sea lo suficientemente grande para los diámetros amplios de los TSVD con parche. La válvula autoexpandible Venus P (MedTech, China) es una válvula percutánea, aprobada recientemente para su uso en tractos nativos de mayor tamaño6.
La estructura de la válvula Venus P está formada por un stent de nitinol y las valvas y el recubrimiento del stent son de pericardio porcino. El nitinol permite al stent adaptarse adecuadamente al tronco pulmonar sin comprimir las estructuras vecinas debido a una menor tensión radial7. Esta válvula está disponible en tamaños desde 28 hasta 36 mm de diámetro, con incrementos de 2 mm. El stent de la válvula Venus P tiene forma de diábolo y mide 10 mm más en los extremos que en la zona central. Al ser más ancha en los extremos, la válvula está diseñada para ser implantada, idealmente, en troncos pulmonares tubulares, sin estenosis distales ni de las arterias pulmonares. La zona central y el extremo proximal están recubiertos de pericardio porcino para evitar fugas paravalvulares, y el extremo distal está sin recubrir, evitando así la oclusión de las arterias pulmonares. El crimpado de la válvula sobre su sistema de liberación se realiza bajo agua helada. En estas condiciones, el nitinol se ablanda y puede crimparse sobre el sistema de liberación. La válvula se fija al sistema de liberación por dos pequeños ganchos. Una vez enganchada y reducido el tamaño, se cubre la válvula con la cápsula de la vaina del sistema de liberación, de tal manera que la válvula entra en el paciente recubierta. Esta vaina es de 22 Fr en las válvulas de 28 y 30 mm, y de 24 Fr en las más grandes (> 30 mm). Una vez situada en el árbol pulmonar en la localización elegida, al retraer la cápsula del sistema de liberación la válvula recuperará su forma de diábolo al entrar en contacto con el torrente sanguíneo, a una temperatura de 36-37 °C3.
El objetivo de este estudio es reportar la experiencia del primer caso de implantación exitosa de válvula pulmonar Venus P en Colombia.
Caso clínico
Paciente de 16 años y 63 kilos, con antecedente de tetralogía de Fallot, a quien se le realizó corrección completa a los once meses de vida y requirió reintervención a los pocos días para reconstrucción del TSVD por aneurisma del parche transanular y presencia de comunicación interventricular residual.
Se encontraba en seguimiento por insuficiencia valvular pulmonar. En los últimos seis meses presentó deterioro clínico dado por cianosis con el ejercicio y progresión de la clase funcional de I a II en la clasificación funcional de la New York Heart Association (NYHA).
Mediante ecocardiograma se evidenció una dilatación importante del ventrículo derecho (diámetro del ventrículo derecho en diástole de 47 mm, Z +3-07) con insuficiencia pulmonar libre. Se realizó resonancia magnética de corazón en la que se reportó diámetro del ventrículo derecho de 58 mm (Z +3.95), con una fracción regurgitante de la insuficiencia pulmonar del 56% y un volumen de fin de diástole del ventrículo derecho de 172 ml/m2. Por medio de angiotomografía de corazón, se logró medir un anillo valvular pulmonar de 29 mm con un recorrido de la arteria descendente anterior en su porción proximal que discurre a 4 mm del plano del anillo valvular pulmonar.
Con base en lo anterior, se discutió el caso en junta multidisciplinaria y se consideró candidato a colocación de válvula pulmonar percutánea autoexpandible.
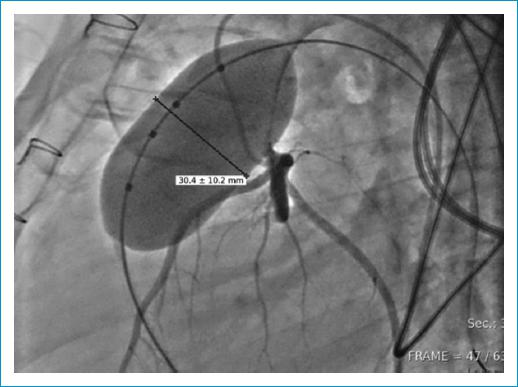
Previo consentimiento informado, se realizó cateterismo bajo anestesia general con el paciente intubado, y heparinización a 100 U/kg. Se canalizó vena femoral derecha e izquierda y arteria femoral izquierda. Se hizo cateterismo cardíaco derecho e izquierdo, con presión del ventrículo derecho de 32/2 mm Hg y arterias pulmonares derecha e izquierda de 34/4/16 y 32/2/16 mm Hg respectivamente, así como tallaje del TSVD que mostró un diámetro de 30 mm (Sizing Balloon, AGA Medical Corp., Estados Unidos), con test coronario que fue negativo para obstrucción (Fig. 1).
Con base en lo anterior, se eligió una válvula 4 mm mayor que la cintura del balón de tallado y con una longitud que permitiera dejar la parte distal a nivel de la bifurcación pulmonar y el extremo proximal del diábolo en el VD, seleccionando una válvula 34 x 30 mm.
Se realizó el montaje de la válvula sin inconvenientes. Se procedió a llevar la guía Lunderquist (Cook Medical, Dinamarca) de alto soporte, hasta la arteria pulmonar izquierda y a través de esta el introductor hasta su origen.
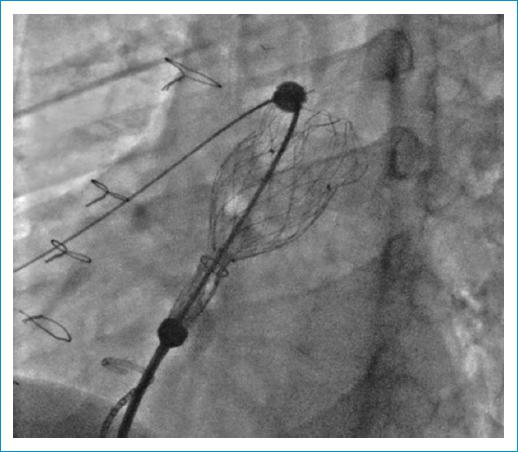
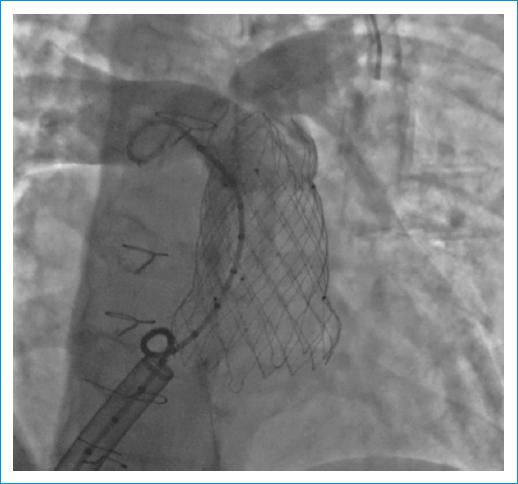
Se inició el despliegue de la válvula en el origen de la rama pulmonar izquierda con controles angiográficos seriados. La orientación inicial de la válvula no se consideró adecuada y se procedió a reposicionar la guía en la rama pulmonar derecha (Fig. 2). Se desplegó el total de la válvula en forma controlada desde la arteria pulmonar derecha, quedando en una posición adecuada (Fig. 3). Se realizó angiografía en la que se no se evidenció insuficiencia pulmonar residual y se hizo test coronario final sin alteraciones. Se tomaron presiones posteriores al procedimiento, con mejoría significativa de la presión diastólica de la arteria pulmonar, la cual cambió de 4 a 14 mm Hg posterior al procedimiento, sin gradiente significativo entre el ventrículo derecho y la arteria pulmonar (2 mm Hg).
Seguimiento posterior al procedimiento
Un mes posterior al procedimiento, el paciente permanece asintomático, con clase funcional NYHA I, sin cianosis ni disnea durante la actividad. Al examen físico, con saturación de oxígeno del 99%, sin anormalidades. El ecocardiograma de control reportó insuficiencia pulmonar trivial, sin estenosis ni fuga paravalvular, con adecuada función biventricular.
Discusión
Hasta el momento existen varios reportes de experiencias en el implante de la válvula Venus P en el mundo, con resultados favorables5,8-10. La colocación de la válvula Venus P, a diferencia de las otras válvulas disponibles, no requiere de un stent para transformar el TSVD en un conducto rígido11,12. Esto reduce el tiempo del procedimiento y la exposición a radiación. Además, la presencia de marcas radiopacas en el extremo distal de la parte recta de la válvula, permite un despliegue y un posicionamiento precisos, evitando que sobresalga sobre la bifurcación de las ramas pulmonares3.
Con relación al costo entre las diferentes válvulas expandibles autorizadas por el ente encargado en nuestro país (INVIMA), la válvula Melody (expandible con balón) tiene un costo menor en comparación con la Venus P (autoexpandible). No obstante, la válvula Melody está diseñada para TSVD «no nativos» con un diámetro de hasta 26 mm. Para el caso de nuestro paciente, con un TSVD de gran tamaño, la válvula autoexpandible diseñada para colocación en posición pulmonar disponible en el país es la Venus P, por lo cual se consideró la ideal en nuestro caso.
Por otra parte, la implantación percutánea de la válvula representa disminución en tiempos de intubación orotraqueal, estancia en la unidad de cuidado intensivo y estancia hospitalaria total. En cuanto a los costos entre el reemplazo quirúrgico y el procedimiento intervencionista, el reemplazo percutáneo tiene un costo mayor debido al valor de la válvula. Sin embargo, en casos específicos, como el de nuestro paciente, quien ya había sido sometido a dos cirugías cardiotorácicas, se considera que el reemplazo percutáneo es el procedimiento indicado, ya que es menos mórbido y puede implicar un riesgo menor de complicaciones.
En pacientes con cardiopatías congénitas reparadas o no reparadas e insuficiencia pulmonar secundaria, puede ser necesario el reemplazo de la válvula pulmonar teniendo en cuenta los síntomas y la repercusión hemodinámica de esta. Los candidatos al reemplazo valvular deben ser evaluados de forma integral con ecocardiograma, resonancia magnética de corazón, prueba de esfuerzo y electrocardiograma Holter. Cuando existen dudas en la medición de los diámetros, la angiotomografía puede ofrecer una medición más precisa con la finalidad de definir el tamaño y la longitud de la prótesis que se va a implantar; sí como para evaluar las características anatómicas del TSVD.
La elección de nuestro paciente basado en las mediciones ecocardiográficas, por angiotomografía, resonancia magnética y con balón de tallaje con balón por cateterismo, fue efectiva y permitió que el procedimiento fuera exitoso. En el caso de nuestro paciente, no se presentaron complicaciones ni descompensación hemodinámica durante el procedimiento. El ecocardiograma del día siguiente, mostró una válvula bien posicionada, sin estenosis ni insuficiencia residual. Además, no hubo complicaciones locales en las zonas de punción y el paciente pudo ser egresado de la institución a las 48 horas posteriores al procedimiento.
En el seguimiento se realizará evaluación de volúmenes ventriculares derechos, función ventricular derecha e izquierda y competencia de la válvula, según lo reportado en la literatura mundial con el implante de este tipo de válvulas8.
Con base en esta experiencia, consideramos que el reemplazo valvular pulmonar percutáneo en TSVD nativos dilatados, es una opción posible y segura para mejorar la insuficiencia pulmonar y la disfunción ventricular derecha en este tipo de pacientes.