Introducción
La enfermedad pulmonar obstructiva crónica (EPOC) es una condición frecuente, prevenible, tratable. Representa la tercera causa de muerte en el mundo (1) y su prevalencia oscila entre 4-10 % (2,3). Sin embargo, en algunas regiones la prevalencia puede ser hasta del 24,3 %, como en el caso de Europa (4). En Latinoamérica la prevalencia sigue siendo mayor al promedio global, la cual se encuentra en el 15,8 % en la población mayor de 40 años según el Chronic Obstructive Pulmonary Disease in Five Latin American Cities (PLATINO) (5). En la población que asiste a centros primarios de atención la prevalencia puede ser de hasta el 20,6 %, como lo reporta el estudio Prevalencia y práctica habitual -diagnóstico y tratamiento- en población de riesgo de EPOC en Médicos generales de cuatro países de América Latina (PUMA) (6). En Colombia, según el estudio PREPOCOL, se registra una prevalencia de la EPOC del 8,9 % (7). A pesar de esta alta frecuencia de la enfermedad, el subdiagnóstico es un problema que se presenta en todas las regiones del mundo y en Colombia puede llegar hasta el 87,4 % (7).
Se ha considerado que el subdiagnóstico pueda deberse, en parte, a la dificultad al acceso de pruebas espirométricas de calidad, así como problemas en la interpretación y aplicación de sus resultados (8). Una de las estrategias para detectar pacientes con EPOC es la utilización de cuestionarios estandarizados que buscan, a partir del interrogatorio de síntomas cardinales y factores de riesgo de la enfermedad (9-12), dar un puntaje que oriente al médico sobre la necesidad de la espirometría y ofrecer así una mejor capacidad de detección de la enfermedad (10-12).
Entre los diferentes cuestionarios desarrollados, se encuentra el COPD Diagnostic Questionnaire (CDQ) (13), diseñado para personas mayores de 40 años. Este consta de 8 preguntas sencillas relacionadas con síntomas y antecedentes. En su formato original tiene un sistema de puntuación de tres niveles, con dos puntos de corte (16,5 y 19,5) interpretados como baja probabilidad de EPOC un puntaje CDQ ≤ 16,5, probabilidad intermedia de EPOC un puntaje CDQ > 16,5 y < 19,5, y probabilidad alta de EPOC un puntaje CDQ ≥ 19,6.
Adicionalmente, cuenta con validaciones internacionales en Europa, Australia y en clínicas hospitalarias en pacientes ambulatorios en Japón (13-15); ha sido utilizado en países centroamericanos con traducción en español (16), convirtiéndolo en una herramienta útil para detectar pacientes que se benefician de espirometría para el diagnóstico de la EPOC.
En el metaanálisis de Haroon et al. se reportó que el cuestionario CDQ con un puntaje ≥ 19,5 tiene una sensibilidad del 64,5 % y una especificidad del 65,2 %, mientras que un punto de corte ≥ 16,5 tiene una sensibilidad mayor al 87,5 % y especificidad de 38,8%, con un número necesario para diagnosticar una persona con EPOC (NND) en los puntos de corte ≥ 19,5 y ≥ 16,5 de 11 (IC95%: 7-15) y 13 (IC95%:11-16), respectivamente (9), características favorables para una herramienta diagnóstica. A pesar de esto, el rendimiento de cuestionarios que pueden tener cierta utilidad diagnóstica puede variar geográficamente y en el caso del CDQ, hasta el momento, la mayor información sobre su rendimiento se encuentra en países europeos (13). Motivo por el cual, en este estudio se busca determinar la validez de criterio para el diagnóstico de la EPOC con esta herramienta diagnóstica en Colombia.
Materiales y métodos
Se realizó un estudio de cohorte prospectivo para el análisis de validez de criterio y reproducibilidad intraevaluador del puntaje de CDQ como prueba diagnóstica, en una población de individuos mayores a 40 años que asistieron por consulta externa para la realización de una prueba espirométrica en la Clínica Universidad de la Sabana en Chía, Cundinamarca (institución de tercer nivel de atención). El periodo de recolección de la información se llevó a cabo a partir de septiembre del año 2018 hasta enero del 2020.
Como criterios de inclusión se tuvieron en cuenta sujetos mayores de 40 años (1-4), programados para la realización de espirometría solicitada por el médico general o de cualquier especialidad (por cualquier indicación) y firma del consentimiento informado. Los criterios de exclusión fueron los siguientes: las espirometrías que no cumplieran con los criterios diagnósticos de acuerdo con las guías de la American Thoracic Society (ATS) (17), los cuestionarios incompletos respecto a las preguntas relacionadas con tos, exposición al humo de leña , tabaquismo, sibilancias o con alguna condición que generara incapacidad para la comunicación y el entendimiento para el desarrollo de cuestionario o la realización de espirometría: discapacidad intelectual, hipoacusia, sordera o desconocimiento del idioma español.
Se realizó espirometría y curva flujo volumen pre y post B2, para la definición de EPOC se cumplieron los criterios de diagnóstico de la ATS, donde la relación VEF1/CVF < 0,7 post broncodilatador se consideró diagnóstico de la enfermedad.
Para la realización de las pruebas espirométricas se contó con la participación y realización por parte de personal capacitado y calificado, como lo es una terapeuta respiratoria, con previa calibración del equipo y con la medición de todas las espirometrías por el mismo instrumento. Se aplicó el cuestionario CDQ, el cual comprende 8 preguntas: 1. Edad, 2. Tabaquismo en paquetes/año, 3 Índice de masa corporal 4. ¿El clima afecta la tos?, 5 ¿Con el frío presenta tos y expectoración?, 6 ¿Usualmente presenta tos y flema en la mañana? 7. ¿Presenta sibilancias? (silbido al pecho), 8. ¿Ha tenido alergias?; En el cual cada pregunta tiene opciones de respuesta que puntúan en un rango de 0 a 10 puntos. El sistema de puntuación final se divide en tres niveles con 2 puntos de corte 16,5 y 19,5. Se aplicó el cuestionario CDQ de forma presencial el mismo día de la realización de la prueba espirométrica. En una segunda visita de seguimiento, que tuvo lugar en un período no menor a 15 días, se aplicó nuevamente el cuestionario CDQ de manera presencial. Se obtuvieron, adicionalmente, las variables de edad, sexo, medidas antropométricas, antecedentes médicos, antecedentes a exposiciones, alergias y las variables espirométricas de CVF, VEF1, VEF1/CVF pre y post B2.
El tamaño de la muestra se calculó según el estudio de Anthony J. Stanley et al. (18), donde se encontró una sensibilidad del 79 %, y una especificidad del 46 % para el cuestionario CDQ, para un nivel de confianza del 95 %, precisión del 5 % y prevalencia de la enfermedad del 20,1 %, se requerían un mínimo de 1 269 sujetos. Estos eran invitados para el ingreso del estudio en el laboratorio de función pulmonar del centro de investigación el día de la realización de la espirometría, su ingreso fue de manera secuencial de acuerdo con su llegada, los datos obtenidos tenían doble digitación para su ingreso a la base de datos.
El análisis fue realizado en el programa SPSS (versión 25). Se compararon entre el grupo de sujetos con EPOC y sin EPOC las variables cualitativas por prueba de Chi cuadrado y las variables cuantitativas con T de Student o U de Mann-Whitney, esto según su distribución. Se realizo una comparación de cada una de las respuestas del cuestionario CDQ entre los sujetos con y sin enfermedad en dos momentos; posteriormente se calculó con el puntaje total del cuestionario CDQ el coeficiente de relación intraclase (CCI) entre las respuestas obtenidas en los dos momentos de la realización del cuestionario, considerándose valores de 0,4 como poca reproducibilidad y valores mayores de 0,75 como excelente (9). Se determinaron además los tres niveles de interpretación del cuestionario puntaje CDQ < 16,5: baja probabilidad; puntaje CDQ 16,5 a 19,5: probabilidad media; puntaje CDQ > 19,5: probabilidad alta en los dos momentos de realización y, se calculó un kappa ponderado para buscar la concordancia entre estos niveles de clasificación; adicionalmente, se estableció el alfa de Cronbach para evaluar la consistencia interna del puntaje (19) y para la validez en términos de exactitud de la prueba diagnóstica, se construyó el área bajo la curva de características operativas del receptor (ACOR) con el puntaje total del cuestionario para el diagnóstico o no de la EPOC. Se consideró una p estadísticamente significativa < 0,05.
El protocolo de investigación siguió los lineamientos internacionales para la investigación en seres humanos, fue aprobado por el Comité de ética de la Universidad de la Sabana y de la Clínica Universidad de la Sabana; todos los sujetos incluidos firmaron un consentimiento informado.
Resultados
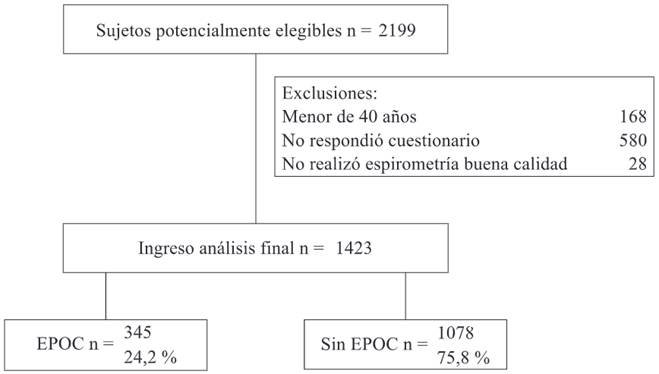
Ingresaron 2.199 pacientes potencialmente elegibles para la aplicación del cuestionario CDQ, donde 1.423 de ellos realizaron el cuestionario de manera completa e ingresaron al análisis final; el flujo de ingreso de los pacientes al estudio se contempla en la Figura 1. La prevalencia de EPOC fue del 24 %, el 44 % era de sexo masculino y el promedio de edad fue de 65 años. Las características de la población se observan en la Tabla 1. En los pacientes con EPOC el 26,9 % tenía antecedente de tabaquismo y el 29,3 % exposición al humo de leña. La diferencia en el tiempo de exposición al humo de leña entre los sujetos que desarrollan EPOC y no EPOC fue de tres años. El subdiagnóstico de la EPOC fue de 51 %, y de sobrediagnóstico fue de 22 %.
Tabla 1 Características generales de la población de estudio CDQ
| Variables | iuPoblación total n = 1423 | EPOC n = 345 | No EPOC n = 1078 | Valor p** |
|---|---|---|---|---|
| Edad x (de)*‡ | 65,4 (11,7) | 69,9 (10,8) | 64 (11,6) | <0,01 |
| Sexo masculino n (%) † | 633 (44) | 194 (56) | 439 (41) | <0,01 |
| Años completos de estudio x(de)*‡ | 8,9 (5,6) | 7,3 (5,5) | 9,4 (5,5) | <0,01 |
| Síntomas clínicos n (%) † | ||||
| Síntomas respiratorios | 1220 (86) | 312 (90) | 908 (84) | 0,004 |
| Edad inicio de síntomas x(de)*‡ | 58 (16,9) | 58 (19,3) | 57 (16) | 0,15 |
| Sibilancias n (%) † | 431 (30) | 139 (40) | 292 (27) | <0,01 |
| Antecedentes patológicos | ||||
| Tabaquismo n (%) † | 661 (46) | 178 (52) | 483 (45) | 0,11 |
| Edad de inicio tabaquismo x (de)*‡ | 19 (6,2) | 17 (5,2) | 19 (6,5) | <0,01 |
| Edad de finalización de tabaquismo x (de)*‡ | 42 (16,3) | 45 (16,5) | 41 (16,1) | <0,01 |
| IPA § M (RIQ)†† | 6,2 (1,5-23,4) | 12 (3-33) | 5,3 (1-18,8) | <0,01 |
| Fumador pasivo n (%) † | 267 (19) | 65 (19) | 202 (19) | <0,01 |
| Exposición humo de leña n (%) | 800 (56) | 235 (68) | 565 (52) | <0,01 |
| Años de exposición al humo de leña x (de)*‡ | 23 (4,7) | 25 (4,6) | 22 (4,8) | 0,003 |
| Historia de atopia n (%) † | 431 (30) | 139 (40) | 292 (27) | <0,01 |
| Diagnóstico previo de EPOC || n (%) | 403 (28) | 168 (49) | 235 (22) | <0,01 |
| Diagnóstico previo de Asma n (%) † | 200 (14) | 63 (18) | 137 (13) | 0,01 |
| Resultados de espirometría | ||||
| Peso x (de)*‡ | 70,9 (13,7) | 68,1 (13,4) | 71,8 (13,7) | <0,01 |
| Talla x (de)*‡ | 159,8 (9,1) | 159,9 (9,1) | 159,8 (9,1) | 0,79 |
| VEF1/CVF pre B2 ¶ | 73,1 (13,1) | 57 (10,4) | 78,2 (9,1) | <0,01 |
| VEF1/CVF post B2 ¶ | 75,9 (12,1) | 59,4 (9,3) | 81,2 (7,1) | <0,01 |
*de: desviación estándar; †n: número o frecuencia; ‡x: promedio; §IPA: Índice paquetes/año; EPOC: enfermedad pulmonar obstructiva crónica; ¶CVF = Capacidad vital forzada. VEF1 = Volumen espiratorio forzado en un segundo; ††M - Mediana, RIQ: Rango intercuartil, **Significancia Estadística <0,05. Fuente: creación propia
En las respuestas del primer cuestionario CDQ observadas en la Tabla 2, la mayoría de los pacientes fueron mayores de 70 años (38 %) y tuvieron un intervalo de exposición al cigarrillo entre 0 a 14 años en ambos grupos; adicionalmente, hasta el 45 % de los pacientes se encontraba en sobrepeso y refería que el clima afectaba la tos; por otro lado, los síntomas menos frecuentes fueron sibilancias y tos con flema en la mañana (< 31 %). Cabe resaltar que hasta el 76 % de los pacientes en el grupo de la EPOC tuvo un puntaje CDQ ≥ 16,5 y hasta el 61 % presentó un puntaje CDQ ≥ 19,5.
Tabla 2 Respuestas Primer Cuestionario CDQ
| Preguntas CDQ | Población total n = 1423 | EPOC n = 345 | No EPOC n = 1078 | Valor p* |
|---|---|---|---|---|
| ¿Cuál es su edad en años? n (%) ‡ | ||||
| 40 a 49 años | 153 (11) | 22 (6,3) | 131 (12) | |
| 50 a 59 años | 272 (19) | 32 (9,3) | 240 (22) | <0,01 |
| 60 a 69 años | 452 (32) | 100 (29) | 352 (33) | |
| Mayor de 70 años | 546 (38) | 191 (55) | 355 (33) | |
| ¿Cuál es total en número de años que usted ha fumado? n (%) ‡ | ||||
| 0-14 | 1132 (80) | 246 (71) | 886 (82) | |
| 15-24 | 92 (6,4) | 27 (7,8) | 65 (6,0) | <0,01 |
| 25-49 | 106 (7,4) | 38 (11) | 68 (6,3) | |
| Más de 50 | 93 (6,5) | 34 (9,9) | 59 (5,5) | |
| Peso IMC (kg/m2) † n (%) ‡ | ||||
| Menor de 25 | 432 (30) | 129 (37) | 303 (28) | |
| 25,4 - 29,7 | 627 (44) | 155 (45) | 472 (44) | <0,01 |
| Mayor a 29,7 | 364 (26) | 61 (18) | 303 (28) | |
| ¿El clima afecta la tos? n (%) ‡ | ||||
| Sí | 845 (59) | 234 (68) | 611 (57) | <0,01 |
| No | 578 (41) | 111 (32) | 467 (43) | |
| ¿Con el frío presenta tos y expectoración? N (%) ‡ | ||||
| Sí | 845 (46) | 234 (55) | 611 (43) | <0,01 |
| No | 578 (54) | 111 (45) | 467 (57) | |
| ¿Usualmente presenta tos y flema en la mañana? n (%) ‡ | ||||
| Sí | 439 (31) | 134 (39) | 305 (28) | <0,01 |
| No | 984 (69) | 211 (61) | 773 (72) | |
| ¿Presenta sibilancias (silbido al pecho)? n (%) | ‡ | |||
| Muy frecuente | 442 (31) | 142 (41) | 300 (28) | <0,01 |
| Nunca | 981 (69) | 203 (59) | 778 (72) | |
| ¿Ha tenido alergias? n(%)‡ | ||||
| Sí | 308 (22) | 73 (21) | 235 (22) | 0,802 |
| No | 1115 (78) | 272 (79) | 843 (78) | |
| Puntaje CDQ baja, media, alta probabilidad n(%)‡ | ||||
| Puntaje CDQ ≤16,5 (baja) | 615 (43) | 82 (24) | 533 (49) | |
| Puntaje CDQ >16,5 <19,5 (media) | 252 (18) | 62 (18) | 190 (18) | <0,001 |
| Puntaje CDQ ≥19,6 (alta) | 556 (39) | 201 (58) | 355 (33) | |
| Puntaje CDQ | ||||
| Puntaje CDQ ≥16,5 n (%) ‡ | ||||
| Sí | 808 (57) | 263 (76) | 545 | <0,001 |
| No | 615 (43) | 82 (24) | 533 | |
| Puntaje de CDQ ≥19,5 n (%) ‡ | ||||
| Sí | 596 (42) | 212 (61) | 384 | <0,001 |
| No | 827 (58) | 133 (39) | 694 |
*Significancia estadística <0,05; † IMC: Índice de masa corporal; ‡ n: número o frecuencia. Fuente: creación propia
Por otro lado, en cuanto a las características de la población en relación con la función pulmonar, el 65 % de los pacientes del estudio se encontraba en GOLD 2.
En la Tabla 3, se observa las respuestas del cuestionario CDQ aplicado por segunda vez a un total de 509 individuos. No se encontró una diferencia estadísticamente significativa en el índice de masa corporal, el efecto del clima en la tos o el antecedente de alergias, entre sujetos con y sin EPOC. Adicionalmente, hasta el 64% de los pacientes con EPOC presentaron con el frío tos con expectoración.
Tabla 3 Respuestas Segundo Cuestionario CDQ

* Significancia estadística <0,05; † IMC: Índice de masa corporal. ‡ n: número o frecuencia. Fuente: creación propia
El ACOR del CDQ fue de 0,68, se encontró un coeficiente de correlación intraclase (CCI) de 0,781 (IC 95: 0,744-0,813) (p < 0,001) y una kappa para la concordancia de los resultados del cuestionario en baja, media y alta probabilidad de 0,65 (p < 0,001) (Tabla 4.). El alfa de Cronbach fue de 0,877, la sensibilidad y la especificidad para el punto de corte de 16,5 fue de 79 % y 44 %, respectivamente. La sensibilidad y la especificidad para el punto de corte de 19,5 fue de 62 % y 64,3 %, respectivamente.
Tabla 4 Características ACOR y CCI del cuestionario CDQ
| ACOR | IC 95 % | valor p* | |
|---|---|---|---|
| 0,68 | 0,647 0,712 | <0,01 | |
| CCI | IC 95 % | valor p* | |
| 0,781† | 0,744 0,813 | <0,01 | |
| 0,877‡ | 0,854 0,897 | <0,01 | |
| Kappa ponderada entre los resultados de baja, media y alta | IC 95 % | valor p* probabilidad | |
| 0,65 | 0,591 0703 | <0,01 |
*p <0,05 estadísticamente significativa; †Coeficiente correlación intraclase medidas simples; ‡Coeficiente correlación intraclase medidas promedio. Fuente: creación propia
Discusión
Se han realizado estudios buscando cuestionarios que sean útiles para detectar pacientes con EPOC de forma temprana (9-12,20,21). Sin embargo, la información del rendimiento diagnóstico de cuestionarios para la población colombiana es escasa. El cuestionario CDQ en validaciones internacionales (13-15) ha mostrado un buen desempeño para discriminar pacientes que requieren de espirometría para el diagnóstico de la EPOC. En este estudio, el puntaje mostró un rendimiento regular para el diagnóstico, su reproducibilidad intraevaluador fue buena y, con un punto de corte de 16,5, mantiene una buena sensibilidad.
El ACOR encontrada entre los diferentes cuestionarios desarrollados (9-12) se encuentra en un rango entre 0,65 y 0,81. La aplicación del cuestionario CDQ en la población colombiana se encuentra cercano a los valores inferiores de las ACOR reportadas, a pesar de que las características de la población estudiada son similares en cuanto a edad y sexo. Es probable que la exposición a otros factores como el humo de leña en nuestra población pueda repercutir en el puntaje del CDQ para el diagnóstico de la EPOC. La frecuencia de los síntomas respiratorios influenciados por la edad (14) puede ser otro factor que impacta en el desarrollo de este tipo de cuestionarios. Sin embargo, se incluyó una población mayor de 40 años, edad en la que se han encaminado los esfuerzos para detectar la enfermedad.
Con un punto de cohorte de 19,5 el cuestionario CDQ en la población colombiana muestra una sensibilidad y especificidad similar a la reportada en los estudios iniciales de validación del CDQ, donde se reportaron valores de sensibilidad del 64,5 % y especificidad del 65,2 %; con un punto de cohorte de 16,5 hay un aumento de sensibilidad, pero este valor no logra el rango de sensibilidad del 89-94 % reportado por Harron S et al. en una revisión sistemática donde se evaluaron diferentes puntos de cohorte para el cuestionario CDQ (9,13-16). No obstante, al considerarse que un cuestionario puede ser una herramienta de tamización en los sujetos con EPOC, utilizar el punto de cohorte de 16,5 en el cuestionario CDQ mejora la sensibilidad a un rango aceptable para orientar la realización de las pruebas diagnósticas complementarias, como la espirometría. La consistencia interna evaluada a través del alfa de Cronbach (19) en el estudio muestra una buena asociación entre los ítems que integran el cuestionario. No obstante, podría ser útil en nuestra población un ítem que evalúe entre los factores de riesgo la exposición al humo de leña (22-28).
Cuando se evalúan las posibles diferencias de este cuestionario con otros cuestionarios realizados para el diagnóstico de la EPOC, como el Lung Functional Questionnaire (LFQ) o el Chronic Obstructive Pulmonary Disease-Population Screener (COPD PS), la formulación, el número y el sistema de calificación de las preguntas es diferente. El cuestionario CDQ tiene 8 ítems donde la edad y el tabaquismo se clasifican en cuatro categorías, el índice de masa corporal en 3 y las 5 preguntas restantes en respuestas dicotómicas (13). Por el contrario, el cuestionario LFQ tiene 5 preguntas todas con 5 opciones de respuestas (11) y el cuestionario COPD-PS también tiene 5 preguntas, 1 de ellas con 3 respuestas y otra pregunta con 4 respuestas (12); además, la población en las cohortes de validación y la puntuación de cada cuestionario es diferente, lo que puede explicar, en parte, la variación en su rendimiento (11-13,25,26). Por otra parte, resaltamos que el aumento en el número de preguntas del CDQ con respecto a los cuestionarios previamente mencionados puede ser un factor que influye en la detección de sujetos que requieren de espirometría poco sintomáticos; ya que, al tener un mayor número de preguntas que incluyen variables no relacionadas con los síntomas, se disminuye la dependencia que tienen otros cuestionarios de la aparición y mantenimiento de la sintomatología en los pacientes (22-30), lo que representa un obstáculo en el reconocimiento de la enfermedad en un estadio temprano (8).
Entre las debilidades de este estudio se encuentra la pérdida de participantes a lo largo del seguimiento. Lo anterior debido a la participación en la segunda visita fue menos de la mitad de los que respondieron el cuestionario por primera vez, siendo esta una limitación frecuente en los estudios prospectivos. Asimismo, el estudio se realizó en un solo centro de salud de III nivel de atención, lo que aumenta el riesgo de sesgo de selección, ya que la población que se atiende en la institución puede tener características regionales propias y, por lo tanto, no representa todo el contexto en el que se desarrolla la enfermedad en el país. A pesar de estas limitaciones, consideramos que el número de sujetos incluidos en el estudio es adecuado y puede ser representativo de los sujetos con EPOC. El cuestionario CDQ puede ser considerado como una opción adicional entre las diferentes herramientas evaluadas para la búsqueda de pacientes con EPOC en la atención médica, sin que tenga un rendimiento claramente superior con respecto a otros cuestionarios.
Finalmente, vale la pena aclarar que la utilización de los cuestionarios diagnósticos da una aproximación a la enfermedad (8,9) y, en todos los casos, se requiere de estudios complementarios como la espirometría para definir el diagnóstico de la EPOC.