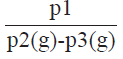Introducción
El almidón se usa en la preparación de alimentos como agente espesante, es decir, que proporciona textura, apariencia y forma (Saartrat, Puttanlek, Rungsardthong y Uttapap, 2005; Agudelo, Sepúlveda y Restrepo, 2015). Es extraído comúnmente de cereales, pseudocereales y de rizomas como el sagú, también conocido como achira, risgua, arawac, imocoma, chisgua, maraca y capacho que es una planta perenne de la familia cannaceaenativa de los Andes en América del Sur (Andrade-Maecha, Tapia-Blácido y Menegalli, 2012; Wafa et al., 2016). Es cultivada en países latinoamericanos como Bolivia, Ecuador (Garcés y Carbo, 2013), México, Brasil y Perú (Hernández-Medina et al. 2008) y en países asiáticos (Andrade-Maecha et al., 2012). En Colombia, tiene fines comerciales, ornamentales (Andrade-Maecha et al., 2012) y se usa para la fabricación de productos especializados de pan y sus derivados (Ayala, Agudelo y Vargas, 2012). Se encuentra distribuido en la región andina colombiana y es promisorio debido a su rusticidad, tolerancia a plagas (Garcés y Carbo, 2013) y rendimiento de producción hasta de 3.42 ton ha-1, mayor a la batata (1 ton ha-1) (Rojas-Mercado y Seminario-Cunya, 2014). Su extracción se ha mecanizado, pero también se realiza a mano; el proceso inicia con el lavado de las raíces, liberación del almidón, tamizado, sedimentación y secado. Algunas variaciones incluyen rallado (Ayala et al., 2012), licuado (Pérez-Rea et al., 2012; Fuentes et al., 2019) y con molino (Fatima, Umali y Tayobong, 2019, Andrade-Maecha et al., 2012) utilizando como disolventes agua, etanol, éter dietilico o éter de petróleo, pero con rendimientos máximos en agua (Gaur, 2014). Además, se reporta el uso de K2S2O5 tanto para limpieza como para evitar la oxidación del material cuando es cortado (Andrade-Maecha et al., 2012). Pese a reportarse diferentes métodos de extracción, poca atención se ha prestado al impacto que ejercen en las características funcionales y composicionales del almidón. Por lo anterior, el objetivo de esta investigación fue evaluar el efecto de dos métodos de extracción (licuado y rallado) de almidón de canna indica L. sobre sus propiedades físicoquímicas.
Materiales y métodos
Materiales
Se utilizaron rizomas de canna indica L. de un cultivo establecido en la granja La María ubicada en la Universidad Pedagógica y Tecnológica de Colombia con sede en la ciudad de Tunja, Departamento de Boyacá, coordenadas 5 ° 33 ' 7'' N y 73 ° 21 ' 23 '' W a una altura de 2730 msnm, temperatura media de 21 ° C.
Proceso de extracción del almidón
Los rizomas se lavaron con agua destilada y se les retiró la capa externa; se dividieron en dos partes, la primera se utilizó para extraer almidón por el método de licuado (LI) con una licuadora (Oster®, modelo 4655, EE. UU.) de tres velocidades y la otra mitad por el método de extracción por rallado (RA). El material se recogió y se depositó en vasos de precipitado de 250 mL con 150 mL de agua destilada. Se dejó en suspensión por 3 h, se retiró la fibra y el almidón sedimentado se filtró. Luego, se hicieron tres lavados con 150 mL de agua destilada cada uno. En el método por LI, el almidón se secó a 60 ° C, y en el método por RA a temperatura ambiente (21° C) por 48 h, este último fue secado tal como se realiza en las condiciones de extracción tradicional.
Caracteres evaluados
Calidad composicional
Tanto en el almidón como en el rizoma, se determinó el contenido de: materia seca (%) (MS) a partir de muestras dejadas a 60° C durante 48 h en una estufa universal (Memmert®, modelo UN55, Alemana), y el contenido de humedad (%) (H) por diferencia de peso; cenizas (%) (CEN), incinerando las muestras a 550° C en una mufla (Thermolyne®, modelo F48010-33, EE. UU.), extracto etéreo (%) (EE) por el método Soxlet y proteína cruda (%) (PC) por el método de KJeldahl. El contenido de azucares reductores (mg.g-1) y no reductores (mg.g-1) se halló por la prueba cuantitativa de Benedict (Chen, Klemm y Jeng, 1989) pero en este último se agregó 1 mL de HCl y 5 mL de NaOH a las soluciones problema.
Índice de absorción de agua (g agua. g-1almidón) (IAA), solubilidad en agua (%) (ISA), poder de hinchamiento del almidón (g agua. g-1 almidón) (PI) y temperatura de gelatinización (° C) (TG)
El IAA, el ISA y el PI del almidón se determinaron por el método propuesto por Anderson, Conway, y Peplinski (1970), a partir de una solución con 1.2 g de almidón en 50 mL de agua destilada que se depositó en un tubo de centrifuga, y se calentó a 60° C con agitación constante durante 30 minutos y posteriormente se centrifugó a 2000 rpm el mismo tiempo. El IAA se calculó mediante la diferencia entre el peso del gel precipitado (pl) que se formó después del tratamiento térmico y el peso de la muestra de almidón utilizado inicialmente (p2). Mientras que el ISA se determinó a partir del peso del sobrenadante residual suspendido (p3) que fue secado a 60° C durante 24 h. El poder de hinchamiento se calculó por la siguiente expresión matemática:
Y la temperatura de gelatinización se halló con el método propuesto por Narayama y Narasinga-Rao (1982) a partir de muestras de 1 g de almidón en un volumen de 50 mL de agua destilada.
Viscosidad en medios ácidos del almidón (d Pa●s)
Se determinó a partir de la metodología de Santos, Bonomo, Fontan, Santos y Silva (2009), en soluciones de 20 g L-1 con un buffer (0.1 M) elaborado con citrato de sodio y ácido cítrico a pH de: 3; 3,5; 4,5; 5,5; 6,5 y 7. Tres buffer (3; 3,5; 4,5) se mezclaron con almidón extraído por el método RA y tres (5,5; 6,5 y 7) con almidón extraído por el método LI. Todas las muestras se calentaron a 80° C y se leyó su viscosidad a 21° C con un viscosímetro (Brookfield Ametek ® modelo LVDVE 115, EE. UU.) y aguja 0.2.
Análisis estadístico
Se empleó un diseño completamente al azar con seis tratamientos que corresponden a la combinación de dos métodos de extracción (licuado y rallado) y tres pH diferentes para cada método (Tabla 1) cada tratamiento tuvo tres repeticiones, y cada unidad experimental correspondió a un frasco donde se depositó el almidón extraído de doce rizomas.
Tabla 1 Descripción de los tratamientos
| Tratamiento | Método de extracción | pH |
|---|---|---|
| T1 | Rallado | Buffer pH 3 |
| T2 | Rallado | Buffer pH 3.5 |
| T3 | Rallado | Buffer pH 4.5 |
| T4 | Licuado | Buffer pH 5.5 |
| T5 | Licuado | Buffer pH 6.5 |
| T6 | Licuado | Buffer pH 7 |
Fuente: elaboración propia
Se hizo un análisis de varianza y donde hubo diferencia, se aplicó la prueba de comparación de promedios DMS (p<0,05). Para el análisis de las características químicas del almidón se usó la prueba de comparación de medias de dos poblaciones normales (licuado y rallado) con el estadístico t student (P ≤ 0,05). Asimismo, se estableció si existía correlación entre el pH del sobrenadante y la viscosidad con la prueba de Pearson. Todos los análisis se realizaron en el sofware SigmaPlot12®.
Resultados
Calidad composicional
La Tabla 2 muestra los resultados composicionales del almidón y rizoma de canna indica L., se observa que este último presentó alto contenido de humedad (49.59 ± 2.76) relacionada con tendencia a putrefacción, que se caracteriza por un proceso de oxidación y cambio de coloración en la superficie una vez se extrae el almidón.
Tabla 2 Características composicionales del almidón extraído y del rizoma completo de canna indica L.
| Característica composicional | Almidón extraído | Rizoma completo |
| Materia seca (%) | 93,01 ± 1,96 | 50,41 ± 2,76 |
| Humedad (%) | 6,99 ± 1,96 | 49,59 ± 2,76 |
| Cenizas (%) | 0,22 ± 0,02 | 4,66 ± 0,03 |
| Proteína (%) | 1,75 ± 0,01 | 3,51 ± 0,02 |
| Extracto etéreo (%) | 0,43 ± 0,02 | 0,29 ± 0,01 |
| AR (mg. g -1) | 0,12 ± 0,01 | 0,14 ± 0,01 |
| ANR (mg. g -1) | 0,08 ± 0,01 | 0,10 ± 0,01 |
| pH | 5,91 ± 0,01 | 6,43 ± 0,01 |
AR: azúcares reductores, ANR: azúcares no reductores, ±: error estándar (n=3)
Fuente: elaboración propia.
Características químicas del almidón
Los valores de IAA (g agua. g-1 almidón), ISA (%), PI (g agua. g-1 almidón) y TG (° C) se presentan en la Tabla 3 . Solo hubo diferencias significativas (p <0,01) en la TG (° C) del almidón de acuerdo al método de extracción.
Tabla 3 Características químicas del almidón de canna indica L. obtenido con diferente método de extracción
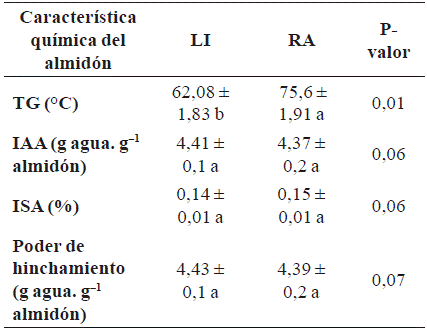
TG: temperatura de gelatinización IAA: índice de absorción de agua, ISA: índice de solubilidad de agua, LI: extracción por licuado, RA: extracción por rallado. Promedios seguidos de letras diferentes presentan diferencias estadísticas con la prueba de t student (p<0,05) para cada variable. ±: error estándar.
Fuente: elaboración propia
Viscosidad en medios ácidos del almidón (d Pa●s)
Se incrementó con el aumento de la velocidad de agitación logrando mantenerse por encima de 11 N.m a partir de 50 rpm. Esto se debe a que las fuerzas generadas por agitación a alta velocidad actúan en los gránulos hinchados y los interrumpen (Saartrat et al., 2005). Se presentaron diferencias estadísticas entre las viscosidades a distinto pH y entre el método de extracción (p <0,01) pero no existió ninguna correlación (p >0,05). Se observó que la viscosidad en el almidón extraído por RA y secado a temperatura ambiente (21 °C) aumentó con el pH de la solución, contrario al almidón extraído por LI y secado a 60 °C que fue expuesto a los buffer 5,5; 6,5 y 7, como se observa en la Tabla 4.
Tabla 4 Viscosidad del almidón de sagú a diferente pH
| Solución | Viscosidad (dPa●s) a 50 rpm | Viscosidad (dPa●s) a 60 rpm | Viscosidad (dPa●s) a 100rpm |
| RA. Buffer pH 3 | 38,2 ± 2,22 a | 38,4 ± 2,05 a | 40,6 ± 2,33 a |
| RA. Buffer pH 3.5 | 39,6 ± 3,95 a | 40,2 ± 3,53 a | 42,9 ± 2,75 a |
| RA. Buffer pH 4.5 | 45,9 ± 8,23 a | 45,4 ± 6,88 a | 46,1 ± 4,11 a |
| LI. Buffer pH 5.5 | 22,8 ± 0,26 b | 24,1 ± 0,15 b | 28,5 ± 0,19 b |
| LI. Buffer pH 6.5 | 27,5 ± 0,90 b | 28,8 ± 0,95 b | 33,7 ± 1,12 b |
| LI. Buffer pH 7 | 22,0 ± 0,72 b | 24,9 ± 2,4 b | 28,2 ± 0,93 b |
RA: tratamiento por rallado, LI: tratamiento por licuado. rpm: revoluciones por minuto. Promedios seguidos de letras diferentes presentan diferencias estadísticas entre columnas con la prueba DMS de Fischer (p <0.05). ±: error estándar.
Fuente: elaboración propia
Variación del pH en el sobrenadante de extracción del almidón
En el sobrenadante de extracción el pH disminuyó con tendencia lineal en 0,0267 con intervalos de una h en el método RA, mientras que en de LI fue mayor con 0,3533 con diferencias estadísticas a las 3 h (p ≤ 0,05) (Figura 1).
Discusión
El rizoma de canna indica L. obtuvo 4,66 ± 0,03 % de cenizas, mayor a lo reportado por Mohan y Kalidass (2010) (3,14 ± 0,01%). Se observó bajo contenido de grasa (0,29 ± 0,01 %) y de proteína (3,51 ± 0,02 %) aunque estos valores pueden variar entre 4,31 - 4,35 % y 4,81 - 6,34% respectivamente (Okonwu y Ariaga, 2017; Mohan y Kalidass, 2010). Las características composicionales del almidón de canna indica L. se encuentran dentro de los parámetros de buena calidad de acuerdo a los estándares Codex, con valores similares a los observados por Fatima et al., (2019) en almidón extraído con molino (0,24 ± 0,04% de proteína cruda, 0,24 ± 0,01% de grasa cruda, 2,21 ± 1,03 % de proteína cruda) y con Ayala et al., (2012) en almidón extraído con el método de rallado ( 0,24 ± 0,01% cenizas, 0,60 ± 0,11% proteína cruda, 0,38 ± 0,05% grasa cruda,), de modo que el proceso de extracción no afectó la calidad nutricional, la cual está relacionada con el manejo del cultivo, el lugar de origen y con las condiciones agroecológicas por influencia en el metabolismo de las plantas (Thitisaksakul, Jiménez, Arias y Beckles, 2012). La presencia de proteína y lípidos en el almidón no es deseable debido a que forman el complejo amilosa-lípidos que inhibe el poder de hinchamiento y la gelatinización (Lindeboom, Chang y Tyler, 2004), y la amilosa que es un polímero lineal de unidades de glucosa unidas por enlaces a (1-4) y algunos enlaces a (1-6), no es soluble en agua (Hernández-Medina et al., 2008) y puede retardar la hidrólisis (Guillén, Oria y Salvador, 2018). Por ello, bajo contenido de proteína en el almidón de canna indica L. es ideal porque acelera su gelatinización cuando se realiza cocción (BeMiller y Whistler, 2009).
La TG cambió de acuerdo con el método de extracción: 62,08 ± 1,83 °C (LI) y 75,6 ± 1,91 °C (RA) (p <0,01) (Tabla 3). Los valores están entre el rango reportado en almidón colombiano (59,9 ± 0,1 - 71,6 ± 0,9 °C) (Andrade-Maecha et al., 2012), pero fueron inferiores a lo observado por Fatima et al., (2019) (76,33 ± 3,06 °C) para almidón extraído con molino. Dicha variación se relaciona con la altitud en la que crecen las plantas (Fuentes et al., 2019) y con los diferentes grados de reducción de la resistencia del almidón, por destrucción de la barrera física durante la extracción como se sucede con la molienda y la hidrólisis de proteasas por un efecto enzimático (Ma y Boye, 2016), acompañado con variación del pH en el sobrenadante como en este estudio. Aunque no se descarta un efecto protector por el contenido de proteína y grasa en el almidón (Andrade-Maecha et al., 2012). Por otro lado, el IAA (4,41± 0,1 y 4,37 ± 0,2 g agua/ g-1 almidón), el ISA (0,14 ± 0,01 % y 0,15 ± 0,01 %) y el PI (4,43 ± 0,1 y 4,39 ± 0,2 g agua. g-1 almidón) no presentaron cambios significativos de acuerdo al método de extracción (p ≥ 0,05). Pero son menores a lo observado por Fatima et al., (2019) de 9,81 ± 0,10 % ISA, 6,63 ± 1,42 (g agua/ g-1 almidón) IAA, en almidón extraído con molino. El IAA fue similar a lo observado por Andrade-Maecha et al., (2012) en almidón colombiano (4,4-45,7 g agua/ g-1 almidón IAA) pero superior a almidón de canna indica de Brasil (2,4-24,0 g agua/ g-1 almidón IAA), extraídos ambos con molino.
Estas variaciones en el IAA, ISA y el PI, se deben a que dichos parámetros dependen de la relación amilosa / amilopectina, estructura, tamaño y peso del gránulo (Lindeboom et al. 2004), pero a partir de 60 °C los valores de estas características aumentan y llegan al máximo valor a los 90 °C (Hernández-Medina et al. 2008). El IAA es mayor en almidones con menos complejos lipídicos por una menor disposición cristalizada de las cadenas de polisacáridos en B-gránulos (una mayor proporción de zonas amorfas más accesible para el agua) (Lindeboom et al. 2004), pero mayor en almidones con presencia de celulosa y aminoácidos polares hidrofílicos (Andrade-Maecha et al., 2012), lo que a su vez puede influir en la viscosidad, la cual es directamente proporcional al pH del medio, es decir que a medida que el pH disminuye también la viscosidad, sin embargo, el almidón extraído por rallado obtuvo valores más altos en medios más ácidos (40,6 ± 2,33 dPa●s, pH 3), lo que puede deberse al mayor tamaño de los gránulos por efecto mecánico durante la extracción, en comparación con almidón extraído por rallado (28,5 ± 0,19 dPa●s, pH 3) lo que se asocia con el rompimiento de la estructura del almidón (Saartrat et al. 2005).
Conclusiones
El método de extracción de almidón afectó la temperatura de gelatinización (TG) y la viscosidad por un efecto mecánico y por influencia en la variación en el pH del sobrenadante. Con la extracción por licuado se necesitó menor temperatura para que el almidón de canna indica L. se gelatinizara (TG 62,08 ± 1,83 °C) comparado con el método rallado (TG 75,6 ± 1,91 °C). La viscosidad varió con diferentes buffer y velocidades de agitación, el mayor valor se obtuvo para el método rallado a pH 4,5 y 100 rpm (46,1±4,11); y en el método licuado se obtuvo mayor viscosidad con pH 6,5 y 100 rpm (33,7±1,12). Por la baja retención de agua del almidón de canna indica L. extraído por licuado (4,41 ± 0,1 g agua. g-1 almidón) o rallado (4,37 ± 0,2 g agua. g-1 almidón) no es recomendable en productos donde se pueda presentar retracción del almidón.