Introducción
En el mundo, el cáncer gástrico (CG) es un problema de salud pública. Las altas tasas de incidencia se concentran en países en desarrollo, como Colombia, con un aumento progresivo de la mortalidad específica por cáncer en estos países. Según datos de GLOBOCAN, para el 2020 se presentaron 1.089.103 nuevos casos de cáncer gástrico, con más de 768.793 muertes en el mundo, representando un 5,6 % de los casos nuevos de cáncer y el 7,7 % del total de muertes por cáncer1. Para Colombia, según esta fuente, se detectaron 8214 casos nuevos de cáncer gástrico (7,3 %), ocupando el cuarto lugar en incidencia y representando la primera causa de mortalidad por cáncer, con 6451 fallecidos (1050 casos más en comparación con el 2018)2.
Las primeras publicaciones sobre el uso de la laparoscopia de estadificación (LE) en CG iniciaron en 19843, resaltando la capacidad de este procedimiento para detectar compromiso locorregional avanzado y metastásico a peritoneo, disminuyendo así el número de laparotomías no terapéuticas y aumentando la posibilidad de re-direccionar el manejo en estos pacientes4-6. Diferentes publicaciones reportaron la identificación del compromiso peritoneal no documentado por imágenes en un 18-41 %7-9, lo cual resulta más relevante en países como el nuestro, con alta incidencia de pacientes en estadios avanzados y mayor probabilidad de compromiso metastásico.
La eficacia actual de la LE para la detección del compromiso peritoneal es del 94-100 %10-11 y se estima que permite la re-estadificación y disminuye el número de laparotomías no terapéuticas en alrededor del 44 % de los pacientes11-12. A partir de los primeros estudios que mostraron el beneficio de la terapia neoadyuvante para los pacientes con CG avanzado resecable13, y la posibilidad de brindar manejo quirúrgico en el escenario de la enfermedad metastásica limitada, las indicaciones de la laparoscopia se han extendido; actualmente se recomienda como parte del proceso de estadificación, permitiendo evaluar la resecabilidad y el compromiso metastásico e identificar los pacientes que se benefician de terapia neoadyuvante o de una repleción nutricional previo a un procedimiento quirúrgico curativo o paliativo.
Sin embargo, al revisar las guías y diferentes publicaciones internacionales, no hay unanimidad en las indicaciones para incluir este procedimiento como parte del proceso de estadificación. La National Comprehensive Cancer Network (NCCN) en 2016 13 y las guías japonesas en 2018 14 indican este procedimiento en pacientes T1b en adelante; por otro lado, las guías canadienses15 lo reservan para los pacientes T3 y T4 por imágenes o con alto riesgo para compromiso por metástasis peritoneales (células en anillo de sello, linitis plástica o tumores pobremente diferenciados).
En el servicio de cirugía gastrointestinal del Instituto Nacional de Cancerología, Bogotá, D.C., Colombia16, se analizaron los pacientes con cáncer gástrico llevados a LE, y encontraron una relación estadísticamente significativa con la presencia de carcinomatosis peritoneal para pacientes menores de 65 años (OR=2,0; IC95%:1-4,2), mujeres (OR=2,2; IC95%: 1,06-4,7), localización cardial del tumor (OR=2,6; IC95%: 1,25-5,2), presencia de ascitis (OR=4,3; IC95%: 1,3-15,9) e histología del tipo difuso (OR=3,0; IC95%: 1,5-5,8), sin embargo, esto no implica que, en la práctica, la LE esté reservada exclusivamente para estos casos.
Actualmente no es discutible la utilidad de la LE en la documentación de carcinomatosis peritoneal micro o macroscópica, sin embargo, las tendencias actuales de manejo, el advenimiento de la neoadyuvancia, la cirugía de conversión y la inclusión de algunos pacientes para cirugía peritoneal, ha generado una expansión del horizonte en la intención curativa para los pacientes con CG, ampliando también el papel de la LE. Este trabajo buscaba conocer la situación actual de la LE en el país con base en las tendencias de un grupo de cirujanos afines al manejo de los pacientes con CG, con el objetivo de analizar las indicaciones, utilidad real y aspectos técnicos del procedimiento, acorde a las recomendaciones internacionales.
Métodos
Se realizó un estudio observacional descriptivo con corte transversal y muestreo intencional a través de una encuesta, que se aplicó a los médicos especialistas en cirugía general o subespecialistas afines al manejo de pacientes con cáncer gastrointestinal, y que desempeñaban sus funciones en Colombia.
Los cirujanos fueron contactados a través de redes sociales por mensaje electrónico, solicitando su participación y aclarando el objetivo del estudio; se adjuntó el enlace de acceso directo a un cuestionario en Google Drive como herramienta para la recolección de datos de variables demográficas y preguntas cerradas de selección múltiple en relación con las indicaciones y técnica usada en el procedimiento de LE en CG. Los datos obtenidos fueron tabulados en Microsoft Excel®.
Se describieron las variables de importancia demográficas, así como la tendencia en las indicaciones y técnica usada en el procedimiento. Para el análisis se utilizó el software Stata, versión 14 (StataCorp LP, College Station, TX, USA).
Resultados
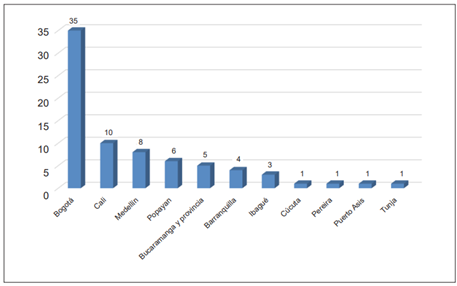
Durante el periodo comprendido entre el 15 de noviembre y el 15 de diciembre del 2021, 74 cirujanos de Colombia afines al manejo del cáncer gastrointestinal respondieron la totalidad de las preguntas de la encuesta. La mayoría de los cirujanos se desempeñaban en la ciudad de Bogotá (47,3 %) (Figura 1). El 23,1 % refirió menos de 5 años de experiencia, 31,3 % entre 10 y 15 años y el 35,4 % de ellos tenía una experiencia superior a 15 años.
Indicaciones
El 43,8 % de los cirujanos refirió que su principal objetivo al realizar la LE era descartar la presencia de compromiso peritoneal, el 39,7 % para evaluar resecabilidad y solo el 16,4 % consideró realizarla para determinar la indicación de neoadyuvancia.
Dentro de las características de los pacientes para definir realizar la LE, el 54,1 % de los cirujanos consideró realizarla en pacientes desde estadios tempranos (menores de T2) y solo el 4,2 % tuvo en cuenta el compromiso linfático (N). El 48,6 % de los cirujanos realizaba el procedimiento en pacientes con sospecha por imágenes de compromiso peritoneal y el 27,8 % tenía en cuenta otras características como la histopatología, el tamaño o la localización tumoral para decidir realizar el procedimiento.
El 78,1 % de los cirujanos realizaba la LE como parte del proceso de estadificación previo a definir el manejo en los pacientes con CG, sin embargo, el 21,9 % la realizaba como procedimiento inicial que precedía a la gastrectomía.
Aspectos técnicos
Para los cirujanos encuestados, la preferencia en la colocación de los puertos es diversa, sin embargo, predominó el acceso con un puerto umbilical y dos puertos laterales (73,6 %) y solo el 16,7 % de los cirujanos manifestaron su preferencia en los puertos sobre la línea media.
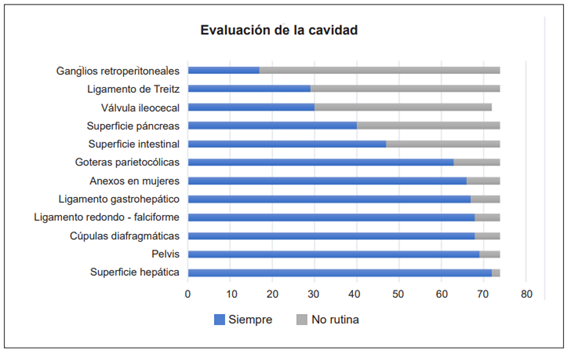
Los sitios anatómicos de la cavidad abdominal evaluados con mayor frecuencia por los cirujanos fueron la superficie hepática (97 %), el ligamento gastrohepático (90,5 %), las cúpulas diafragmáticas (91,8 %), la pelvis (93,2 %), los recesos parietocólicos (85 %) y los anexos en mujeres (89 %). Las superficies anatómicas evaluadas en menor frecuencia fueron la válvula ileocecal (40,5 %), el ligamento de Treitz (39 %) y el retroperitoneo (22,9 %) en búsqueda de adenomegalias a este nivel (Figura 2).
El 97,1 % de los cirujanos tomaba citología peritoneal, sin embargo, de este porcentaje, el 30 % la realizaba solo si había líquido libre y solo el 27,8 % enviaba más de una muestra para citología. El 89 % siempre realizaba biopsia de los implantes peritoneales, usando instrumentos de corte o tracción, sin energía en la mayoría de los casos (85 %). El 77 % de los cirujanos describían el compromiso peritoneal acorde al índice de carcinomatosis peritoneal. Un tiempo quirúrgico promedio de 30 a 60 minutos fue reportado por el 69,4 % de los cirujanos, sin embargo, el 22,2 % invertía usualmente menos de 30 minutos en el procedimiento.
Discusión
La LE es considerada por muchos la mejor herramienta para completar el proceso de estadificación de los pacientes con CG, incluso en estadios tempranos, sin embargo, en la práctica se continúa reservando para pacientes seleccionados, como lo describen Groh y cols.17 en un análisis de 5610 pacientes de la base de datos nacional del programa “Surveillance, Epidemiology, and End Results” (SEER) de los años 2015 a 2018, donde solo al 25 % de los pacientes con CG se les realizó este procedimiento previo a definir su tratamiento.
La inclusión de la laparoscopia dentro de los estudios iniciales en los pacientes con CG, como lo consideró el 78,1 % de los cirujanos encuestados, tiene varias ventajas que han sido soportadas por la literatura, entre ellas la disminución de cirugías innecesarias, reportada entre el 16,2 al 33 % vs. el 8,5 % cuando se compara con un grupo donde solo se realizan imágenes16-18, debido a que la sensibilidad de la tomografía para la detección de compromiso metastásico peritoneal (uno de los criterios más frecuentes de inoperabilidad) es tan baja como del 22-33 %17,18, por la limitación en la identificación de implantes menores a 1 cm (9 % - 28 %)19.
Por otra parte, según un meta-análisis reciente18, el rendimiento de la laparoscopia para la detección de carcinomatosis es del 85 al 100 %, logrando detectar siembras peritoneales en el 13-37 % de los pacientes sin sospecha clínica o imagenológica16,20. Con base en esto, se debería reconsiderar la tendencia de algunos cirujanos de realizar la LE solo bajo la sospecha de carcinomatosis por imágenes, debido a que probablemente cuando el compromiso sea identificado por estos estudios ya no exista una alternativa diferente a la del manejo sistémico paliativo.
Descartar el compromiso peritoneal fue el principal objetivo para el 43 % de los cirujanos encuestados, no obstante, se identificó una tendencia a considerar el procedimiento en estadios tempranos, lo que muestra la adherencia a guías como las de la National Comprehensive Cancer Network (NCCN), la European Society for Medical Oncology (ESMO) y la Asociación Japonesa de Cáncer Gástrico (JGCA).
Tener en cuenta otras características como la histopatología, el tamaño o la localización tumoral en la decisión de realizar el procedimiento, tiene soporte en distintas publicaciones donde se han evaluado factores e incluso puntajes de riesgo para carcinomatosis peritoneal15,18,21. Una de las más conocidas es la de Sarela y colaboradores22, quienes reportaron una asociación del compromiso peritoneal con algunos hallazgos clínicos e imagenológicos como edad menor o igual a 70 años (34 %), lesiones proximales (42 %), compromiso gástrico completo (66 %), adenocarcinoma pobremente diferenciado (36 %), linfadenopatía mayor de un cm por tomografía (49 %) y profundidad tumoral T3 o T4 (63 %), comparado con un 17 % en los pacientes T1-T222,23.
La indicación adecuada de neoadyuvancia en algunos pacientes con CG avanzado ha demostrado tener un impacto positivo en la supervivencia global24. Muchos de los factores anteriormente mencionados, son los mismos que se tienen en cuenta al indicar la LE con este objetivo. El rol de este procedimiento en la identificación de los pacientes que se benefician de neoadyuvancia tiene su base en la baja sensibilidad de las imágenes para detectar no solo el compromiso peritoneal si no también la resecabilidad, por tanto, su uso en aquellos pacientes cT3/T4, cN+ es importante para completar el proceso de estadificación que podría llevar a un cambio en la secuencia de manejo18,25.
A pesar de encontrar literatura y guías que incorporan la laparoscopia en la estadificación desde las lesiones tempranas, consideramos que en este grupo de pacientes el impacto en el cambio de la conducta y el retraso del tratamiento quirúrgico oportuno, son variables que en nuestro medio deben ser tenidas en cuenta antes de considerar su uso rutinario. Sin embargo, con el objetivo de evitar laparotomías innecesarias, cuando se considere un abordaje quirúrgico de entrada en este grupo de pacientes, la revisión inicial de la cavidad abdominal por laparoscopia, durante el mismo tiempo de la gastrectomía, podría cumplir los mismos objetivos, sin un retraso en el tratamiento.
Al realizar la revisión de la literatura con el objetivo de estandarizar algunos aspectos técnicos del procedimiento, se pone en evidencia que existen elementos que están relacionados con la dificultad en la exposición de las diferentes superficies a evaluar, sin embargo, es importante definir los objetivos mínimos que se deben cumplir al finalizar una LE.
La ubicación de los trocares parece no tener un estándar, pero recientes publicaciones11,25destacan la posibilidad de siembras peritoneales en los puertos (0-21 %) y por tanto, la necesidad de ubicar los trocares sobre la línea media. Algunos autores han descrito que los factores asociados con este evento están en relación con las medidas inadecuadas en la manipulación de los puertos y del neumoperitoneo. Por lo tanto, este aspecto técnico está condicionado a la exposición segura que permita evaluar la cavidad abdominal cumpliendo las recomendaciones en el manejo de las muestras de tejido y la aspiración del CO2 previo al retiro de los trocares.
En esta encuesta se encontró una tendencia a la evaluación sistemática de las superficies peritoneales fácilmente asequibles (cúpulas diafragmáticas, superficie hepática y goteras parietocólicas), con un menor número de cirujanos que evalúan puntos críticos como el mesenterio, el retroperitoneo y la superficie intestinal, incluso en sus puntos de fijación (ligamento de Treitz y válvula ileocecal).
Varios autores han descrito secuencias técnicas para lograr los objetivos de la LE. Una de las primeras publicaciones de D’Ugo y cols.11, resalta la necesidad de realizar una estadificación “TNM invertida”, evaluando inicialmente toda la cavidad peritoneal en búsqueda de compromiso metastásico, dejando para el final la manipulación gástrica y así limitar la diseminación de células tumorales. A medida que en el tiempo, el compromiso peritoneal limitado pudiese tener una opción curativa, se ha enfatizado en la valoración estricta de la cavidad abdominal teniendo en cuenta los puntos con mayor riesgo de compromiso peritoneal basados en la fisiología del peritoneo, sin olvidar la necesidad de evaluar el compromiso localmente avanzado que indique irresecabilidad26.
La utilidad de la citología peritoneal está respaldada por diferentes publicaciones, donde se enfatiza la necesidad de descartar la enfermedad peritoneal no visible, dando una posibilidad de re-estadificación en el 29-44 % de los pacientes, con la alternativa de manejo sistémico y posterior cirugía de conversión o citorreducción26-28. En la encuesta se encontró un grupo de cirujanos con la tendencia de realizarla sólo en caso de líquido libre, sin embargo, el procedimiento adecuado implica la aspiración del líquido libre si está presente, asociado a la infusión de 150 a 200 ml de solución salina en ambos recesos parietocólicos y la pelvis, enviando una muestra del receso hepatorrenal y otra de la pelvis, con lo que aumenta el rendimiento del procedimiento en un 23 %27,29,30.
El hallazgo de compromiso peritoneal visible implica siempre biopsia de los implantes, debido a que existen otras lesiones del peritoneo que pueden simular carcinomatosis (tuberculosis, fibrosis, endometriosis peritoneal atípica) y adicionalmente permite el análisis de inmunohistoquimica (HER2), con la opción del uso de terapia dirigida en los pacientes en quienes se confirme un estadio IV. Los hallazgos sugestivos de compromiso secundario peritoneal deben quedar descritos usando el índice de carcinomatosis peritoneal (ICP), el cual permitirá un acercamiento a la carga de enfermedad peritoneal y el seguimiento según sea la conducta para el paciente10,25,31.
Conclusiones
Esta publicación permite obtener un panorama de la situación nacional de los cirujanos frente a la laparoscopia de estadificación en los pacientes con cáncer gástrico, encontrando resultados muy positivos en relación a las indicaciones del procedimiento y algunos aspectos técnicos. Sin embargo, en un país donde el cáncer gástrico es la cuarta causa de cáncer y la primera causa de mortalidad asociada al cáncer, es necesario propender por la estandarización en los procesos de diagnóstico, estadificación y manejo acorde con recomendaciones basadas en la evidencia, por esta razón, como grupo de cirugía gastrointestinal del Instituto Nacional de Cancerología proponemos las siguientes recomendaciones en indicaciones y aspectos técnicos para la laparoscopia de estadificación en los pacientes con cáncer gástrico (Figuras 3 y 4).