Introducción
La fístula enterocutánea se define como una conexión anómala entre el tracto gastrointestinal y la piel. El 75-85 % son de origen iatrogénico, debido a complicaciones quirúrgicas como enterotomías inadvertidas, anastomosis con tensión excesiva o compromiso vascular, o erosión de la pared intestinal por un cuerpo extraño 1. El 15-25 % son causadas por trauma abdominal, condiciones inflamatorias como diverticulitis y apendicitis, neoplasias malignas, isquemia o enfermedad de Crohn; en estos casos pueden ocurrir fístulas entero-entéricas, entero-vesicales y entero-vaginales 2.
Las fallas de índole técnico son debidas a fallas quirúrgicas tales como material de sutura no adecuado y construcción bajo tensión, pero también se deben tener en cuenta factores como la irrigación, la calidad del tejido y la cicatrización deficiente, que a su vez están influenciadas por factores como la edad, la capacidad de oxigenación, el estado nutricional del paciente y la presencia de infección 3.
Clasificación
La clasificación inicial de una fístula se basa en su anatomía y salida de secreción intestinal. La anatomía dicta la nomenclatura y sigue las superficies o lúmenes que están conectados; el nombre comienza con el lugar desde donde se origina la fístula y termina en el órgano adyacente al cual conecta, en este caso, una fístula enterocutánea comienza en el intestino delgado y termina en la piel 4.
Además, se pueden clasificar según distintos aspectos, como su gasto diario de secreción, considerado: alto, producción mayor de 500 ml/día; moderado, de 200-500 ml/día y, bajo, menor de 200 ml/día. Según su localización, se dividen en proximal o distal; según su etiología, en iatrogénica o espontánea 5; de acuerdo con el órgano de origen, también puede clasificarse como tipo 1 (abdominal, gastroduodenal, esofágica), tipo 2 (intestino delgado), tipo 3 (intestino grueso) y tipo 4 (entero-atmosférica, independiente de su origen). Se reconoce una triada clásica de las complicaciones de la fístula enterocutánea que consiste en sepsis, desnutrición y anomalías electrolíticas 6.
Fisiopatología
Después de la pérdida de la continuidad intestinal, el tubo digestivo pasa por tres fases fisiológicas de adaptación 6,7:
1) Fase hipersecretora: esta fase ocurre hasta tres días después de la formación del estoma y puede durar entre 1 y 2 meses. Se caracteriza por pérdidas grandes de volumen.
2) Fase de adaptación: esta fase inicia entre 3-5 días después de la formación del estoma y podría durar hasta 12 meses. Existe disminución del débito de la fístula, pero la velocidad de adaptación depende de las características clínicas del paciente, la gravedad de la enfermedad de base y el segmento intestinal comprometido.
3) Fase de estabilización: Se caracteriza por una mayor disminución de la pérdida de líquidos y electrolitos y la posterior estabilización de la salida de material por el estoma; puede durar hasta dos años.
Epidemiología
Esta enfermedad está asociada con estancias hospitalarias prolongadas y altos costos para el sistema sanitario. La primera serie relevante acerca de fístula enterocutánea en el Hospital General de Massachusetts en 1960, informó una tasa de mortalidad del 44 % 8. Avances recientes basados en el apoyo nutricional, metabólico, cuidado de heridas y mejor técnica quirúrgica, han resultado en disminución de la mortalidad al 5-15 % 9.
Diagnóstico
La mayoría de las fístulas enterocutáneas postoperatorias se identifican en los primeros días y siguen un escenario predecible. Alrededor del quinto día, el paciente presenta fiebre, íleo persistente y aparece un absceso en la herida. Dentro de las 24 horas siguientes, la fístula se hace manifiesta mediante contenido entérico en la herida o los apósitos quirúrgicos 6. El examen físico puede identificar cambios cutáneos, escoriación e irritación; cuanto más proximal es la fístula del intestino delgado, peor será la presentación de la piel a consecuencia de las secreciones gástricas y pancreáticas. El deterioro repentino de los signos vitales, dolor abdominal intenso y signos peritoneales, pueden ser sugestivos de un absceso o fuga intraperitoneal causante de sepsis 10.
Imágenes diagnósticas
La fistulografía con material de contraste hidrosoluble permite identificar la fuente de la fístula, su longitud, trayecto y relación con el intestino, la ausencia o presencia de continuidad intestinal (fístula terminal o lateral), la ausencia o presencia de obstrucción distal, y la ausencia o presencia de una cavidad de absceso en comunicación con la fístula 11.
La tomografía computarizada tiene una especificidad del 97 % y permite detectar colecciones, abscesos, zonas de obstrucción, además de mapear la anatomía 12.
Estado nutricional
La desnutrición es un determinante relevante de los desenlaces clínicos negativos en los pacientes con fístulas enterocutáneas debido a que aumenta el riesgo de resultados adversos como infecciones, sepsis y abscesos intraabdominales. Proporcionar una nutrición óptima, a través de la vías enterales o parenterales, es obligatorio en el abordaje perioperatorio del paciente con una fístula 13.
Existen múltiples factores que contribuyen a la desnutrición en los pacientes con fístulas enterocutáneas. Debido a la fuga de secreciones del intestino delgado, que en situaciones normales serían absorbidas, ocurre una pérdida significativa de líquidos, electrolitos y proteínas (que puede llegar a ser de 75 g/día), lo que sumado a la ingesta calórica inadecuada y al catabolismo relacionado con la sepsis en curso, pueden llevar al síndrome de intestino corto o a una falla intestinal 14,15.
La obtención de los valores de la concentración de proteínas séricas antes y durante la terapia nutricional es un indicador pronóstico de la evolución y un factor importante para la descripción del estado nutricional del paciente; sin embargo, los marcadores nutricionales no son ampliamente utilizados por su baja sensibilidad y especificidad en el diagnóstico de la desnutrición. La evaluación nutricional se debe realizar en el momento en que se hace el diagnóstico de fístula enterocutánea y se recomienda repetirla de forma periódica, por la alta probabilidad de desnutrición en el transcurso de la enfermedad 16,17.
El enfoque “SNAP” (sepsis, nutrición, anatomía y plan), ha sido adaptado ampliamente por diversos equipos quirúrgicos. Se hace énfasis en el control de la sepsis, la optimización del estado nutricional del paciente, la comprensión de la anatomía y la planificación del tratamiento quirúrgico para la fístula. Debido a las alteraciones en la función intestinal de los pacientes sépticos, el apoyo nutricional sólo será efectivo después de controlada la sepsis 18.
El puntaje de control del estado nutricional (CONUT) 19 es una herramienta útil para evaluar los pacientes y hacer un diagnóstico temprano de desnutrición intrahospitalaria. Se calcula a partir de tres parámetros clínicos: albúmina sérica, concentración de colesterol total y recuento total de linfocitos periféricos. Esta escala ha sido utilizada como predictor de severidad y mortalidad en un gran número de condiciones, especialmente cardíacas e intestinales. No se conoce una escala nutricional específica que esté asociada con el cierre de fistulas enterocutáneas, pero se ha documentado que el CONUT es una herramienta eficiente para la detección precoz y el control de la desnutrición en un entorno hospitalario, actuando como indicador para comenzar una intervención nutricional y analizar los efectos terapéuticos. Tiene la ventaja de ser fácil y rápida de aplicar, con un bajo costo 19.
Enfoque terapéutico
Las indicaciones para el manejo nutricional en este tipo de pacientes usualmente se basan en estudios clínicos limitados, de baja evidencia, y normalmente dependen de la experiencia individual e institucional. Los requerimientos de nutrientes específicos, la vía de administración óptima, el papel de la inmunonutrición y el uso de análogos de somatostatina en el tratamiento no están bien definidos 19.
La nutrición parenteral es la piedra angular del apoyo y tratamiento nutricional en estos pacientes, mejorando el estado catabólico y favoreciendo el cierre espontaneo de las fístulas, así como las posibilidades de éxito en caso de manejo quirúrgico 18. La administración de 1500-2000 calorías por día, aumenta el porcentaje de cierre de fístulas y disminuye la mortalidad en comparación con aquellos que reciben menos de 1000 calorías por día 18.
Las guías de la Sociedad Americana de Nutrición Parenteral y Enteral (ASPEN por sus siglas en inglés) y la Federación Latinoamericana de Terapia Nutricional, Nutrición Clínica y Metabolismo (FELANPE) recomiendan proporcionar una ingesta proteica y energética a una tasa de 1,5-2,0 g/kg/día para pacientes adultos con fístula enterocutánea; aquellos pacientes que tengan fístulas de alto gasto pueden requerir hasta 2,5 g/kg/día 15.
En un estudio retrospectivo de 10 años, se encontró que el aumento de la concentración de albúmina sérica posterior al uso de nutrición parenteral estuvo asociado a una disminución importante del gasto por la fístula y a un aumento de la tasa de cierre espontáneo 18,1 veces mayor, en comparación con los pacientes que no tuvieron mejoría en este parámetro 20. En los pacientes con fístulas enterocutáneas con débito menor de 500 ml/día que recibieron nutrición parenteral con aumento de la albúmina sérica, se observó un cierre espontáneo en el 93,3 % de los casos, comparado con una tasa del 70 % de falla de cierre entre los pacientes con bajas concentraciones de albúmina sérica y débito mayor de 500 ml/día 21.
El equilibrio del nitrógeno es un indicador aceptable del estado anabólico, el balance negativo indica que se debe modificar el plan nutricional y el positivo que el paciente está recibiendo las suficientes calorías y se encuentra en una fase anabólica 18,19.
En cuanto a las fórmulas inmunomoduladoras, ningún nutriente como la arginina, los ácidos grasos omega-3 o los nucleótidos han sido evaluados en el contexto de fístula enterocutánea. La glutamina podría contribuir al cierre de la fístula mediante la mejoría del trofismo de la mucosa intestinal y la respuesta inmunológica, pudiendo mejorar la producción de IgA secretora de la mucosa intestinal 22. En un estudio de 28 pacientes adultos con fístula enterocutánea de intestino delgado de alto débito, sin sepsis ni insuficiencia renal o hepática, un grupo recibió glutamina oral (0,3 g/kg/día) y nutrición parenteral y otro únicamente nutrición parenteral, observando menor estancia hospitalaria y mortalidad en el primer grupo 22, sin embargo, son muy pocos los estudios y se condicionan solo a hipótesis 16.
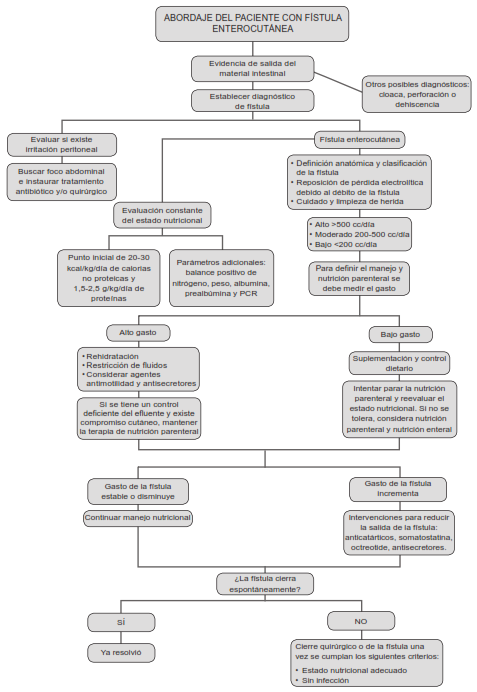
En diferentes ensayos controlados aleatorizados se han evaluado los análogos de la somatostatina para el manejo de las fístulas, observando un efecto favorable al disminuir el volumen de las secreciones gastrointestinales, el tiempo de cierre de la fístula, la duración de la estancia hospitalaria y la necesidad de reintervención. Sin embargo, no se han identificado diferencias entre los fármacos de este grupo 23. En la Figura 1 se esquematiza un abordaje general para el tratamiento de las fistulas enterocutáneas.
La utilización de un sistema de presión negativa favorece la formación de tejido, disminuye el gasto de la fístula, protege la piel y evita los recambios recurrentes de la bolsa. La terapia de cierre asistido por vacío disminuye la mortalidad y las recaídas al reducir el débito de la fístula y conducirla hacia la curación completa. Este tratamiento debe iniciarse de manera gradual, evaluando las presiones para evitar el riesgo de isquemia de los tejidos y el desarrollo de fístulas. Los pegamentos biológicos de fibrina están indicados cuando el paciente presenta una fistula de mediano o bajo gasto y la cirugía no es una opción terapéutica 24.
Tratamiento quirúrgico
Una vez resuelto el estado séptico, hasta el 90 % de las fístulas pueden cerrar durante el primer mes, con un cierre adicional del 10 % en el segundo mes, y muy pocas probabilidades de cierre después de este tiempo 25. En los pacientes con fístulas que no cierran espontáneamente después de tres meses de un adecuado tratamiento médico, está indicado el abordaje quirúrgico, una vez que el paciente recupere su estado nutricional y no presente respuesta inflamatoria, por esto, los pacientes con fístulas enterocutáneas pueden requerir un manejo médico a largo plazo, con nutrición enteral o parenteral, monitoreo de líquidos y electrolitos, y cuidado conjunto con la unidad de clínica de heridas complejas, mientras se consiguen las condiciones óptimas para la intervención quirúrgica 16.
El objetivo de la cirugía en pacientes con fístulas enterocutáneas es recuperar la funcionalidad de todo el tracto intestinal mediante una resección de la fístula y el intestino comprometido, con anastomosis termino-terminal y cierre seguro de la pared abdominal. Para facilitar la alimentación temprana y la descompresión del intestino proximal, en algunos pacientes seleccionados puede estar indicada una gastrostomía, ileostomía de derivación o yeyunostomía 26.
El cierre de la pared abdominal es un desafío por los defectos cutáneos y una mayor probabilidad de contaminación de la herida; las complicaciones de la herida pueden dar lugar a fístulas enterocutáneas nuevas o recurrentes 26. Se ha informado una probabilidad cuatro veces más alta de recurrencia en pacientes en quienes la anastomosis se realizó con sutura mecánica 27. Una vez resecada la fistula, es importante el examen histopatológico para descartar procesos neoplásicos malignos 28.
Conclusiones
El manejo de las fístulas enterocutáneas es un problema complejo en cirugía abdominal y colorrectal, que requiere un tratamiento multidisciplinario basado en la reanimación con líquidos, el control de la sepsis, el estado nutricional y el cuidado de la herida. Un diagnóstico temprano y un tratamiento precoz e individualizado impacta de manera benéfica en el pronóstico de los pacientes, que de lo contrario puede llevar a complicaciones adicionales e incluso a la muerte.