Introducción
Los músculos papilares del ventrículo izquierdo (MP-VI) son unas estructuras anatómicas complejas, que, en ocasiones, pueden ser causa de taquicardia ventricular o extrasístoles ventriculares frecuentes1. Desde el punto de vista técnico, es una zona de difícil acceso para la ablación exitosa; incluso, es un reto al comparar con otras zonas del ventrículo izquierdo. Se ha descrito que los MP-VI muestran morfologías del QRS variables preablación y posablación, con probable conducción anisotrópica ya que tienen cadenas miocárdicas separadas basal y apical; esto dificulta encontrar el punto de ablación exitoso, considerando que la arritmia ventricular de los músculos papilares proviene del miocardio y no del endocardio o red Purkinje. La condición antes descrita hace que se requiera mayor profundidad y estabilidad del catéter, y que, por tanto, haya, mayor riesgo de recidiva e incluso complicaciones del procedimiento, como perforación o disfunción de la válvula mitral, y en ocasiones mayor tiempo de procedimiento cuando se utiliza radiofrecuencia2.
La crioablación es una técnica relativamente nueva que consiste en una sonda rígida, puntiaguda, y que con nitrógeno líquido alcanza temperaturas negativas de -160°3. Logra mejor adherencia y estabilidad del catéter al pasar los -80° por lo que se ha informado que es segura y efectiva para el tratamiento de las arritmias cardiacas (taquicardia ventricular, fibrilación auricular), así como también es una alternativa a la ablación con radiofrecuencia2.
Caso clínico
Paciente de sexo masculino, de 19 años de edad, con antecedente de dos ablaciones en 2014 y 2016, respectivamente, por vía accesoria posterolateral izquierda en relación a taquicardia ortodrómica por vía accesoria oculta. Desde hace varios meses refiere palpitaciones diarias, disnea clase funcional III/IV con deterioro progresivo de la misma, y varios episodios de presíncope y uno de síncope. En electrocardiograma Holter de 24 horas se documentaron extrasístoles ventriculares muy frecuentes (30 533 ectopias ventriculares con carga del 31%) con episodios de bigeminismo y trigeminismo; extrasístole con morfología de bloqueo de rama derecha, eje superior, S profunda en V6 con origen en el músculo papilar anterolateral (Fig. 1).
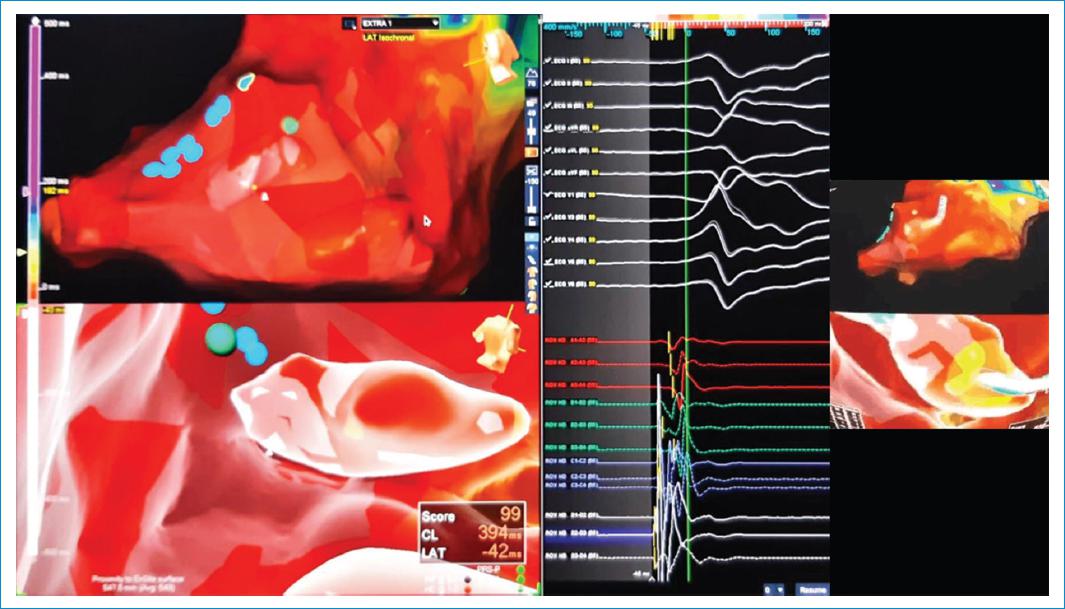
Figura 1 A la izquierda se identifica la reconstrucción anatómica tridimensional del músculo papilar anterolateral. En el centro de la imagen se aprecia la morfología de la extrasístole, así como la concordancia de la morfología (99%) al realizar el mapeo sobre dicha estructura, y a la derecha la posición del catéter durante crioablación.
Procedimiento - Crioablación
Bajo visión de ecografía intracardiaca y previa aplicación de dos bolos de heparina, manteniendo ACT 300-350, se realizó punción transeptal con camisa Agilis®. Se pasó un catéter HD Grid® (EnSite Velocity and Precision, St. Jude Medical Inc.), se obtuvo mapa anatómico y mapa de activación de alta densidad del ventrículo izquierdo (10 500 puntos de activación) con catéter HD Grid® (EnSite Velocity and Precision, St. Jude Medical Inc.) observando zona de mayor preactivación en la base del músculo papilar anterolateral (Fig. 1). Se intercambió el catéter de mapeo por catéter de ablación Freezor® MAX (Medtronic), para lo cual se realizaron seis aplicaciones de 240 segundos y se alcanzaron temperaturas de hasta -75 °C, desapareciendo la extrasístole ventricular.
La crioenergía se administró en sitios miocárdicos que exhibían la actividad bipolar más temprana o el patrón de QS unipolar local o en una red de Purkinje con una actividad temprana anterior al inicio de QRS.
El punto final de la ablación con catéter fue la eliminación y la no inducibilidad de los AV durante la infusión de isoproterenol (2 a 10 mg/min) y con la estimulación en ráfagas desde el ventrículo derecho hasta una duración del ciclo tan corta como 300 ms. El éxito del procedimiento se definió como la abolición de la arritmia ventricular inducible o espontánea.
En el seguimiento al mes posterior en consulta externa, se observó mejoría de los síntomas, y ausencia de palpitaciones, síncope y extrasístoles ventriculares.
Discusión
Las arritmias ventriculares (AV) son alteraciones de la conducción cardiaca que van desde el complejo ventricular prematuro, hasta la taquicardia ventricular sostenida o no sostenida y la fibrilación ventricular. Estas arritmias pueden ser silentes o sintomáticas (palpitaciones o deterioro de la clase funcional); pudiendo incluso presentarse en el contexto de una parada cardiorrespiratoria. En cuanto al pronóstico, existen diferentes marcadores clínicos y paraclínicos que se correlacionan con eventos adversos a largo plazo, en los que la edad, el antecedente de muerte súbita familiar, mutaciones específicas, así como las características de la arritmia en holter-electrocardiograma figuran como los factores más importantes4.
Estas arritmias ventriculares pueden originarse en múltiples estructuras; las del músculo papilar anterolateral se caracterizan por tener en el electrocardiograma discordancia inferior (DII negativa y DIII positiva, característica de estructuras mediocavitarias) con morfología en V1 de bloqueo de rama derecha, R menor de S en V5, así como patrón de R, Rsr o qR en V15,6.
La indicación de ablación con catéter para la arritmia ventricular refleja el análisis de la severidad de los síntomas, la afección de la arritmia en la función del ventrículo izquierdo, la presencia de un sustrato para la misma y la anticipación (o concurrencia) de los efectos adversos de la terapia médica antiarrítmica1. La ablación en los músculos papilares es un reto terapéutico ya que estas estructuras tienen amplia variabilidad anatómica y movimiento significativo durante el ciclo cardiaco7. Se reconoce que la tasa de éxito agudo y de recurrencia es mayor en las arritmias ventriculares originadas en los músculos papilares cuando se comparan con otros sitios8.
Se propone la crioablación como una estrategia terapéutica superior a la radiofrecuencia para el manejo de estas arritmias9,10. Una de las características determinantes en el éxito de la ablación es el mantenimiento de la estabilidad del catéter durante la aplicación, condición que es difícil de conseguir bajo esta modalidad; además, el cambio de morfología durante la aplicación (cambio en la salida de la AV) puede invitar a realizar aplicaciones de radiofrecuencia en sitios opuestos al lugar inicial de ablación, peculiaridades que pueden convertir en un verdadero reto la aproximación terapéutica por dicho método.
En 2016, Rivera et al.11 compararon el rendimiento de la ablación por radiofrecuencia vs. la crioablación, e identificaron mayor tasa de éxito agudo (100% crioablación vs. 78% radiofrecuencia), mejor estabilidad (100% crioablación vs. 25% radiofrecuencia), así como menor recurrencia a seis meses de seguimiento (0% crioablación vs. 44 % radiofrecuencia). Estos datos concuerdan con el comportamiento clínico descrito en el caso que se expone.
Gordo et al.12 reportaron la experiencia del tratamiento de AV originadas en los músculos papilares luego de falla en la ablación por catéter, y obtuvieron un éxito cercano al 100% haciendo mención a una desventaja de la crioablación, que es la menor capacidad relativa de maniobrabilidad con el cateter, y, además, se presentó una disección aórtica aguda como única complicación.
El mapeo de alta resolución (HD Grid Mapping Catheter)13 utilizado en nuestro caso, fue de vital importancia para realizar una confirmación rápida de la participación del músculo papilar anterolateral en el origen de la arritmia teniendo en cuenta la característica móvil de esta estructura. Como complemento de la aproximación multimodal se usó la ecocardiografía intracardiaca, que permitió realizar un adecuado posicionamiento de los catéteres (mapeo y ablación), verificando así la estabilidad durante la crioablación. Otra utilidad es la rápida detección de complicaciones.
En los últimos años ha tomado gran auge la crioablación que permite mayor estabilidad del catéter, adherencia y éxito en el manejo de la AV. En la literatura se reporta como una técnica factible, que, incluso, guiada por ecocardiograma intracardiaco sin mapeo 3D, es efectiva. En nuestro caso se utilizaron las dos formas como guía que permiten brindarle al paciente y al médico mayor seguridad e incluso mejores resultados en una estructura anatómica compleja, como lo es el músculo papilar9. Se reporta el primer caso en Colombia de crioablación exitosa, de una AV originada en el músculo papilar anterolateral, apoyándose con mapeo de alta resolución y ecocardiografía intracardiaca.














