Introducción
Los carbonatos de calcio de diferentes morfologías y tamaños han despertado el interés de muchos investigadores en los últimos años, puesto que han demostrado excelentes propiedades que han impactado la industria biomédica. Ejemplos de esto puede ser sensores ópticos y electrónicos, la catálisis, dispositivos para almacenamiento de energía, pigmentos magnéticos, entre otros (Sung et al., 2005; Zhang et al., 2008). El carbonato de calcio (CaCO3) es uno de los minerales que puede formar compuestos híbridos orgánicos/inorgánicos con estructura y propiedades controladas. Dichas propiedades pueden ser la estructura del cristal, el tamaño de la partícula y la morfología del mineral. La característica morfológica es la que puede establecer la propiedad de la partícula, definiendo así también su aplicación (Stocks-Fischer et al., 1999).
En la biosíntesis de carbonato de calcio, algunos de los microorganismos más conocidos pertenecen al género Bacillus spp. (Bachmeier et al., 2002; Dupraz et al., 2009). Se ha documentado el impacto de estos microorganismos en diversos procesos geológicos, evaluando su potencial para precipitar vaterita o calcita (Mitchell et al., 2013; Sung et. al, 2005; Zhang et al., 2008). Lo anterior, da pie a pensar en aplicar los mecanismos de mineralización bacteriana en procesos a nivel industrial, debido a que es un proceso innovador el cual se puede ejecutar bajo condiciones ambientales (Daskalakis et al., 2015; Montoya et al., 2005; Singh et al., 2016).
Varios estudios han mostrado el impacto de ciertos parámetros sobre la cristalización de carbonatos de calcio y el control de la morfología (incluyendo la estructura, tamaño y forma), lo cual es importante pues cada vez se buscan partículas uniformes y de tamaños micro o nanométricos (Henderson et al., 2008; Wada et al., 2001). Los mecanismos de biomineralización pueden ser afectados por factores como la sobresaturación de iones de calcio, la disponibilidad de nutrientes o fuentes de energía bacteriana en el medio de cultivo (carbono, nitrógeno, oxígeno disuelto, minerales, entre otros) y la relación estequiométrica entre ellos, el pH, la temperatura (Bachmeier et al., 2002; Dupraz et al., 2009; Mitchell et al., 2013). Por lo tanto, este proceso puede ser manipulado de varias formas. Una de ellas es el uso de aditivos como el Tween® 80, tensoactivo que actúa sobre la mineralización del carbonato de calcio, controlando su morfología cristalina.
El polioxietileno-80-sorbitán monooleato (Tween® 80) se ha reconocido como un desaglomerante en procesos de síntesis química, físicos y biológicos. influyendo sobre la morfología de las partículas de carbonato de calcio más reducidas y uniformes, al actuar sobre planos cristalinos específicos del mineral, inhibiendo el crecimiento en esas zonas, sin afectar la reacción de precipitación (Sung et al., 2005; Zhang et al., 2008).
Con base en lo anterior, en este estudio se evaluó qué efecto tiene el Tween® 80 a tres concentraciones: 0.00% p/v, 0.25% p/v y 0.50% p/v, sobre la bioprecipitación de carbonato de calcio, empleando una cepa de Bacillus cereus. De antemano, se tuvo presente que este compuesto no inhibe el crecimiento bacteriano e incluso puede contribuir a que las células presenten una mayor estabilidad térmica de las enzimas dentro de este microorganismo (Evans & Abdullah, 2012; Nakahara et al., 1979). Se emplearon técnicas de caracterización mineralógica con el fin de confirmar los cambios morfológicos y el tipo de mineral obtenido.
Materiales y métodos
Microrganismo
Se utilizó una cepa de Bacillus cereus U1/UPB, aislada de material terroso procedente de los jardines de la Universidad Pontificia Bolivariana (Medellín, Colombia) y conservada en el Cepario del Laboratorio de Biofenix S.A.S. Se identificó molecularmente por el Laboratorio del Centro Nacional de Secuenciación Genómica (CNSG) de la Universidad de Antioquía, utilizando la técnica molecular de reacción en cadena de la polimerasa (PCR). Se realizó la extracción de ADN y la amplificación del gen 16S, la secuenciación del gen 16S y el análisis filogenético. La cepa tuvo una adaptación previa al proceso de biomineralización de carbonato de calcio al medio M3 modificado (0.50% de acetato de calcio y 0.40% de triptona), en varias etapas consecutivas, con duración de 6 días cada una, hasta no observar variaciones entre réplicas, respecto a valores como pH y la cantidad de precipitado generado.
Los inóculos para cada cultivo bacteriano a diferentes concentraciones en peso de Tween® 80 (0.00%, 0.25% y 0.50%) se prepararon en Erlenmeyer de 250 mL, usando un volumen de trabajo de 100 mL y una relación de 1 mL de inóculo bacteriano por cada 9 mL de medio M3 modificado (con la respectiva concentración de Tween® 80 evaluada). Las cepas se incubaron por 6 días en un agitador orbital, a una temperatura de 30°C ± 1°C y una velocidad de agitación de 180 rpm ± 2 rpm.
Ensayos de bioprecipitación de carbonato de calcio
Cada ensayo fue preparado en Erlenmeyer de 250 mL, con un volumen de trabajo de 100 mL y una relación de 1 mL de inóculo bacteriano por cada 9 mL de medio de cultivo M3 modificado, variando la concentración de Tween® 80 (porcentajes en peso): 0.00%, 0.25% y 0.50%. Cada ensayo tuvo su respectiva réplica y control abiótico (sin presencia de microorganismos). Todos los experimentos fueron incubados por 6 días a las mismas condiciones de temperatura y agitación utilizadas en la preparación de los inóculos.
Los experimentos se monitorizaron con mediciones de pH, utilizando un pH-metro HACH HQ 30d. Al finalizar cada ensayo, se calculó la cantidad de precipitado producido, para lo cual se tomó 80 mL de cada erlenmeyer y se centrifugó a 3500 rpm por 10 minutos. Pasado ese tiempo, se descartó el sobrenadante y el precipitado se lavó 4 veces con agua destilada y 4 más con alcohol al 90%, agitando en vórtex por 1 minuto y nuevamente centrifugando a 3500 rpm. Posteriormente, se secaba la muestra a temperatura ambiente. El producto final se utilizó para determinar la cantidad de precipitado formado por litro de medio, dividiendo el peso obtenido sobre el volumen inicial empleado.
Análisis mineralógicos
Se estableció la composición mineralógica de las muestras mediante difracción de rayos X (XRD), análisis por espectroscopia de infrarrojo por Transformada de Fourier (FTIR) y microscopía electrónica de barrido (SEM). Para todos los análisis, se utilizaron las muestras sin someterse a ningún proceso de tamizaje, ni se utilizó alguna mezcla en polvo para la purificación del precipitado. Tampoco se usó ninguna transformación de tamaño de partícula.
Para XRD, el precipitado se analizó en un difractómetro marca Rigaku Miniflex II, con radiación K(, mediante el método paso a paso, en el intervalo 2θ entre 5° y 70°, tamaño del paso de 0.05°, con un tiempo de conteo de 50 segundos. Los minerales presentes en el precipitado fueron cuantificados mediante refinamiento de Rietveld, cuyas simulaciones y cálculos se llevaron a cabo en el programa X’Pert HighScore Plus©, las bases de datos PDF-4-2012 y American Mineralogist Crystal Structure Database (Downs & Hall-Wallace, 2003). Los análisis de FTIR se hicieron en un espectrómetro marca Thermo Scientific Nicolet, utilizando el modo ATR con la muestra pura, con un intervalo de número de onda entre 400 cm-1 y 4000 cm-1 y 32 barridos, a una resolución espectral de 4 cm-1. En el caso de SEM, la muestra fue recubierta con una fina capa de plata. La técnica de recubrimiento “sputtering” o pulverización catódica se realizó con un equipo DENTON VACUUM DESK IV. El análisis se hizo en un microscopio electrónico de barrido marca JEOL JSM-6490LV, con un voltaje de 20 kV. Adicionalmente, se utilizó una microsonda de Rayos X - EDS, referencia INCA PentaFETx3 Oxford Instruments, para hacer los análisis microquímicos de la muestra.
Resultados
Ensayos de bioprecipitación de carbonato de calcio
La figura 1 muestra el comportamiento del pH para todos los ensayos. En general, se evidenció un aumento en los valores de pH por encima de 8.9. El ensayo sin adición de Tween® 80 mostró un incremento continuo en los valores de pH, en contraste a los ensayos con Tween® 80 que no presentaron una variación significativa entre los días 1 y 2 de proceso. No obstante, todos los ensayos presentaron una tendencia similar en los días siguientes, indicando que hubo crecimiento bacteriano en todos los experimentos. Por otra parte, los controles negativos, no evidenciaron cambios en los valores del pH, manteniendo el mismo valor inicial durante todo el proceso (datos no mostrados).

Figura 1 pH vs. tiempo durante el proceso de bioprecipitación de calcio a diferentes concentraciones de Tween® 80.
La figura 2 muestra la cantidad de carbonato de calcio sintetizado por la cepa Bacillus cereus. El ensayo sin adición del surfactante (0.00%) mostró mayor precipitación (3.23 g/L), en comparación a los demás ensayos, los cuales obtuvieron una producción similar, alrededor de 2.90 g/L.

Figura 2 Bioprecipitado de carbonato de calcio sintetizado por Bacillus cereus, empleando las concentraciones de Tween® 80 (0.00%,0.25%,0.50%).
Análisis mineralógicos
La figura 3 muestra los difractogramas de rayos X para los precipitados obtenidos en los ensayos. Todos evidenciaron picos asociados a vaterita y calcita. No obstante, el ensayo con Tween® 80 al 0.50% mostró mayor intensidad en los picos asociados a vaterita y casi no se evidenciaron picos asociados a calcita.
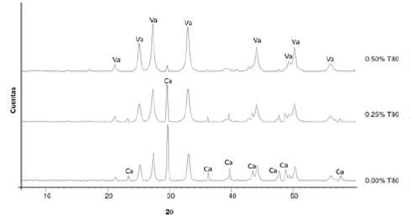
Figura 3 Difractogramas de los precipitados para cada ensayo a diferentes concentraciones de Tween® 80. Va: Vaterita, Ca: Calcita.
Mediante el refinamiento Rietveld de los difractogramas, la tabla 1 constata las proporciones semicuantitativas de las fases cristalinas de vaterita y calcita en todos los precipitados, con un perfil residual ponderado (weighted residual profile: Rwp) por debajo del 10%, el cual no difería más del 20% respecto al perfil residual esperado (residual expected: Rexp). Estos parámetros determinaron que los modelos de refinamiento fueron buenos para aceptar los valores obtenidos (Kniess et al., 2012; McCusker et al., 2011). La proporción de calcita fue menor, en la medida que incrementaba la concentración de Tween® 80, disminuyendo a la mitad al emplear 0.25%, mientras que con una concentración de 0.50%, el porcentaje de calcita fue de 1.6%.
Tabla 1 Porcentaje de calcita y vaterita en fase cristalina de los precipitados obtenidos en los ensayos a diferentes concentraciones de Tween® 80.

La figura 4 muestra los espectros de FTIR para todos los precipitados y la tabla 2 muestra la identificación de las bandas y su respectiva asignación (Daskalakis et al., 2015; DePaula et al., 2013; Montoya et al., 2005; Patil et al., 2014; Saikia & Das, 2014; Sevcík et al., 2015; Silverstein et al., 2014; Singh et al., 2016; Trushina et al., 2015; Wang et al., 2016; Wang et al., 2013; Zhou et al., 2010). Se corroboró la presencia de calcita y vaterita en todos los precipitados. La banda a 713 cm-1 indica la presencia de calcita en los ensayos 0.00% T80 y 0.25% T80, siendo el ensayo sin adición de Tween® 80 donde se presentó en mayor intensidad. La banda a 1087 cm-1, asociada a vaterita, se muestra con mayor amplitud en los ensayos con Tween® 80, probablemente asociado a la mayor concentración de este polimorfo en dichos ensayos. La banda a 1707 cm-1 hace referencia a vestigios de materia orgánica, posiblemente proveniente de alguno de los compuestos del medio de cultivo o de alguno de los productos del metabolismo de los microorganismos. La banda a 1648-1653 cm-1 revela la presencia de humedad natural o alguna pequeña fracción de carbonato hidratado y la banda a 3282-3287 cm-1 indica las interacciones O-H, probablemente correspondientes al alcohol remanente de la etapa de lavado o a absorción de humedad, cuando se secó a temperatura ambiente.

Figura 4 Espectros de FTIR de los precipitados para cada ensayo a diferentes concentraciones de Tween® 80.
Tabla 2 Bandas de los espectros de FTIR de los precipitados obtenidos en los ensayos a diferentes concentraciones de Tween® 80.

*Los ensayos tienen solo una banda que está entre estos valores, los cuales representan una misma asignación.
La figura 5 muestra las imágenes obtenidas a partir de microscopía electrónica de barrido. El ensayo sin adición de Tween® 80 presentó formaciones de carbonato de calcio tipo corazas huecas, biomineralizadas a partir de la morfología bacilar de las bacterias. En contraste, en los ensayos con adición de Tween® 80 se observó disgregación o desaglomeración de estas estructuras (figuras 5b y 5c), así como películas de carbonato de calcio depositadas (figuras 5d y 5e). Sin embargo, la figura 5f indica que algunas de las corazas todavía se mantuvieron definidas y además se evidenciaron partículas esféricas, relacionadas con la vaterita (figura 5f).

Figura 5 Imágenes de SEM de precipitados para ensayos a diferentes concentraciones de Tween® 80. (a) 0% Tween® 80, (b) 0.25% de Tween® 80, recubrimientos biomineralizados aglomerados, (c) 0.25% de Tween® 80, corazas biomineralizadas y partículas esféricas de vaterita, (d) 0.25% de Tween® 80, películas de carbonato aglomeradas, (e) 0.50% de Tween® 80, películas de carbonato aglomeradas y (f) 0.50% de Tween® 80, recubrimientos biomineralizados definidos.
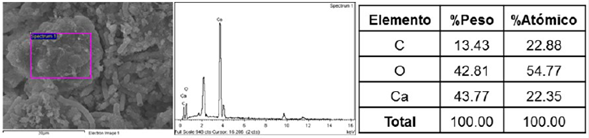
A partir de los análisis de SEM, se hicieron análisis microquímicos sobre las estructuras de carbonato de calcio obtenidas en los ensayos. La figura 6 hace referencia a los precipitados obtenidos en los ensayos sin adición de Tween® 80. Al compararse con las relaciones atómicas ideales de carbonato de calcio (20% Ca: 20% C: 60% O), da indicio de que dichas partículas, o sus alrededores, presentan componentes de materia orgánica, posiblemente proveniente de algunos compuestos precipitados, producto de los mecanismos de reacción del microorganismo o vestigios de las bacterias que estaban dentro de las estructuras.

Figura 6 Análisis microquímico sobre partículas que recubren los recubrimientos de los microorganismos biomineralizados (0.00% Tween® 80).
La figura 7 muestra el análisis microquímico realizado sobre una película de carbonato formada en el ensayo en el cual se adiciono 0.25% de Tween® 80. La proporción atómica entre el calcio y el carbonato es aproximadamente de 1:1, denotando que se obtuvieron partículas de mayor pureza, que las obtenidas en el ensayo sin adición de Tween® 80 (figura 6).
Discusión
Es importante señalar que la medición de pH muestra de manera indirecta el crecimiento celular en este proceso en particular y permite dar a entender de forma cualitativa cómo los microorgansimos actúan dentro del proceso. El aumento en los valores de pH (figura 1) puede ser explicado por el CO2, que se produce a partir de la amonificación generada por la actividad metabólica microbiana, lo cual alcaliniza el medio y contribuye a la cementación de carbonato de calcio (figura 2), en presencia de la sal de acetato (Liang et al., 2013). Por otra parte, la tendencia a estabilizar este valor, en los últimos días de proceso, podría deberse a un agotamiento de la fuente de carbono (triptona) y los iones de calcio (acetato de calcio) disponibles en el medio y necesarios para que se dé la respiración celular (Stocks-Fischer, Galinat, & Bang, 1999; Wong, 2015).
Los recubrimientos biomineralizados de carbonato de calcio (figura 5) se pudieron generar a partir de la interacción estequiométrica de los iones Ca2+ del medio con grupos CO3 2- cargados, presentes en la membrana externa de la bacteria, permitiendo la deposición mineral y generando paredes bacilares (figuras 5 y 6) (Douglas & Beveridge, 1998; Komala & Khun, 2013). Después de la precipitación, la segunda etapa implicaría el aumento de la concentración de carbonato de calcio y la saturación de la superficie celular, generando una aglomeración y precipitación fuera de la célula (figura 7), la cual no es controlada por el microorganismo, sino por el ambiente físico-químico de la superficie, alrededor de cada bacteria (Douglas & Beveridge, 1998).
Teniendo en cuenta los resultados de EDS (figuras 6 y 7), el mayor valor de precipitado en el ensayo sin adición de Tween® 80 (figura 2), podría estar relacionado con una porción de materia orgánica que precipitó junto al carbonato, la cual pudo provenir de algún subproducto del medio. Sin embargo, con base en las investigaciones preliminares, relacionadas con la cristalización de carbonato de calcio bajo diferentes condiciones, este hecho también pudo estar relacionado con la propagación y metabolismo del microorganismo que favorece la síntesis del mineral de interés, ya que, al no tener agregado el Tween® 80, este podría segregar metabolitos que acelerarían la hidratación de CO2, regulando las concentraciones de CO2 y HCO3 - y modificando el pH del medio (Matahwa et al., 2008; Parks, 2009; Stocks-Fischer et al., 1999).
Aunque los ensayos con adición de Tween® 80 presentaron alrededor de 10% menos peso de precipitados que el ensayo sin el aditivo (figura 2), la morfología y el tamaño de partícula obtenido fue diferente (figura 5), así como se pudo evidenciar un producto de mayor pureza (figura 7). El Tween® 80 es un aditivo alimentario con acción detergente emulsionante, el cual pudo actuar como un agente dispersante en el proceso de producción de carbonato de calcio, contribuyendo a disgregar cúmulos o las estructuras biomineralizadas de los microorganismos. En investigaciones sobre síntesis química de calcita, se ha encontrado que este tensoactivo no iónico tiene un efecto significativo sobre la morfología de los cristales, ya que se adsorbe y forma enlaces con una cara cristalina específica, inhibiendo el crecimiento del mineral en esa zona, pero sin afectar la reacción entre los iones Ca2+ y el CO3 2- hidratado, lo cual solo induciría a un cambio de la forma, pero no del producto (Patil et al., 2014; Zhang et al., 2008).
En cuanto a las variaciones de las proporciones de vaterita y calcita, observadas en los análisis de XRD (tabla 1), estas contrastan con los resultados obtenidos en procesos de síntesis química, donde se ha evidenciado que la inclusión de Tween® 80 solo promueve una leve formación de vaterita (con predominio de calcita) y, además, este polimorfo tendería a desparecer y transformarse en calcita (Patil et al., 2014).
La estabilidad de la biovaterita podría explicarse por el efecto de los microorganismos sobre la formación de carbonato, gracias a la producción de biomoléculas por la pared celular de las bacterias, donde compuestos iónicos de fósforo, grupos carboxílicos o polisacáridos presentes en ella juegan un papel importante en coordinar la orientación del calcio y el carbonato (Daskalakis et al., 2015).
De acuerdo con los resultados obtenidos, fue posible evidenciar la formación de carbonatos de calcio en todos los experimentos, independiente de la concentración de Tween® 80 empleada. Esto indica posiblemente que las células pueden crecer, desarrollarse y formar carbonatos de calcio de manera tal que este aditivo no es un inhibidor celular, por lo menos a las concentraciones evaluadas en este estudio. Adicionalmente, este tensoactivo pudo incrementar el rendimiento en la formación de los compuestos necesarios para la estabilización de la vaterita, sin afectar la síntesis bioquímica de la bacteria, obteniéndose una biomineralización de carbonatos de mejor calidad con una morfología controlada, reducida y uniforme, ya que los análisis de FTIR (figura 4) y EDS (figura 7) mostraron presencia poco significativa de componentes adsorbidos sobre el precipitado, diferentes al carbonato de calcio (Dupraz et al., 2009; Evans & Abdullah, 2012; Weiner & Dove, 2003).
Conclusiones
El proceso de biomineralización de carbonato de calcio mediado por Bacillus cereus, permite, en su mayoría, la formación de estructuras en forma de coraza con morfología bacilar y centro hueco, las cuales se componen de partículas de carbonato de calcio (vaterita-calcita). No obstante, incluir el tensoactivo Tween® 80 en el medio de cultivo puede ayudar a disgregar dichas formaciones, en el caso que se consideren indeseables en algún tipo de proceso específico, actuando además como agente de dispersión, en procesos que puedan ser ejecutados comercialmente, ayudando a la formación de partículas de menor tamaño y de mejor calidad.
Aunque los microorganismos utilizados en este proyecto tuvieron mayor tendencia a formar partículas de carbonato de calcio en forma de vaterita, siempre existe un porcentaje de calcita en el precipitado final. Sin embargo, el Tween® 80 contribuyó a incrementar la proporción de biovaterita, indicando su capacidad de modificar algunas condiciones del bioproceso que favorezcan este fenómeno. Futuras investigaciones podrían centrarse en evaluar qué parte del proceso es la que afecta el surfactante, por ejemplo, su efecto sobre las enzimas que forman los subproductos que ayudan a estabilizar la proporción de vaterita.
Cabe señalar que la vaterita es de gran importancia dentro del área de la medicina, ya que tiene muchas aplicaciones dentro de la industria biomédica, en la preparación de drogas y cosmética, siendo apreciado por sus propiedades cristalinas particulares. De acuerdo a las concentraciones de Tween® 80 evaluadas, puesto que con 0.50% se obtuvo un 98% de biovaterita, una concentración ligeramente superior podría ser suficiente para obtener un mineral de mayor pureza.