Caso clínico
Paciente femenina de 63 años, procedente de la zona rural del departamento de Risaralda, con antecedentes de HTA, cirrosis en estudio y reemplazo articular de rodilla derecha ocho meses antes del inicio del cuadro. Se encontraba en tratamiento con: Propanolol, Enalapril, Espironolactona, Furosemida y Atorvastatina. Ella presenta un cuadro clínico de aproximadamente tres días de evolución de edema en miembros inferiores de predominio derecho, asociado a sintomatología general. Consultó inicialmente la unidad local de salud donde se encuentra que tiene tendencia a la hipotensión; también presenta desaturación, con oliguria y episodios de hipoglicemia. Ante sospecha de choque de origen a esclarecer, se decide trasladarla al centro de referencia del municipio de Pereira, donde se realizan estudios en los que se evidencian hemograma con leucocitosis, neutrofilia y trombocitopenia, función hepática con hiperbilirrubinemia a expensas de la bilirrubina directa y transaminasas con leve aumento. Se sospecha choque séptico secundario a posible proceso infeccioso en la rodilla derecha, por lo que se inicia manejo con terapia antibiótica de amplio espectro, posterior a toma de hemocultivos en la unidad de cuidados intensivos. La paciente inicia deterioro clínico: presenta encefalopatía hepática, empeoramiento de la función renal y hepática, y la aparición de ascitis. Se sospecha síndrome hepatorrenal por lo que se inicia tratamiento para el mismo. Posteriormente presenta coagulopatía y trombocitopenia severa, requiriendo múltiples transfusiones de plasma fresco congelado y aféresis de plaquetas. Por parte del servicio de ortopedia se descarta un foco séptico en su rodilla; se continúan estudios que revelan una trombosis venosa de miembro inferior derecho, pero no es posible el inicio de la anticoagulación pues la paciente a este punto presenta coagulopatía. Además, se realizan hemocultivos que dan positivo para Staphylococcus Aureus sensible a la meticilina, por lo que se ajusta a terapia antibiótica. Inicia con choque refractario a pesar de un manejo medico optimo y fallece tras 15 días de estancia hospitalaria en la unidad de cuidados intensivos.
Introducción
La falla hepática aguda sobre crónica (ACLF) es una patología cada vez más reconocida, caracterizada por un deterioro agudo de la función hepática en pacientes con cirrosis de base, generalmente asociado a un factor desencadenante, el cual puede ser tanto hepático (como el caso de reactivación de una hepatitis viral) o extrahepático (en casos de infecciones bacterianas o incluso alcoholismo). Aunque su fisiopatología exacta aún no está completamente clara, se cree que la respuesta inflamatoria no regulada es un factor que contribuye de manera importante al desarrollo de la enfermedad (1).
En 2009, (2) definió por primera vez la ACLF como: “un insulto hepático agudo manifestado en forma de ictericia (Bilirrubina ≥5mg/dL) y coagulopatía (INR ≥1,5), complicado en el plazo de cuatro semanas con ascitis o encefalopatía”.
En el 2012, el estudio CANONIC, realizado por el European Association for the Study of the Liver - Chronic Liver Failure (EASL-CLIF) consortium, un estudio de cohorte que incluyo 1.343 pacientes con cirrosis hepática ingresados en 29 unidades especializadas en patología hepática, definió la falla hepática sobre crónica teniendo en cuenta la descompensación aguda (definida por encefalopatía, ascitis, sangrado del tracto gastrointestinal o infección bacteriana) que desarrolla una disfunción orgánica de acuerdo con los criterios del CLIF-SOFA (tabla 1), una versión modificada del índice Sequential Organ Failure Assessment score (SOFA). Se demostró que los pacientes que cumplían con dichos criterios tenían un pronóstico diferente a los pacientes con cirrosis descompensada (4).
La disfunción renal es una complicación, una condición grave y de frecuente aparición en pacientes con disfunción hepática, la cual puede ser de aparición aguda o tener un curso crónico. Los pacientes en quienes coexisten estas dos condiciones habitualmente presentan hipertensión portal secundaria a cirrosis, hepatitis alcohólica grave o patología neoplásica hepática, aunque también puede presentarse en insuficiencia hepática fulminante. La importancia de esta condición radica en que su aparición supone un pronóstico ominoso para el paciente (27).
En 2007, el club internacional de la ascitis (ICA) realizó el primer consenso, en el que clasificó el síndrome hepatorrenal (SHR) en tipo 1 y tipo 2 (SHR-1 y SHR-2). El SHR tipo 1 se caracteriza por un deterioro rápido en la función renal, el cual generalmente aparece posterior a un evento precipitante. Por su parte, en el SHR tipo 2 se presenta como una disfunción renal moderada de progresión lenta, la cual a menudo ocurre sin identificarse un precipitante evidente. Clínicamente, el SHR-1 se caracteriza por la insuficiencia renal aguda, mientras que el SHR-2 es más caracterizado por la ascitis refractaria (28).
En una nueva reunión de consenso en el 2012, el ICA intentó llegar a una nueva definición de lesión renal aguda (LRA) en pacientes con cirrosis para lograr un diagnostico más temprano y, por ende, un tratamiento precoz que mejorase el pronóstico de los pacientes (20). Recientemente, por medio de un documento de posición, dos hepatólogos (miembros del ICA) y dos nefrólogos dedicados en el estudio de la disfunción renal en cirrosis intentaron proporcionar una actualización acerca de la definición, clasificación, diagnóstico, fisiopatología y tratamiento del SHR.
Falla hepática aguda sobre crónica (ACLF)
Criterios diagnósticos
Según los resultados descritos por el estudio CANONIC, la ACLF se define como un síndrome caracterizado por una descompensación aguda de la cirrosis, asociado a falla de algunos órganos y una elevada mortalidad a corto plazo (tabla 2). Este estudio caracterizó a los pacientes con ACLF: la mayoría eran jóvenes y alcohólicos con infecciones bacterianas asociadas, y presentaban reporte de leucocitosis y PCR elevada en paraclínicos (3).
La disfunción se evalúo utilizando el CLIF-SOFA. De acuerdo con el número y el tipo de fallos de órgano, se definió la presencia de ACLF y se clasificó su gravedad en tres estadios. Tanto un puntaje CLIF-SOFA como un recuento leucocitario elevado fueron predictores independientes de mortalidad en estos pacientes (3).
La puntuación CLIF-SOFA es una modificación de la puntuación de SOFA (Sequential Organ Failure Assessment) para el estudio CANONIC, ya que algunos componentes de esta última no tenían en cuenta algunas características específicas de los pacientes con cirrosis. Al igual que la puntuación SOFA, la puntuación CLIF-SOFA incluye valores de cero a cuatro, incrementando el puntaje a medida que aumenta el compromiso del órgano/sistema. Los grados de encefalopatía hepática corresponden a la clasificación de West-Haven. Las zonas en negrilla definen la falla del órgano/sistema en cuestión.
Fisiopatología
La fisiopatología de la ACLF aún no está del todo descrita; sin embargo, se plantea que hay una alteración de la respuesta inmune a la injuria aguda, a la infección y a una respuesta inflamatoria no controlada que, en conjunto, lleva a los daños propios de la ACLF (3).
La aparición de ACLF es consecuencia de un factor precipitante en un paciente que tuviese una cirrosis compensada. El factor puede empeorar el daño hepático de manera directa, tal como ocurre en las hepatitis alcohólicas, virales, isquémicas o trombosis de la vena porta. De igual manera, puede ocurrir de manera extrahepática en casos como trauma, cirugía, sangrado variceal e infecciones (6). Es importante aclarar que, a pesar de la amplia variedad de posibles eventos precipitantes, en hasta un 40% de los pacientes no se logra identificar una causa que explique la aparición de ACLF (7).
El óxido nítrico (NO), cuya producción es estimulada por la inflamación y el estrés oxidativo, parece explicar la aparición de trastornos circulatorios y renales presentes en la ACLF (8). Además, junto con las citoquinas proinflamatorias, se ha relacionado con la aparición de encefalopatía gracias al efecto modulador que podría tener sobre las concentraciones de amonio (9).
Se ha descrito que los defectos inmunológicos encontrados en la ACLF son similares a los hallados en pacientes con sepsis, basado en evidencias de choque progresivo con vasodilatación y falla multiorgánica (8). El defecto más relevante es la falla funcional de los neutrófilos con disminución de su capacidad fagocítica, y alteraciones del estrés oxidativo, el cual se ha relacionado con un aumento en el riesgo de infecciones, y con la aparición posterior de la falla orgánica que deriva ulteriormente en muerte (10).
Otras células de la inmunidad innata, como los monocitos y las células NK, también se ven afectadas, así como las células de la inmunidad adquirida donde se evidencia una falla en la proliferación y en el incremento de la apoptosis (7).
Encefalopatía hepática
La encefalopatía hepática (EH) se presenta en un 30-60% de los pacientes cirróticos. Es una expresión clínica de un grupo de anormalidades neuropsiquiátricas potencialmente reversibles, secundarias al acumulo de sustancias neurotóxicas en el tejido cerebral, proporcional a la función sintética y de reserva del hígado (11).
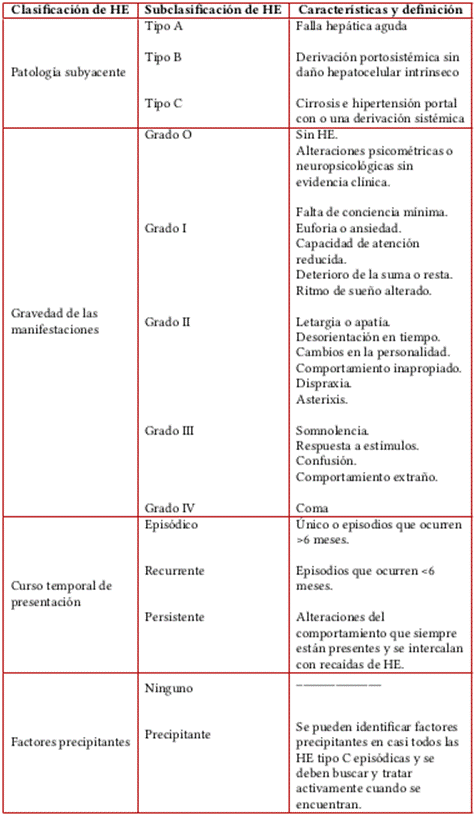
La EH se clasifica de acuerdo con cuatro factores (tabla 3): la enfermedad subyacente, la gravedad de las manifestaciones, la temporalidad y la existencia de factores precipitantes. En cuanto a la enfermedad subyacente, ésta se divide en tres tipos dependiendo del contexto clínico en el que ocurra: tipo A, en pacientes con falla hepática aguda; tipo B, en el contexto de una derivación portosistémica sin enfermedad hepática intrínseca; y tipo C, en el contexto de cirrosis con hipertensión portal o una derivación sistémica. De acuerdo con la gravedad de las manifestaciones, estas se en clasifica en: mínima u oculta, grado I, grado II, grado III y grado IV, según las características clínicas (cambios conductuales, confusión, bradipsiquia, alteraciones del ciclo sueño-vigilia, lenguaje incoherente, letargia, estupor y coma) y alteraciones neurosicológicas o psicométricas que presente el paciente. En cuanto al curso temporal, puede ser episódica, recurrente (dos o más episodios de EH que ocurren en seis meses o menos) o persistente (patrón de alteraciones de la conducta que siempre están presentes sin periodos de normalidad). Finalmente, los episodios de EH se describen como no precipitados o precipitados en relación con si se encuentra o no un factor desencadenante (11).
Otra clasificación particularmente útil para el cálculo del CLIF-SOFA se basa en los criterios de West Haven, los cuales tienen en cuenta las manifestaciones neurológicas de los pacientes (12) (tabla 4).
El principal objetivo del manejo de la EH es la identificación del factor precipitante, pues así, es posible evitar el empeoramiento del estado de consciencia. En caso de que se desconozca, se deben tomar medidas generales e iniciar manejo basándose en la sospecha clínica. Por ejemplo, si se sospecha de algún foco infeccioso, se deberá iniciar terapia antibiótica empírica.
La disminución de los niveles de amonio es crucial, pues es una de las moléculas más toxicas que llevan a la aparición de EH. Para ello, se han usado disacáridos no absorbibles como la lactulosa, la cual actúa cortando las cadenas de ácidos grasos con la ayuda de la flora bacteriana del colon, logrando así una acidificación del medio y favoreciendo la conversión del amonio en una molécula no absorbible: el amoniaco (13).
El objetivo del tratamiento es que el paciente tenga de dos a tres deposiciones blandas diarias. La dosis oral de lactulosa es de 20 mL cada ocho horas. Si el número de deposiciones aumenta, se debe suspender o disminuir la dosis del medicamento (14). Otra de las opciones de tratamiento para la disminución de los niveles de amonio es inhibir la flora proteolítica del colon; entre los medicamentos usados están: Neomicina, Paromicina, Metronidazol, Amoxicilina/Clavulanato y Rifaximina. Sin embargo, el único medicamento que ha demostrado controlar la encefalopatía aguda y el control crónico de los síntomas es la rifaximina (15).
El tratamiento de la EH depende del grado de esta; la intubación orotraqueal sólo está indicada en aquellos que se encuentran en coma (EH grado IV) con el fin de prevenir la broncoaspiración.
Síndrome hepatorrenal
El síndrome hepatorrenal (SHR) es una forma característica de insuficiencia renal que ocurre en los pacientes con cirrosis hepática, inicialmente planteado como de carácter funcional como consecuencia de una vasoconstricción severa de la circulación renal causada por una disfunción circulatoria sistémica (16). Se trata de una condición que aparece en fases avanzadas de la cirrosis y se asocia a un pronóstico ominoso. Recientemente, se ha logrado demostrar precisamente en relación con la ACLF que además de la vasodilatación sistémica hay otros factores que aportan a dicha disfunción circulatoria, tales como la inflamación sistémica inducida por patrones moleculares asociados a patógenos (PAMP) o patrones moleculares asociados a daños (DAMPS). Asimismo, en contra del carácter enteramente funcional de esta patología, se han venido encontrando cada vez más pacientes con enfermedad renal crónica asociada en pacientes con cirrosis, esto debido a la coexistencia de cirrosis con el síndrome metabólico (5).
Esta condición se presenta en aproximadamente el 10% de los pacientes con cirrosis en etapas avanzadas o con insuficiencia hepática aguda. El porcentaje aumenta cuando se tienen en cuenta los pacientes que simultáneamente presentan cirrosis y ascitis, pues en este grupo asciende al 18% a un año y a 39% a cinco años (16).
El diagnóstico del SHR es de exclusión, dado que los pacientes con cirrosis hepática también podrían presentar insuficiencia renal por diversas causas (nefrotoxicidad, necrosis tubular aguda, insuficiencia renal prerrenal, etc.) (17,19). En 2015, el Club Internacional de la Ascitis (ICA) publicó los criterios con los que actualmente se realiza el diagnostico de insuficiencia renal aguda (IRA) en pacientes cirróticos (tabla 4). Teniendo estos criterios en cuenta, se fijaron tres estadios de la enfermedad, así como la progresión y la respuesta al tratamiento, y se dieron recomendaciones para el tratamiento de esta patología (18).
Tabla 4 Definiciones para el diagnóstico y tratamiento de la IRA en pacientes con cirrosis hepática del ICA*
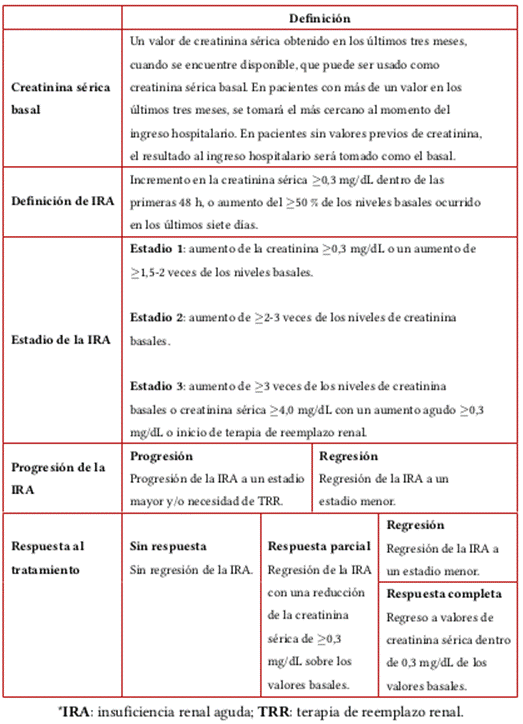
Fuente: adaptado de (18).
Existen dos tipos diferentes de SHR según la severidad y la progresión de la insuficiencia renal: el SHR1 y SHR2. Estos se describen a continuación:
El síndrome hepatorrenal tipo 1 (SHR 1) se presenta como una insuficiencia renal rápidamente progresiva en hasta un 33% de los pacientes con SHR 1 que presentan hiponatremia hipervolémica debido a una alteración de la capacidad renal para la excreción de agua libre de solutos.
Además de la insuficiencia renal severa y de rápida progresión, los pacientes con SHR 1 pueden presentar signos de compromiso circulatorio tales como hipotensión arterial (PAM ≤70 mmHg) y resistencias vasculares sistémicas muy bajas. Dado esta asociación, en ocasiones, es difícil hacer diferencia entre SHR 1 y sepsis grave. Del mismo modo, los pacientes con SHR 1 tienen signos de enfermedad hepática avanzada, con ictericia, coagulopatía, encefalopatía hepática, desnutrición y ascitis (20).
El síndrome hepatorrenal tipo 2 (SHR 2) se presenta con una insuficiencia renal funcional moderada que generalmente se mantiene estable y cuyos niveles de creatinina varían entre 1,5 a 2 mg/dL. Habitualmente presentan menos manifestaciones clínicas; sin embargo, es la ascitis la más característica en este grupo de pacientes, la cual frecuentemente es refractaria dado factores asociados como la retención de sodio, la disminución de la filtración glomerular y niveles elevados de aldosterona y noradrenalina (20).
Los pacientes con SHR 2 tienen riesgo de desarrollar SHR 1, lo que puede ocurrir de forma espontánea o como consecuencia de algún factor precipitante.
Los pacientes con SHR tipo 1 tienen una tasa de mortalidad mayor que los pacientes con SHR tipo 2 (figura 1).
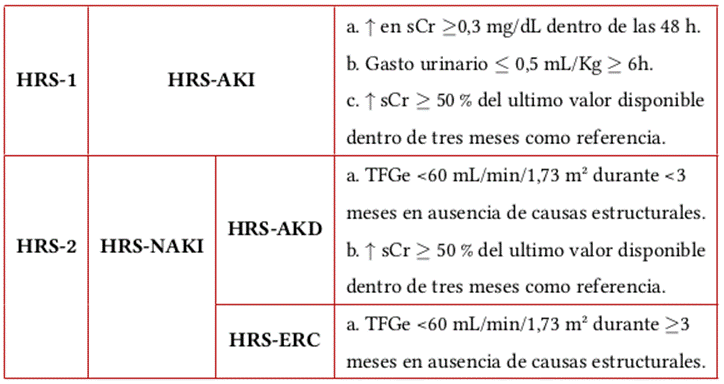
Recientemente se ha planteado una revisión acerca de la nomenclatura del síndrome hepatorrenal en función de los cambios en la creatinina sérica y/o cambios en el gasto urinario, esto definido por los criterios KDIGO, convirtiéndose así el SHR tipo 1 en SHR-AKI. Lo anterior sucede con el fin de lograr un inicio de tratamiento más precoz, incluso cuando el aumento de creatinina sérica sea pequeño (tabla 5).
En cuanto al SHR tipo 2, las anomalías crónicas en la creatinina sérica sin un periodo de tiempo definido en las mismas dificultan adaptar su definición. Por ello, la Asociación Europea para el Estudio del Hígado (EASL) propuso que el SHR tipo 2 debe denominarse como SHR-NAKI (síndrome hepatorrenal no AKI) (30). Se ha postulado que el mismo se realice en el contexto de enfermedad renal aguda (AKD) o enfermedad renal crónica (CKD), dado que en ambos casos se cumplen criterios para daño renal agudo, sin olvidar que difieren en su duración, siendo >90 días en CKD y >90 días en AKD (29).
Conclusión
A pesar de los avances en el conocimiento acerca del SHR, las posibilidades de tratamiento siguen siendo limitadas. Por ahora, se basan en recomendaciones generales, manejo farmacológico, derivación portosistémica intrahepática transyugular (TIPS) y trasplante hepático.
En cuanto a recomendaciones generales, se debe restringir el consumo de sal a 80-120 mmol/día, eliminar los nefrotóxicos y tener precaución con el uso de diuréticos (22). Igualmente, se debe hacer manejo individualizado, y los pacientes con SHR tipo 1 deben ser tratados en unidad de cuidados intensivos o intermedios, especialmente si esto significa recibir un manejo con vasoconstrictores y albumina (23).
El manejo con vasoconstrictores y albumina es el tratamiento de elección para pacientes con SHR tipo 1. El objetivo del tratamiento es causar una vasoconstricción en el lecho vascular esplácnico, así como reducir la volemia efectiva, logrando así la disminución de la activación de los sistemas vasoconstrictores endógenos, y aumentando la perfusión renal y el filtrado glomerular. El medicamento de elección es la terlipresina, un agonista de los receptores V1 de la vasopresina, que actúa en el musculo liso a nivel vascular.
La administración combinada de terlipresina y albumina ha demostrado ser eficaz en revertir el SHR en un 40-50% de los casos; los valores basales de creatinina y el aumento de la presión arterial durante el tratamiento son factores predictivos de respuesta favorable en pacientes con SHR tipo 1 (24).
La derivación portosistémica intrahepática transyugular (en inglés, transjugular intrahepatic portosystemic shunt) es una prótesis que establece una comunicación entre la vena porta y una vena hepática, reduciendo de esta manera la presión portal. Se ha propuesto como manejo para pacientes con SHR tipo 1; sin embargo, requiere investigación y su aplicación puede verse limitada por insuficiencia hepática avanzada en este grupo de pacientes (25).
El trasplante hepático es el tratamiento de elección para pacientes con SHR tipo 1. Generalmente no se requiere trasplante renal, pues el SHR es reversible después del trasplante hepático, a menos que se haya requerido más de 6-8 semanas de terapia de reemplazo renal, puesto que, en este subgrupo de pacientes, la reversibilidad de la insuficiencia renal es muy poco probable (26).