Introducción
Los paragangliomas (PG) son tumores neuroendocrinos muy poco frecuentes, que surgen de las células cromafines dentro de los tejidos paraganglionares del sistema nervioso autónomo; tienen un origen embriológico común de las células de la cresta neural 1. Generalmente son benignos y de crecimiento lento.
Los tejidos paraganglionares de la cabeza y el cuello se distribuyen alrededor de las estructuras vasculares, pero se encuentran especialmente en el área de la bifurcación carotídea y el bulbo yugular. Los paragangliomas en la región de cabeza y cuello (PGCC) se clasifican en tumores del cuerpo carotídeo (TCC) y no TCC 1. Representan el 0,6 % de los tumores de cabeza y cuello 2,3 y se sitúan más comúnmente en el cuerpo carotídeo (65 %), seguidos por los PG intravagales (5 %).
En su etiología existe las variantes esporádicas y familiares. Las tasas de variantes familiares en la población difieren según la ubicación del PG. Para los PGCC este porcentaje puede llegar hasta el 35 % 4. Debido a la dificultad diagnóstica de malignidad y el riesgo quirúrgico, Shamblin propone una clasificación basada en la relación macroscópica tumor-vaso, dividiéndolos en tres grupos 5.
Generalmente son asintomáticos, por lo que el diagnóstico de estos tumores es tardío e incidental. La edad promedio de presentación está en la quinta década de la vida; la presencia de este tumor a edades tempranas es infrecuente 6. El objetivo de este artículo fue presentar el caso de una paciente de 15 años, con aumento de tamaño del lado derecho del cuello sin otros síntomas, cuyos estudios preoperatorios resultaron compatibles con un tumor del cuerpo carotideo.
Caso clínico
Paciente femenina de 15 años, con antecedente de dermatitis atópica, quien consultó en pediatría por aumento de volumen cervical de un año de evolución, sin otros síntomas. Al examen físico se palpó una masa submandibular derecha, de 4 cm de diámetro, móvil e indolora. En el laboratorio se destacó velocidad de eritrosedimentación (VES) de 114 mm/h e IgG para Bartonella positivo, por lo que se indicó tratamiento antibiótico.
Al control del mes, tanto la lesión como los exámenes de laboratorio no presentaron cambios. Se solicitó tomografía computarizada (TC) de cuello que mostró una masa sólida en el espacio carotídeo derecho, de 50x31x30 mm, a la altura de bifurcación carotídea, englobando ambas arterias carótidas. Se diagnosticó TCC y se completó el estudio con angiorresonancia magnética (angioRM) de cerebro y cuello (Figura 1), en la cual impresiona una lesión en la bifurcación carotídea derecha de contornos definidos y lobulados, de 37x37x49 mm, desplazando la carótida interna hacia atrás, clasificación de Shamblin III 5. Se realizó la prueba de oclusión carotídea preoperatorio con blush o rubor tumoral en relación con la bifurcación de la arteria carótida derecha, negativo para isquemia clínica, con competencia adecuada del polígono de Willis.
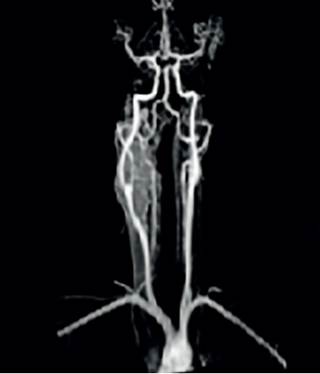
Figura 1. Angio resonancia de cuello y cerebro donde se observa una lesión en la bifurcación carotídea derecha, de contornos definidos y lobulados, de 37x37x49 mm, clasificación de Shamblin III.
Se efectuó la resección de tumor, identificando en el intraoperatorio una arteria carótida interna muy friable, por lo cual se realizó puente carótida común-carótida interna con injerto de vena safena invertida (Figuras 2, 3 y 4). La paciente evolucionó satisfactoriamente, con descenso de VES a 78 mm/h en el postoperatorio inmediato y a 44 mm/h a los seis meses postoperatorios, asumiendo inflamación peritumoral o arteritis. Presentó disfonía por compromiso del nervio laríngeo superior, sin otras complicaciones.
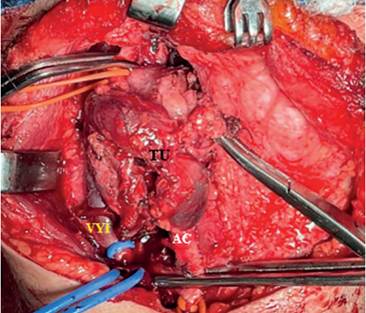
Figura 2. Imagen intraoperatoria. Tumor in situ que compromete y engloba completamente la arteria carótida interna. AC: Arteria carótida común; VYI: Vena yugular interna; TU: Tumor de cuerpo carotideo.

Figura 3. Imagen intraoperatoria posterior a la resección del tumor carotideo, con puente carótida común-carótida interna con safena invertida. ACI: Arteria carótida interna; VYI: Vena yugular interna; VS: Vena safena invertida.
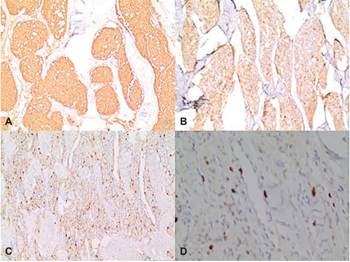
La biopsia confirmó paraganglioma de 5x4 cm, con permeaciones vasculares venosas presentes (pequeñas vénulas en pseudocápsula tumoral), bordes quirúrgicos negativos e inmunohistoquímica con reacciones positivas con anticuerpos contra cromogranina-A, sinaptofisina y anticuerpos contra S-100 (Figuras 5 y 6), con Ki-67 bajo y 5 ganglios linfáticos negativos para metástasis. A los 6 meses postoperatorios la paciente había evolucionado de manera favorable, con recuperación total de la voz, permeabilidad completa del puente vascular a la ecografía Doppler de control y normalización de la VES.
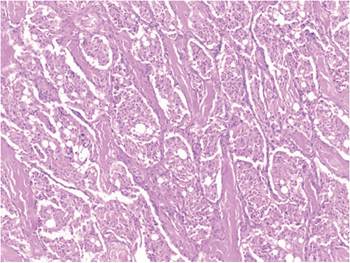
Figura 5. Imagen histológica del tumor, con distribución celular en nidos de organoides, rodeados por estroma vascular, compatible con patrón de Zellballen.
Discusión
El TCC es una patología poco frecuente, presentándose habitualmente desde los treinta años a la quinta década de vida. En el estudio de Erickson D, et al. 7, con 236 pacientes con paragangliomas benignos, la edad media en el momento del diagnóstico fue de 47 años. Sin embargo, los pacientes con paragangliomas de la base del cráneo y el cuello tienden a ser un poco mayores al momento de la presentación en comparación con aquellos con paragangliomas abdominales 8.
Entre los factores de riesgo de TCC se menciona la hipoxia crónica. En aquellos pacientes que viven a grandes alturas, como también en quienes presentan cardiopatía congénita crónica y enfermedad pulmonar obstructiva crónica se manifiestan más frecuentemente los TCC esporádicos. Sin embargo, se desconoce la asociación entre los TCC y residir a grandes alturas 9. En el caso descrito, la edad de presentación no es habitual y no tiene factores de riesgo presentes, lo que dificultó la sospecha diagnóstica, siendo fundamental el estudio imagenológico para el diagnóstico y la planificación quirúrgica; esto debe hacerse de forma precoz, evitando que se presenten síntomas por compresión.
El diagnóstico de los PGCC se puede realizar con imágenes, considerando sus características típicas y su ubicación. En la TC, estos tumores suelen ser sólidos, bien delimitados, con una densidad similar a la del músculo y un realce intenso del contraste. La relación anatómica con las principales estructuras vasculares se muestra en la angio-TC 10; en el caso de los TCC, estos provocan el ensanchamiento de la bifurcación carotídea. La angioRM ha superado a la TC para la valoración de los PGCC, ya que aporta más información diagnóstica, sobre todo por el mejor contraste de tejidos blandos 10,11. También es fundamental la evaluación vascular de la permeabilidad del polígono de Willis para planificar un adecuado control vascular en la cirugía (derivación o baipás de alto flujo).
Los TCC pueden ser esporádicos o familiares; este último se presenta en un 10 % y se transmite de manera autosómica dominante. La subunidad D (SDHD) del complejo enzimático heterotetramético succinato deshidrogenada (SDH; complejo mitocondrial II) es el primer gen identificado del paraganglioma. Posteriormente, las mutaciones fueron identificadas en las subunidades SDHC y SDHB. Las mutaciones SDH que predisponen a PG son heterocigóticas, se transmiten en línea germinal y causan pérdida de función. En el caso presentado, se podría plantear un estudio familiar; las variantes familiares tienden a tener antecedentes familiares positivos, una edad de inicio más temprana y una mayor probabilidad de múltiples PG 12.
Los paragangliomas no tienen diferencias anatomopatológicas, la mayoría son de forma lobulada u ovoide, independiente su origen topográfico, con una cápsula fibrosa y de superficie roja o gris rosada. En su histología, los PG se componen por células ovales o poligonales (células principales), con núcleos uniformes o pleomórficos, vesiculares o hipercromáticos dispuestos en nidos de organoides, rodeados por un estroma vascular (patrón de Zellballen). Su malignidad es confirmada con la presencia de metástasis en los ganglios linfáticos regionales, huesos, pulmón e hígado. Las células tumorales principales son positivas para sinaptofisina, cromogranina y enolasa neuroespecífica al estudio inmunohistoquímico. Las células de soporte son positivas para la proteína S-100 y la proteína fibrilar ácida de la glía. En el caso descrito, la biopsia confirmó la misma inmunohistoquímica mencionada en la literatura, con ganglios negativos, lo que demostró ser un TCC sin malignidad, a pesar de su compromiso perivascular asociado 13. En este caso, el compromiso carotídeo está dado no por infiltración tumoral, sino por el compromiso circunferencial de los vasos y probable inflamación que hizo necesaria una resección carotidea.
El estándar de tratamiento de los TCC es la cirugía 11,14. La primera escisión exitosa de TCC se realizó en 1889 realizada por Albert. Posteriormente Gordon-Taylor describió una disección subadventicia segura en 1940 15. Desde finales de la década de 1980, la técnica más utilizada ha sido la desvascularización del TCC mediante la ligadura de las ramas tributarias de la arteria carótida externa, mientras que la disección del TCC se inicia en la bifurcación carotídea y continúa en dirección cefálica. Con esta técnica las tasas de mortalidad y accidente cerebrovascular disminuyen de forma significativa. También se ha propuesto la disección del tumor en dirección cefalocaudal, siguiendo el curso de la arteria faríngea ascendente distal, que se sugiere como el principal suministro de sangre proximal del tumor. Esta arteria generalmente se origina dorsalmente en la arteria carótida externa; cráneo-dorsalmente desde el TCC, esta arteria forma un bucle y alimenta el TCC desde su lado craneal, facilitando el control proximal temprano sobre la mayoría de los nervios adyacentes en la zona de disección 16. Con la disección cefalocaudal descrita se ha reportado disminución tanto del sangrado intraoperatorio como de la disfunción postoperatoria de los nervios craneales.
El papel de la embolización preoperatoria sigue siendo controvertido. Aunque el beneficio teórico se basa en la disminución del flujo de entrada en un tumor muy vascularizado antes de la resección, algunos estudios no han podido demostrar ningún beneficio en la disminución de la pérdida de sangre o lesión de los nervios craneales y podría presentar complicaciones graves 17. En nuestra paciente, el estudio vascular no demostró un vaso tributario susceptible de embolizar.
El manejo multidisciplinario entre cirujanos de cabeza y cuello y cirujanos vasculares ha demostrado mejores resultados. En la revisión de Mohebali J, et al. 17 de 74 resecciones de TCC en 64 pacientes con manejo multidisciplinario, compuesto por un cirujano de cabeza y cuello y un cirujano vascular, mostraron buenos resultados en relación con el tiempo operatorio, la pérdida de sangre estimada, la necesidad de transfusión intraoperatoria, los cambios electroencefalográficos intraoperatorios, la lesión de nervio craneal, y el accidente cerebrovascular, entre otros. El tipo de cirugía a realizar depende del tamaño tumoral y la clasificación de Shamblin 5. Se puede realizar una disección roma y resección tumoral única o una resección tumoral con resección de estructuras vasculares (carótida externa, carótida interna o carótida común), por esto es fundamental el estudio imagenológico y vascular preoperatorio y la participación de un equipo multidisciplinario.
Conclusión
Resulta relevante y de interés clínico el reporte de casos que se presentan fuera de la frecuencia descrita en la literatura. Dada su edad temprana de presentación, podría corresponder a un tumor de etiología familiar, lo que resulta complejo para realizar un diagnóstico precoz. Se hace necesario complementar el estudio en este tipo de paciente con exámenes de imágenes para así saber el nivel de compromiso vascular y hacer la planificación quirúrgica respectiva con el equipo multidisciplinario.