Para la revisión temática se utilizaron las bases de datos de Scopus y Pubmed. En los criterios de inclusión se consideraron los artículos científicos y de revisión que tuvieran los términos: "tuberculosis" y "Mycobacteryum tuberculosis" relacionados con los términos "drug resistant" y "molecular mechanism". Se realizó busqueda boleana y se utilizaron diferentes combinaciones de términos en lenguaje controlado y natural. Se excluyeron los documentos en idioma diferente a inglés a español y no hubo restricción temporal en los resultados de la búsqueda. Se encontraron 186 documentos, de los cuales 33 son específicos a abordar el entendimiento de los mecanismos y las bases moleculares de la resistencia de MTB a medicamentos anti-TB.
La Organización Mundial de la Salud (OMS) declaró en 1993 la tuberculosis (TB) como una emergencia sanitaria mundial y es considerada como la segunda causa de muerte por enfermedad infecciosa, después del virus de la inmunodeficiencia humana (VIH) 1,2. Según reportes de la OMS, un tercio de la población mundial está infectada con Mycobacterium tuberculosis (MTB) y aproximadamente el 10% desarrollará la enfermedad a lo largo de su vida 3. En el año 2015, se reportaron 10,4 millones de casos incidentes y 1.4 millones de muertes a causa de esta enfermedad 4.
El esquema terapéutico en Colombia para pacientes con TB fármaco-susceptible, se basa en el tratamiento acortado directamente supervisado (DOTS/TAES) el cual incluye dos fases: una fase inicial de dos meses con los medicamentos de primera línea: isoniacida (INH), rifampicina (RIF), etambutol (EMB) y pirazinamida (PZA), seguida de una fase de tratamiento continuo de cuatro meses con INH y RIF 5. Este esquema puede alcanzar tasas de curación superiores al 90% 6. Sin embargo, la convergencia de múltiples factores como esquemas de tratamiento inapropiados, falta de supervisión en la administración de los antibióticos, dificultad de acceso a los servicios de salud y al tratamiento, se asocian con irregularidades en la toma de los medicamentos, abandonos de tratamiento y fracasos terapéuticos. La interrupción del tratamiento puede resultar en la supresión parcial del crecimiento bacteriano, generando condiciones favorables para la aparición y diseminación de casos de TB multi-fármaco-resistentes (TB-MDR), la cual es definida como aquella que presenta resistencia a INH y RIF 1,5-9. Los datos de la OMS de 2014, indicaron que el 3.5% de los nuevos casos de TB y el 20.5% de casos previamente tratados tuvieron TB-MDR 4,10.
El tratamiento de la TB-MDR se basa en los llamados medicamentos de segunda línea: fluoroquinolonas (FQS), aminoglicósidos (AMGS), etionamida (ETH), D-cicloserina (DCS) y ácido p-amino salicílico (PAS). Este grupo de antibióticos produce más reacciones adversas que implican interrupciones en el tratamiento, son más costosos y pueden ser incluso menos efectivos contra MTB 6,8. Una desafortunada consecuencia en el tratamiento de TB-MDR, es que estos medicamentos también han generado resistencia 11, conllevando a la aparición de casos de TB con resistencia extendida (TB-XDR), un término definido en el 2006 como aquellos casos de TB que son resistentes a INH y RIF, a una FQ y un AMGS inyectable 12. Para el año 2013, la OMS reportó que la proporción de casos de TB-MDR con TB-XDR fue 9%. 4,10.
En Colombia en el 2014, se notificaron 12 415 casos de TB donde la incidencia fue de 26 casos por 100 000 habitantes 13. La última encuesta nacional de TB-MDR realizada en el año 2005 reportó una incidencia de 2.38% para casos nuevos y 31,44% para casos previamente tratados. Entre los grupos más afectados para la TB-MDR están los co-infectados con VIH y los privados de la libertad en donde la incidencia llega al 5,6%. También se han reportado casos de TB-XDR, los cuales a finales del 2012 sumaban ya 32 casos. 14-16.
La circulación de aislamientos de MTB-MDR/XDR se convierte en una situación preocupante, debido a la complejidad para hacer los diagnósticos oportunos, por los riesgos de transmisión, lo complejo y prolongado del tratamiento y el impacto económico que puede tener esta enfermedad en el sistema de salud de un país 17-19. Con el objetivo de mejorar el entendimiento sobre los mecanismos de resistencia utilizados m. tuberculosis presentamos la siguiente revisión de tema.
Mecanismos de resistencia a medicamentos anti-tuberculosos en Mycobacterium tuberculosis
Varios factores que promueven la resistencia antimicrobiana (RAM) podrían estar implicados en el aumento de los casos de TB-MDR/XDR en diversas regiones del mundo. Dentro de las propiedades de las micobacterias, se incluyen factores que se han relacionado con resistencia constitutiva y resistencia adquirida a medicamentos anti-TB 20-22.
Fármaco-resistencia constitutiva
La resistencia constitutiva o intrínseca, se define como la fármaco-resistencia de cualquier especie bacteriana que no ha sido adquirida como resultado de la exposición a antibióticos 20.
Permeabilidad reducida de la pared celular mico-bacteriana
La resistencia intrínseca en MTB se ha atribuido al hecho de poseer una pared celular compleja constituida por una gran cantidad de lípidos, proteínas y polisacáridos que le confieren una característica hidrófoba con permeabilidad celular restringida para un gran número de compuestos antibacterianos 23-25. Las capas de péptidoglicano y arabinogalactano limitan la entrada de moléculas hidrófobas, mientras que la capa de ácidos micólicos limita el acceso de ambas moléculas 26. Antibióticos hidrofóbicos pueden ingresar a la célula por difusión a través de la bica-pa hidrofóbica, mientras que los antibióticos hidrofílicos que no se pueden difundir a través de la pared celular utilizan canales como las porinas 27. Hasta la fecha, las porinas MspA y OmpATb han sido identificadas y caracterizadas en m. smegmatis y MTB, respectivamente 27, aunque no es claro cuál es el papel que desempeñan estas proteínas en la fármaco-resistencia de micobacterias, específicamente en MTB.
Modificación y degradación enzimática de medicamentos
La producción de enzimas es quizá un mecanismo de respuesta bacteriana a los antibióticos, ya que estas utilizan una serie de estrategias para superar las propiedades tóxicas de los antibióticos. Un ejemplo de esto, es la modificación de medicamentos a través de kinasas, acetiltransferasas, adenilitransferasas, glicosiltransferasas y ADP-ribosiltransferasas 28. En MTB, la modificación enzimática de medicamentos se debe principalmente a la metilación del ARNr. Por ejemplo, la resistencia intrínseca de MTB a los macrólidos y lincosamidas, se debe al gen erm37, el cual codifica una metiltransferasa ARNr 29. Esta enzima altera las estructuras de los ribosomas de MTB a través de la metilación del 23S ARNr reduciendo la afinidad de los macrólidos y lincosamidas a los ribosomas e impidiendo su actividad inhibitoria en la síntesis de proteínas 30. Otro ejemplo es la metilación del ARNr que genera resistencia a capreomicina (CAP) y viomicina, dos medicamentos utilizados para tratar la TB-MDR. La CAP interactúa con las hélices 69 y 44 de las proteínas ribosomales 16S y 23S RNAr respectivamente, resultando en la inhibición de la síntesis de proteínas 31. Estudios genéticos, han sugerido que la resistencia a estos dos medicamentos se debe a mutaciones en el gen tlyA, el cual codifica para una metiltransferasa (2'- O-metiltransferasa) 32. El gen tlyA metila los nucleótidos C1409 en la hélice 44 de la proteína 16S ARNr y C1920 en la hélice 69 de la proteína 23S ARNr. La pérdida de estas metilaciones confiere resistencia a CAP y viomicina 33 La degradación enzimática de medicamentos, es un mecanismo que se ha estudiado principalmente en los β-lactámicos. Las β-lactamasas, hidrolizan el anillo β-lactámico proporcionando resistencia a este grupo de medicamentos 34. La β-lactamasa más importante en MTB es la BlaC 35,36, la cual tiene actividad contra los carbapenémicos, que son generalmente resistentes a las β-lactamasas de otras bacterias. Adicionalmente, MTB codifica otros tres genes con función β-lactamasa: blaS, rv0406c y rv3677c, los cuales han mostrado menor actividad que BlaC 37.
Bombas de eflujo como mecanismo de resistencia a medicamentos anti-TB
Las bombas de eflujo, son proteínas transportadoras localizadas en la membrana citoplasmática de todos los tipos de células y actúan como transportadores activos, ya que requieren una fuente de energía para realizar su función. En sistemas de eflujo bacterianos, probablemente su papel fisiológico, es proteger a la célula contra moléculas tóxicas, incluyendo antibióticos clínicamente importantes, al transportarlos una vez que ingresan a la célula bacteriana hacia el ambiente extracelular 38,39. Esta característica reduce la concentración intracelular de los antibióticos a niveles sub-1NHibitorios y de esta manera se piensa que promueven la emergencia de fármaco-resistencia 40,41. Genes que codifican bombas de eflujo están constitutivamente expresados en células wild-type; por lo que se ha sugerido que dichos sistemas confieren resistencia de bajo nivel a múltiples medicamentos, sus actividades brindan una mejor tolerancia a los medicamentos y potencian la adquisición y acumulación de mutaciones cromosomales que confieren altos niveles de resistencia 39,42. Se ha observado que de los aislamientos de MTB resistentes a medicamentos anti-TB, entre un 20-30% de los resistentes a INH, aproximadamente el 5% con resistencia a RIF y alrededor de un 15-58% de aquellos resistentes a FQS no presentan alteraciones genéticas asociadas con dicha fármaco-resistencia 11,43-45, lo que sugiere que otros mecanismos pueden contribuir a la fármaco-resistencia en MTB, dentro de los cuales se incluyen las bombas de eflujo.
Basado en perfiles estructurales y bioenergéticos, las bombas de eflujo se clasifican en dos grupos: (i) trans portadores primarios, a los cuales pertenece la familia de casete de unión a ATP (ABC) y utilizan la energía libre de la hidrólisis de ATP 46; y (ii) transportadores secundarios, que se caracterizan por utilizar el gradiente de protones o iones de sodio como fuente de energía 39,41 y se dividen en 4 familias: Superfamilia de Máximo Facilitador (MFS), Familia Multi-fármaco Resistencia Pequeña (SMR), Resistencia a División por Nodulación (RND) y Familia de Expulsión de Compuestos Tóxicos y multi-fármacos (MATE) 39,41,47 (Tabla 1).
Tabla 1 Transportadores involucrados con fármaco-resistencia en Mycobacterium tuberculosis

ABC, Casete de unión a ATP; MFS, Superfamilia de Máximo Facilitador; SMR, Familia Multi-fármaco Resistencia Pequeña; RND, Resistencia a División por Nodulación; FQ, fluoroquinolona; RIF, rifampicina; STR, estreptomicina; EMB, etambutol; OFL, ofloxacina; KAN, kanamicina; TET, tetraciclina; ER, eritromicina; THZ, thioridazina; AMP, ampicilina; CLO, cloranfenicol; NOV, novobiacina ND, no determinado; ATP, trifosfato de adenosina; PMF, fuerza motriz de protones. *Genes evaluados en este estudio. a Se determinó el N° del gen al que corresponde en la cepa de referencia CDC1551, sólo para los genes que codifican bombas de eflujo tipo ABC, ya que son los genes de interés en este estudio.
Fármaco-resistencia adquirida
En bacterias, la resistencia genética generalmente es mediada a través de la adquisición de genes exógenos a través de plásmidos, transposones, integrones y bacteriófagos 21. Sin embargo, en MTB no se han reportado mecanismos de adquisición de genes de resistencia por dichos elementos. Por lo tanto, la resistencia a medicamentos anti-TB se debe principalmente a alteraciones en genes que codifican blanco de antibióticos, en productos genéticos involucrados en la activación de pro-fármacos o regiones reguladoras 9,11,48. No obstante, no se conoce una alteración genética que por sí misma, dé lugar al fenotipo de TB-MDR/XDR. Sin embargo, numerosos estudios se han realizado para describir los mecanismos genéticos de resistencia en MTB, en los cuales se ha observado que la acumulación de mutaciones en diferentes loci de genes específicos dan origen a los fenotipos resistentes MDR y XDR (Tabla 2) 9,11,49. La transmisión y adquisición de fármaco-resistencia puede depender del linaje genético. Se ha sugerido, que diferentes linajes pueden compensar el "costo del fitness" de la resistencia adquirida, lo cual contribuye a mejorar la transmisión de aislamientos fármaco-resistentes o en otros casos llevando a la rápida aparición de fármaco-resistencia durante el tratamiento anti-TB debido a mayores tasas de mutación 50,51. Esta observación, es apoyada por el hecho de que en aquellas zonas con mayor proporción de aislamientos de MTB-MDR se han asociado con aislamientos que pertenecen al linaje Beijing 52,53.
A continuación, se explicarán brevemente los mecanismos genéticos conocidos que confieren resistencia a los principales medicamentos anti-TB (INH, RIF, FQS y AMGS).
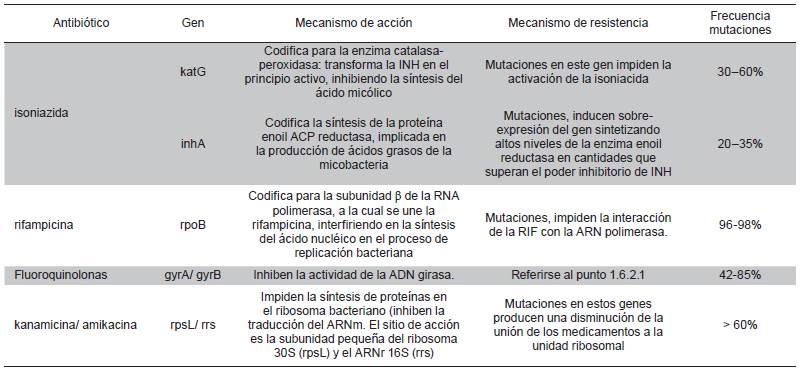
Resistencia a isoniacida
La INH es un profármaco que es activado por la enzima catalasa-peroxidasa (KatG), la cual es codificada por el gen katG para generar una gran variedad de especies reactivas las cuales atacarán múltiples blancos en MTB 54-56. Aunque el mecanismo de acción de la INH as'í como los mecanismos que confieren resistencia son complejos ya que se ven involucrados varios blancos en la micobacteria, se cree que el principal blanco de este medicamento es la enzima enoil-ACP reductasa (INHA), la cual está involucrada en la elongación de los ácidos grasos de cadena larga y la síntesis de ácidos micólicos 57. Las especies reactivas producidas como consecuencia de la acción del katG sobre INH, reaccionan con el NAD(H) para formar el aducto INH-NAD, el cual detiene la actividad de la enzima INHA 58. Mutaciones en varios genes, incluyendo katG, ahpC, INHA, kasA y ndh se han asociado con resistencia a INH 59-61. Sin embargo, dos mecanismos moleculares han mostrado ser la principal causa de resistencia a este medicamento: mutaciones en los genes katG, INHA y su región promotora.
Resistencia a rifampicina
Debido a su eficiente acción antimicrobiana, la RIF junto con la INH, es considerada el núcleo del tratamiento acortado debido a su alta acción bactericida 62. La resistencia a RIF aparece después de la resistencia a otros medicamentos anti-TB, y es por esto que se ha convertido en un marcador de TB-MDR 63. El mecanismo de acción de la RIF es iNHibir la subunidad β de la enzima ARN polimerasa (codificada por el gen rpoB), impidiendo que esta enzima se una al ADN, bloqueando el inicio de la transcripción del ARN 64.
Resistencia a fluoroquinolonas
La actividad de las FQS contra MTB, su buena distribución tisular y celular, así como los bajos efectos adversos hacen que las FQS sean utilizadas para el tratamiento de aislamientos de MTB-MDR, el tratamiento empírico en comunidades con una alta tasa de MDR o el tratamiento de pacientes con reacciones adversas a los medicamentos de primera línea 6,65-67.
Las FQS tienen como blanco las topoisomerasas bacterianas II y IV 67,68. En las células, su función específica es catalizar la relajación y el súper enrollamiento del ADN (80). MTB carece de la topoisomerasa IV e incluye sólo la topoisomerasa II o ADN girasa, un tetrámero que consiste en dos subunidades A y dos subunidades B, codificadas por los genes gyrA y gyrB respectivamente 11,69.
Resistencia a aminoglucósidos
Dentro del grupo de los AMGS, la amicacina (AMK) y la kanamicina (KAN) son los medicamentos inyectables de segunda línea más usados para el tratamiento de la TB-MDR. Se ha sugerido, que la resistencia a KAN, es una de las características que define la presencia de aislamientos de MTB-XDR 70. El mecanismo de acción de los AMGS es INHibir la síntesis de proteínas al actuar sobre la subunidad pequeña 30S del ribosoma, específicamente en las proteínas ribosomales S12 y 16S ARNr codificadas por los genes rpsL y rrs, respectivamente. La unión al ribosoma interfiere con la elongación de la cadena peptídica causando lecturas incorrectas del código genético generando proteínas anómalas 71.
La resistencia fenotípica de alto nivel a los AMGS (MIC > 80 (g/ml) se ha asociado principalmente a mutaciones en la región de 1.400-bp del rrs 72. La mutación A1401G es la alteración más reportada, se ha identificado entre el 3090% de los aislamientos de MTB resistentes a KAN y se ha asociado con resistencia cruzada a la AMK y CAP 73,75 ♦