Introducción
Colombia es reconocido mundialmente como el segundo país megadiverso (Minciencias, 2016), debido a factores como la posición geográfica, los accidentes geográficos (lo que influye en la variedad de pisos térmicos existentes) y la ausencia de estaciones (que facilita el crecimiento y la conservación de distintas especies de flora y fauna).
En lo que concierne a la riqueza vegetal, Colombia con 0,7 % del área continental contiene 10 % de la diversidad total de las plantas angiospermas (Vásquez y Buitrago, 2011), lo que convierte a este tipo de plantas en objeto de investigación, especialmente las que presentan actividad de tipo medicinal.
Teniendo en cuenta lo anterior, las especies vegetales que conforman la familia Fabaceae están distribuidas mayoritariamente en Suramérica y Centroamérica (Cabral, 2010). La especie vegetal Senna spectabilis (Fabaceae) posee un gran valor medicinal, razón por la cual se ha empleado para tratar dolores de cabeza, inflamaciones, gripes, heridas, entre otros usos etnobotánicos (Viegas et al. 2004). Tradicionalmente es conocida como “flor amarillo”, “vainillo” o “monedero” en Colombia, y se encuentra distribuida en los departamentos de Antioquia, Boyacá, Caldas, Cauca, Cesar, Caquetá, Casanare, Cundinamarca, Guajira, Huila, Magdalena, Meta, Nariño, Norte de Santander, Quindío, Risaralda, Santander, Tolima y Valle (Catalogo de la Biodiversidad Colombiana, 2009).
Algunas de las especies vegetales que conforman a la familia Fabaceae son reconocidas por tener compuestos químicos que presentan actividad biológica, estos se encuentran presentes en la corteza, las hojas y las raíces principalmente; en esta familia se han reportado y caracterizado químicamente metabolitos secundarios tales como alcaloides, flavonoides y polifenoles (Pino et al., 2004). Los estudios químicos y biológicos muestran que la bioactividad de estos metabolitos secundarios está asociada a efectos antidiabéticos, antimicrobianos, antiinflamatorios y anticancerígenos (Ojeda et al., 2015).
En el género Senna se puede destacar la presencia de metabolitos tales como esteroides, quinonas y senósidos, que se encuentran principalmente en hojas y tallos (Torrenegra y Jiménez, 2002). Paralelamente, los estudios biológicos en el género Senna han demostrado numerosas bioactividades, de las cuales se pueden destacar antimicrobiana, hematológica, antiinflamatoria, antiproliferativa y anticancerígena (Morales y Bachiller, 2007). En la especie Senna spectabilis (especialmente en corteza, hojas y raíces) se han determinado numerosas sustancias químicas con bioactividad antifúngica, antibacterial, antioxidante, anticonvulsiva y sedante (Sangetha et al., 2009). De esta especie vegetal se han caracterizado y reportado alcaloides, flavonoides y polifenoles mayoritariamente (Viegas et al., 2013). Por otra parte, la especie Senna spectabilis ha presentado estudios en hojas, tallos y raíces, en los cuales ha presentado una diversidad fitoquímica interesante (Selegato et al., 2017).
Teniendo presente que Colombia es uno de los países en los que Senna spectabilis se distribuye, este trabajo de investigación se orientó a realizar un aporte al conocimiento químico y biológico de esta especie, por medio del estudio fitoquímico de sus metabolitos fijos y la evaluación de su capacidad antioxidante.
Metodología
Recolección del material vegetal
La especie fue obtenida en el municipio de Guaduas, Cundinamarca (5° 05’ 16,4” N 74° 36’ 54,3” O). Se recolectaron 3773 g de flores frescas, las cuales fueron secadas a temperatura ambiente de Bogotá (18 °C y humedad relativa de 77 %); una muestra testigo se envió al Herbario Nacional de Colombia para su determinación taxonómica, la cual fue clasificada bajo el código COL 600165 como Senna spectabilis.
Obtención de extractos y fracciones
Las flores secas y trituradas de Senna spectabilis (2000 g) fueron sometidas a una extracción con etanol al 96 % a temperatura ambiente por el método de maceración en frío. El extracto obtenido (E.EtOH.Ss.F) se filtró y concentró a presión reducida de 120 mbar y a una temperatura de 40 °C obteniendo 100 g de extracto total, luego fue floculado en una proporción 1:1 EtOH/H2O para continuar con el fraccionamiento. Se realizaron pruebas químicas de precipitación y coloración para determinar la posible presencia de metabolitos secundarios mayoritarios en la muestra (Sanabria, 1999).
100 g de E.EtOH.Ss.F fueron sometidos a un proceso de extracción líquido-líquido continuo con solventes de polaridad creciente, obteniéndose las fracciones de heptano (Fx.Hept.Ss.F 0,85 g, 0,85 %), diclorometano (Fx.DCM.Ss.F 14,9 g, 14,9 %), acetato de etilo (Fx.AcOEt.Ss.F 0,55 g, 0,55 %) y un residuo hidroalcohólico (Fx.Hidroalcohólico.Ss.F, 83.7 g, 83,7 %). Cada una de estas fracciones fue sometida a separaciones continuas a través de CC y CCF para finalmente aislar dos compuestos y tres mezclas.
A 0,6 g de la fracción de (Fx.Hept.Ss.F) después de una CC, utilizando como fase móvil heptano: AcOEt en una proporción 8:2, se obtuvieron 92 fracciones, las cuales después del monitoreo por CCF fueron reunidas en 9 subfracciones. La fracción número 2 (Fx.Hept.Ss.F2) produjo 0,18 g de un sólido color naranja denominado Mezcla SsF1, el cual fue analizado por CG-EM. En la fracción número 3 (Fx.Hept.Ss.F3) se obtuvieron 0,096 g de un sólido naranja denominado Mezcla SsF2, el cual fue analizado por CG-EM.
1,5 g de la fracción de diclorometano (Fx.DCM.Ss.F) se fraccionaron por CC, utilizando como fase móvil DCM: MeOH en una proporción 9:1, obteniendo 70 fracciones, las cuales después del monitoreo por CCF fueron reunidas en 12 subfracciones. En la fracción 1 (Fx.DCM.Ss.F1) se obtuvieron 0,040 g de un sólido color amarillo denominado Mezcla SsF3, el cual fue analizado por CG-EM. En la fracción 8 (Fx.DCM.Ss.F8) se obtuvieron 0,146 g, los cuales fueron nuevamente fraccionados por CC utilizando como fase móvil AcOIs: MeOH en una proporción de 9,8:0,2, obteniendo 128 fracciones, las cuales después del monitoreo por CCF fueron reunidas en 15 subfracciones. En la fracción número 10 (Fx.DCM.Ss.F8.SF10) se obtuvieron 3,3 mg de un sólido color blanco denominado Compuesto SsF4, el cual fue analizado por CG-EM.
0,4 g de la fracción de acetato de etilo (Fx.AcOEt.Ss.F) se fraccionaron por CC utilizando como fase móvil AcOEt - DCM en proporciones 9.5:0.5, obteniendo 209 fracciones reunidas en 27 subfracciones. Posteriormente, en la fracción 4 (Fx.AcOEt.Ss.F4) se obtuvieron 0,9 mg de un sólido blanco denominado Compuesto SsF5, el cual fue analizado por CG-EM.
Técnicas para la elucidación estructural y la caracterización de los compuestos aislados
Para determinar tentativamente la mezcla y los compuestos obtenidos se utilizó un cromatógrafo de gases con detector selectivo de masas Shimadzu QP2010 plus, ubicado en el laboratorio de química de la Universidad Distrital Francisco José de Caldas. La separación se realizó en una columna capilar SHRXi-5MS de 30 m de longitud x 0,25 mm x 0,25 μm con una inyección en modo Split (10:1); el gas de arrastre utilizado fue helio (grado 5,0) con flujo constante de 1,2mL/min. La programación de la temperatura del horno fue de 50 °C (2 min) con incrementos de 15 °C/min hasta 200 °C (2 min), finalmente se incrementaron 10 °C/min hasta 300 °C (10 min) para un tiempo total de análisis de 34 min; la temperatura de la línea de transferencia fue de 275 °C y la de la cámara de ionización de 230 °C. Los espectros de masas de los compuestos aislados fueron tomados en un equipo Shimadzu QP2010 plus dotado con una sonda de inserción directa y un analizador de masas cuadrupolar, utilizando un modo de ionización electrónica (IE) a 70 eV y una temperatura de la cámara de ionización de 230 ºC.
Evaluación de la capacidad antioxidante
Para la evaluación de la capacidad antioxidante se utilizó el extracto etanólico (E.EtOH.Ss.F) y las fracciones de heptano (Fx.Hept.Ss.F), diclorometano (Fx.DCM.Ss.F) y acetato de etilo (Fx.AcOEt.Ss.F).
El ensayo se realizó utilizando 10 mg del radical DPPH disueltos en 10 mL de metanol grado analítico y mediante su lectura en un espectrofotómetro FLUOstar Optima BMG Labtech, se estableció la absorbancia entre 0.7- 0.9 a una longitud de onda de 516 nm, en donde el radical tiene su máximo pico de absorción y por ende un comportamiento lineal de las absorbancias al mezclarse con el extracto, lo que permite que los datos sean más precisos (Molyneux, 2004). Cada extracto se diluyó en diferentes volúmenes de etanol obteniendo concentraciones entre 50 y 5.000 ppm.
A 25 μL de cada fracción y extracto de la especie Senna spectabilis se agregaron 275 μL de solución DPPH y se leyó su absorbancia a 520 nm; las absorbancias se registraron teniendo en cuenta intervalos de tres min ente 0 y 120 min respectivamente. Para conocer la capacidad antioxidante de los tratamientos ensayados se elaboraron curvas estándar de ácido ascórbico y un antioxidante sintético de referencia (Trolox). (Metodología modificada de Brand-Williams et al., 1995)
Cuantificación de compuestos fenólicos y flavonoides
La cuantificación de compuestos fenólicos se realizó preparando una curva de calibración con ácido gálico en agua desionizada con concentraciones de entre 50 y 500 mg L-1 a partir de un stock de ácido gálico de 1.000 mg L-1. A 125 µL de los patrones, blanco y muestras (diluidas a 1.000 mg L-1) se agregaron 200 µL de agua destilada y 25 µL del reactivo Folin-Ciocalteu, se dejó incubar por 6 min a temperatura ambiente para después adicionar 12 µL de carbonato de sodio al 5 % y se incubó por 30 min a 42 °C para favorecer la reacción; posteriormente se realizaron las lecturas de absorbancia a 740 nm en intervalos de 10 min durante 2 h.
Para la cuantificación de flavonoides se preparó una curva de calibración de quercetina en etanol al 96 % a concentraciones entre 1 y 50 mg L-1 a partir de un stock de 1.000 mg L-1 de quercetina. A 125 µL de los patrones, blanco y muestras (diluidas a 1.000 mg L-1) se agregaron y se mezclaron 125 µL de cloruro de aluminio al 2 %, se incubó por 30 min a 42 °C para favorecer la reacción y seguido a esto se realizó la lectura de absorbancias a 420 nm en intervalos de 10 min por 2 h.
Resultados
Análisis fitoquímico preliminar
Los resultados del análisis fitoquímico preliminar de la especie Senna spectabilis (Tabla 1) dan indicios de la presencia de metabolitos secundarios como taninos, alcaloides, terpenos y probablemente flavonoides (solo una de las tres pruebas dio resultado positivo). Por el contrario, no presenta cumarinas, saponinas y carotenoides, esto coincide con reportes químicos de especies de la familia Fabaceae como Bauhinia purpurea, Bauhinia variegata (Martínez et al., 2011), Senna reticulata (Matulevich-Peláez, 2017), Senna alata y Senna bicapsularis que no reportan este tipo de metabolitos secundarios (Barrese et al., 2005).
Tabla 1 Análisis fitoquímico preliminar para flores de Senna spectabilis
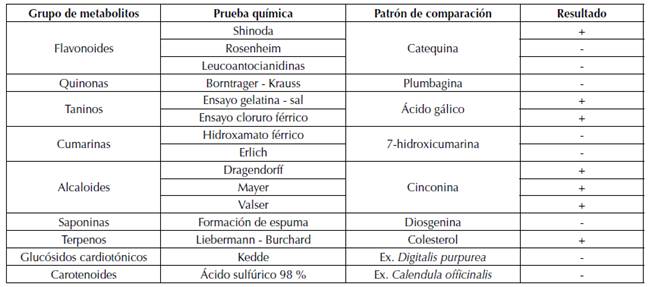
(+) Prueba positiva; (-) Prueba negativa
Para la especie Senna spectabilis los resultados son consecuentes, debido a que presenta flavonoides (Singh et al., 2013), terpenos (Mallaiah et al., 1984; Ashok y Sarma, 1988) y alcaloides aislados en diferentes órganos de la especie vegetal (Viegas et al., 2004; Jäger et al. 2009; Viegas et al. 2013).
Metabolitos secundarios aislados
La separación y purificación de las fracciones de heptano, diclorometano y acetato de etilo obtenidas a partir del extracto etanólico total de las flores de la especie Senna spectabilis permitió la identificación tentativa de tres mezclas y dos compuestos: la primera mezcla conformada por dos ésteres (9-oxo-nonanoato de etilo y palmitato de etilo) y una cetona (pentadecan-2-ona) fue designada como Mezcla SsF1. En la mezcla designada como SsF2 se encontró nuevamente al palmitato de etilo junto con una antraquinona (1,8-dihidroxi-3-metil-antraquinona). La tercera mezcla conformada por un monoterpeno oxigenado (Linalool) y un derivado de ácido cinámico (cinamato de metilo) fue designada como Mezcla SsF3. Los compuestos aislados y designados como SsF4 y SsF5 fueron identificados como cinamato de metilo y cafeína respectivamente.
Composición de la mezcla SsF1
La mezcla SsF1 (18,3 mg) se obtuvo como un sólido color naranja a partir de la fracción de heptano, la cual en el monitoreo por CCF presentó manchas naranjas, rojas y azules en el revelado con luz ultravioleta a 366 nm. Por otra parte, la corriente iónica total (TIC) del análisis por CG-EM arrojó tres señales significativas de alta intensidad con tiempos de retención de 11,273 min, 15,163 min y 16,192 min. La comparación de los espectros de masas de las respectivas señales con los de la librería NIST-08 indican que corresponden al 9-oxo-nonanoato de etilo, palmitato de etilo y pentadecan-2-ona, con porcentajes de coincidencia de 94 %, 97 % y 94 % respectivamente. El compuesto 9-oxo-nonanoato de etilo se reporta por primera vez en las flores de la especie vegetal objeto de estudio. La pentadecan-2-ona ha sido reportada en la familia Fabaceae (Chaverri y Cicció, 2015), particularmente en las hojas y flores de la especie vegetal Gliricidia sepium, la cual se emplea como expectorante y febrífugo, además como antimalárico. El palmitato de etilo ha sido reportado en la familia Fabaceae, particularmente en la especie vegetal Retama monosperma, especie que demostró tener alta capacidad antioxidante específicamente en la fracción de acetato de etilo (Abdelmadjide et al., 2020).
Composición de la mezcla SsF2
La mezcla SsF2 (8,1 mg) se obtuvo como un sólido de color naranja también obtenido de la fracción de heptano, la cual en el monitoreo por CCF presentó manchas naranjas y amarillas en el revelado con luz ultravioleta a 366 nm. La corriente iónica total (TIC) del análisis por CG-EM arrojó dos señales significativas de alta intensidad en tiempos de retención de 16.172 min y 19.896 min. La comparación de los espectros de masas de las respectivas señales con los de la librería NIST-08 fueron identificados como palmitato de etilo y 1,8-dihidroxi-3-metil-antraquinona con un porcentaje de coincidencia de 93 % y 97 % respectivamente. El palmitato de etilo había sido previamente encontrado en la mezcla SsF1; la 1,8-dihidroxi-3-metil-antraquinona ha sido reportada en la familia Fabaceae y en el género Senna (Valiente y Torrenegra, 2003), particularmente en la especie vegetal Senna bicapsularis (L) que posee ciertas características de color y pigmentación en las especies vegetales, debido a los dobles enlaces conjugados que presenta la estructura química de 1,8-dihidroxi-3-metil-antraquinona; además se ha demostrado su actividad antimicrobiana en las hojas y raíces (Torrenegra y Jiménez, 2002)
Composición de la mezcla SsF3
La mezcla SsF3 (40,7 mg) se obtuvo como un sólido amarillo a partir de la fracción de diclorometano, la cual en el monitoreo por CCF presentó manchas azules y verdes en el revelado con luz ultravioleta a 366 nm y en el revelado con Vainillina/H2SO4. Por otra parte, la corriente iónica total (TIC) del análisis por CG-EM arrojó dos señales en tiempos de retención de 7.480 min y 10.333 min, la comparación de los espectros de masas de las respectivas señales con los de la librería NIST-08 permitió establecer la presencia de Linalool y cinamato de metilo, con porcentajes de coincidencia del 98 % y 96 % respectivamente. El Linalool ha sido reportado en la familia Fabaceae, en el género Senna y está presente en la especie vegetal Senna spectabilis (Sangetha et al., 2009) que posee ciertas características en el aroma debido a varios compuestos volátiles presente en el aceite esencial y que entre los más destacados son compuestos terpénicos. El cinamato de metilo ha sido reportado en la familia Fabaceae (Tava et al., 2007) en las hojas y flores de la especie vegetal Bituminaria bituminosa, la cual ha mostrado actividad larvicida contra Aedes aegypti (Fujiwara et al., 2017). En el género Senna este compuesto ha sido identificado en la especie Senna occidentalis (Murugan et al., 2015), de la cual se destaca la actividad mosquitocida y antiplasmódica contra Anopheles stephensi y Plasmodium falciparum (Murugan et al., 2015)
Compuesto SsF4
El compuesto SsF4 (3,3 mg) se obtuvo como un sólido blanco a partir de la fracción de diclorometano. La corriente iónica total (TIC) del análisis por CG-EM exhibió una señal de alta intensidad en el tiempo de retención de 10.329 min. La comparación de los espectros de masas de la respectiva señal con los de la librería NIST-08 fue identificada como cinamato de metilo con un 97 % de coincidencia, este compuesto es reportado por primera vez en la especie vegetal; sin embargo, ha sido encontrado en otras especies vegetales como Ocimum basilicum L. var basilicum, O. basilicum L. var purpurenscens, O. gratissimum L. y O. tenuiflorum L. (Acosta et al., 2003).
Compuesto SsF5
El compuesto SsF5 (6,5 mg) se obtuvo como un sólido blanco cristalino a partir de la fracción de acetato de etilo, el cual en el monitoreo por CCF presentó una marcha negra intensa en el revelado con luz ultravioleta a 254 nm. Por otra parte, la corriente iónica total (TIC) del análisis por CG-EM arrojó una señal de alta intensidad en un tiempo de retención de 12.741 min, tras la comparación de los espectros de masas de la respectiva señal con los de la librería NIST-08 que fue identificada como cafeína con un 97 % de coincidencia. La cafeína ha sido reportada en la familia Aquifoliaceae, en las hojas de las especies Ilex paraguariensis e Ilex guayusa, que es usado en América del sur como brebaje para controlar afecciones estomacales (Seigler, 2002). En la especie Senna spectabilis se ha reportado la presencia de cafeína en el extracto etanólico de hojas, tallo y raíces (Selegato et al., 2017). Por otra parte, la cafeína posee una conocida y extensa historia como ayudante analgésico. Se han realizado estudios sobre la acción antinociceptiva intrínseca de la cafeína, en los que se establece que la dosis antinociceptiva se encuentra en el rango de 25 a 100 mg L-1 (Tavares y Sakata, 2012). La cafeína es reportada por primera vez para las flores de Senna spectabilis en Colombia.
Evaluación de la capacidad antioxidante
Para realizar la determinación de la capacidad antioxidante del extracto etanólico y las correspondientes fracciones se utilizaron datos cuyo valor de porcentaje de inhibición estaba en el rango entre 30 % y 90 %, esto tomándose como referencia el equivalente medio de la actividad presentada por los patrones de Trolox y Vitamina C, estos porcentajes correspondientes al IC50, cuyo cálculo se realizó teniendo en cuenta los valores estadísticos de la pendiente, la intersección que presentaba con el eje y el coeficiente de correlación (R2), estableciéndose así una relación lineal de pendiente positiva entre la inhibición al 50 % y la concentración. Fueron analizadas cuatro muestras a diferentes concentraciones para DPPH; sin embargo, la fracción de heptano (Fx.Hept.Ss.F) no presentó porcentajes de inhibiciones con valores superiores al 30 %, probándose en concentraciones superiores a 5000 mg L-1; los resultados obtenidos para el método de DPPH se muestran en la Tabla 2, siendo el mejor resultado el de la fracción de diclorometano (Fx.DCM.Ss.F), pues el tiempo transcurrido fue de 78 min, a este tiempo se obtuvo un coeficiente de correlación de 0,9846, que refleja un coeficiente de variación del 3,35 % entre el promedio y la desviación estándar (328,7 ppm ± 11,0294).
Los resultados obtenidos de la capacidad antioxidante de cada uno de los tratamientos ensayados comparados con el patrón de vitamina C y Trolox se ilustran en la figura 1. En esta se muestra que el extracto etanólico (E.EtOH.Ss.F) y las fracciones de diclorometano y acetato de etilo (Fx.DCM.Ss.F; Fx. AcOEt.Ss.F) presentan un porcentaje de inhibición superior al 30 %; en todas las muestras se evidencia la relación directamente proporcional entre la concentración y el porcentaje inhibitorio.
Los mejores resultados en la capacidad antioxidante los muestra la fracción de diclorometano, pues a bajas concentraciones (comparadas con las concentraciones que requirieron las otras fracciones y el extracto) presenta un aceptable porcentaje de inhibición. Comparado con los patrones, es posible notar que es semejante con la capacidad antioxidante del Trolox, pues a bajas concentraciones es capaz de inhibir el radical. Por lo tanto, solo la fracción de diclorometano (Fx. DCM.Ss.F) obtenido a partir de la especie vegetal Senna spectabilis presenta promisoria capacidad antioxidante según la evaluación del método DPPH; esto concuerda con los resultados obtenidos en la cuantificación de flavonoides donde en la fracción de diclorometano se encontró la mayor concentración.
Con respecto al tiempo que tardaron los compuestos en completar la reacción, se tiene esto como una ventaja del método pues permite que reaccione toda la muestra y se da el tiempo necesario para que el DPPH reaccione frente a antioxidantes débiles (Prakash, 2001). Sin embargo, es importante mencionar que el DPPH es sensible a algunos tipos de bases y solventes de Lewis, así como al oxígeno (Ancerewicz et al., 1998). Una investigación realizada a la especie Senna reticulata (Matulevich-Peláez, 2017) evidenció potencial antioxidante en la fracción etanólica y de diclorometano, lo cual coincide con los resultados hallados en este estudio, los cuales destacan a la fracción de diclorometano (Fx.DCM.Ss.F) como la que presenta mayor capacidad antioxidante. Por otra parte, estudios realizados a las flores de Senna multiglandulosa (Ojeda et al., 2015) mostraron que la fracción con mejor capacidad antioxidante es la de cloroformo, la cual es una fracción con polaridad muy similar a la de diclorometano. Una investigación realizada a fracciones de diversas polaridades a hojas y tallos de Senna singueana muestra que los valores más altos de IC50 se dieron en la fracción obtenida por éter de petróleo, seguido de cloroformo, metanol y acetona (Gebrelibanos et al. 2007).
Karau realizó estudios a la capacidad antioxidante con DPPH en las hojas y la corteza del tallo de la especie Senna spectabilis, reportando un 88,98 % y 90,95 % de inhibición para hojas y tallo respectivamente (Karau, 2014); a nivel comparativo con esta investigación, se encuentra que estos órganos tienen mayor porcentaje de inhibición respecto a las flores. Sin embargo, la investigación no reporta las concentraciones de las fracciones, por lo que no se podría dar una veracidad en cuanto a la comparación entre la capacidad antioxidante de diferentes órganos.
La capacidad antioxidante evidenciada en la fracción de diclorometano (Fx.DCM.Ss.F) se debe a los compuestos presentes en esta fracción que son de polaridad intermedia-baja, principalmente compuestos hidroxilados y nitrogenados (alcaloides), ya que los alcaloides de cualquier tipo de estructura han mostrado capacidad antioxidante ante compuestos que tienen alta tendencia a ser oxidados (Chávez et al. 1996). Es importante recordar que en otros estudios a la misma especie vegetal se encontró presencia de metabolitos secundarios como flavonoides, alcaloides (como la cafeína) y antraquinonas hidroxiladas, que por su estructura y los estudios previos que se han realizado, muestran capacidad antioxidante (Selegato et al., 2017).
Cuantificación de fenoles
Con la curva de calibración realizada con los patrones de ácido gálico (Tabla 3) se encontró la función lineal que representaba la relación (Absorbancia = 0,0019* (concentración de ácido gálico en mg L-1) - 0,0143), se realizó la lectura espectrofotométrica del extracto y las fracciones, se hizo la correlación entre la curva y los valores obtenidos, los cuales se muestran en la tabla 4.
La tabla 4 muestra que la mayor cantidad de compuestos fenólicos está presente en la fracción de diclorometano (Fx.DCM.Ss.F), seguida por el extracto total (E.EtOH.Ss.F), el de heptano (Fx.Hept.Ss.F) y en menor cantidad la fracción de acetato de etilo (Fx.AcOEt.Ss.F). Esto puede relacionarse con los resultados obtenidos en la capacidad antioxidante, que muestran a la fracción de diclorometano (Fx.DCM.Ss.F) como la de mayor capacidad inhibitoria oxidante, a su vez esto permite establecer que aproximadamente el 70 % de los compuestos presentes en la fracción de diclorometano son polifenoles (Viegas et al., 2013; Tai et al., 2015).
Cuantificación de flavonoides
Con la curva de calibración realizada con los patrones de quercetina (Tabla 5), se realizó la relación lineal que arrojó la función lineal absorbancia = 0,02296* (concentración de quercetina) - 0,0739. Bajo las mismas condiciones se midieron las absorbancias de las soluciones del extracto y las fracciones, y tras realizar la correlación entre la curva y los valores obtenidos se tienen los resultados consignados en la tabla 6:
La tabla 6 muestra que la fracción de diclorometano (Fx.DCM.Ss.F) tiene la mayor cantidad de flavonoides (según el patrón de quercetina) entre las muestras, lo que coincide también con la mayor cantidad de polifenoles totales medidos.
Los resultados obtenidos concuerdan con lo mostrado por Viegas et al (2013), quienes han reportado en la especie, flavonoides como la luteolina y la metoxiluteolina en las flores y los frutos verdes. Por su parte, Singh et al. (2013) estudiaron las partes aéreas de Senna spectabilis aislando dos flavonas glicosiladas, la 6-hidroxi-4’-metoxiflavona-6-O-arabinopiranosa y la 3,5-dihidroxi-7,3’,4’-trimethoxi-flavona-3-O-arabinopiranosa del extracto etanólico de la planta; adicionalmente, Singh et al. encontraron la presencia de otros flavonoides como la 5,4’-dihidroxi-7,3’-dimethoxiflavona-5-O-β-D(+)- glucopiranosa (Singh et al., 2013).
Es importante señalar que la capacidad antioxidante está relacionada con los compuestos fenólicos totales determinados en los extractos y las fracciones, además como mencionan Rižner et al. (2000), se deben tener en cuenta aspectos como la existencia de agliconas libres y su incorporación a la determinación, además el hecho de que pueden ocurrir interacciones entre los componentes del extracto, esto recordando que la sinergia de los flavonoides con tocoferoles, ascorbil palmitato y ácido cítrico ya ha sido reportada (Rižner et al., 2000).
Los resultados mostrados en la presente cuantificación de flavonoides arroja valores menores a los determinados en la cuantificación de fenoles, esto está dentro de lo esperado, debido a que los flavonoides son un subgrupo de los compuestos fenólicos.
Conclusiones
El trabajo fitoquímico desarrollado realizó el aporte al conocimiento químico de las flores de la especie vegetal Senna spectabilis, permitió el aislamiento y la purificación de dos compuestos denominados cinamato de metilo y cafeína; y tres mezclas, la primera conformada por dos ésteres (9-oxo-nonanoato de etilo y palmitato de etilo) y una cetona (pentadecan-2-ona), en la segunda mezcla se encontró nuevamente al palmitato de etilo junto con una antraquinona (1,8-dihidroxi-3-metil-antraquinona), y la tercera mezcla conformada por un monoterpeno oxigenado (Linalool) y un derivado de ácido cinámico (cinamato de metilo). En cuanto al conocimiento biológico, se muestra que la fracción de diclorometano de las flores de Senna spectabilis (Fx.DCM.Ss.F) tiene los resultados más efectivos para actuar como una mezcla de sustancias con capacidad antioxidante; así mismo, esta fracción mostró la mayor cantidad de fenoles, evidenciando así la relación entre la capacidad antioxidante y la cantidad de polifenoles y flavonoides presentes en la fracción de diclorometano de las flores de la especie Senna spectabilis.





















