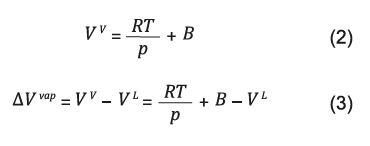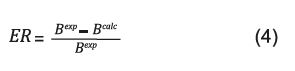Introdução
Densidade ou volume molar é uma propriedade do combustível muito importante uma vez que ela influência nos processos de produção, transporte e distribuição tão bem quanto nos processos que ocorrem nos motores de combustão interna. Conhecendo-se a densidade de combustíveis é possível projetar sua produção e as facilidades básicas de manufatura para ele, tais como: reatores, tanques e unidades de distribuição e destilação; estabelecimento de fluxos de calor e massa através de desses equipamentos; projeto de sistemas de bombeamento e válvulas, transferência em válvulas de segurança, etc.1 Densidade, junto com outras propriedades como a pressão de vapor, difusividades, tensão superficial, viscosidade influenciam na estrutura do combustível pulverizado, combustão e características da emissão, formação e depósito em motores e o comportamento de motores em climas frios.2), (3), (4), (5
Uma forma de estimar a densidade de um composto, em fase gasosa, seria através de estimativas por equações de estado ou de predição com o auxílio de valores experimentais. A equação virial permite a determinação da densidade de fluidos gasosos, entretanto é preciso estimar o segundo coeficiente virial ou medi-lo de forma experimental, o que demanda recursos e tempo. Nos estudos do significado físico dos coeficientes viriais observa-se que levam em conta as interações moleculares, ou seja, o segundo coeficiente virial representa os desvios do comportamento de gás ideal provocados por interações entre duas moléculas, o terceiro coeficiente virial expressa os desvios causados por interações entre três moléculas, e assim por diante.6
Os coeficientes das equações viriais são determinados experimentalmente através de diversas medições quantitativas, como p-V-T, velocidade do som, Joule-Thomson, índice de refração e de permitividade relativa, mistura de gases, solubilidade em gases comprimidos e cromatografia gás-líquido.7), (8Em todos esses casos, o valor determinado para os coeficientes tem custo elevado e tempo extenso, mas segundo Oreski (2012), uma maneira simples e rápida de estimar coeficientes viriais é a correlação e predição com métodos empíricos programados em computador.9
Nesse trabalho propõe-se estimar o segundo coeficiente virial (B) através do uso da equação de Clausius-Clapeyron.10 Os dados necessários para a predição serão estimados por equações da literatura, tais como a equação de Riedel para entalpia de ebulição normal, a equação de Watson para entalpia de vaporização (.H vap ) em outras temperaturas (T) e a equação de Antoine para pressão de saturação (P sat ).11),(12
Material e métodos
Uma forma de apresentar a equação de ClausiusClapeyron é a de se considerar que o volume de um gás (V V ) seja muito maior do que o líquido (V L ), o que é permitido para sistemas que não se encontram próximos do ponto crítico, e que a fase de vapor pode ser analisada como sendo gás ideal: 7),(10
Para o cálculo das equações de estado são utilizadas propriedades críticas específicas para cada substância analisada: temperatura crítica (TC), pressão crítica (PC) e fator de compressibilidade crítica (ZC):
Resultados e discussão
O cálculo da estimativa do segundo coeficiente (B) da equação virial foi aplicado para os álcoois:1 e 2-propanol, etanol, n-butanol, 1-decanol e 1-dodecanol, utilizando as informações apresentadas na literatura:10
Tabela 1 Variáveis usadas no cálculo do coeficiente virial de cada álcool, cujos valores já estão tabelados na literatura10

Para os álcoois em que os valores não estão disponíveis utilizou-se da lei dos estados correspondentes considerando Zc com valor padrão de 0,27, para assim se obter volume crítico (Vc) de cada substância. A equação de Riedel foi usada para obtenção da entalpia de ebulição
do álcool.Em todos os casos, foi calculado, apenas teoricamente, valores da estimativa do segundo coeficiente da equação virial (B), cujos resultados não foram correlacionados a nenhum dado, devido à inexistência de referencial teórico experimental em literaturas. Os valores de temperatura foram estabelecidos dentro dos limites da equação de Antoine para que quaisquer erros acarretados fossem de menor impacto para o valor final, porém mesmo com esse método, alguns compostos não obtiveram resultados satisfatórios (Tabela 2):
Através dos valores obtidos para cada álcool a uma determinada temperatura, foram construídos gráficos relacionados ao segundo coeficiente virial (B) em função da temperatura pré-determinada, como pode ser observado na Figura 1 a seguir.

Figura 1 Segundo coeficiente virial em função da temperatura (( 2-propanol; + 2-pentanol; . 1-hexanol; A 1-decanol) (Fonte: Relatório de trabalho da disciplina Tópicos II - 2017)
Analisando isoladamente o álcool 2-propanol, da faixa de temperatura adequada, onde obtevepropôs-se cálculos experimentais com se apenas dois resultados para as temperaturas temperaturas pré-estabelecidas, dentro e fora apresentadas. A Tabela 3 ilustra os resultados.
Tabela 3 Resultados de B (cm³/mol) do 2-propanol puro em temperaturas moderadas

Fonte: (a) Long; Duan, 2007, (b) Tsonopoulos et.al., 1989.
Para dados comparativos dos coeficientes viriais referenciados na literatura, correlacionando os encontrados, experimentalmente, relacionou-se dados obtidos para obter estudo mais detalhado determinadas substâncias com sistemas teste (Tabela 4):
Tabela 4 Comparação entre valores experimentais e os obtidos para B (cm³/mol) álcoois com (C1 - C4)
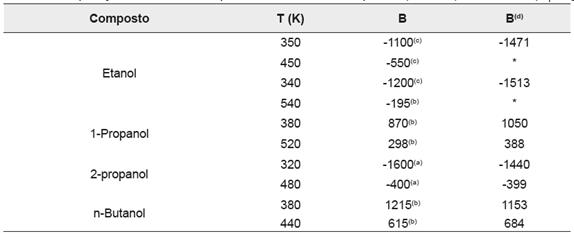
Long e Duan, 2007; (b) Tsonopoulos et.al., 1989 , (c) Oreski, 1969 , (d) Este trabalho, * psat (pressão de saturação) fora da faixa de temperatura.52rev.ion. 2019;32(1):49-53. Bucaramanga (Colombia).
A partir dos sistemas testes, calculou-se também o erro relativo (ER) de cada valor, utilizando o método de comparação:
Cabe salientar que o erro cometido no valor do coeficiente virial irá refletir na mesma ordem de grandeza na estimativa da densidade do composto.
Conclusão
De uma maneira geral o segundo coeficiente virial (B) reduz de valor, em módulo, com o aumento da temperatura do sistema. Isso foi observado ao se trabalhar com álcoois de cadeia curta e longa.
A comparação do valor de B com aqueles já publicados na literatura mostra um desvio razoavelmente pequeno demonstrando que o critério adotado para predição da grandeza é favorável à boa estimativa de densidade destes sistemas gasosos em temperaturas moderadas e altas.