Introducción
Los coronavirus son una especie importante de virus RNA, que reciben su nombre por su apariencia de “corona” en la microscopia electrónica, y es capaz de producir infección en humanos y en animales. En diciembre 2019, se identificó un nuevo coronavirus que es capaz de producir neumonía e insuficiencia respiratoria, en Wuhan, provincia de Hubei en China, y fue nombrado SARS-CoV-2 (severe acute respiratory syndrome coronavirus 2, por sus siglas en inglés)1. No pasó mucho tiempo hasta generar un impacto en salud en toda China; desde luego, comenzaron a aparecer un número de casos crecientes en otros países del mundo. En febrero de 2020, la Organización Mundial de la Salud (OMS), nombró a la enfermedad que produce como “COVID-19”, que significa enfermedad por coronavirus 20192. El 6 de marzo de 2020, se reportó el primer caso de COVID-19 en Colombia, una mujer 19 años proveniente de Milán, Italia3. Poco tiempo después, el 11 de marzo de 2020, la organización mundial de la salud declara al COVID-19 como una pandemia mundial4. Hasta el 3 de junio de 2020, reportaron 6 416 828 casos en todo el mundo, con 382 867 muertes confirmadas y 216 países afectados5. En Colombia, a esa misma fecha, se reportaron 33 354 casos, con 1 045 muertes confirmados y 12 288 pacientes recuperados6,7,8.
El SARS-CoV-2 tiene un periodo de incubación que oscila entre 2 y 14 días después de la exposición9 , con una presentación clínica muy variada, desde pacientes asintomáticos, pasando por casos leves, hasta pacientes críticamente enfermos con SDRA, microtrombosis, coagulación intravascular diseminada (CID), disfunción multiorgánica y muerte10. Los factores de riesgo para el desarrollo de COVID-19 grave incluyen enfermedad pulmonar obstructiva crónica, asma moderada a severa, enfermedad cardiaca previa, obesidad, diabetes mellitus, enfermedad hepática crónica, enfermedad renal crónica en grados avanzados y pacientes inmunodeprimidos con cáncer en tratamiento con quimioterapia, antecedente de trasplante, infección por virus de inmunodeficiencia humana (VIH), uso de drogas inmunosupresoras o corticoides11. Nuestro objetivo principal es mostrar la literatura más relevante disponible, con referencia a la utilidad de la anticoagulación en el manejo de la hipercoagulabilidad en los pacientes con COVID-19 grave.
Metodología
Se realizó una revisión narrativa a partir de la búsqueda avanzada con los términos DeSC: Infecciones por Coronavirus; SARS-CoV; Coagulación Sanguínea; Coagulación Intravascular Diseminada; Disfunción orgánica múltiple; Sepsis; Síndrome de respuesta inflamatoria sistémica; Lesión renal aguda. Se utilizaron los motores de búsqueda Clinical Key, Embase, PubMed y Ovid, obteniendo un total de 143 resultados, entre artículos originales, reportes de casos, series de casos y revisiones de la literatura, se seleccionaron un total de 56 artículos que fueron utilizados para la elaboración de la presente revisión de tema.
Hipercoagulabilidad y anticoagulación en COVID-19
La pandemia nos ha enfrentado a un gran número de pacientes con una nueva enfermedad para la cual nadie tenía inmunidad y la ciencia aún no tiene cura. En los últimos cinco meses la enfermedad nos ha avasallado con miles de artículos que buscan desentrañar la etiología, fisiopatología y clínica para garantizar un diagnóstico y manejo oportuno, que cambien el fatal desenlace en los pacientes más críticos. El fervor desenfrenado por establecer la fisiopatología, un mecanismo causal que nos lleve a una estrategia terapéutica acertada ha llevado a la ciencia a buscar caminos conocidos y otros nunca transitados. Uno de ellos es la ya conocida vía común de la inflamación y coagulación con activación de un estado de hipercoagulabilidad12. Recientes publicaciones han mostrado una alta tasa de eventos tromboembólicos, arteriales y venosos, que podrían explicar la morbimortalidad en algunos pacientes críticos con COVID-1913,14. Lo anterior ha llevado a proponer intervenciones farmacológicas de anti-inflamatorios y anticoagulación. juiciosa evaluación de los riesgos contrastados con los beneficios, a la luz de la mejor evidencia.
En el paciente crítico, a pesar que su principal patrón de afección es respiratorio, se ha descrito compromiso de diferentes sistemas, dentro de los cuales están importantes trastornos hemostáticos, como es la trombocitopenia, con una prevalencia cerca del 44 % de los pacientes en UCI15. Otra alteración hemostática notable es la CID, cuya presencia influye en la morbimortalidad de los pacientes críticos, por lo que se ha vuelvo un foco de atención para el desarrollo de nuevas estrategias terapéuticas16,17.
La sociedad internacional de trombosis y hemostasia (ISTH) define CID como un síndrome adquirido que se caracteriza por la activación intravascular de la coagulación con lo cual se desencadena la producción de grandes cantidades de trombina y fibrina intravascular que puede, a su vez, dañar la microvasculatura y generar disfunción multiorgánica18.
La fisiopatología de la CID clásica implica la producción sistemática de trombina intravascular, que conlleva a disfunción multiorgánica con el consecuente sangrado por consumo plaquetario, fibrinógeno y otros factores de la coagulación, además de hiperfibrinólisis secundaria. Sin embargo, existen escenarios de CID donde su condición fisiopatológica principal es la hiperfibrinolisis primaria, donde no necesariamente hay formación de coagulo, pero sí sangrado excesivo, configurando un evento catastrófico en la homeostasis, tal como se evidencia en los casos de sangrado obstétrico, leucemia promielocítica aguda y el cáncer19,20.
Hasegawa, et al. explicaron los cambios fisiopatológicos relacionados con la cascada de la coagulación que se describían en pacientes con sindróme de distress respiratorio del adulto (SDRA). En su investigación demostraron que el 26 % de los pacientes con SDRA, incluyendo a los pacientes con sepsis que desarrollan SDRA (con una prevalencia del 40 %), presenta coagulopatía que impactan en los días de estancia en UCI y tiempo de ventilación mecánica21.
Las complicaciones hematológicas en los pacientes con infecciones de tipo viral se han descrito a través del tiempo. En 1999 fue publicado un artículo de revisión donde se describieron las características clínicas y hematológicas que presentaban este tipo de pacientes, siendo esto un punto de inflexión positivo en la curva de conocimiento que se viene adelantando vertiginosamente en este campo22. Para esto es necesario traer a colación la revisión publicada por Yang y Tang. donde se plantea la hipótesis sobre el impacto de los procesos infecciosos, dado entre otros por la aberrante activación de células endoteliales, sobre la homeostásis de la coagulación23. Con base en ello, debería tenerse en cuenta que los pacientes con infección por SARSCoV-2 pueden cursar con tiempos de protrombina prolongado y/o dímero D elevado, asociandose con mal pronóstico, desarrollo de SDRA y alta mortalidad24,25,26.
El incremento del dimero D, se presenta por la proteólisis de la fibrina extravasada del epitelio alveolocapilar secundario al proceso inflamatorio inducido por la infección del SARS-CoV-2. En el instante en el que el virus infecta el epitelio alveolar se genera activación de macrófagos alveolares, quimiotaxis de neutrófilos mediado por citoquinas y activación plaquetaria con la subsecuente formación de fibrina. En el momento de la lesion endotelial, los neutrófilos activados fagocitan al virus, pero también atrapan la fibrina extravasada, generando así proteólisis de la misma y como resultado elevación sérica del dímero D27,28,29.
En consecuencia, a lo anterior descrito, se podría disernir que el mecanísmo fisiopatológico por el cual se afecta el sistema respiratorio y hematológico, es secundario la activación de los altos niveles de citoquinas proinflamatorias (IL-2, IL-7, factor estimulador de granulocitos, MCP1, MIP1A, IP10 y FNT-a), las cuales inducen la triada de Virchow: estado hipercoagulable, injuria endotelial y estasis del flujo sanguíneo. Estos hallazgos se han encontrando ampliamente en los pacientes hospitalizados en unidad de cuidados intensivos30. El sistema respiratorio también exhibe consecuencias de la traida de Virchow, como es el daño alveolar difuso que conlleva al SDRA producido por el SARS-COV, el cual se podría explicar por la fibrinolisis secundaria, asociado a un incremento en la actividad plasminógeno-plasmina y el posterior aumento en los depósitos alveolares de fibrina. Esta evidencia se obtuvo de estudios preliminares en modelos animales infectados por SARS-CoV y actualmente se sugiere que podrían compartir el mismo mecanísmo fisiopatológico con el actual SARS-CoV-231.
En una serie de casos reportados por Yao, et al. histológicamente demostraron la presencia de microtrombos asociados a lesión alveolar difusa en pacientes con SDRA por COVID-19, sumado a la presencia de microtrombos glomerulares a nivel renal32. Entonces aparece el concepto de tromboinflamación, el cual se refiere a la íntima interacción que existe entre las diferentes vías o mecanismos de inflamación que incluyen a la IL6, complemento, PAMPs, NETs, polifosfatos y otras citoquinas, con la subsecuente activación de los factores de la coagulación y la eventual micro o macrotrombosis33,34.
Curiosamente y diferente a otras entidades infecciosas, la coagulopatía asociada a COVID-19 consumé poco los factores de la coagulación, con niveles normales o elevados de fibrinógeno y ocasionalmente trombocitopenia, por lo que sugiere un perfil trombogénico contrario a la CID, donde predomina más la fibrinólisis y una tendencia a la hemorragia, y que se presenta en aproximadamente el 38 % de los pacientes críticos con COVID-1935,36.
Este perfil trombogénico ha llevado al planteamiento de multiples mecanismos fisiopatológicos que expliquen esta entidad. Obviamente la inflamación endotelial es uno de ellos, generando altos niveles de antígeno del factor de von Willebrand (vWF:Ag) y el factor de coagulación VIII (FVIII), generando una cascada procoagulante. La vasoconstricción secundaria a la hipoxemia en los capilares pulmonares, conlleva a la reducción del flujo sanguíneo y oclusión vascular37. En recientes publicaciones sugieren la activación del complemento como un mecanismo procoagulante asociado, y se presenta en respuesta a la lesión endotelial, generando niveles altos de C5a y así promoviendo la activación del factor tisular y su unión al factor VII (F. VII), aumentando los niveles del factor Xa, trombina y fibrina, configurando la triada de Virchow antes descrita38. Prueba de ello, en un reporte de casos se encontró lesiones tromboembólicas microvasculares generalizadas que afectaban los pulmones y la piel, y estas estaban mediadas por el complemento. En dichas lesiones se aisló grandes depósitos del complejo C5b9, C4b y MASP2, siendo el primero una característica que comparte con síndromes microtromboticos como el síndrome hemolítico urémico, síndrome antifosfolípidos y la purpura fulminante39,40,41,42.
Por todo lo anteriormente descrito, la infección viral por SARS-CoV-2 en la fase grave de la enfermedad, se asocia con coagulopatía, exhibiendo un comportamiento clínico y paraclínicos similar a la coagulopatía inducida por sepsis. Si bien, la incidencia de enfermedad tromboembólica venosa (TEV) en la neumonía grave por SARS-COV2 está alrededor del 25 %, y que no difiere de la incidencia de TEV en los pacientes críticos (alrededor del 13 al 30 %), cabe resaltar que un registro reciente reportó una tasa de incidencia del casi el 70 % de trombosis venosa profunda periférica (TVP) y del 23 % de embolia pulmonar (EP)43,42,43,44.
Una cohorte prospectiva en pacientes con COVID-19 que ingresaban a UCI por falla respiratoria aguda hipoxémica, evidenció una alta prevalencia de tromboembolismo pulmonar (16,7 %) a los pocos días de su estancia, a pesar de tener tratamiento anticoagulante profiláctico o anticoagulación a dosis plena45. Durante un estudio en China, donde se realizó el score de Padua para evaluar el riesgo tromboembólico, se encontró que los pacientes con COVID-19 con alto riesgo tenían un pobre pronóstico comparado con los pacientes con bajo riesgo46. Todo lo anterior sugiere la necesidad de estrategias diagnósticas dirigidas a la detección temprana y así al tratamiento oportuno de complicaciones tromboembólicas en los pacientes con SARS-CoV-247.
Otras complicaciones tromboembólicas que cabe mencionar en los pacientes con COVID-19, son el accidente cerebrovascular isquémico y síndrome coronario agudo, aunque estos son de menor frecuencia comparados con la embolia pulmonar y TEV periférico35,48. En un reciente reporte de caso, se describió el priapismo como otra posible complicación tromboembólica en pacientes con COVID-19, y que requirió manejo emergente (Aspiración de sangre cavernosa e inyección de un agente simpaticomimético a nivel intracavernoso)49.
Por estas razones, la tromboprofilaxis rutinaria y la anticoagulación, son estrategias a considerar en el arsenal terapéutico de esta enfermedad, equilibrando el riesgo de sangrado. Se sabe que la tromboprofilaxis en pacientes críticamente enfermos reduce hasta el 50 % los eventos tromboembólicos venosos50,51.
Los resultados iniciales indican un posible beneficio clínico con las heparinas de bajo peso molecular (HBPM) en las infecciones graves por COVID-19. Tang, et al. en un estudio retrospectivo de 449 pacientes, evaluaron la intervención con HBPM o heparina no fraccionada (HNF) y su impacto en la supervivencia a los 28 días. Así, el uso de ésta estrategia terapéutica tiene un efecto protector en la supervivencia (OR: 0.44 IC (0,22-0,85), p=0,017), logrando su mayor impacto en pacientes con dimero D mayor de 6 veces el límite superior de la normalidad (LSN) y un score SIC >o=452. La escala SIC, de sus siglas en inglés (Sepsis-induced coagulopathy), fue validada por Iba, et al. con el objetivo de predecir una CID inducida por28. Por ende, se resalta la importancia de una intervención terapéutica temprana con anticoagulantes, donde ha demostrado mayor beneficio (ver Figura 1 adaptada de recomendaciones en china y EEUU)53,54.
En 4 registros clínicos con un total 387 pacientes con COVID-19, donde se tenía como objetivo relacionar el dímero D, conteo de plaquetas y tiempo de protrombina en presencia de una condición severa de la enfermedad, se evidenció claramente la asociación de niveles elevados de dímero D con la severidad de dicho cuadro clínico. No obstante, no fue posible relacionar las variables anteriores con los niveles de plaquetas y tiempo de protrombina, puesto que estos pacientes manejaron valores normales independientemente de la gravedad de la infección (ver Tabla 1)25,55,56,57). Sumado a la evidencia descrita, una revisión sistemática de 9 estudios clínicos realizada por Violi, et al. encontraron una relación entre los niveles de dímero D elevados y la mortalidad de los pacientes con COVID-19, no siendo así con el recuento de plaquetas, tiempo de protrombina y la gravedad del espectro clínico58.
Tratamiento
A pesar de la poca evidencia existente con alto nivel estadístico del beneficio absoluto de la terápia anticoagulante y tromboprofilaxis, contamos con investigaciones que apoyan esta hipótesis, como lo demostró Tang, et al. 52 Adicionalmente las guías de manejo recomendan la anticoagulación o tromboprofilaxis sobre la ausencia de tratamiento59,60,61.
En consecuencia, en todos pacientes hospitalizados en sala general y unidad de cuidados intensivos, en ausencia de complicaciones tromboembolicas y contraindicaciones para la terapia, se recomienda la tromboprofilaxis con heparina de bajo peso molecular, heparina no fraccionada y el fondaparinux61. Cabe resaltar, que existe preferencia sobre la heparina de bajo peso molecular y la heparina no fraccionada frente el fondaparinux, sobre todo en el paciente crítico59,60. No se recomienda el manejo antiplaquetario como prevención de TEV61.
En pacientes sin evidencia clínica de TVP o PE, no se recomienda la tromboprofilaxis ambulatoria al momento del alta. Sin embargo, se debe considerar tromboprofilaxis en pacientes con bajo riesgo de sangrado y alto riesgo de TEV, dado por Padua score > o = 4, dimedo D > 3000 ng/ml o que haya cursado con formas graves de COVID-19 asociado a alguna de las siguientes: ferritina >1000 ng/ml, IL-6 > 40 pg/ml, linfopenia <800/mm3 y dimero D >1500 ng/ml. En los pacientes con TVP/EP confirmado, sin interección medicamentosa, se sugiere la anticoagulación con apixaban, dabigatran o rivaroxaban por 3 meses61.
En los casos de diagnóstico positivo para TVP/ EP en pacientes en hospitalización general o UCI, sin choque o falla cardíaca derecha, se sugiere la anticoagulación parenteral con heparina de bajo peso molecular o heparina no fraccionada. Los pacientes con complicaciones tromboembólicas asociadas a choque o falla cardiaca derecha, se recomienda la trombolisis sistémica. En la administración de la terapia trombolítica se prefiere el uso de un acceso periférico frente al acceso central61.
Se aconseja no realizar la búsqueda activa de complicaciones tromboembólicas en pacientes asintomáticos o sin sospechas de EP. En los pacientes con episodios de TVP/EP recurrente con COVID-19, a pesar del tratamiento anticoagulante con heparina de bajo peso molecular, se recomienda aumentar la dosis en un 25 al 30 %. En los casos de anticoagulación con anticoagulantes orales y persistencia de complicaciones tromboembólicas, se sugiere el cambio a esquema con heparina de bajo peso molecular61.
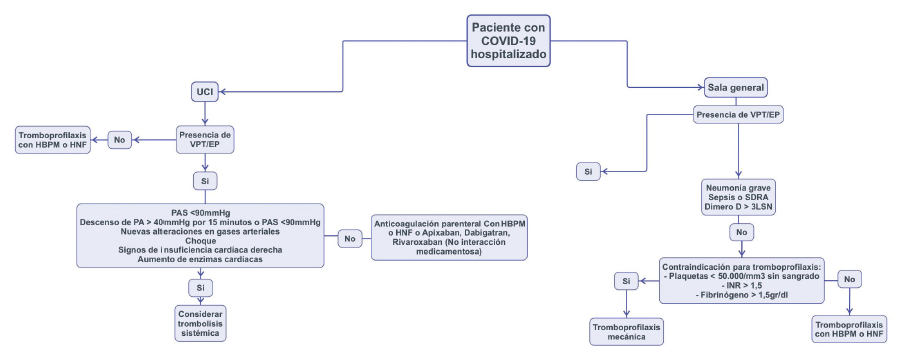
En la Figura 1 abajo planteamos un algoritmo de abordaje de pacientes con COVID-19 dependiendo de su estancia hospitalaria y la presencia de TVP y/o EP. En las Tablas 2 y 3 se describen las dosis profilácticas de heparina de bajo peso molecular.
Conclusión
En conclusión, existe evidencia que en fase avanzada de COVID-19 hay un riesgo aumentado de coagulación intravascular diseminada, parecido a lo observado en la coagulopatía inducida por sepsis, pero con un fenotipo predominantemente trombótico. Por lo tanto, el manejo con heparinas debe ser considerado como una estrategia terapéutica. Continuamos con la necesidad de futuros estudios que indagen interrogantes en el paciente COVID-19 hospitalizado, especialmente que definan, evaluando riesgo/beneficio, que se justifica o no con respecto a la anticoagulación plena en algunos pacientes específicos con COVID-19.