1 Introducción
La producción ganadera posee una importancia abrumadora, debido a que es fuente para el sustento de familias rurales, con el paso del tiempo esta se ha visto afectada por la presencia de ectoparásitos como es el caso de las garrapatas. Las garrapatas son artrópodos hematófagos consideradas como el grupo más importante de patógenos que causan enfermedades porque se pueden encontrar en hábitats muy variados, desde los más secos hasta los más húmedos y sobrevivir durante varios años sin alimentarse [1]. Se estima que aproximadamente mil millones de bovinos se encuentran en zonas tropicales y subtropicales a nivel mundial, los cuales son expuestos a las infestaciones por garrapatas y/o agentes patógenos que transmiten los cuales pueden o no causar enfermedad, generando pérdidas significativas en la producción pecuaria [2]. R. (B) microplus es la especie con mayor incidencia en Colombia y es considerada como uno de los factores sanitarios más importantes que limita la ganadería, porque posee la capacidad de transmitir patógenos causantes de enfermedades relevantes para los animales, como Babesia spp y Anaplasma spp [3], causando pérdidas directas e indirectas a los animales y productores al evidenciarse disminución en la ganancia de peso, anemia, lesiones en piel, costos en tratamientos reproductivos y disminución en la producción de carne y leche [4].
A nivel mundial se estiman pérdidas económicas de aproximadamente US$7 billones, de los cuales un billón de dólares corresponde a Latinoamérica [5]; en Colombia calculando una población bovina aproximada de 20 millones de cabezas, y una pérdida calculada por cabeza/año de US$7,3, las pérdidas se encuentran alrededor de los US$146 millones [6]. El control seguro y efectivo de las garrapatas se ha vuelto fundamental para la producción pecuaria y en la salud humana, por lo que se han manejado diferentes estrategias como el uso de vacunas, hongos, y productos químicos sintéticos, siendo este último es el método más empleado [7]. Sin embargo, el uso indebido e indiscriminado, la rigurosidad en el mecanismo de aplicación de los productos, la frecuencia de aplicación, la selección y rotación de moléculas acaricidas y la falta de una base epidemiológica para el control de los ectoparásitos, ha propiciado a la generación de resistencia a los medicamentos en todas las especies de garrapatas, dificultando su control [8].
Ante esta problemática es necesario encontrar alternativas para controlar las infestaciones de garrapatas en el futuro, las cuales puedan contribuir en la disminución de los costos de producción, que sean seguras y no afecten negativamente al medio ambiente. A raíz de esto, se ha presentado un gran interés de investigar las propiedades acaricidas de un gran número de especies de plantas que poseen acción repelente [9, 10].
De acuerdo a estas consideraciones, este estudio tiene como objetivo determinar la eficacia in vitro de Phytolacca bogotensis (guaba) y Alnus acuminata (aliso) en el control de la garrapata adulta R. (B) microplus y brindar una alternativa de control natural.
2 Materiales y métodos
El estudio fue de tipo in vitro y se desarrolló en tres fases. La primera se basó en la recolección de las plantas y la elaboración de los extractos. La segunda fase consistió en la colecta de garrapatas de bovinos parasitados naturalmente en el municipio de Nuevo Colón y el mantenimiento de las mismas y la tercera fase, comprendió la evaluación de la eficacia ixodicida de cada extracto y sus diluciones, en la exposición de las garrapatas adultas R. (B) microplus.
2.1 Material Vegetal y Preparación de extractos
Se seleccionaron dos plantas: P. bogotensis y A. alcuminata, que fueron recolectadas en la Granja la María de la Universidad Pedagógica y Tecnológica de Colombia (UPTC), ubicada en la ciudad de Tunja localizada en la región del Altiplano Cundiboyacense, sobre la Cordillera Oriental de los Andes, con una altura promedio de 2.804 msnm, con 50 32'07" N y 73° 22'04" O, temperatura media anual de 12,8°, precipitación media de 917 mm y humedad relativa media que oscila entre 77 y 83%.
Se recolectaron únicamente las hojas de las plantas en floración, siendo cortadas de forma manual con tijeras hasta alcanzar una cantidad superior a 5 kg y se transportaron en bolsas de papel hasta el laboratorio de Nutrición Animal de la UPTC, para su respectivo secado donde fueron separadas y se mantuvieron a temperatura ambiente, en un lugar aireado, cubierto y seco.
El método empleado para la elaboración de los extractos de las plantas analizadas fue la extracción en caliente "Soxhlet". El material vegetal se fraccionó, con el fin de aumentar la superficie de contacto del solvente con el material para facilitar la mayor disolución de principios activos. Se tomó aproximadamente 200 gr de cada planta y se colocaron en la cámara de extracción del equipo Soxhlet, luego se calentó el etanol situado en el recipiente contenedor evitando que llegara a ebullición; el vapor del solvente ascendió hasta el condensador, dando como resultado el extracto vegetal.
Para dicha extracción se emplearon 150 mL de solvente (etanol al 96% de pureza), de los cuales se recuperó aproximadamente el 50% mediante concentración en el rotaevaporador a una temperatura de 78°C y 60 rpm, el producto final fue de 20 mL de extracto puro.
Se sometieron los extractos obtenidos a cuatro pruebas para la determinación de metabolitos secundarios. Se inició con la prueba de reacción de saponinas, en el cual para cada extracto se diluyó 5 veces su volumen en agua destilada, se agitó durante 30 segundos y se dejó en reposo durante 15 minutos, luego se evaluó la proporción de saponinas respecto a la altura de la espuma sobrenadante [11]. Para la identificación de flavonoides, se realizó la prueba de Shinoda, la cual consistió en agregar de forma lenta limaduras de magnesio al extracto, seguido de ácido clorhídrico; después de 2 min se esperó un cambio de coloración verde violeta lo que indica positivo a flavonoides [12]. En relación con la identificación de alcaloides, se llevó a cabo por medio de la prueba de Wagner, en el cual se adicionan 2 gotas de reactivo Wagner (yodo, y yoduro de potasio), se agitó y se esperó 2 min con el fin de observar un cambio de coloración [13]. Por último, se procedió a la identificación de cumarinas mediante la reacción Legal, adicionando 2 mL de solución de nitroprusiato de sodio 0.5% y 2 gotas de KOH 2N en cada una de las muestras de extractos, se esperó a la presencia de una coloración roja, que se interpreta como positiva [14].
2.2 Recolección y mantenimientos de Garrapatas
Las garrapatas adultas R. (B.) microplus, se colectaron de animales parasitados naturalmente, en Nuevo Colón, municipio que pertenece a la provincia de Márquez, Ventaquemada y Rondón, localizada a los 05° 21' 30" de latitud norte y 73° 27' 38" longitud oeste, a una altura de 2.500 msnm; temperatura media anual de 16 °C. Posteriormente se colocaron en envases de vidrios para ser transportadas al laboratorio de Nutrición animal de la UPTC. Las garrapatas se lavaron con agua para retirar los restos de materia orgánica, y se sumergieron durante un minuto en una solución de hipoclorito de sodio al 1% para desinfectarlas y evitar una posible contaminación, seguido se secaron suavemente con papel absorbente y se pesaron individualmente con el fin de obtener el peso promedio y conformar grupos homogéneos [15]; se descartaron garrapatas lesionadas, que tuvieran alguna alteración de consistencia o color y se identificaron como R. (B) microplus utilizando las claves taxonómicas descritas por [16]. Una vez en el laboratorio las garrapatas fueron mantenidas en una cámara bajo condiciones controladas a temperatura constante de 27 °C y humedad relativa (HR) de 85%.
Las garrapatas previamente seleccionadas se dividieron al azar teniendo en cuenta características como peso aproximado de 1 gr ± 0,10 y un tamaño de 5 a 8 mm, para conformar grupos de 10 garrapatas y 3 repeticiones.
2.3 Evaluación del efecto ixodicida de los extractos puros y las diluciones
La exposición de las garrapatas, se realizó mediante, la técnica de inmersión de adultas descrita por Drummond [17]. Se depositaron 5 mL del extracto (puro o dilución) en una caja de Petri, seguido se depositaron allí las garrapatas (n = 10), las cuales se sumergieron completamente durante 15 minutos en el extracto con la ayuda de una aguja punta roma, evitando el daño en la cutícula. Al terminar este periodo de tiempo, se retiró el extracto en su totalidad, dejando así, las garrapatas en un medio seco. Las cajas fueron tapadas con un lienzo, rotuladas exteriorizando el nombre del extracto, dilución y hora de exposición [18].
Los extractos se probaron mediante el modelo experimental de mínimas y máximas de efectividad biológica, es decir la mínima concentración a la cual se consigue efectividad y la máxima concentración a la cual se consigue su efecto, por lo que la concentración del extracto se aumentó o disminuyó. Las diluciones se realizaron con agua destilada a partir del extracto puro de cada planta, se efectuó una dilución 1:2, si esta superaba una mortalidad del 60% (tomada como mínimo eficaz), esta dilución se disminuyó a una concentración 1:4, y así sucesivamente hasta que no mostrara efectividad. De la misma forma, y siguiendo la metodología para la exposición de las garrapatas a los extractos, se trabajó con un grupo control positivo, en el que se utilizó un ixodicida comercial a base de cipermetrina al 15% preparado según las indicaciones de la etiqueta (dilución 1:1000 en agua). Se contó con tres grupos control negativo, un grupo no expuesto a sustancias, otro empleando agua y el último expuestos a etanol al 96%.
La mortalidad se evaluó a las 24, 48, 72 y 96 horas post aplicación del extracto, en donde se consideró como garrapatas muertas, aquellas que al ser expuestas a una fuente de calor (Lámpara halógena 6 V; 25 W), durante 10 min mostraran ausencia de movimiento en sus patas. Se tomó como valor mínimo de eficacia, una mortalidad del 60%, valores por debajo de este rango fueron tomados como ineficacia y se tomó como valor aceptado una mortalidad no mayor al 10% en los grupos control de lo contrario se sospecharía de una inadecuada manipulación del material [19].
Se realizaron observaciones diarias y se llevó un seguimiento de los datos; hasta lograr calcular la eficacia de los extractos naturales en la supervivencia de las garrapatas, tanto de los grupos control como de los grupos experimentales, de la siguiente manera:
La eficacia de mortalidad de los extractos fue evaluada a través, de la mortalidad de teleoginas del grupo control y de cada tratamiento con la siguiente formula:
gc: Grupo Control y gt: Grupo Tratado.
2.4 Análisis estadístico
El experimento se desarrolló empleando un diseño completamente al azar con un análisis multivariado. El análisis de datos se realizó por medio del programa SPSS versión 23. Los porcentajes de mortalidad fueron sometidos a los supuestos de normalidad a través del estadístico de Shapiro-Wilk y homogeneidad por prueba de Levene. Comprobados los supuestos se realizó un análisis de varianza (ANOVA), y las diferencias estadísticas se determinaron mediante la prueba de comparación de medias de Tukey (p < 0,05).
3 Resultados y discusión
Una vez obtenidos los extractos puros de P. bogotensis y A. alcuminata, se presentaron características físicas diferentes, el extracto de guaba presento un olor característico a la planta de origen y un color verde pasto y el aliso mostró un olor a melaza y un color marrón oscuro, todos los extractos presentaron aspecto líquido.
3.1 Análisis preliminar de metabolitos secundarios
Se evidenció la presencia de cumarinas en ambas plantas y variación de los demás metabolitos (tabla 1).
Tabla 1 Metabolitos secundarios en los extractos
| Extracto | Saponinas | Alcaloides | Cumarinas | Flavonoides |
|---|---|---|---|---|
| A. acuminata | - | + | + | - |
| P. bogotensis | + | - | + | + |
Nota: (+) = positivo, (-) = negativo
Fuente: Autores
Los alcaloides, esteroides, terpenos, fenil-propanoides, lignanos, flavonoides y amidas destacan como moléculas bioactivas prometedoras de las plantas para el control de las garrapatas [20]. Se ha reportado que la especie Phytolacca, contiene dos triterpenos pentacíclicos y cinco saponinas triterpénicas; la presencia de estas saponinas puede explicar su utilidad en el control de las garrapatas [21].
3.2 Evaluación de la mortalidad con el extracto de P. bogotensis
Se observa una mortalidad acumulada en aumento desde las 48 hasta las 96 horas post-aplicación, en el extracto puro y sus diluciones. Se prepararon 2 diluciones, 1:2 y 1:4 con las que se presentaron mortalidades de 66,6% y 40% respectivamente, y con el extracto puro una mortalidad del 80% a las 96 horas, observándose diferencias estadísticas significativas (p < 0,05) con el extracto puro y la dilución 1:2 (figura 1).

Nota: Promedios con letras distintas indican diferencias significativas (P < 0,05).
Figura 1 Mortalidad de la garrapata R. (B) microplus expuesta a extracto de P. bogotensis
El extracto de P. bogotensis, alcanzó resultados efectivos teniendo en cuenta que la eficacia de mortalidad mínima para este estudio fue del 60%, llegando a obtener mortalidades del 80%, 66,6% y 40% con el extracto puro y sus diluciones respectivamente. Al determinar la presencia de saponinas y flavonoides en el extracto, se puede afirmar que estos componentes se encuentran altamente ligado a las mortalidades presentadas, ya que son sustancias que interrumpen el proceso de alimentación de la garrapata tras un consumo inicial del extracto y conducen a la muerte por inanición o intoxicación [22]. Se ha evidenciado que P. bogotensis presenta metabolitos secundarios como saponinas, cumarinas y flavonoides, obteniendo la mayor eficacia en el control de garrapatas, demostrando una mortalidad acumulada en aumento usando la raíz y la hoja en el extracto puro y sus diluciones [9].
Sin embargo, otros autores atribuyen este efecto acaricida a la presencia de cumarinas en los extractos [23, 24]. Las cumarinas son potentes inhibidores de la coagulación actuando sobre las serina proteasa envueltas en la activación del factor XII de coagulación [25], su capacidad acaricida se ha asociado a la inhibición de enzimas digestivas que pertenecen a las endopeptidasas tipo serina, cisteína, aspartato, metaloproteasas, tripsina, quimotripsina y catepsinas, enzimas con capacidad proteolítica de R. microplus quienes son las encargadas de la digestión de la hemoglobina y actúan como proteínas de reserva durante la embriogénesis [26].
3.3 Evaluación de la mortalidad con el extracto de A. acuminata
El extracto puro de A. acuminata (aliso), no supero el mínimo de eficacia de mortalidad (60%), teniendo como resultado una mortalidad acumulada a las 96H de 53,33% (figura 2).

Nota: Promedios con letras distintas indican diferencias significativas (P < 0, 05)
Figura 2 Mortalidad de la garrapata R. (B.) microplus expuesta a extracto de A. acuminata.
En el extracto natural de A. acuminata, no hubo presencia de saponinas y flavonoides, lo cual difiere con lo reportado por Amado & Chocontá [27], quienes evidenciaron la presencia de cumarinas, flavonoides y saponinas en hojas y corteza. La ausencia de estos compuestos en este estudio, pudo presentarse por diferentes factores como las condiciones ambientales, tipo de suelo y manejo del cultivo ya que estos aspectos pueden variar la composición química de la planta [28].
Teniendo en cuenta que para este estudio la eficacia de mortalidad fue de 60%, se observa que los resultados para A. acuminata no fueron los esperados, presentando mortalidades inferiores, esto posiblemente a que no hubo presencia de flavonoides, y saponinas en el análisis cualitativo de metabolitos. Se conoce que estos dos componentes poseen actividad acaricida sobre R. (B.) microplus al interrumpir su alimentación [29, 30]. Por su parte, González et al., [31] determinaron la presencia de flavonoides y taninos mediante placas analíticas de cromatografía en tres genotipos de Leucaena spp. y observaron mortalidades de 91,68, 82 y 54,06% con diferentes concentraciones de los extractos en larvas y de 50% en garrapatas adultas de la especie de R. (B.) microplus, relacionando la presencia de estos metabolitos secundarios con las mortalidades observadas.
Sin embargo, Pulido et al., [9] reporta que el extracto de A. acuminata obtenido por el método Soxhlet mostró un porcentaje de inhibición de la ovoposición de R. (B.) microplus de 98,88% y la presencia de alcaloides y cumarinas. Se conoce que los alcaloides poseen gran importancia por su actividad contra el ataque y proliferación de insectos, han demostrado fuerte toxicidad contra larvas de crustáceos de mar como Artemia salina y del mosquito Aedes aegypti, vector del virus causante de la fiebre amarilla [32]. Al evidenciar que los componentes activos de las plantas pueden variar por múltiples factores, es recomendable, estudiar la acción de esta planta utilizando diferentes partes de la ella, cultivada en varios ambientes y con otros métodos de extracción.
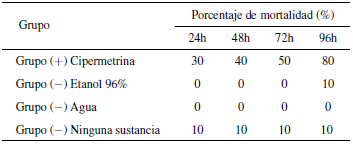
En los grupos control, para el caso de la cipermetrina se observó una mortalidad del 80% y para los grupos control negativo, se observó una mortalidad no mayor al 10%, esto indica que no intervinieron factores ambientales en la mortalidad de las garrapatas de los grupos tratados (tabla 2.)
4 Conclusiones
Teniendo en cuenta que los componentes activos de las plantas pueden variar por múltiples factores, es recomendable, estudiar la acción ixodicida de diferentes partes de las plantas, además de muestras cultivadas en diversos ambientes, con varios métodos de extracción. Se evidencia que el extracto natural de P. bogotensis posee una acción efectiva como acaricida y que, en las condiciones planteadas en la investigación, puede constituirse como fuente de principios activos que contribuyan al descubrimiento de ixodicidas de origen natural, los cuales pueden ser utilizados como línea base para la síntesis de moléculas útiles a nivel farmacéutico. Es necesario trabajar este extracto en los diferentes estados del ciclo biológico de R. (B.) microplus, y en condiciones in vivo, e in-suto que permitan comparar los resultados obtenidos en este estudio.