INTRODUCCIÓN
Scomberomorus sierra (Jordan y Starks) o sierra castilla, como es llamada por los pescadores en el Pacífico de Colombia, es una especie pelágica, altamente migratoria que forma bancos numerosos y se encuentra entre 2 y 63 m de profundidad (Rubio, 2007; Vega et al, 2013). Se distribuye desde la costa del golfo de California (México) hasta Perú (Collette, 1995) y en el Pacífico colombiano se ha registrado en los departamentos del Chocó (municipios Cupica, Cabo Marzo, Bahía Solano, Charambirá y golfo de Tribugá), Cauca (isla Gorgona) y Nariño (municipios Tumaco y Francisco Pizarro) (Invernar et al, 2006, 2009; IIAP, 2007; Tobón-López et al, 2008). Aproximadamente 85% de la población de la costa del Pacífico de Colombia manifiesta el sustento directo o indirecto de la pesca artesanal (INPA, 2000; Ministerio de Comercio, Industria y Turismo, 2000; Marviva, 2011; Incoder, 2013) y la sierra castilla se encuentra entre las especies ícticas de mayor explotación en este tipo de pesca (Castillo, 1998; Rubio, 1988; De la Hoz et al, 2015). Para 2006, 2007 y 2009 fue el recurso más abundante con capturas de 375.80, 463.00 y 562.90 t, respectivamente (CCI et al, 2006; CCI y MADR, 2007, 2009). En 2013 representó 17% del total de captura de peces (634.16 t) y en 2015 79%, reiterando a través del tiempo su importancia como recurso comercial (Aunap y Universidad del Magdalena, 2013; De la Hoz et al, 2015).
Para el manejo de recursos pesqueros, aspectos reproductivos como la madurez gonadal pueden ser evaluados directamente en cualquiera de las etapas de desarrollo de los peces, examinando las gónadas en escala macroscópica o realizando cortes histológicos que proporcionan información más detallada (Icon-Institut, 2009). Esta información permite obtener indicadores de la actividad reproductiva (Vega et al., 2013) y asociado a ello se pueden establecer épocas y sitios determinados de reproducción. Por otra parte, el estudio de la fecundidad analizada en conjunto con variables morfométricas contribuye al conocimiento del potencial reproductivo de una especie, y es fundamental en el entendimiento de la dinámica de las poblaciones explotadas, generando herramientas para la evaluación y diseño de estrategias en el manejo y la conservación de los recursos pesqueros (Murua et al., 2003; Saborido-Rey, 2004; Arellano-Martínez et al,, 2006; Camacho, 2011).
A pesar de la importancia comercial de la sierra castilla en Colombia, poco se conoce sobre su biología reproductiva. En este sentido, el presente manuscrito tuvo como objetivo estimar la fecundidad y describir el desarrollo ovocitario de S. sierra en el Pacífico colombiano, como aspectos reproductivos de la especie que pueden ser usados por las instituciones competentes en el manejo del recurso.
El Pacífico colombiano se localiza geográficamente desde la zona norte en los límites con Panamá, siguiendo por Juradó y el golfo de Tribugá, Chocó, continuando hacia la zona centro-sur por el golfo Tortugas, Buenaventura, Guapi, Sanquianga y la ensenada de Tumaco en el sur en Nariño, hasta la frontera con Ecuador (Tobón-López et al., 2008; Díaz et al., 2011; Rodríguez et al., 2015). La sierra castilla es capturada en toda la costa del Pacífico con énfasis en los puntos de desembarco más importantes de la pesca artesanal, sobre la base de los volúmenes de captura (Buenaventura, Tumaco, Guapi y Bahía Solano: CCI et al, 2006; CCI y MADR, 2009; De la Hoz et al, 2015). Las embarcaciones que se utilizan en la pesca artesanal son canoas que se impulsan con remos o velas, lanchas de madera o fibra de vidrio de 9 a 15 m de eslora con motores fuera de borda y las faenas pueden durar de 8 a 12 días (Buenaventura) o de 5 a 8 días (Bahía Solano) (CCI y MADR, 2011). Las principales artes de pesca utilizadas son la red de enmalle (66%), espinel (12%) y línea de mano (7%) y la sierra castilla es el principal producto íctico capturado por éstas (CCI y MADR, 2007; De la Hoz et al, 2015). Debido a lo anterior, se seleccionaron los puntos de desembarco de Utría, departamento de Chocó, Buenaventura, departamento del Valle del Cauca, Guapi, departamento del Cauca, Bazán y Tumaco, departamento de Nariño, para la colecta de material biológico.
MATERIALES Y MÉTODOS
Fase de campo
La temporada reproductiva de la sierra castilla para el Pacífico colombiano se da entre noviembre y abril (Castillo, 1998; Tobón-López et al., 2008; CCI y Ministerio de Agricultura y Desarrollo Rural, 2009; Rueda et al., 2011); por lo anterior, desde noviembre de 2013 hasta abril de 2014 en los diferentes puntos de desembarco seleccionados se compró el material biológico (sierra castilla). Con balanzas electrónicas (de 1 g de precisión), se registró el peso total de cada individuo en gramos (PT), se midieron (con precisión de ± 1 cm) la longitud total (LT), la longitud horquilla (LH) y la longitud estándar (LS), siguiendo el protocolo colombiano de mediciones pesqueras (Agudelo et al, 2011). Posteriormente, al retirar el contenido visceral, se obtuvo el peso del pez eviscerado (PEV) y se retiraron las gónadas, se fijaron con formol al 4% y se transportaron hasta el laboratorio para su posterior análisis.
Análisis en laboratorio
En el laboratorio las muestras gonadales fueron revisadas para verificar el sexo y estado de madurez sexual unificando los criterios de clasificación macroscópica de Nikolsky (1963), Castillo (1998) y Aguirre-Villaseñor et al. (2006), de tal modo que se trabajó con cinco estados de desarrollo (I: inmaduro, II: inicio del desarrollo, III: en desarrollo, IV: maduro, V: desovado). Las gónadas fueron separadas y pesadas (PG; con precisión de ± 0.0001 g). Para verificar el estado de desarrollo gonadal (Claramunt et al, 2009), se realizaron cortes histológicos de la parte media de uno de los lóbulos y se aplicó la técnica de tinción de hematoxilina-eosina (Muñetón-Gómez et al, 2000; Gómez-León, 2006). La clasificación microscópica correspondió a la representatividad de la célula en fase más avanzada y se realizó según los criterios de Wallace y Selman (1981), Vélez (1995), Lucano-Ramírez et al. (2001) y Saborido-Rey (2004). Sumado a esto, se describieron los estados gonadales encontrados durante el estudio. Mediante una cámara digital Nikon DS-Fi2 con controlador DS-U3 (DS: Digital Sight) ensamblada a un microscopio Nikon Eclipse E200 y el software NIS-Element-F Versión 4.0 ®, se obtuvieron fotografías de cortes histológicos de 20 ovarios para las mediciones de los oocitos en las diferentes etapas encontradas. Se empleó un total de 40 fotografías correspondientes a dos campos escogidos aleatoriamente de cada ovario, las cuales fueron analizadas mediante el programa de libre acceso Govocitos® y en total fueron contabilizados y medidos 1357 oocitos.
De 30 gónadas completamente maduras (estado IV) se tomó el otro lóbulo y se estimó la fecundidad siguiendo el método gravimétrico (Holden y Rait, 1974; Saborido-Rey, 2004), combinado con análisis de imágenes (Bustos-Montes et al, 2015). De la parte media de cada gónada se aisló una submuestra de 0.1 g en cajas de Petri, se agregó hipoclorito de sodio a 1.5% para que los oocitos se desprendieran uno de otro y aproximadamente a los 30 minutos se lavaron con agua, se colocaron sobre placas Bogorov, se observaron en el estereoscopio, y se realizó la separación manualmente hasta que la totalidad de la muestra se repartió en campos de conteo. Con la cámara Optikam Microscopy Digital USB Camera vinculada directamente al estereoscopio y el programa Optika Vision Pro®, se tomaron fotografías en un objetivo de 0.8X. Éstas se procesaron con el software de libre distribución Image J® siguiendo las pautas de Klibansky y Juanes (2008) y Camacho (2011). Para el conteo de los oocitos se usó la medición de diámetro promedio realizada por Castillo (1998), considerando para la estimación de fecundidad únicamente los oocitos encontrados entre 0.4 y 0.9 mm de diámetro.
Análisis de información
La fecundidad parcial (Fp), definida como el número de huevos que en una época reproductiva están preparados para desarrollarse y ser liberados (Saborido-Rey, 2004), se estimó mediante la ecuación Fp = [(No. x PG)/PM], donde, No es el número de oocitos contabilizados en la muestra, PG es el peso total gonadal y PM es el peso de la muestra gonadal, que en todos los casos fue de 0.1 g (Lucano-Ramírez et al. 2005). Para la estimación del diámetro, se midió la longitud de los ejes mayor y menor, con esto se calculó el diámetro geométrico para cada uno de los oocitos con la siguiente ecuación (Camacho, 2011): diámetro oocito (mm) = [(longitud eje mayor (mm) * longitud eje menor (mm)] 0.5.
Se usaron como medidas de tendencia central y precisión el promedio y el error estándar, respectivamente. Para definir la función que mejor explicaba la relación entre las variables morfométricas (LT, LS, PT y PG) con la fecundidad parcial y el diámetro ovocitario se evaluaron modelos de regresión lineal, potencial y exponencial, que fueron comparados entre sí a través del coeficiente de determinación R2 y su nivel de significancia (Guisande-González et al, 2006). La talla de madurez sexual (LT50) entendida como longitud a la cual 50% de los individuos se encontraban maduros sexualmente, se modeló ajustando a la función logística PLT = 1/[1+e(aLT+b)] la proporción de hembras maduras (PLT) con intervalo de talla de 1 cm de LT. La curva se ajustó con mínimos cuadrados usando una regresión no lineal para estimar los parámetros a y b, y la LT50 se calculó con la razón -a/b (King, 2007), con un nivel de confianza de 95%.
RESULTADOS
Fueron capturados 79 ejemplares que midieron entre 39.0 y 85.0 cm LT (57.48 cm ± 0.93) y pesaron entre 300 y 2850 g PT (1033.67 g ± 55.16). Aunque a nivel macroscópico se determinó que eran 74 hembras y 5 machos, la validación a través del análisis histológico mostró que realmente eran 75 hembras y 4 machos. El análisis comparativo de la asignación del estado de madurez macroscópico con el microscópico, reflejó un bajo porcentaje de coincidencia 11.39% (n= 9), mientras las diferencias se vieron representadas por 88.61% (n=70). La imprecisión más frecuente se observó entre determinaciones macroscópicas de hembras en estado III que luego del análisis histológico resultaron ser hembras en estado IV (24.05 %, n =19) (Tabla 1).
Tabla 1 Sexo, estado de madurez, talla y localidad de captura de los 79 peces recolectados en el presente estudio. El porcentaje de diferenciación de la determinación macroscópica comparada con la microscópica, se realiza teniendo en cuenta que las confusiones posibles siempre se efectúan ubicando inicialmente el sexo y estado macroscópico.
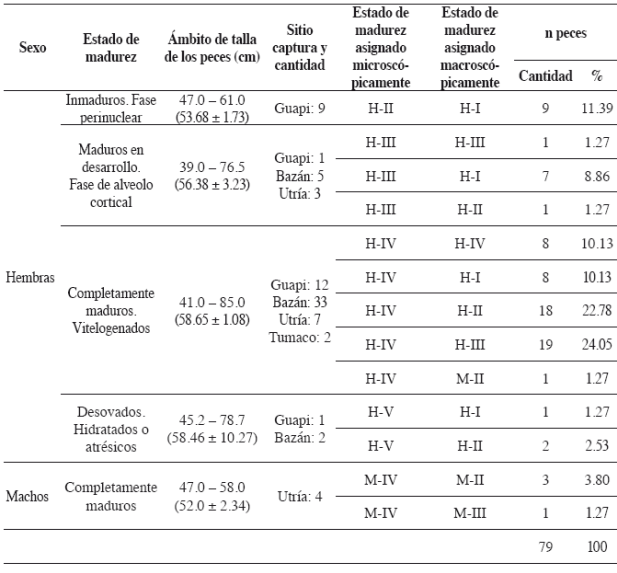
En Guapi las capturas fueron en noviembre de 2013 y se presentaron hembras en diferentes estados de madurez. Todos los machos se encontraron completamente maduros y únicamente aparecieron en la ensenada de Utría en enero de 2014. Durante el mismo mes en las capturas de Bazán dominaron las hembras maduras y en abril se recolectaron dos en Tumaco. Solo se evidenció desove en tres gónadas femeninas: una de Guapi en noviembre y dos de Bazán en enero (Tabla 1).
Se presenta la clasificación gonadal de los estados encontrados en el análisis histológico, el tamaño de los oocitos hace referencia al diámetro:
Estado II (Inmaduro): Macroscópicamente los ovarios son pequeños, de aspecto liso y vasos sanguíneos incipientes. A nivel microestructural, las células ováricas entran a una fase perinuclear, en la que los oocitos aumentan de tamaño (111.11 ± 1.65 um; n= 441), el citoplasma es basófilo y se encuentra bien definido. Se destaca la presencia de varios nucléolos pequeños ubicados en la periferia del núcleo (Figura 1). De las muestras colectadas se observaron nueve hembras en este estado (Tabla 1).
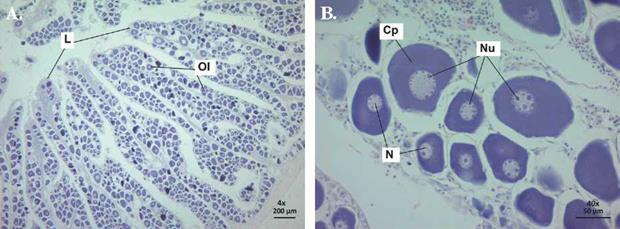
Figura 1 Microfotografía de ovario de Scomberomorus sierra en estado II (Inmaduro) en vista 4x (A) y 40x (B). L: lamelas, OI: ovocito inmaduro, Cp: citoplasma, N: núcleo, Nu: nucléolo.
Estado III (En maduración): Las gónadas son voluminosas y turgentes, con marcada irrigación y se observan huevos de color naranja. A nivel histológico, su principal característica es la vacuolización del citoplasma y la aparición de alvéolos corticales (vesículas que no presentan ninguna afinidad hacia los colorantes). En la fase inicial son pocos los alvéolos y se distribuyen en todo el citoplasma; sin embargo, a medida que avanza el desarrollo éstos tienden a ubicarse alrededor del núcleo (Figura 2). El diámetro promedio de los oocitos en esta etapa es de 168.75 ± 3.86 um (n= 145).
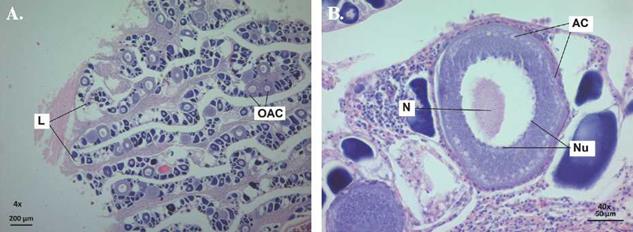
Figura 2 Microfotografía de ovario de Scomberomorus sierra en estado III (En maduración) en vista 4x (A) y 40x (B). L: lamelas, OAC: ovocito alveolo cortical, N: núcleo, Nu: nucléolo, AC: alvéolo cortical.
Estado IV (Maduros): En este estado los ovarios ya han alcanzado su máximo tamaño, con la irrigación sanguínea mucho más prominente con relación al estado anterior. Microscópicamente los oocitos aumentan considerablemente su tamaño (324.08 ± 5.89 |xm; n= 196), debido a la incorporación de vitelo en el citoplasma depositándose en forma de gránulos, vesículas y gotas lipídicas. Los pequeños gránulos de vitelo que se forma inicialmente se ubican por todo el citoplasma entre los alvéolos corticales y aumentan progresivamente (Figura 3). Se observaron un total de 54 hembras maduras en este estudio. En cuanto a los machos, a nivel macroscópico, el testículo tiene una apariencia laminar, de coloración blanca y textura lisa, con poca venación; histológicamente los cistos contienen grandes cantidades de espermatozoides bien diferenciados, aunque también se pueden observar algunos cistos de menor tamaño y proporción hacia la periferia de la gónada con espermatocitos en crecimiento secundario (Figura 3). Se observaron cuatro machos maduros con tallas que oscilaron entre 47.0 y 58.0 cm LT (Tabla 1).
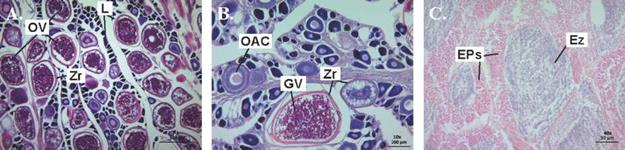
Figura 3 Microfotografía de ovario de Scomberomorus sierra en estado IV (Maduro) en vista 4x (A) y 40x (B). L: lamelas, OV: ovocito vitelogenado, Zr: zona radiada, GV: gránulos de vitelo, OAC: ovocito alveolo cortical. Microfotografía de testículo de S. sierra en estado IV (maduro) en vista 40x (C). EPs: Espermatocitos secundario, EZ: Espermatozoides.
Estado V (Desovado): Histológicamente se puede distinguir la presencia de oocitos hidratados (388.90 ± 8.81 |xm; n= 20) con forma irregular y de gran tamaño; además, se pueden observar oocitos en estados de desarrollo primario y secundario (perinuclear y alvéolos corticales) (Figura 4). Las tallas de las tres hembras analizadas están entre 45.2 y 78.7 cm LT.
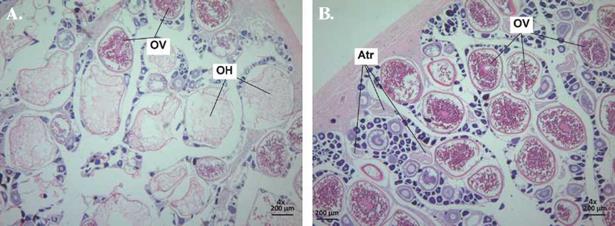
Figura 4 Microfotografías de ovario de Scomberomorus sierra en estado V (Desovado) en vista 4x (A y B). OV: ovocito vitelogenado, OH: ovocito hidratado, Atr: atresia.
A partir del conteo de 12084 oocitos se estimó que la fecundidad parcial (Fp) promedio fue de 194512 ± 21178 oocitos por hembra, con un ámbito de variación entre 52398 y 480803 oocitos por hembra. El tamaño ovocitario osciló entre 0.51 mm y 0.65 mm, con un promedio de 0.551 ± 0.024 mm. La relación entre la fecundidad parcial y las variables morfométricas fue en todos los casos significativa y se ajustó a una ecuación lineal para el caso de LT (Fp = 9255.3LT-363829, r2 = 0.8 F128=46.3, p < 0.05), LS (Fp = 1087.9LS-341163; r2 = 0.68, F128 = 50.1, p < 0.05) y PT (Fp = 161.28PT + 1465.3; r2 = 0.7, F128 = 65.5, p < 0.05), mientras que la relación con el PG (Fp = 5923.9PG0 8869; r2 = 0.76, F(128) = 87.2, p < 0.05) siguió un modelo potencial.
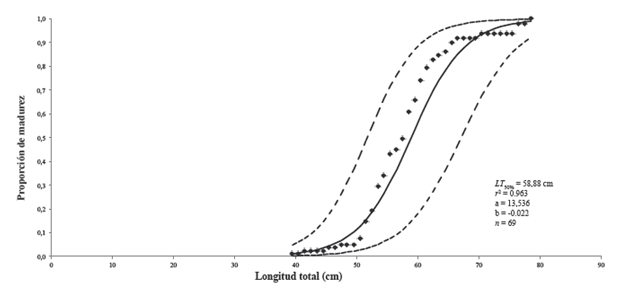
La ojiva de madurez se calculó con un total de 69 hembras maduras (estados de desarrollo III, IV y V). El modelo obtenido fue PLT = 1/[1+e(13.53LT -0.02)] y la talla media de madurez (LT50) se estimó en 58.8 cm de LT, con un amplio intervalo de confianza (51.6 - 67.0 cm de LT; Figura 5). Las hembras de menor y mayor talla con gónadas maduras midieron 39.0 y 85.0 cm LT, respectivamente (Tabla 1).
DISCUSIÓN Y CONCLUSIONES
Debido a que las muestras recolectadas en el presente estudio provenían de capturas comerciales de redes con luz de malla entre 7 y 18 cm (CCI y Ministerio de Agricultura y Desarrollo Rural, 2011; Rueda et al., 2011), la talla promedio de S. sierra registrada en este estudio (56.7 cm LT) es cercana a la media de captura registrada por las entidades que monitorean la pesca artesanal con fines estadísticos ([51 cm LT] AUNAP y Universidad del Magdalena, 2013). En otras áreas del Pacífico (Norteamérica), parece ser que la sierra castilla alcanza tamaños alrededor de 100 cm LT (Collette, 1995; Lucano-Ramírez et al., 2011; Robertson y Allen, 2015), aunque puede ser el efecto de la selectividad del arte empleado en cada investigación o a diferencias poblacionales. A pesar de haber hecho un esfuerzo de muestreo mensual en todos los sitios de desembarco elegidos, la mayoría de las hembras completamente maduras fueron recolectadas entre noviembre y enero, lo que pudo deberse a que muchas especies son más fáciles de pescar cuando se congregan para la reproducción, un fenómeno característico de muchos peces tropicales, en los que la disponibilidad de alimento y las temperaturas apropiadas también forman parte de las condiciones buscadas para el desove (Castillo, 1998; Lucano-Ramírez et al., 2011).
A diferencia de Lucano-Ramírez et al. (2011), se utilizó una escala de madurez macroscópica de cinco estados como propone Aguirre-Villaseñor et al. (2006), dado que no solo considera diferencias morfométricas, sino también la irrigación sanguínea periférica de la gónada, lo que resultó ser una característica clave para la asignación. El desarrollo gonadal es un proceso continuo y su división en estados discretos de madurez es difícil (Saborido-Rey, 2004), esto se evidenció principalmente en la separación entre las hembras en maduración y maduras (estados III y IV), lo que corrobora la importancia de la verificación con el análisis microscópico y la medición del diámetro de los oocitos como criterio adicional.
A nivel histológico, se reconocieron cinco fases de desarrollo oocitario, coincidiendo parcialmente con las descripciones propuestas por Saborido-Rey (2004) y Núñez y Duponchelle (2009). En el presente estudio, aunque en una gónada se presentaran oocitos en fase de vitelogénesis, perinuclear y alvéolo cortical, para la clasificación se tuvo en cuenta la representatividad de la fase de desarrollo más avanzada. Lo anterior puede explicar que se definieran menos estados de madurez comparado con Lucano-Ramírez et al. (2011), quienes identificaron siete en la sierra del Pacífico central mexicano. Se confirma que S. sierra presenta desarrollo asincrónico multiproporcional, ya que en ovarios maduros se observan oocitos en distintas fases (Saborido-Rey, 2004; Lucano-Ramírez et al, 2011), lo cual es propio de peces que desovan varias veces durante una sola temporada reproductiva prolongada (Wallace y Selman, 1981; Nagahama et al. 1995), como por ejemplo Scomberomorus commerson (Mackie et al, 2005).
La estimación del diámetro promedio de los oocitos maduros (0.551 ± 0.025 mm) por el método gravimétrico coincidió con la registrada por Lucano-Ramírez et al. (2011) de 0.500 mm. Estos valores son mayores a las medias obtenidas a partir de las mediciones en placas histológicas (324.08 mm oocitos maduros y 388.90 mm hidratados), porque los reactivos usados en los procesos de fijación e inclusión de las técnicas histológicas hacen que se reduzca el tamaño de las microestructuras. Las especies de fecundidades altas pueden llegar a tener miles y hasta millones de huevos, así como potencial reproductivo elevado (Hempel, 1979; Saborido-Rey, 2004). La sierra castilla mostró valores de fecundidad entre 52398 a 480803 oocitos por hembra, valores que parecen ser intermedios y que favorecerían su estrategia de desovador pelágico, donde los huevos son liberados al exterior como opción para asegurar la descendencia (Saborido-Rey, 2004).
La fecundidad puede variar considerablemente entre individuos de la misma especie y de la misma población hasta en un factor de diez entre un individuo y otro (Csirke, 1980), ya que el desarrollo gonadal se ve afectado por múltiples factores como la disponibilidad de alimento, las condiciones del medio ambiente, la condición energética de los parentales y el nivel de saturación de la población (Csirke, 1980; Murua et al., 2003, Alonso-Fernández y Saborido-Rey, 2011; Cooper et al, 2013; Ganias et al, 2014, 2015; Alfaro-Martínez et al., 2016). En este estudio, aunque el ámbito de la fecundidad parcial fue amplio, se observó una relación directa significativa y positiva entre las medidas morfométricas evaluadas y el número de los oocitos, mostrando que las hembras más grandes y pesadas produjeron una mayor cantidad de huevos, patrón que ha sido descrito para muchas especies ícticas en todos los ambientes (Vera de Mintzer y de Gonzo, 1991; Cerna y Oyarzún, 1998; Marteinsdottir y Begg, 2002; Urriola et al, 2004; Arellano-Martínez et al, 2006, Barros e Iwaszkiw, 2006; Murua et al, 2006; Villamil-Moreno y Arias-Castellanos, 2011, Cooper et al, 2013).
La talla media de madurez presentada en este estudio se estimó solo con 69 individuos, no se incluyeron individuos inmaduros y el intervalo de confianza obtenido es muy amplio, por lo que debe considerarse como una aproximación preliminar. El resultado de la LT50 (58.88 cm LT) es cercano al calculado por Lucano-Ramírez et al. (2011) en el Pacifico central mexicano (59.3 cm LT), y levemente mayor al registrado por Aguirre-Villaseñor et al. (2006; [52.1 cm LT]) en el golfo de California; sin embargo, los dos valores se encuentran dentro del ámbito de talla de madurez estimado en este estudio. Si bien algunas especies de la familia Scombridae pueden realizar migraciones transoceánicas y otras migran regionalmente por alimentación, reproducción y temperatura (Collette, 1995) se desconoce si la especie en el Pacífico oriental está estructurada genéticamente. Por otro lado, la condición maternal modula la variabilidad en los procesos de madurez gonadal en individuos de la misma especie y puede verse afectada por factores ambientales y antrópicos (Saborido-Rey, 2004; Alonso-Fernández y Saborido-Rey, 2011; Cooper et al, 2013; Ganias et al, 2014, 2015). Considerando lo anterior, las diferencias entre las tallas de madurez pueden deberse a que los estudios se realizaron en áreas, épocas y con artes de pesca diferentes.