Introducción
Debido a la exposición a factores medioambientales diferentes a los de su medio y al manejo en cautividad, las aves silvestres son propensas a desarrollar anormalidades del sistema cardiovascular que pueden comprometer su vida y su bienestar. El cambio de temperatura, la humedad, altitud y presión, al igual que la falta de ejercicio y dietas inadecuadas, pueden favorecer la presentación de enfermedades cardiovasculares como arterioesclerosis, hipertensión pulmonar y falla cardiaca congestiva, entre otras. La presentación de anormalidades cardiacas reportadas va desde el 9,7 hasta el 36% (Barreiro Lois et al., 2000).
A pesar de los recientes avances en la detección de enfermedades cardíacas en psitaciformes, todavía existen muchos factores que dificultan su diagnóstico. Generalmente los signos de un loro cardiópata no son específicos y el examen físico del sistema cardiovascular es limitado (Pees & Krautwald-Junghanns, 2009).
Antes de cualquier tipo de evaluación es necesaria la revisión anatómico-fisiológica de este grupo de aves donde el corazón está situado en la parte craneoventral de la cavidad celómica. El ápex cardiaco está rodeado de tejido hepático. Es un corazón de cuatro cámaras como en los mamíferos (Pees, Krautwald-Junghanns & Straub, 2003).
Como la resistencia en el flujo de la circulación pulmonar es mucho más baja el corazón derecho tiene unas paredes muy finas y forma semilunar sobre el corazón izquierdo con un tamaño mucho más grande para poder suplir las necesidades energéticas elevadas de las aves durante el vuelo. Algo que dificulta o no hace posible la evaluación del lado derecho del corazón (Richard & Couto, 2009).
Al contrario que en mamíferos, las aves tienen una válvula tricúspide en el corazón izquierdo, mientras que en el corazón derecho se encuentra una válvula atrioventricular (AV) rectangular única en las aves. La aorta tras su salida se divide en la aorta descendente y dos troncos braquicefálicos que irrigan las alas y la cabeza (Barreiro Lois et al., 2000).
Las aves pueden llegar a aumentar su frecuencia cardíaca hasta en 1000 lpm, para ello tienen un anillo atrioventricular adicional al nódulo AV para permitir una rápida despolarización de los ventrículos. Esto explica que el complejo QRS en aves es negativo. Ya que estas despolarizaciones tienen su origen en los ventrículos en lugar de atrios y, por lo tanto, la dirección de despolarización es opuesta (Pees & Krautwald-Junghanns, 2009).
Los métodos diagnósticos más frecuentes como la radiología, el electrocardiograma o la ecocardiografía pueden complicarse por: el tamaño reducido de algunas especies, las altas frecuencias cardíacas y los escasos valores de referencia. A pesar de ello, es necesario realizar estas pruebas para obtener un diagnóstico ajustado de la patología cardíaca (Pees & Krautwald-Junghanns, 2009; Pees, Krautwald-Junghanns & Straub, 2003).
El presente trabajo tiene como objetivo compilar la información existente sobre la cardiología en psitaciformes mediante sus estudios complementarios para ampliar y facilitar la práctica clínica con estas importantes herramientas diagnósticas y así familiarizar al profesional veterinario en el estudio de la fisiología y patologías del sistema cardiovascular en estas aves.
Examen clínico y anamnesis
Los psitaciformes cuando padecen alguna alteración del sistema circulatorio suelen presentar un cuadro de apatía y debilidad (Barreiro Lois et al., 2000). Los signos más específicos pueden ser la decoloración o cianosis de la piel en la zona del anillo periocular o de la cera, y la presencia de edemas en las extremidades (Pees & Krautwald-Junghanns, 2009). Otros signos que pueden presentarse y así ayudarnos a un diagnóstico de patología cardíaca son: la dilatación del celoma por líquido libre, la disnea o la intolerancia al ejercicio (Nalmas et al., 2007).
La auscultación sin sedación, es factible y permite valorar soplos y arritmias, a pesar de la elevada frecuencia o evaluar el ritmo cardíaco mediante una sonda audio Doppler (Šolc, 2007).
Si la anamnesis recoge una historia clínica de un loro de edad avanzada junto a incorrecciones dietéticas durante años o factores ambientales estresantes (frío o humo de tabaco) podemos orientar las pruebas diagnósticas para descartar una arteriosclerosis (Bavelaar & Beynen, 2004).
Para determinar el origen de un problema cardíaco, son de gran ayuda: hemograma completo, bioquímica sérica y proteinograma, sumado al estado de hidratación, funcionalidad pulmonar, temperatura y pesaje. Además, es interesante realizar un lipidograma en aquellos que se sospecha arteriosclerosis (Beaufrère, 2013). La evaluación de la presión sanguínea en loros se puede realizar de forma rutinaria utilizando un método indirecto y no invasivo para obtener de forma sencilla un valor de presión arterial sistólica mediante la sonda Doppler y un tensiómetro con un manguito de tamaño adecuado. Las mediciones pueden realizarse sobre la arteria metatarsal doral o la cubital, los valores normales de presión arterial sistólica en un psitaciforme despierto están entre 90 y 160 mm Hg, ante una sedación considerar hasta un máximo de 200 mm Hg (Talavera et al., 2008).
Enfermedades cardíacas
En estudios posmortem (Pees & Krautwald-Junghanns, 2009; Pees, Krautwald-Junghanns & Straub, 2003; Rembert et al., 2008) se ha encontrado fallo cardíaco congestivo como causa primaria de la muerte de algunos psitaciformes. Se han descrito efusiones pericárdicas y consecuencias como hipertrofias y dilataciones del miocardio ventricular. Así como infiltrado inflamatorio mixto en el miocardio, coagulación focalizada, infiltración grasa y arterioesclerosis en grandes vasos (Musulin & Adin, 2006).
Esto nos indica que los problemas cardíacos en aves son más prevalentes de lo que sospechamos en la clínica habitual.
Examen físico
En el loro gris africano (Psittacus erithacus) se puede sospechar del síndrome de insuficiencia cardiovascular cuando presenta coloración azulada periorbital o la zona hundida, así como edema en patas o alas. En caso de pericarditis por gota visceral, los niveles de ácido úrico en el plasma estarán elevados (Nap, Lumeji & Stokhof, 1992).
Las efusiones pericárdicas suelen producir disnea grave, debilidad y abultamiento abdominal (Rembert et al., 2008).
La arterioesclerosis es frecuente en el Loro gris o yaco (Psittacus erithacus), Guacamayos de gran talla (Ara spp. y Anodorhynchus spp.) y Amazona spp. por una dieta descompensada a partir de los 15 años de edad (Nap, Lumeji & Stokhof, 1992; Zandvliet, 2005a).
Radiografía
En estas, el corazón se evidencia junto con el hígado formando una silueta de reloj de arena. Es muy difícil valorar aumentos en cámaras cardíacas mediante radiografías, pero es posible valorar cambios secundarios como aumento de radiodensidad en pulmones, hepatomegalia o ascitis en caso de fallo cardiaco congestivo. También podemos apreciar un desplazamiento de los sacos aéreos, pero es difícil diferenciar la causa como dilatación, hipertrofia, efusión pericárdica, granulomas o tumores (Guerrero et al., 2015).
Estados avanzados de arterioesclerosis pueden verse como una combinación del aumento de la radiodensidad alrededor del corazón y un ensanchamiento de la aorta con dilatación ventricular. La pericarditis puede verse como un aumento irregular de la silueta cardiaca (Bavelaar & Beynen, 2004; Beaufrère, 2013).
Una medida orientativa del tamaño cardíaco es la longitud del esternón (medida en el ave). En psitaciformes medianos (200-500gr) el tamaño cardiaco debe ser entre 36-41% de la longitud del esternón o 51-61% del ancho del tórax (medido en una radiografía VD: Ventrodorsal). Estas medidas siempre se toman en la proyección ventrodorsal con una perfecta alineación de la columna con la quilla (Nalmas et al., 2007).
Ecocardiografía
La ecocardiografía es un método de diagnóstico importante para evaluar la función y la estructura cardíaca. Para realizarla en psitaciformes se requiere un equipo con un alcance mínimo de 100 frames por segundo, una sonda de 7,5 MHz o superior microconvexa o sectorial con función Doppler color, pulsátil y continuo, y preferiblemente con electrocardiógrafo acoplado (Rembert et al., 2008). La sonda se aplica, en este grupo de aves, de forma ventromedial directamente detrás del esternón. Es recomendable el ayuno breve (2-4 horas en psitaciformes) antes de la ecocardiografía puesto que el tracto gastrointestinal nos puede dar interferencias. El ayuno del transporte puede ser suficiente en aves débiles o anoréxicas (Guerrero et al., 2015). En las débiles, se puede realizar el estudio sin sedación, si esta no es muy reacia al manejo, incluso de pie en la mesa de exploración, mientras que en algunas aves se requerirá la anestesia. Es difícil de realizar ecocardiografía en aves despiertas, por riesgo a altos grados de estrés, pero la anestesia inhalatoria con isofluorano puede generar alteraciones como: arritmias, bloqueos AV de segundo y tercer grado, depresión de la onda T y contracción atrial prematura (Zandvliet, 2005b).
Existen dos accesos factibles para el examen ecocardiográfico:
Ventana Paraesternal Derecha.
Ventana Ventromedial: acceso más usado en loros en general ya que permite obtener dos imágenes del eje longitudinal del corazón al rotar la sonda 90º: vista horizontal (4 cámaras) y vista ventral (2 cámaras).
El estudio Doppler pulsado permite medir la velocidad del flujo sanguíneo a nivel de las aberturas atrioventriculares y de los grandes vasos del corazón. Se toman medidas a partir del acceso ventromedial con la vista horizontal de las 4 cámaras. Existen valores de referencia para la velocidad del flujo de entrada del ventrículo izquierdo, ventrículo derecho y el flujo aórtico de salida (Pees, Krautwald-Junghanns & Straub, 2003).
El estudio Doppler color, en loros, permite evaluar disfunciones valvulares, pero su uso se ve limitado por la frecuencia cardiaca de estas especies ya que implica una reducción de la frecuencia de frames por segundo (Zandvliet, 2005b).
Tabla 1 Parámetros ecocardiográficos de referencia en 3 grupos de psitaciformes (valor medio + desvío estándar).

Se deben medir las dimensiones (largo y ancho) internas de las cámaras en sístole y diástole (DDVI: Diámetro Diastólico del Ventrículo Izquierdo y DSVI: Diámetro Sistólico del Ventrículo Izquierdo), el grosor de la pared del septo interventricular y el diámetro aórtico. A partir de estas medidas se puede calcular la fracción de acortamiento (FA), el cual es uno de varios parámetros (Zandvliet, 2005b), que representa la capacidad de contracción ventricular:
Donde la FA, considerada fisiológica, en psitaciformes es de 23,1±4,6%.
También la relación entre la longitud y el ancho del ventrículo izquierdo permite una valoración de la contracción ventricular y corresponde a un valor constante en los psitaciformes (vista vertical: 0,33 en sístole y 0,40 en diástole), existiendo una correlación (tabla 2) entre la longitud el ventrículo izquierdo (LVI) y la longitud del esternón (LS) (Richard & Couto, 2009).
Electrocardiografía
El electrocardiograma permite obtener un registro gráfico de la actividad eléctrica del corazón. El sistema de conducción eléctrica está formado por el nodo sinusal (SA), el nódulo atrioventricular y la red de Purkinje, al igual que en los mamíferos. El SA es el marcapasos principal del corazón, donde se genera el impulso eléctrico que se dirige hacia el nódulo atrioventricular. A diferencia de la despolarización subendocardial de los mamíferos, la despolarización ventricular de los psitaciformes es subpericárdica y se propaga por el miocardio hacia el endocardio. Esta peculiaridad es la que explica que el complejo QRS en el electrocardiograma aviar sea negativo (Pees & Krautwald-Junghanns, 2009).
Aunque la técnica electrocardiográfica en psitaciformes es similar a la utilizada en mamíferos (sistema de 6 derivaciones), existen algunas diferencias y pueden requerir restricción química o anestesia general durante el procedimiento, así como el uso de electrodos subcutáneos. El examen electrocardiográfico bajo anestesia general con Isoflurano (entre el 1 y 4%), según algunos autores (Pees & Krautwald-Junghanns, 2009; Pees, Krautwald-Junghanns & Straub, 2003), es seguro y permite obtener un trazado de muy buena calidad para la mayoría de los ECGs registrados, con poco ruido causado por movimientos del animal o de los electrodos. Sin embargo, en algunos estudios se han encontrado efectos negativos con el uso del Isofluorano por lo que recomiendan la utilización de equipos portátiles que no necesitan la conexión de electrodos lo que evita la sedación del paciente (Zandvliet, 2005a).
El equipo debe permitir de frecuencias cardíacas elevadas (superiores a 250 ppm) por lo que se necesita una velocidad de papel de 100mm/s por la alta frecuencia cardíaca. Los electrodos deben estar en contacto con la piel de cada una de las extremidades, con gel ecográfico como material conductor al cual se le puede añadir anestésico local (lidocaína) por si el estudio se realiza con el ave despierta. Se recomienda el uso de pinzas atraumáticas o unidas a agujas hipodérmicas (Zandvliet, 2005b).
Tabla 3 Valores de referencia para el Electrocardiograma normal en algunos psitaciformes (valor medio + desvío estándar).
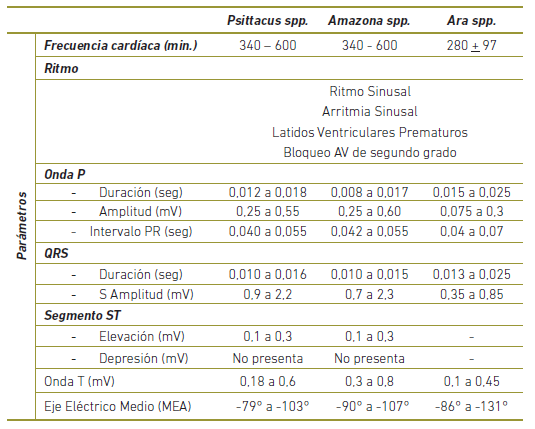
El electrocardiograma normal de un psitaciforme (Tabla 3) también inicia con una onda P que corresponde a la despolarización atrial. Le sigue una depresión en el intervalo PR, que representa la repolarización atrial, la cual es normal en psitaciformes. En cambio, en mamíferos este fenómeno se denomina onda T auricular (Ta) y suele corresponder a una hipertrofia del atrio derecho. El segmento QRS corresponde a la contracción ventricular. La onda Q, que es la primera depleción negativa, suele ser de amplitud pequeña o ausente. La onda S es, como peculiaridad en todas las aves, la siguiente depleción negativa en el electrocardiograma. El segmento ST suele ser corto o ausente y cuando está presente suele estar elevado sin implicar ninguna anomalía cardíaca. La onda T siempre es positiva en la derivación II. En Amazona spp. y Psittacus spp. es un hallazgo normal encontrar las ondas T y P superpuestas (Nap, Lumeji & Stokhof, 1992).
Tomografía computada (TC)
Este método complementario permite una mejor identificación de las estructuras del sistema cardiovascular sin interferencia de las estructuras subyacentes de la cavidad celómica observadas por ejemplo en imágenes radiográficas, ya que la TC proporciona imágenes en secciones, sin superposición de tejidos.
Según estudios de Dos Santos et al. (2020) la TC permitió en psitácidos evaluar los siguientes parámetros: longitud del corazón (mm) desde la base hasta el ápice; proyección lateral y corte sagital; ancho del corazón (mm) proyección ventrodorsal y sección dorsal; ancho del celoma (mm) proyección ventrodorsal; proporción entre el ancho de la silueta cardíaca y el ancho del celoma (%). En comparación a la radiología, la TC arroja valores menos a los de referencia para psittaciformes, esta diferencia puede deberse a que los métodos de formación de imágenes son diferentes en ambas modalidades, con radiografías, la imagenología es bidimensional y la TC, tridimensional. También los autores recomiendan que va mayor evaluación de las estructuras en la TC debe utilizarse contraste yodado por ejemplo para captar las cuatro cámaras cardíacas y evaluar, por ejemplo, en aves gerontes, una de las entidades más comunes como la esclerosis.
Posibilidades terapéuticas
Cuando tratamos loros con enfermedades cardíacas nos percatamos que siempre son diagnosticados en un estado de descompensación, por esto todas las aves con un problema cardíaco deben ser consideradas como casos de emergencia (Bavelaar & Beynen, 2004) que pone en peligro la supervivencia del animal.
Generalmente existen tres pilares para el tratamiento de estas patologías: medicación para el sistema circulatorio, drenaje quirúrgico del líquido (pericardiocentesis, celiocentesis) y terapia de soporte (Beaufrère, 2013). Sobretodo tratamiento de la causa primaria si la patología cardíaca es secundaria a otro proceso (Musulin & Adin, 2006).
Pericardiocentesis
La pericardiocentesis ecoguiada es muy útil en derrames pericárdicos de gran volumen y se debe considerar que en una efusión pericárdica al ser tan poco el volumen una pericardiocentesis seria riesgosa (Bavelaar & Beynen, 2004). No se puede retirar más de 10 ml/kg de masa corporal por día para no provocar un shock hipovolémico (Pees & Krautwald-Junghanns, 2009). Para llegar al pericardio es necesario puncionar el hígado, pero no parece que tenga ningún efecto negativo. Este procedimiento solo se puede realizar bajo anestesia para evitar los movimientos bruscos y generar graves daños al animal (Beaufrère, 2013).
Terapia de soporte
Cuando se produce un fallo cardíaco, los órganos como el hígado y el riñón se ven afectados, uno por congestión y el otro por falta de perfusión. La terapia con IECAs ayudará a la perfusión renal y bajará la precarga reduciendo la congestión hepática. Así como otras medidas de soporte deben mantenerse condiciones de temperatura y humedad adecuadas (25 ºC y 60% o superiores), reducción del estrés y fluidoterapia. Se deben suplementar electrolitos o vitaminas en caso necesarios. Si sospechamos de arterioesclerosis una terapia de soporte con vitamina A, vitamina C, vitamina E y selenio estaría recomendada (Zandvliet, 2005b).
Medicación cardíaca
Los medicamentos digitálicos se usan solo para estabilizar animales en situaciones de emergencia, pero tienen un margen terapéutico pequeño y a largo plazo los efectos secundarios son iguales que los signos clínicos, pueden causar la muerte súbita (Richard & Couto, 2009).
Los estudios recomiendan una dosis inicial de digoxina a 20-50 mcg/kg BID y una dosis de mantenimiento de 10 mcg/kg BID (8). Si son arritmias ventriculares la digoxina no sería el medicamento de elección (Rembert et al., 2008).
Antes de usar antiarritmicos, se deben valorar que la arritmia no sea secundaria a un desequilibrio electrolítico del potasio.
Los betabloqueantes como en exprenolol (2 mg/kg SID) reducen el desarrollo de arterosclerosis (Bavelaar & Beynen, 2004).
Los inhibidores de la enzima convertidora de angiotensina (IECAs) son efectivos y seguros, a 10 mg/kg en psitaciformes de menos 250 g, 1 mg/kg BID especies de pesos medios (Ej.: amazonas y yacos) y 1,25 mg/kg BID especies mayores de 900 g (Nap, Lumeji & Stokhof, 1992).
Para una terapia inicial de insuficiencia cardíaca en psitaciformes se recomienda una combinación de Digitálicos, IECAs y Diuréticos (Musulin & Adin, 2006).
La furosemida (0,1-0,2 mg/kg/d, IM) está indicada en edema y efusión pericárdica. Contraindicada en taponamiento cardíaco. Una sobredosificación puede producir una hipokalemia que causará arritmias (Musulin & Adin, 2006; Zandvliet, 2005a; Zandvliet, 2005b).
Conclusiones
La realización de los estudios descriptos amplía la información existente sobre la cardiología en psitaciformes para así facilitar la práctica clínica de estas importantes herramientas diagnósticas y contribuir así al, estudio de la fisiología y patologías del sistema cardiovascular en estas aves.
















