INTRODUCCIÓN
El hipoclorito de sodio (NaClO), es un compuesto químico ampliamente utilizado por sus propiedades desinfectantes. Es un compuesto altamente tóxico por lo cual se vende en concentraciones relativamente bajas a nivel comercial (0,5 a 5,25%) debido a los efectos tisulares que podría causar cuando no se manipula correctamente (Juárez y Lucas, 2001). Dentro de los usos más comunes se cuentan labores de limpieza doméstica, en industria para el tratamiento y potabilización del agua, como blanqueador de textiles y diversos procedimientos en medicina e investigación que requieren de condiciones asépticas como la limpieza de equipos, medios de cultivo y en odontología en campos como la endodoncia (Manrique et al., 2011).
El vertimiento de residuos tóxicos a las aguas es un problema de salud pública de suma importancia; el uso común de soluciones que contienen hipoclorito lo convierte en uno de los principales componentes de las aguas residuales (Pathiratne et al., 2015), está demostrado que estos compuestos al entrar en contacto con afluentes de agua naturales podrían afectar de manera directa a los organismos, de importancia ecológica como los peces (Shrivastava, 2015; Hemachandra y Pathiratne, 2016). Algunas plantas son utilizadas como bioindicadores para evaluar el efecto que tienen los contaminantes químicos en los ecosistemas; esto es debido a que las plantas poseen algunas ventajas en comparación con otros organismos, debido a que pueden almacenarse en forma de semilla por periodos prolongados de tiempo, costo de mantenimiento mínimo, cromosomas de gran tamaño (Iannacone y Alvariño, 2005).
Los ápices radiculares de varias especies de plantas se han utilizado para el estudio inducido de aberraciones cromosómicas (CAs) y la presencia de micronúcleos (MNi); debido a que los meristemos de la raíz contienen una proporción alta de células en mitosis lo que facilita la incidencia de contaminantes tóxicos en células vegetales, específicamente en lo que tiene que ver con la reproducción celular (Prajitha y Thoppil, 2016). Una de las especies vegetales más empleadas para la detección de diferentes tipos de cambios genéticos causados por radiaciones y substancias químicas es Allium cepa L. mediante la cual se hacen pruebas para la vigilancia del medio ambiente (Nefic et al., 2013).
En un estudio realizado por Manrique et al. (2011), quienes evaluaron el potencial genotóxico del hipoclorito de sodio en bulbos de cebolla y semillas de lechuga como bioindicadores. encontraron que ocasiona aberraciones mitóticas en las células que forman las zonas de crecimiento de las raíces e inhibición de la elongación de las mismas; donde llegando a la conclusión que el hipoclorito en altas concentraciones ( 250 ppm, 175 ppm, 50 ppm y 25 ppm) podría causar daños irreparables en las células vegetales.
La mayoría de las investigaciones realizadas por muchos autores concuerdan en que los ensayos con plantas son eficientes y confiables para pruebas de detección rápida y efectos sobre las células de productos químicos relacionados con mutagenicidad, efectos citotóxicos y aberración cromosómica; y la especie Allium cepa L. ha demostrado ser eficaz, altamente sensible y menos costosa, utilizado para las potenciales pruebas tanto en los procesos celulares mitóticos como meióticos (Khanna y Sharma, 2013). Por tal razón, el objetivo de esta investigación fue evaluar el efecto citotóxico del hipoclorito de sodio (NaClO) en células apicales de raíces de cebolla derivado del proceso de división celular.
METODOLOGÍA
Área de estudio
Este estudio se realizó en el laboratorio de genética de la Universidad de Córdoba ubicada a 8°47’15,71” N y 75°51’28,01” W, en la ciudad de Montería en el departamento de Córdoba, Caribe colombiano. Según el Instituto de Hidrología, Meteorología y Estudios Ambientales (IDEAM) la temperatura promedio es de 27,8ºC. La humedad relativa del aire oscila durante el año entre 76 y 82%, siendo mayor en los meses de octubre y noviembre.
Métodos
Se prepararon cinco soluciones de NaClO, diluidas en agua destilada a distintas concentraciones en partes por millón (ppm), las cuales fueron: 5, 2, 1, 0,5 y 0,2 mg L-1 y una solución control de agua destilada, se implementó el protocolo de Manrique et al. (2011), con ciertas modificaciones. Se utilizaron tres bulbos de cebolla para cada concentración en recipientes desechables; se registró el crecimiento de la longitud de las raíces durante 3 d haciendo mediciones cada 24 h. Al tercer día, se realizaron pruebas para mitosis en los ápices radiculares, se calculó el índice mitótico general y por fases, y se identificaron las anomalías celulares.
Análisis de microscopía
Se realizaron pruebas para mitosis, cortando los ápices radiculares (3 mm) y se sumergieron en ácido clorhídrico 1 N durante 15 min para romper las paredes celulares. Posteriormente se trasladaron a una placa porta objetos donde fueron teñidos con aceto-orceina 1 N durante 10 min, y se observaron en microscopios ópticos Leica DM500.
Índice mitótico
Este índice permite conocer si existe inhibición en el proceso de división celular, si se obtienen valores inferiores a los de la solución control se puede decir que existe inhibición, caso contrario si se obtienen valores mayores lo cual indicaría que existe un aumento en la división producto de la aplicación de los compuestos o sustancias químicas (Restrepo et al.,2012).
Se utilizaron las siguientes fórmulas: índice mitótico general (IMg) = número de células en división/número de células totales; índice mitótico profase (IMp) = número de células en profase/número de células en división; índice mitótico metafase (IMm) = número de células en metafase/número de células en división; índice mitótico anafase (IMa) = número de células en anafase/número de células en división; índice mitótico telofase (IMt) = número de células en telofase/número de células en división.
Cálculo de índice de anomalías celulares
Se utilizó la fórmula: número de células anómalas/número de células totales. Esto para cada concentración, donde se utilizó la metodología usada (Akinboro et al., 2011).
Análisis estadístico
Se realizó un análisis de varianza (ANOVA) y prueba de rangos múltiples mediante el método de diferencia mínima significativa (LSD) utilizando el software estadístico Statgraphics Centurion versión XVI.I. Para la realización y edición de las gráficas y tablas se utilizó el programa Microsoft Excel 2010.
RESULTADOS
Crecimiento de las raíces
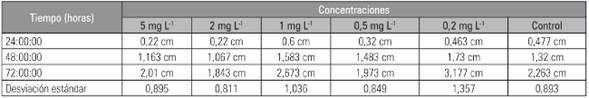
Durante las 72 h que permanecieron los bulbos de cebolla expuestos a las distintas concentraciones de hipoclorito, se observó crecimiento en longitud de las raíces, en las concentraciones de 0,2 y 1 mg L-1 hubo mayor crecimiento (Tab. 1).
Mediante el análisis estadístico se encontró que no existe (P>0,05) una diferencia estadísticamente significativa entre los tratamientos lo que podría significar que el hipoclorito no inhibió el proceso de crecimiento de las raíces (Tab. 2).
En la Tabla 3 se muestran los resultados para la prueba de rangos múltiples LSD, se encontró que no existe diferencia entre pares de tratamientos.
Pruebas celulares
Índice mitótico
Los índices mitóticos general y por fases se muestran en la Tabla 4.
Tabla 4 Índice mitótico general e Índices mitóticos por fases mitóticas para las distintas concentraciones.

La concentración donde se presentó un mayor índice mitótico general fue 1 mg L-1, seguido por la concentración Control, en tales concentraciones la actividad celular fue mayor. Las demás concentraciones presentaron porcentajes de inhibición significativos (Tab. 5).
Anomalías celulares (cromosómicas)
Se reportan anomalías celulares en todas las concentraciones a excepción del control, las más frecuentes fueron múltiples lesiones nucleares como espacios vacíos dentro de los núcleos y rompimiento de los mismos (Tab. 6). Se puede apreciar que el mayor número de anomalías en las concentraciones más altas (5 y 2 ppm) corresponden a lesiones nucleares y a medida que disminuye la concentración de hipoclorito aparecen otras anomalías como la hipercromasia.
Tabla 6 Anamalías celulares y número de células anómalas encontradas en las respectivas concentraciones. “C” indica células anómalas.

En la Figura 1 se muestran algunas de las células donde se observaron las anomalías encontradas en las distintas concentraciones, se evidenciaron principalmente: anafase con puente entre cromosomas, ausencia de núcleo, coagulación en metafase, hipercromasia, lesiones nucleares, rompimiento de cromosomas en anafase y metafase, originando micronúcleos.
Índice de anomalías celulares
Se muestran los índices de anomalías celulares de cada concentración, los valores más altos corresponden a las concentraciones de 5 mg L-1 seguido por 0,2 y 1 mg L-1 (Fig. 2).
DISCUSIÓN
Crecimiento en longitud de las raíces Producto de la exposición de las raíces a sustancias químicas, las raíces sufrirán alteraciones de sus características normales, como puede ser su forma, longitud y coloración. El grado de alteración de las raíces dependerá de la naturaleza y toxicidad de las sustancias y el tiempo que estas permanezcan expuestas (Khanna y Sharma, 2013). Además, esta prueba es una importante prueba in vivo, donde las raíces crecen en contacto directo con las sustancias de interés que permiten un posible daño al ADN, lo que podría inferir una correlación con la exposición a dichas sustancias por parte de los seres humanos, puesto que los cromosomas de las planta y los animales son morfológicamente similares, y parecen responder a tratamiento con agentes mutagénicos de forma similar a la de los mamíferos y otros eucariotas (Hemachandra y Pathiratne, 2015; Nefic et al., 2013).
Al someter a hidratación un bulbo de cebolla se produce una estimulación del crecimiento de las células, lo cual permite la elongación de las raíces de la planta. Sin embargo, cuando la absorción se lleva a cabo en presencia de sustancias orgánicas o inorgánicas tóxicas la división celular de los meristemos radiculares puede inhibirse, ya sea retardando el proceso de mitosis o destruyendo las células. Este tipo de alteraciones generalmente impide el crecimiento normal de la raíz y, por tanto, su elongación (Restrepo et al., 2012). Sin embargo, en el presente estudio, no se reportaron diferencias significativas en el crecimiento.
Una disminución del crecimiento radicular más del 45% indica la presencia de las sustancias en ambientes naturales y demuestra efectos “subletales” sobre las plantas, causando no solo retraso en crecimiento radicular, si no también conllevando a las células a mostrar alteraciones genéticas (Khanna y Sharma,2013).
Los resultados obtenidos concuerdan con los obtenidos por Manrique et al. (2011), quienes reportan que para concentraciones de 5 mg L-1 la inhibición del crecimiento en longitud de las raíces de cebolla tratadas con hipoclorito de sodio comienza a disminuir.
Índice mitótico (IM)
Se encontró que existe inhibición en el proceso de mitosis, ya que se obtuvieron valores en el IM de las concentraciones 5, 2, 0,5 y 0,2 mg L-1 inferiores al grupo control, diferentes estudios evidencian que algunas sustancias de naturaleza química u orgánica causaron disminución mitótica en la división de células meristemáticas de las raíces de cebolla (Berrocal et al., 2013) la disminución de IM sugiere la supresión de la actividad mitótica en cebolla, a causa del hipoclorito de sodio, puesto que IM es una estimación cuantitativa de las actividades mitóticas en un organismo o un órgano en particular (Berrocal et al., 2013). La reducción de IM podría deberse a los elementos que constituyen el hipoclorito de sodio que a su vez tienen efectos citotóxicos sobre A. cepa L. Este índice (IM) es una medida aceptable de citotoxicidad en todos los organismos vivos. El nivel de citotoxicidad podría determinarse por la disminución de la tasa de IM. Una disminución de IM por debajo del 22% en comparación con controles negativos podrían tener un impacto letal en el organismo, mientras que una disminución por debajo del 50% suele tener efectos subletales y se denomina valor límite citotóxico (Prajitha y Thoppil, 2016). La disminución del IM explica la citotoxicidad potencial y sugiere un efecto de inhibición, del hipoclorito de sodio sobre las células meristemáticas radiculares de cebolla lo que podría inducir a una serie de anomalías mitóticas. La reducción de la actividad mitótica podría deberse a la inhibición de la síntesis de ADN o a un bloqueo en la fase G2 del ciclo celular, evitando que la célula entre en su ciclo mitótico (Haq et al., 2017). También puede deberse a una alteración de la síntesis de nucleoproteínas y un nivel reducido de ATP para proporcionar energía para el alargamiento de los microtúbulos que conforman las fibras del huso, lo que posiblemente disminuiría la dinámica y movimiento cromosómico (Haq et al., 2017; Hemanth et al., 2015).
Aunque se obtuvo un dato atípico en la concentración de 1ppm cuyo IM fue superior al de las concentraciones mayores, esto se podría interpretar como el hecho de que una concentración elevada detiene los procesos celulares sin importar la fase en la que se encuentren, lo cual permite observar células en todas las fases del ciclo; por su parte, las concentraciones bajas permiten que continúe el ciclo celular, aparentemente, hasta la interfase, y así se produce un estancamiento en ella (Freyre et al., 2009).
Anomalías celulares
Las aberraciones cromosómicas se caracterizan por cambios bien sea en la estructura o en el número total de cromosomas, que pueden ocurrir tanto espontáneamente como también puede ser el resultado de la exposición a agentes físicos o químicos (Hemachandra y Pathiratne, 2015; Restrepo et al., 2012) En el presente estudio, la mayor frecuencia se encontraron aberraciones cromosómicas en los bulbos de cebolla expuestos a la concentración de 5 mg L-1.
Las anomalías encontradas en este estudio concuerdan con las reportadas por varios autores quienes expusieron bulbos de cebolla a soluciones de diferentes sustancias químicas con potencial citotóxico (Marcano et al., 2001; Marcano et al., 2004; Restrepo et al., 2012; Freyre et al., 2009; Prajitha yThoppil, 2016); trastornos anormales como rompimiento de cromosomas en metafase y anafase (aberración clastogénica), células binucleadas en interfase, la presencia de células binucleadas ha sido reportada por varios investigadores (Pandey et al., 2014). Las células binucleadas pueden surgir como el resultado de un proceso incompleto de división celular, es decir, cariocinesis con citocinesis incompleta. Estas células también pueden surgir debido a la supresión de la formación de placas celulares durante la telofase temprana, los cromosomas que no se incorporaron al núcleo principal durante el ciclo de división forman estas alteraciones (Haq et al., 2017). La anafase con puente entre cromosomas, otras de las anomalías encontradas en este estudio; los puentes cromosómicos se producen por la ruptura de los brazos cromosómicos en el momento de división celular (telofase). Durante la mitosis, los dos centrómeros se mueven hacia los polos opuestos y pueden quedar estables formando “puentes” debido a la resistencia física que estos ofrecen (Llontop y Vargas, 2016). Ausencia de núcleo, hipercromasia, lesiones nucleares y micronúcleos también fueron encontrados en este estudio, los micronúcleos formados han demostrado que los errores en la mitosis generan ruptura del ADN, que subyace a la formación de micronúcleos que contienen cromosomas enteros los cuales experimentan replicación de ADN defectuosa y asincrónica que fragmenta ampliamente el ADN (Kuchy et al., 2016).
Las presencia de anomalías celulares está determinada por el aumento en las concentraciones de agentes mutagénicos. Si se aumentan las concentraciones de estos agentes las mutaciones genéticas crecerán de forma directa y las anomalías lo harán de forma exponencial (Hemachandra y Pathiratne, 2015). Esto indica que entre menores sean las concentraciones en las cuales se encuentren mutaciones génicas y anomalía celular, mayor será el grado de toxicidad de los compuestos estudiados. La presencia de anomalías en la concentración más baja (0,2 mg L-1) permite clasificar al hipoclorito de sodio como una sustancia altamente tóxica.
Está demostrado que Allium cepa expuesto a sustancias tóxicas, específicamente en este estudio, donde se utilizó hipoclorito de sodio, probablemente generó condiciones de estrés genómico que pudieron dar como resultado, roturas cromosómicas, y así generar distintas anomalías. Muchos estudios han indicado que las posiciones de ruptura no parecen ser al azar sino que se producen en una región de heterocromatina y podrían llevar a los cromosomas a una translocación, inversión o eliminación (Berrocal et al., 2013).
CONCLUSIONES
Allium cepa es una especie que ofrece un modelo experimental factible de implementar en el laboratorio para evaluar el efecto citotóxico de cualquier sustancia, en este caso de hipoclorito de sodio.
El hipoclorito de sodio generó anomalías celulares (cromosómicas) en todas las concentraciones de las cuales las más abundantes fueron lesiones nucleares.
El hipoclorito de sodio ocasionó inhibición en la división celular en todas las concentraciones a excepción de la concentración 1 mg L-1 donde se presentó un aumento de la división celular contrastada con la concentración control.
Se pudo clasificar al hipoclorito de sodio como una sustancia altamente citotóxica, ya que generó anomalías celulares en concentraciones inferiores a 5 ppm.