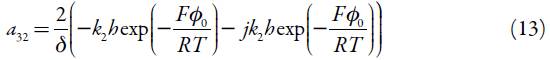INTRODUÇÃO
Uma das infrações frequentes, cometidas pelos desportistas no mundo inteiro é a dita dopagem bioquímica [1-2], cujo desiderato é o fortalecimento desigual do organismo com vistas ao aumento de produtividade física. É proibida nas competições [3-5]. Além disso, em alguns países, como Austrália, Áustria, França e Itália, a dopagem bioquímica, usada pelos esportistas, é equiparada à fraude e, por conseguinte, punida legalmente [5].
Uma das substâncias, consideradas um dopante, é a nandrolona (Número CAS: 434-22-0; 7β-[[(Sodiooxi)sulfonil]oxi]estr-4-en-3-ono;(17beta)-Hydroxyestr-4-en-3-ono-17-sulfato de sódio) (ver figura 1) [6-12], um androgeno sintético, existente sob várias formas. Por exemplo, o sulfato de sódio e de nandrolona, que, diga-se a verdade, pode ser considerado um semiéster ou um semissal, é um colírio, usado como fármaco de uso oftálmico na Espanha, na Dinamarca, na Suíça, na França, na Bélgica e em Portugal [6]. Em Portugal, ele é vendido como Nandrain®, na Espanha e na Bélgica, Nandrol (e) e na Dinamarca, na Suíça e na França, Keratyl® [8]. Nos Estados Unidos de América (EUA) também é usado e incluído na dita Pasta 3 [9].
Além do uso como fármaco oftálmico, é, também, utilizado para o tratamento de anemias, carcinoma de pulmões, angioedemas hereditárias, deficiências de antitrombina III, excessos de fibrinogênio, falhas de crescimento e síndrome de Taylor. Também é indicado na prevenção de angioedemas hereditárias [9].
Os seus efeitos colaterais podem incluir as anomalias hepáticas como neoplasmas, hepatites holestáticas [10], náuseas, vômitos, diarreias, insónias, acne [11], efeito de estimulação e dopagem, razão por que não é recomendada aos desportistas, entre outros efeitos de vários cunhos. Destarte, o desenvolvimento dos métodos eficientes de determinação eletroquímica desta substância é, deveras, um problema atual [12], e os métodos eletroquímicos dar-lhe-iam um bom serviço.
Vários métodos eletroquímicos foram elaborados para a detecção eletroquímica da nandrolona, em que vários modificadores de elétrodos foram usados, como fulerenos, grafeno e polímeros condutores [13-15]. Outro modificador de elétrodo poderia ser o oxihidróxido de vanádio (VO(OH)), um composto com comportamento eletroquímico flexível, mas mais acentuado para as propriedades redutoras [16]. No entretanto, até ao momento da submissão do presente trabaho, nenhum trabalho experimental acerca da modificação do elétrodo por VO (OH) para fins eletroanalíticos tem sido publicado, e a introdução de um novo modificador de elétrodo pode acarretar os problemas como:
Todos esses problemas podem ser resolvidos, sendo feita uma análise teórica do desempenho do oxihidróxido de vanádio, incluindo a elaboração e a análise de um modelo matemático, capaz de descrever adequadamente o desempenho do sistema. Outrossim, a modelagem permitir-nos-á comparar o desempenho deste sistema com o dos semelhantes, prevendo as divergências de comportamento sem ensaios experimentais.
Destarte, o desiderato do nosso trabalho é análise mecanística teórica do desempenho de oxihidróxido de vanádio na determinação eletroquímica da nandrolona. Para apro-pinquar-nos a ele, alcançamos os objetivos específicos como:
- Sugerir um mecanismo de desempenho do oxihidróxido de vanádio na detecção eletroquímica da nandrolona.
- Desenvolver o modelo matemático, condizente com os processos, que levam à aparição do sinal analítico.
- A partir da análise do modelo, detectar as condições do melhor desempenho do sensor (estado estacionário estável) e das instabilidades, se as pode haver.
- Comparar o comportamento deste sistema com o dos semelhantes [19-21]
O SISTEMA Ε O SEU MODELO
O desempenho de VO(OH) como modificador de elétrodo para a detecção da nan-drolona dar-se-á como exposto na figura 2:
A melhor eficácia de VO(OH) como modificador de elétrodo pode ser alcançada em meios moderadamente ácido a neutro. O meio fortemente ácido pode dissolver o material, formando os íons V3+.
e o comportamento do VO(OH) em meios fortemente ácidos analisar-se-á nos nossos próximos trabalhos.
Destarte, a maior eficácia do oxihidróxido de vanádio como modificador de elétrodo dar-se-á em meios menos ácidos. Como os prótons participam do sistema eletroanalí-tico, este se descreverá, no caso mais simples, pelas três variáveis:
n: a concentração da nandrolona na camada pré-superficial;
v: a concentração do dióxido de vanádio no cátodo;
h: a concentração dos prótons na camada pré-superficial.
Para simplificar a modelagem, supomos que o reator esteja agitando-se intensamente, de modo que possamos menosprezar o fluxo de convecção, que o eletrólito de suporte esteja em excesso, para menosprezar o fluxo de migração. Também supomos que a camada pré-superficial esteja de espessura constante, igual a δ, e que o perfil concentracional dos dois analitos seja linear.
É possível mostrar que, supondo o supracitado, o sistema se descreve mediante um conjunto de equações diferenciais (2):
em que Δ e D são coeficientes de difusão da nandrolona e dos prótons, n0 e h0 são suas concentrações no interior da solução, Vé a concentração superficial máxima do dióxido de vanádio e os parâmetros r, as velocidades das respectivas reações, que se obtêm como:
Em que os parâmetros k são constantes das respectivas reações, F é o número de Faraday, φ 0 é o salto do potencial, relativo ao potencial da carga zero, R é a constante universal de gases, T é a temperatura absoluta.
O oxihidróxido de vanádio representa um comportamento eletroquímico flexível. Mas, ao contrário do oxihidróxido de cobalto, por mais semelhante que seja a sua estrutura à do VO(OH), este representa inclinação para os processos catódicos em meios ácidos, o que se mostrará abaixo.
RESULTADOS Ε DISCUSSÃO
Para investigar a estabilidade do estado estacionário do sistema da detecção eletroquí-mica da nandrolona, assistida por VO(OH), analisamos o conjunto de equações diferenciais (2) mediante a teoria de estabilidade linear. A matriz funcional de Jacobi, cujos membros são calculados para o estado estacionário pode ser descrita como:
Em que:
Analisando as expressões (6), (11) e (14), que representam os elementos da diagonal principal da matriz, podemos ver que o comportamento oscilatório, neste caso, é possível, porque há, de fato, um elemento, capaz de ser positivo e, por conseguinte, de ser responsável pela positiva conexão de retorno. Como nos sistemas semelhantes, a única causa do comportamento oscilatório neste sistema são as influências do processo da ele-trorredução na dupla camada elétrica (DCE), descritas pela positividade do elemento  . As oscilações se esperam frequentes e de pequena amplitude.
. As oscilações se esperam frequentes e de pequena amplitude.
Para analisar a estabilidade do estado estacionário, aplicamos ao conjunto de equações diferenciais (2) o critério de estabilidade de Routh-Hurwitz. Simplificando o jacobiano, introduzimos as novas variáveis, obtendo-lhe o determinante como:
Abrindo os parênteses e aplicando a condição de Det J<0, saliente do critério, obteremos a condição de estabilidade como:
Que é uma expressão típica para um processo eletroanalítico eficiente e estável, controlado pela difusão, como nos casos semelhantes [18-21]. Neste caso, os prótons participam diretamente do processo eletroanalítico e não só a difusão do analito, mas, outrossim, a sua. Assim, o sistema eletroanalítico apresentar-se-á como eficiente, em soluções leve e moderadamente ácidas, pois os prótons participam diretamente da ele-trorredução do dióxido de vanádio até VO(OH).
No entretanto, não se pode exagerar o papel estabilizador do estado estacionário, que desempenham os prótons neste sistema. As soluções fortemente ácidas saem do quesito deste modelo, e o comportamento do VO(OH) nelas descrever-se-á num dos nossos próximos trabalhos.
A condição da instabilidade monotônica, relativa ao limite de detecção, para este sistema descreve-se conforme:
realizando-se, neste ponto, a igualdade das influências estabilizadoras a desestabilizadoras.
Quanto ao uso do VO(OH) em meio alcalino, ele pode até ser considerável para apoiar até alguns processos anódicos com alguns analitos, capazes de ser oxidados pelo vanádio tetra ou pentavalente em meio alcalino. VO(OH) interagirá com a hidroxila, formando, a depender da concentração e do potencial anódico, VO2 , VO3-, VO4 3- ou decavanadatos. Sem embargo, a assistência ao processo anódico não é característica para o VO(OH), cujo comportamento é mais favorável para ser mediador de processos catódicos.
CONCLUSÕES
Da análise do comportamento do sistema eletroanalítico, baseado em oxihidróxido de vanádio na detecção eletroquímica da nandrolona, é possível concluir que:
- O oxihidróxido de vanádio pode ser um modificador eficiente na determinação da nandrolona no cátodo. No entretanto, ao contrário do composto análogo de cobalto, o seu comportamento é fortemente inclinado para as propriedades redutoras e, destarte, o seu desempenho eletroanalítico dar-se-á em condições diferentes.
- O processo eletroanalítico é eficiente e controlado pela difusão tanto da nandrolona, como dos prótons. Sem embargo, se o pH do sistema é inferior a certo valor marginal, correspondente à formação dos cátions V3+, o presente modelo falhará na descrição do comportamento do sistema, haja vista o serem menosprezadas as influências superficiais e capacitadoras da dissolução do oxihidróxido de vanádio.
- O comportamento oscilatório neste sistema, como nos semelhantes, é possível, sendo causado pelos fatores da influência da eletrorredução na estrutura da dupla camada elétrica.