INTRODUCCIÓN
Según información de la International Agency for Research on Cancer, Agencia Internacional para Investigaciones en Cáncer (IARC), la neoplasia maligna de mama para el 2020 fue el cáncer más frecuente en mujeres a nivel mundial, con 1.948.321 casos nuevos, con un total de 513.525 defunciones por esta causa 1; comparativamente, para ese mismo año en Colombia se estima que se presentaron 15.509 casos nuevos y 4.401 muertes 2; para Antioquia, en el año 2018 se reportó una incidencia de cáncer de mama de 1.891 casos, y una mortalidad de 490 casos 3.
El cáncer de mama se caracteriza por la heterogeneidad entre diferentes tumores, y un comportamiento biológico particular según la expresión de los genes implicados en la carcinogénesis 4. Técnicas moleculares como los microarreglos genómicos han permitido identificar la presencia de patrones genéticos, que han llevado a la clasificación biológica del cáncer de mama en subtipos moleculares, que pueden predecir la respuesta de los tumores a determinadas terapias 5.
En 2010, Blows et al. subtipificaron los tumores según su expresión proteica y describieron la respuesta clínica según el tipo de tumor, encontrando que los que expresan receptores de estrógenos y progestágenos, están mejor diferenciados y tienen mejor pronóstico, mientras que aquellos sin expresión de receptores son pobremente diferenciados y de peor pronóstico, en especial los que tienen expresión del gen HER2 (receptor epidérmico humano) y el índice de proliferación celular Ki67 más alto 6. Basados en este comportamiento biológico, en el año 2013, el Consenso Internacional de Expertos de St Gallen 7, clasificó el cáncer de mama en cinco subtipos moleculares según su expresión génica: 1) luminal A: receptores hormonales (estrógenos y progesterona) positivos, HER2 negativo, con un índice de proliferación celular Ki67 menor al 20 %; 2) luminal B HER2 negativo: positivo para receptores hormonales, HER2 negativo y con índice Ki67 mayor 20 %; 3) luminal B HER positivo: positivo para receptores hormonales y para HER2; 4) HER2 puro: positivo para HER2 y negativo para receptores de hormonas; y 5) triple negativo: el cual no expresa receptores hormonales ni HER2 7.
La quimioterapia neoadyuvante (NACT) basada en antraciclinas (doxorrubicina), ciclofosfamida, taxanos (paclitaxel, doxetacel) y platinos (carboplatino) se convirtió en el estándar para el tratamiento de los subtipos moleculares agresivos como los triple negativo y HER2 positivo, y en el cáncer en estadio localmente avanzado 8,9, estadios IIB, IIIA, IIIB, IIIC según la clasificación TNM (tumor, nodo, metástasis) definida por el American Joint Committe on Cancer (AJCC-TNM) (AJCC) 10. La clasificación molecular es fundamental para escoger la terapia dirigida, pues los tumores que expresan receptores hormonales son candidatos para recibir terapia endocrina (tamoxifeno, inhibidores de aromatasa) y los tipos HER2 positivo a recibir diferentes tipos de terapias dirigidas como los anticuerpos monoclonales contra HER2 (trastuzumab, pertuzumab) 8,11. El objetivo de la NACT es hacer un control sistèmico y ganglionar, reducir el tamaño tumoral y, en algunos casos, permitir un manejo quirúrgico conservador en las pacientes 11-13.
La forma objetiva de medir la respuesta a la NACT se realiza mediante la respuesta patológica completa (RPC) y la respuesta clínica o radiológica, esta última definida por los criterios de la Organización Mundial de la Salud (OMS) 14 y criterios RECIST (Response evaluation criteria in solid tumors) 15. La RPC se ha definido por las características anatomopatológicas de las piezas quirúrgicas con distintos criterios basados en diferentes autores 16,17. Definir la respuesta clínica o radiológica y la RPC de las pacientes que recibieron NACT es importante, porque el tener una respuesta completa es un marcador de mejor pronóstico y se relaciona con mejor sobrevida global (SG), OS (Overall survival), y sobrevida libre de la enfermedad, DFS (Disease-free survival) 18,19.
Algunos estudios han evaluado la respuesta tumoral a la quimioterapia neoadyuvante según subtipos moleculares en Colombia 20,21, estos fueron llevados a cabo entre 2013 y 2017. Para un mejor entendimiento del curso clínico de esta enfermedad en nuestro entorno es importante aportar información de manera continua, por lo tanto, el objetivo de este estudio es describir la respuesta clínica y patológica según subtipos moleculares en pacientes con cáncer de mama estadios II y III pertenecientes a la región noroccidental de Colombia.
MATERIALES Y MÉTODOS
Diseño y población. Cohorte retrospectiva, descriptiva. Se incluyeron mujeres mayores de 18 años, con diagnóstico histológico de carcinoma invasivo de mama, en estadios IIA, IIB, IIIA, IIIB y IIIC, con clasificación por subtipos moleculares, que hubieran recibido quimioterapia neoadyuvante, y sometidas posteriormente a tratamiento quirúrgico, que consultaron entre el 1 de julio de 2017 al 30 de julio de 2019 en la clínica Medellín, institución orientada a la atención oncológica de alta complejidad, que atiende población perteneciente al régimen contributivo de los trabajadores y al régimen subsidiado por el Estado, en el Sistema General de Seguridad Social en Colombia (SGSS). Se excluyeron los casos no clasificables por subtipo molecular y aquellos en que se verificó que no recibieron NACT. Se implementó un muestreo consecutivo estricto a partir del universo de pacientes atendidas en la institución participante durante el periodo de estudio.
Procedimiento. Se seleccionaron las historias clínicas en el sistema de gestión de historias clínicas SERVINTE® de la Clínica Medellín en el periodo a estudio. Las pacientes candidatas a ser parte del estudio se identificaron mediante la búsqueda de los siguientes códigos de la clasificación internacional de enfermedades, décima edición (CIE-10): tumor maligno del pezón y de la areola mamaria (C500), tumor maligno de la mama, parte no especificada (C509).
En la institución, el diagnóstico de cáncer de mama se realizó con biopsia con aguja gruesa del tumor, tomada por un especialista en radiología experto en mama. Esta muestra fue sometida al estudio de patología básico e inmunohistoquímica para los receptores de estrógenos, progesterona, HER2, KI67; con esta muestra se hizo el diagnóstico histológico de malignidad, el tipo de cáncer y el grado histológico, y posteriormente se determinó la clasificación TNM; para la medición del tumor se utilizó cinta métrica, y para la evaluación ganglionar la palpación axilar; con respecto a la afectación por metástasis, para el estadio II se enviaron estudios usuales de estadificación tales como radiografía de tórax y ecografía de abdomen total, y para el estadio III se envió tomografía de tórax y abdomen contrastado junto con gamagrafía ósea.
El tratamiento NACT estándar utilizado incluía quimioterapia citotóxica basada en el esquema doxorrubicina junto con ciclofosfamida (AC) por 4 ciclos, y paclitaxel (T) por 12 ciclos; en total, el esquema de AC-T tenía una duración de 6 meses. En los tumores que sobreexpresan HER2 se utilizó trastuzumab, también se permitió la inclusión de terapia endocrina neoadyuvante. La secuencia del tratamiento y su dosis fue ajustada según cada paciente, sus comorbilidades y a juicio clínico del oncólogo tratante.
Al terminar el tratamiento las pacientes son remitidas nuevamente a mastología, donde se realiza el examen clínico de la mama con nueva medición del tamaño tumoral con cinta métrica y palpación axilar, determinando la respuesta del tumor y dando paso a la programación quirúrgica, la cual es determinada por el estadio, la extensión de la enfermedad y la respuesta a la NACT, e incluye cirugía de conservación (cuadrantectomía) o radical (mastectomía), al finalizar se realiza estudio patológico del espécimen quirúrgico, describiendo las características micro y macroscópicas, incluyendo presencia o no de tumor residual y el diámetro mayor del lecho tumoral; se consideró RPC a la ausencia de componente infiltrante, sin tener en cuenta el componente in situ.
Tres investigadores revisaron de forma independiente las historias de las mujeres que cumplieron con los criterios de selección, se procedió con la extracción de datos de interés y su almacenamiento en una base de datos construida en Excel. Para el análisis de calidad del dato se realizaron cortes de ingreso de información a la base de datos, cuando se tuvo el 10 % de los datos ingresados y una vez terminada la recolección. Posteriormente, se hizo una selección aleatoria del 10 % de los datos, en la que se compararon con las historias clínicas y la base de datos, los cuales no mostraron discrepancias relevantes.
Variables medidas. Edad, régimen de seguridad social, historia familiar de cáncer de mama en primer y segundo grado de consanguinidad, estadio clínico TNM, grado histológico, clasificación en subtipo molecular, tipo de cirugía, compromiso ganglionar, respuesta clínica y patológica posquimioterapia en las siguientes categorías: respuesta completa (RC), cuando no hay evidencia de masa; respuesta parcial (RP), con reducción del 30 % de tamaño del tumor; no respuesta (NR), no cumple con la definición de respuesta parcial o progresión y, por último, progresión (P), aquella lesión con aumento de 20 % de su tamaño 16,17.
Análisis estadístico. Descriptivo, las variables categóricas se presentan por medio de frecuencias absolutas y relativas, mientras que las variables cuantitativas se presentan por medidas de tendencia central y de dispersión. El análisis estadístico se realizó en el programa SPSS 23 ® (Statistical Package for the Social Sciences). Se presentan las proporciones de respuesta por subtipo molecular y por estadio clínico.
Aspectos éticos. La investigación contó con el aval del comité de ética de la Corporación Universitaria Remington (Acta 092020) y de la Clínica Medellín (Acta 10-2020), clasificada sin riesgo acorde a lo expuesto en la Resolución 8430 de 1993. Se respetó la privacidad de las pacientes del estudio y los acuerdos de la declaración de Helsinki.
RESULTADOS
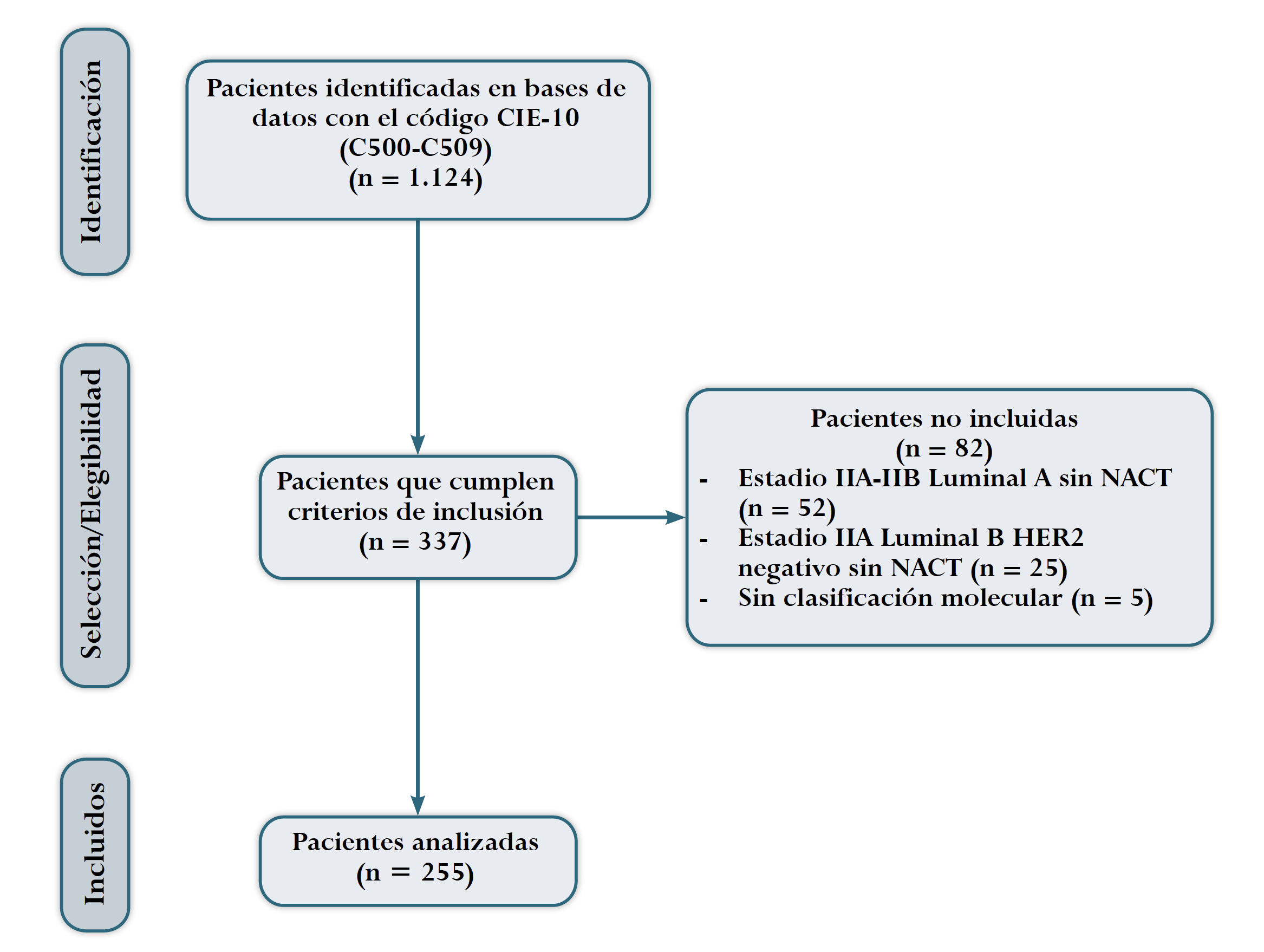
Se revisaron 1.124 historias clínicas, de las cuales se incluyeron 255 pacientes con diagnóstico de cáncer de mama que cumplieron criterios de inclusión (Figura 1). La media de edad fue de 55,6 años (min-max = 27-86), el 46,7 % (n = 119) pertenecían al régimen contributivo y el 38,8 % al subsidiado, y 14,5 % (n = 37) no tenían dato, el 17 % (n = 45) tenían historia familiar en 1 o 2° grado de consanguinidad de cáncer de mama, mientras que el 69 % no tenían antecedente y el 13,3 % (n = 34) no tenían dato.
En cuanto a las características clínicas, histológicas y la clasificación TNM, se clasificó como IIIB (28,6 %), seguido del IIB (26,3 %) y el IIIA (24,7 %). En cuanto al grado histológico, el 48,2 % tuvo grado 3 y el 37,3 % grado 2. El subtipo molecular más prevalente fue el luminal B HER2 negativo en 101 mujeres (39,6 %), seguido del triple negativo en 59 mujeres (23,1 %), el luminal B HER2 positivo en 35 mujeres (13,7 %), el HER puro en 34 mujeres (13,3 %) y, por último, el luminal A en 26 mujeres (10,2 %) (Tabla 1).
Tabla 1 Características clínicas, histológicas y clasificación TNM de las pacientes con cáncer de seno estadios II y III en la Clínica Medellín (Colombia), 2017-2019.
Fuente: elaboración propia.
El esquema de neoadyuvancia preoperatoria incluyó 1 caso (0,39 %) a base de terapia endocrina con inhibidor de aromatasa (letrozol), los demás correspondieron a terapia citotóxica (99,6 %, n = 224). La cirugía más frecuentemente realizada fue la mastectomía con vaciamiento axilar (54,9 %), el 25,5 % de las pacientes presentaron compromiso tumoral ganglionar axilar.
Al evaluar la respuesta clínica global, el mayor número de pacientes presentó respuesta parcial en 135 (52,9 %), la completa se presentó en 103 pacientes (40,4 %), sin respuesta en 12 pacientes (4,7 %) y progresión en 5 (2 %). Respecto a la respuesta patológica esta fue completa en 97 pacientes (38 %) y parcial o no respuesta en 158 (62 %).
La respuesta patológica completa por estadio fue del 50 % en estadio IIA, 34 % en IIB, 36 % en estadio IIIA, 34 % en estadio IIIB y 83 % en estadio IIIC (Tabla 2). La respuesta clínica completa posquimioterapia por subtipo molecular fue: luminal A (26,9 %), luminal B HER2 negativo (37,6 %), luminal B HER2 positivo (48,6 %), HER2 puro (41,2 %), triple negativo (45,8 %) y se logró respuesta patológica completa por subtipo molecular así: luminal A (19,2 %), luminal B HER2 negativo (32,7 %), luminal B HER2 positivo (54,3 %), HER2 puro (50 %), triple negativo (42,4 %) (Tabla 3).
Tabla 2 Respuesta patológica del cáncer de seno según estadio clínico en la Clínica Medellín Colombia), 2017-2019.
| Variable | Estadio | ||||
|---|---|---|---|---|---|
| IIA | IIB | IIIA | IIIB | IIIC | |
| n = 255 | n = 46 | n = 67 | n = 63 | n = 73 | n = 6 |
| n (%) | n (%) | n (%) | n (%) | n (%) | |
| Respuesta completa | 23 (50) | 23 (34,3) | 23 (36,5) | 25 (34,2) | 5 (83,3) |
| No respuesta completa | 23 (50) | 44 (65,7) | 40 (63,5) | 48 (65,8) | 1 (16,7) |
Fuente: elaboración propia.
Tabla 3 Respuesta clínica y patológica del cáncer de seno según subtipo molecular en la Clínica Medellín (Colombia), 2017 - 2019.
Fuente: elaboración propia.
DISCUSIÓN
Los resultados de este estudio indican que en pacientes con cáncer de mama localmente avanzado la respuesta clínica y patológica completa es mayor en los subtipos Luminal B HER 2 positivo y menor en los Luminal A y Luminal B HER 2 negativo. Respecto a HER puro la repuesta patológica es mejor que la respuesta clínica y para el triple negativo la repuesta clínica es mejor que la respuesta patológica.
Con respecto a la respuesta patológica de los subtipos moleculares del cáncer de mama, nuestros resultados son similares a los presentados por Haque et al. 22 (n = 13.939) quienes informan que se presentó RPC en el 18,8 %, con la siguiente distribución: luminal A (0,03 %), luminal B (18,7 %), HER2 (33,5 %), triple negativo (47,8 %). Así mismo, Lakshmanan et al. 23 analizaron la respuesta radiológica con una técnica de ultrasonido, de acuerdo con las características moleculares, evidenciando que los subtipos más agresivos (HER2 positivo y triple negativo) tuvieron mayor respuesta radiológica comparado con los tumores que expresan receptores hormonales (luminal A y B). En Colombia, Díaz et al. evaluaron 414 pacientes con diagnóstico de cáncer de mama que recibieron NACT y manejo quirúrgico entre 2013 y 2017 20, e informan una distribución por subtipos similar luminal A (19,8 %), luminal B HER2 negativo (32,4 %), luminal B HER2 positivo (18,1 %), HER2 puro (8,9 %), triple negativo (20,8 %); con respecto a la respuesta clínica y patológica completa (Clasificación Chevallier clase 1 + 2) reportan la siguiente distribución: luminal A (7,3 %), luminal B HER2 negativo (15,7/10,5 %), luminal B HER2 positivo (28/33,3 %), HER2 puro (35,1/56,7 %), triple negativo (18,6/26,7 %) como en el presente estudio, mayor para subtipos Her2 positivos y triple negativos. En el estudio de González et al., que ingresó pacientes atendidas entre 2013 y 2017 21, la distribución por subtipos fue luminal A (17,5 %), luminal B HER2 negativo (29,6 %), luminal B HER positivo (27,1 %), HER2 puro (6,4 %) y triple negativo (19,4 %). En cuanto a la RPC por subtipos ellos informan la siguiente distribución: luminal A (12,7 %), luminal B HER2 negativo (21,5 %), luminal B HER2 positivo (42,4 %), HER2 puro (55 %) y triple negativo (50,8 %). En ambos estudios los resultados son similares a nuestros hallazgos.
Por otra parte, nuestros resultados difieren de los presentados por Kunnuru et al. 24 (n = 60), quienes informan una respuesta clínica y patológica completa para los subtipos luminal A (clínica/patológica) (21,1 %/15,7 %) y luminal B (45,5 %/13,6 %), mientras que se tuvo una menor respuesta para los subtipos triple negativo (22,2 %) y HER puro (0/%). Se presentó respuesta clínica parcial a la quimioterapia en el 50 %, seguido de respuesta completa (26,6 %), no respuesta (13,3 %) y progresión de la enfermedad (10 %), se resalta la similitud en el orden en que se presentan las distintas respuestas clínicas, siendo la respuesta parcial la más frecuente. Además, Bonnefoi et al. 25 hacen un análisis secundario de la RPC en 1.212 (65 %) de 1.856 pacientes aleatorizadas. La RPC ocurrió en 222 de 1.212 (18 %) pacientes: 37 de 496 (7,5 %) luminal A, 22 de 147 (15 %) luminal B/ HER2 negativo, 51 de 230 (22 %) luminal B/HER2 positivo, 43 de 118 (36 %) HER2 positivo/no luminal, 69 de 221 (31 %) triple negativo (TN), encontrando menor respuesta en todos los subtipos con respecto al presente estudio.
Para la RPC, según estadio clínico, en el estudio de Díaz et al. 20 se distribuyó: IIIA (20,9 %, n = 18), IIB (16,0 %, n = 15), IIIB (14,2 %, n = 30) y IIIC (n = 0); a diferencia de este estudio, no se incluyó el estadio IIA, y el estadio IIIC fue el que presentó mayor RPC. Es posible que la alta RPC para el estadio IIIC sea debido al pequeño número de pacientes incluido en nuestro estudio.
Dentro de las limitaciones del estudio está la pérdida de datos desde fuentes secundarias de información, además su naturaleza retrospectiva, y que no se hizo seguimiento de la duración de la respuesta tumoral.
CONCLUSIONES
En la práctica clínica, la clasificación por subtipos moleculares en cáncer de mama permite hacer una aproximación a la respuesta de la quimioterapia neoadyuvante. Se requieren más estudios prospectivos regionales para determinar el desempeño predictivo de la respuesta patológica completa en relación con sobrevida global y libre de enfermedad.