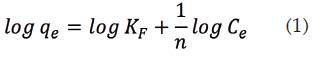1. INTRODUCCIÓN
Los colorantes son compuestos altamente coloreados y difíciles de descomponer biológicamente 1, los desechos de pigmentos en aguas residuales se consi deran un tipo de contaminante objetable debido a su alta toxicidad tanto para el ecosistema como para la salud humana 2. Esto ha creado una gran preocupa ción medioambiental acerca de las condiciones de los cuerpos de agua, lo que ha llevado a la necesidad de buscar técnicas eficaces para remover estos pigmentos de los efluentes y solucionar los problemas de conta minación 3.
Uno de los colorantes más utilizados, tanto en las industrias como a nivel de laboratorio, es el azul de metileno, ya que es un colorante modelo para colorear fácilmente cualquier superficie y para realizar expe rimentos científicos, además es abundante y fácil de obtener 4. El azul de metileno es un colorante uti lizado en la industria textil, cosmética, farmacéutica, alimenticia, de plásticos, papel, educativa, investiga tiva, entre otras 5. Las descargas de estas industrias contiene tintes los cuales son altamente visibles a bajas concentraciones y producen problemas de contamina ción como aumento de la demanda química de oxí geno y de la toxicidad, además de la disminución de la penetración de la luz y por ende de la fotosíntesis, sin mencionar, el efecto estético sobre la superficie del agua 6-8.
La adsorción con diferentes materiales absorbentes de bajo costo, se ha visto como una tecnología eficaz para la remoción de trazas de contaminantes en soluciones acuosas 9. Actualmente existe una alta generación de desechos agrícolas de bajo costo 10, algunos de estos desechos agrícolas son la cáscara de arroz, la cáscara de coco, la cáscara de tamarindo, la cáscara de yuca, entre otros 11, los cuales mediante una modificación física o química han dado muy buenos resultados en procesos de adsorción de colorantes 12.
Este trabajo evaluó la perspectiva del proceso de re moción del azul de metileno a partir de un adsorbente de bajo costo (Manihot esculenta) modificado con ácido fosfórico, se analizaron soluciones con concentracio nes específicas de azul de metileno y se estudiaron las condiciones de equilibrio y cinética de remoción.
1.1 Modelos de isotermas de adsorción
Las isotermas de adsorción son la representación grá fica de la relación entre la cantidad adsorbida por una unidad de peso de adsorbente y la concentración de adsorbato restante en un medio de ensayo a una tem peratura constante bajo condición de equilibrio 13.
En este trabajo se exploraron diferentes modelos de adsorción que se mencionan a continuación.
1.1.1 El modelo de isoterma de Freundlich
La ecuación de isoterma de equilibrio de Freundlich es una ecuación empírica utilizada para la descripción de la adsorción de múltiples capas con la interacción entre las moléculas adsorbidas (12), la cual se presenta en la ecuación 1.
Donde:
Kf: constante de isoterma de Freundlich (mg1-(1/n) L1/ng-1).
n: intensidad de adsorción
Ce: concentración de equilibrio del adsorbato (mg/L),
qe: capacidad de adsorción en equilibrio (mg/g).
1.1.2 El modelo de isoterma de Langmuir
La isoterma de adsorción de Langmuir (13) describe la superficie como homogénea asumiendo que todos los sitios de adsorción tienen igual afinidad con el absorbato y que la adsorción en un punto no afecta la adsorción en el punto adyacente. Se presenta en la ecuación 2.
Donde:
Q0: capacidad de adsorción de monocapa (mg/g)
b: reciproco de la concentración a la que se alcanza la mitad de la saturación del adsorbente.
1.1.3 El modelo de isoterma de Flory-Huggins
El modelo de isoterma de Flory-Huggins 14 deriva el grado de cobertura de superficie adsorbido sobre adsorbente, expresa la viabilidad y la naturaleza es pontánea de adsorción. La ecuación de la isoterma de Flory-Huggins es como se muestra en la ecuación 3.
Donde Θ indica el grado de cobertura de la superficie del adsorbente, K FH y n FH son las constantes de equilibrio Flory -Huggins (L/mg). El grado de cobertura de la superficie del adsorbente se calcula utilizando la ecuación 4.
1.2 Modelos cinéticos
La elucidación de la cinética de sorción es esencial para el diseño del sistema de adsorción y para definir su viabilidad global 15. En este trabajo se exploraron los siguientes modelos cinéticos:
1.2.1 Modelo de pseudo primer orden
La ecuación de Lagergren es la más ampliamente apli cada, esta fue la primera ecuación de velocidad para la sorción de los sistemas líquido-sólido basado en la capacidad sólida 16. Este modelo se define mediante la ecuación 5.
Donde:
qt: cantidad de soluto adsorbido en el equilibrio por unidad de masa de adsorbente en el tiempo, (mg g-1).
K1: constante de velocidad de pseudo primer orden, (s-1).
1.2.2 Modelo de pseudo segundo orden
Este modelo fue desarrollado por Ho y McKay 17 y dado a conocer en 1999. En el modelo de pseudo se gundo orden la ecuación cinética está representada por la ecuación 6.
Donde:
K2: constante de velocidad de pseudo segundo orden, (g mg-1 s-1).
1.2.3 Modelo de Elovich
Este modelo, de aplicación general en procesos de quimisorción, supone que los sitios activos del biosorben te son heterogéneos 18 y por ello exhiben diferentes energías de activación, basándose en un mecanismo de reacción de segundo orden para un proceso de reacción heterogénea. Se define mediante la ecuación 7.
Donde α (g mmol-1 s-1) es la velocidad inicial de ad sorción (g mmol-1 s-1) y p es la constante de desorción.
1.2.4 Modelo de Difusión Intrapartícula
La hipótesis sobre el mecanismo de difusión intrapartícula está basada en el transporte de soluto a través de la estructura interna de los poros del adsorbente y la difusión propiamente dicha en el sólido. La ecuación que define la difusión intrapartícula viene dada por la ecuación 8.
Donde k (mmol g-1 -s1/2) es la constante de velocidad de difusión intrapartícula.
2. METODOLOGÍA
2.1 Materiales
La cáscara de yuca se obtuvo del municipio de San Juan de Betulia, departamento de Sucre, Colombia. El azul de metileno, grado analítico fue obtenido de ABC Laboratorios. El ácido fosfórico 85%, grado analítico, fue adquirido de J.T Baker. El agua utilizada para pre parar todas las soluciones fue destilada y desioniza da. Todos los demás reactivos utilizados fueron grado analítico.
2.2 Equipos
La determinación de la concentración de azul de metileno se realizó espectrofotométricamente utilizando un espectrofotómetro Evolution 60S (Thermo Scienti fic). Los análisis de infrarrojo se realizaron en un es pectrómetro FTIR IRAffinity-1 (Shimadzu) utilizando el método de pastillas de KBr. La determinación de la cantidad de fósforo de la muestra se realizó en un es pectrómetro TXRF S2 Picofox (Bruker).
2.3 Preparación de las muestras
La cáscara de yuca se secó al sol durante 3 días, lue go se molió hasta tamaño de partícula entre 0.5 y 1 mm, se lavó con agua desionizada hasta pH cons tante y por último, se secó en horno a 105°C por 24 horas. La muestra se guardó en un desecador para su posterior uso.
2.4 Modificación de la cáscara de yuca
La muestra de cáscara de yuca seca se mezcló con áci do fosfórico concentrado en relación variable de 1:0.5 a 1:1.5 peso/peso, posteriormente se calentó en un horno a temperaturas variables de 113 a 127°C a un tiempo de reacción constante de 14 horas. La cáscara de yuca modificada se lavó con agua destilada y una solución 0.08 M de bicarbonato de sodio hasta pH de 7.3, se secó a 80°C por 3 horas y se tamizó a tamaños de partícula entre 0.150 -0.250 mm.
2.5 Caracterización de la cáscara de yuca modificada y sin modificar
Las cáscaras de yuca modificada y sin modificar se ca racterizaron mediante espectroscopia de infrarrojo con transformada de Fourier (FTIR) con frecuencia de 400 a 4000 cm-1; análisis próximo: contenido de humedad (ASTM D3173), material volátil (ASTM 3175), conteni do de cenizas y carbono fijo (ASTM D-3172); análisis último utilizando la norma ASTM D3176.
Por otro lado, la cáscara de yuca modificada con mejo res cualidades adsorbentes se caracterizó mediante el índice de yodo para el que se utilizó la Norma Técnica Colombiana (NTC) 4467, y densidad aparente según la Norma ASTM D-2854-70. Además, se analizó el con tenido de fósforo en las cáscaras de yuca sin modificar y después de modificar mediante espectroscopia de fluorescencia de rayos X de reflexión total (TXRF).
2.6 Preparación de las soluciones
Se preparó una solución "stock" de 1000 mg/L de azul de metileno disolviendo 1.000 g de azul de metileno en 1000 mL de agua destilada, esta solución se diluyó para preparar las soluciones requeridas de 100, 200, 300, 400, 500, 600, 700 y 800 mg/L.
2.7 Ensayos de adsorción con azul de metileno
Se tomaron Erlenmeyers de 50 mL y se introdujeron 20 mL de solución de azul de metileno en concentracio nes de 100 a 800 mg/L. posteriormente, se adicionaron 0.2 g de yuca modificada y se sometió a agitación du rante 3 horas.
La capacidad de adsorción de azul de metileno en el equilibrio se puede calculó con la ecuación 9.
Donde qe es la cantidad de adsorción en el equilibrio, Co es la concentración inicial en la fase líquida del colorante, Ce es la concentración en equilibrio en la fase líquida del colorante, V es el volumen de solución y W es la masa del adsorbente usado.
El porcentaje de remoción se calculó mediante la ecua ción 10.
2.8 Cinética de adsorción
Para la determinación de la cinética de adsorción, la cáscara de yuca modificada se puso en contacto con una solución de azul de metileno a una concentración inicial de 465 mg/L. Se tomaron alícuotas de 10 ml a diferentes tiempos y los datos se ajustaron a los dife rentes modelos descritos anteriormente.
3. RESULTADOS Y DISCUSIÓN
3.1 Caracterización de la cáscara de yuca modificada y sin modificar
En la tabla 1 se presentan las principales característi cas de la cáscara de yuca sin modificar y modificada a 127°C y relación biomasa:ácido de 1:1, donde se resal tan algunas diferencias entre ellos, que pueden servir para entender su comportamiento en los procesos de adsorción.
Como se puede observar en la tabla 1, en el análisis próximo tanto la cáscara modificada como la cáscara de yuca sin modificar tienen un bajo contenido de hu medad lo que favorece la molienda e inhibe las po sibles aglomeraciones, el contenido de materia volátil aumenta en la cáscara de la yuca modificada lo cual puede deberse a un posible efecto catalítico del ácido fosfórico durante la pirólisis en los ensayos de los aná lisis próximos 19; por otro lado el porcentaje de ceni zas es bajo y similar en las dos cáscaras; el contenido de carbono fijo es superior en la cáscara de yuca sin modificar, lo cual concuerda con el posible efecto ca talítico del ácido fosfórico; finalmente el contenido de azufre en ambas cáscaras es bajo, lo cual es favorable para el control de la contaminación del medio ambien te, en un posible proceso de disposición de residuos.
Tabla 1 Resultados de la caracterización de la cáscara de la yuca sin modificar y modificada a 127 °C y relación biomasa:ácido 1:1.
| Parámetro | Cáscara de yuca sin modificar | Cáscara de yuca modificada (temperatura de reacción 127 °C, relación biomasa:ácido 1:1) |
|---|---|---|
| Análisis próximos en base seca | ||
| Humedad residual (%) | 7.29 | 7.75 |
| Materia Volátil (%) | 8.15 | 54.40 |
| Ceniza (%) | 1.92 | 6.8 |
| Carbono Fijo (%) | 82.64 | 31.05 |
| Azufre (%) | 0.04 | 0.07 |
| Análisis último | ||
| Carbono (%) | 40.21 | 51.45 |
| Hidrógeno (%) | 6.60 | 5.055 |
| Nitrógeno (%) | 0.90 | 0.527 |
| Oxígeno (%) | 52.29 | 42.96 |
| Otros parámetros | ||
| Fósforo (g/kg) | 0.31 | 14.7 |
| Área Superficial, basado en índice de yodo (m2/g) | - | 320 |
| Densidad aparente (g/ml) | 0.41 | 0.545 |
En el análisis último se puede observar que la yuca modificada posee menor contenido de hidrógeno, ni trógeno y oxígeno, y mayor contenido de carbono en comparación con su precursor. Se infiere que el carbo no e hidrógeno encontrados en la cáscara modificada constituyen la formación de hidrocarburos complejos en mayor medida que en su precursor, por otro lado, el menor contenido de oxígeno en la yuca modificada indica un menor grado de oxidación de éste en com paración a su precursor. La concentración de fósforo de la cáscara de yuca modificada es significativamente alta en comparación con la de la cáscara de yuca sin modificar, lo que sugiere que sí hubo una modifica ción química en términos de inclusión de grupos fos fatos en el adsorbente.
En la figura 1.a se presenta el espectro de la cáscara de la yuca sin modificar y la cáscara de yuca modi ficada con ácido fosfórico a 127°C, relación biomasa: ácido 1:1 con la que se obtuvieron los mejores resulta dos. La banda 3640-3610 cm-1 presenta estiramientos O-H que refleja la presencia de alcoholes primarios, secundarios y terciarios, además de fenoles, ácidos carboxílicos y humedad. Además, presenta una banda entre 500-600 cm-1 que representa flexiones de materia mineral. Se observa una banda entre 600-900 cm-1, que corresponde a estiramientos C-H, los cuales señalan la presencia de vibraciones de hidrógenos enlazados en varias localidades de anillos aromáticos, característi cos de la lignina contenida en la cáscara de la yuca. La banda entre 1000-1100 cm-1 representa estiramientos de C-O-C destacando la presencia de éteres, se observa una banda entre 1580-1650 cm-1 que representa flexio nes de N-H los cuales señalan la presencia de aminas primarias. Se observa una banda entre 1760-2000 cm-1 muestra sobretonos que son característicos de aromá ticos monosustituidos. Se presenta una banda entre 2300-2400 cm-1 que muestra sobretonos característicos de enlaces de carbonos conjugados o disustituidos in saturados o posiblemente CO2 adsorbido producto de la descarboxilación de la biomasa. El espectro FTIR de cáscara de Manihot esculenta sin modificar sugiere una mayor presencia de alcoholes, fenoles, ácidos carboxílicos, aromáticos en comparación a la cáscara de yuca modificada, esto podría ser causado por la destrucción de estos grupos catalizadas por el ácido fosfórico aún a temperaturas tan bajas como las utilizadas en la modificación.

Figura 1 Espectros FTIR para la cáscara de yuca sin modificar y modificada con diferentes relaciones de ácido fosfórico:biomasa y temperaturas de reacción. El orden de los espectros es de arriba hacia abajo tal y como apa recen listados.
De igual manera en la figura 1.b y 1.c pueden obser varse las cáscaras modificadas a distintas relaciones biomasa:ácido comparadas con la cáscara de la yuca sin modificar, donde se puede observar las mismas flexio nes y picos, solo variando el grado de concentración de pendiendo de cada relación aplicada, concluyendo así que las cáscaras de yuca modificada conservan en gran medida las características químicas y estructurales de su precursor.
3.2 Análisis de la remoción de azul de metileno
Los resultados de las variables de respuesta capacidad de ad sorción y porcentaje de remoción se muestran en la tabla 2.
Tabla 2 Porcentaje de remoción y capacidad de adsorción en el equilibro para la remoción de azul de metileno de soluciones acuosas bajo las condiciones estudiadas.
| Temperatura de reacción (°C) | Relación biomasa: ácido | Concentración inicial de azul de metileno (mg/L) | Porcentaje de remoción (%) | Capacidad de adsorción qe (mg/g) |
|---|---|---|---|---|
| 127 | 1:1 | 400 | 99.984 | 39.994 |
| 120 | 1:0.5 | 400 | 99.893 | 39.957 |
| 125 | 1:0.8 | 600 | 99.925 | 59.955 |
| 115 | 1:1.2 | 600 | 99.930 | 59.958 |
| 120 | 1:1.5 | 400 | 99.955 | 39.982 |
| 125 | 1:1.2 | 200 | 99.958 | 19.992 |
| 120 | 1:1 | 100 | 99.896 | 9.990 |
| 113 | 1:1 | 400 | 99.890 | 39.956 |
| 120* | 1:1 | 700 | 99.944 | 69.961 |
| 115 | 1:0.8 | 600 | 99.864 | 59.918 |
| 120 | 1:1 | 400 | 99.946 | 39.978 |
| 115 | 1:1.2 | 200 | 99.874 | 19.975 |
| 125 | 1:0.8 | 200 | 99.945 | 19.989 |
| 120 | 1:1 | 400 | 99.944 | 39.977 |
| 125 | 1:1.2 | 600 | 99.969 | 59.981 |
| 115 | 1:0.8 | 200 | 99.722 | 19.944 |
Al realizar un análisis estadístico de los resultados ob tenidos en la matriz del diseño experimental, se puede observar, a través del análisis de los efectos princi pales, que para el porcentaje de remoción la variable más influyente es la temperatura de modificación de la cáscara de yuca, ya que al aumentar la temperatu ra de 115 a 125°C el porcentaje de remoción aumen ta de 99.88% a 99.98%, la relación biomasa:ácido y la concentración inicial del colorante influyen en menor medida. Por otro lado, la capacidad de adsorción se favorece a concentraciones altas de azul de metileno.
3.3 Isotermas de adsorción
Las isotermas mostradas en la figura 2 se agruparon por relaciones de biomasa:ácido fosfórico. Para ello se usaron los datos de remoción del colorante a las con centraciones iniciales de 300 a 800 mg/L. Obteniéndo se un mejor ajuste con el modelo de Freundlich, como se muestra en la figura 2 para el ensayo realizado con la cáscara de yuca modificada a 120 °C y relación biomasa:ácido fosfórico 1:1.5. Las isotermas de Freun dlich para la adsorción de azul de metileno utilizando cáscara de yuca modificada se aprecian en la figura 3 y los parámetros del modelo en la tabla 3.
Como se puede observar en la figura 2, los modelos de isotermas de adsorción de Langmuir y Flory-Hu ggins presentaron bajos coeficientes de correlación, lo que confirma la no aplicación de éstos modelos para la descripción del proceso de adsorción de azul de metileno en la cáscara de yuca modificada.

Figura 2 Isotermas para la adsorción de azul de metileno usando como adsorbente cáscara de yuca modificada con relaciones de biomasa:ácido fosfórico 1:1.5 a) Freundlich, b) Langmuir y c) Flory-Huggins.

Figura 3 Isoterma de Freundlich para la adsorción de azul de metileno usando como adsorbente cáscara de yuca modificada con relaciones de biomasa:ácido fosfórico a) 1:0.8, b) 1:1.2, c) 1:1.5, d) 1:0.5, e) 1:1
Según la teoría de Freundlich, n revela si la adsorción es favorable: cuando n<1 la adsorción es desfavorable, cuando n=1 la adsorción es lineal, cuando n>1 la ad sorción es favorable (20). De acuerdo con los resulta dos obtenidos, se puede inferir que se obtuvo una ad sorción favorable para la cáscara de yuca modificada a las temperaturas altas de 120, 125 y 127°C, siendo la más favorable ésta última. La mayor adsorción con la cáscara modificada a temperaturas altas se explica por una mayor extensión de la modificación a estas tem peraturas, lo cual al final aumenta la cantidad de sitios activos de adsorción.
Tabla 3 Parámetros del modelo de Freundlich para la adsorción de azul de metileno sobre cáscara de yuca mo dificada con diferentes relaciones de biomasa:ácido fosfórico y temperaturas de reacción.
| Relación biomasa:ácido fosfórico | Temperatura (°C) | n | kf (mg/g) | R2 |
|---|---|---|---|---|
| 1:1 | 127 | 1.925 | 9.138 | 0.928 |
| 120 | 1.016 | 9.261 | 0.008 | |
| 120* | 0.971 | 9.321 | 0.025 | |
| 113 | 0.836 | 7.709 | 0.210 | |
| 1:0.8 | 125 | 1.163 | 8.300 | 0.958 |
| 115 | 0.458 | 6.756 | 0.911 | |
| 1:1.2 | 125 | 1.107 | 11.009 | 0.950 |
| 115 | 0.759 | 9.335 | 0.930 | |
| 1:1.5 | 120 | 1.254 | 8.963 | 0.989 |
| 1:0.5 | 120 | 1.279 | 6.389 | 0.973 |
3.4 Cinética de adsorción
La cinética de adsorción se estudió para la cáscara de yuca modificada que mostró mejores cualidades ad sorbentes, esto es, la cáscara modificada que se activó a una temperatura de 127°C y una relación en peso de biomasa:ácido de 1:1, los ajustes a los modelos ci néticos se muestran en la figura 4. El mejor ajuste se encontró para el modelo de pseudosegundo orden. Este resultado concuerda con otras investigaciones en la cuales para la adsorción de compuestos en solución acuosa utilizando biomasa modificada y sin modificar, el modelo de pseudosegundo orden es el que da mejo res resultados 21, 24).
En la figura 4 a) se muestra el modelo de pseudo pri mer orden, se observa linealidad en los primeros 8 minutos que es donde la adsorción se da de manera más rápida y luego se desvía. El modelo de Elovich mostrado en la figura 4 c) no presenta linealidad en ningún momento del período de adsorción. El mo delo de intrapartícula ayuda a identificar las diver sas etapas de proceso de adsorción (transferencia de masa externa y difusión de los poros) mostrando una serie de zonas lineales de los datos de adsorción. En la figura 4 d) se puede observar la naturaleza multi lineal, esto es, la presencia de dos curvas lineales. Lo que indicó que la primera parte lineal corresponde a la transferencia de masa externa o película de difusión durante los primeros 8 minutos, luego de éste tiempo la difusión de poros o difusión intrapartícula domina en el segundo tramo lineal. Dado al bajo coeficiente de correlación obtenido, este modelo no describe del todo el proceso de cinética de adsorción. Por otro lado, la figura 4 b) representa el modelo de pseudo segundo orden, se puede observar que los datos de adsorción mantienen su perfil lineal durante todo el período de tiempo, además presenta el mayor valor del coeficien te de correlación, lo que sugiere la aplicabilidad de éste modelo para el proceso de adsorción. Esto indica que el proceso está controlado por la adsorción quími ca o quimisorción, involucrando fuerzas de atracción debidas a las valencias o intercambio de electrones entre adsorbente y adsorbato, cabe anotar que las in teracciones físicas eficaces también pueden conducir a esta situación.
Los parámetros de la ecuación de este modelo son qe= 46.696 mg/g, el cual se aproxima al valor experimen tal obtenido, y su respectiva constante de velocidad k es de 0.056 g.mg-1.min-1 (9.3x10-4 g.mg-1.s-1). Una ob servación reportada anteriormente por Ballesteros L. y Villanueva L. 24 afirman que los constante cinética de pseudosegundo orden en la remoción de azul de metileno utilizando como adsorbente carbón activa do granular comercial para una concentración inicial de colorante de 1000 mg/L es k= 3.5x10-5 g.mg-1.s-1. Como se puede observar, la constante de velocidad de los carbones activados comerciales es mucho menor que la de la cáscara de la yuca modificada con ácido fosfórico, por lo que la velocidad de adsorción es ma yor en esta última, para la cual el equilibrio se alcanza a los 124 minutos mientras que para los carbones co merciales se logra a los 600 minutos.
3.5 Superficies de respuesta
En la figura 5 se muestran las superficies de respuesta para el porcentaje de remoción a las concentraciones iniciales de azul de metileno de 100 a 800 mg/L, con base a los resultados obtenidos para la cáscara de la yuca modificada a distintas relaciones biomasa-ácido y en la tabla 4 se observan los respectivos coeficientes de correlación.

Figura 5 Superficie de respuesta para el porcentaje de remoción de azul de metileno a las concentraciones ini ciales de adsorbato de a) 100 mg/L, b) 200 mg/L, c) 300 mg/L, d) 400 mg/L, e) 500 mg/L, f) 600 mg/L, g) 700 mg/L, h) 800 mg/L.
Tabla 4 Coeficientes de correlación para la superficie de respuesta del porcentaje de remoción
| Concentración inicial de azul de metileno (mg/L) | R2 |
|---|---|
| 100 | 0,773 |
| 200 | 0,782 |
| 300 | 0,833 |
| 400 | 0,890 |
| 500 | 0,932 |
| 600 | 0,920 |
| 700 | 0,974 |
| 800 | 0,99 |
Cómo se puede observar en la Figura 5, al aumen tar la temperatura de modificación y la relación biomasa:ácido fosfórico aumenta el porcentaje de re moción de azul de metileno. Además, de acuerdo con los ajustes mostrados en la tabla 4, el porcentaje de remoción se favorece a concentraciones altas de azul de metileno, lo cual sugiere que aún a estas concen traciones no hay saturación del adsorbente, a pesar de la baja área superficial del mismo, lo cual, aunado con los resultados de las isotermas de adsorción, sugiere nuevamente adsorción en múltiples capas.
4. CONCLUSIONES
Se encontró que la cáscara de la yuca modificada es un buen adsorbente para el azul de metileno, la capa cidad de adsorción de la yuca modificada aumenta al aumentar las concentraciones iniciales del colorante y el porcentaje de remoción tiene un ligero aumento del 99.88% al 99.98% al aumentar la temperatura de 115 a 125 °C. Se obtuvieron diferencias significativas en los espectros IR y contenidos de fosfatos al caracterizar la cáscara de cáscara de yuca sin modificar y la cáscara de yuca modificada con ácido fosfórico, lo que evidencia una modificación efectiva. Se observó un buen ajuste de los datos experimentales a la isoterma de Freundlich con un R2 cercano a 1. La cinética de adsorción de azul de metileno se ajusta al modelo de pseudo segundo or den, lo que sugiere que el proceso está controlado por la adsorción química o quimisorción.