INTRODUCCIÓN
El aguaymanto (Physalis peruviana L.) pertenece a las solanáceas originarias de los Andes. Actualmente, su cultivo se realiza en diversos países de América y Europa (Fischer y Melgarejo, 2020) en donde es conocido con diversos nombres en diferentes países como el de uchuva en Colombia o cereza del Perú en México, siendo aguaymanto el termino común en Perú (El-Beltagi et al., 2019). Su composición química reporta concentraciones importantes de fibra cruda (4,61 g/100 g), azúcares totales (8,79 g/100 g), de los cuales, más del 90 % corresponde a azúcares reductores (8,03 g/100 g), vitamina C (26,70 g/100 g), carotenoides (5,95 μg/g), con la una acidez titulable de 1,25 % el cual es expresado como ácido cítrico (Guiné et al., 2020). En cuanto a la concentración de minerales, Muñoz et al. (2021) reportan concentraciones de 256,32, 20,04, 17,80, 16,87 y 94,75 mg/100 g de fruto fresco para potasio, magnesio, calcio, sodio y fósforo respectivamente, no obstante, la composición química durante el almacenamiento es variable con lo que tiende a disminuir su calidad afectando su comercialización, por lo cual su manera más común de comercialización es deshidratada.
La panela es considerada como un azúcar natural obtenida por deshidratación del jugo de caña (Saccharum officinarum), es rica en compuestos bioactivos con propiedades antioxidantes y otros compuestos propios de la caña de azúcar (Alarcon et al., 2021), posee un elevado contenido de azúcares como sacarosa, fructosa y glucosa, los sólidos solubles son de 92,4 °Brix, pH de 6,00, humedad del 7,60 % y azúcares reductores de 6,02 g/100 g (Mesias et al., 2020). Resulta ser un sustituto ventajoso del azúcar blanco debido a que su procesamiento químico, que es mínimo, permite retener una variedad de minerales como hierro, calcio, fosforo, potasio, magnesio, cobre, manganeso, sodio y zinc, además de conservar en gran medida vitaminas como la A, C y D.
En la industria alimentaria, una de las técnicas empleadas cuya finalidad es prolongar la vida útil de los productos alimentarios, conservando la calidad de frutas, hortalizas incluso carnes, es la deshidratación osmótica u osmodeshidratación (OD) que consiste en sumergir el material vegetal es soluciones hipertónicas logrando eliminar el agua con el consecuente flujo de solutos desde la solución osmótica al interior del material vegetal. Este proceso tiene lugar tanto por flujo capilar y difusión dentro de la estructura celular del alimento (Pandiselvam et al., 2021), evitandoel desarrollo de reacciones de pardeamiento enzimático en el alimento tratado a raíz de la disminución de agua, que reduce considerablemente la movilidad; también, se reporta que la disminución de la actividad del agua (aw) impide el desarrollo de microorganismos perjudiciales, por lo que se considera a la OD como una tecnología simple, que requiere bajos costos para su implementación y logra preservar muchas de las propiedades físicas y nutricionales de las muestras alimentarias tratadas (Khuwijitjaru et al., 2022).
La inmersión de alimentos en una solución hipertónica da como resultado un proceso de deshidratación osmótica u osmodeshidratación (OD) con pérdida de agua (WL) del alimento a la solución y ganancia de sólidos de la solución (SG) por parte del alimento. Por esta razón, la OD se usa comúnmente para producir alimentos semideshidratados o enriquecidos por incorporación (Feng et al., 2022); aunque la mayoría de los estudios se centran en los procesos WL y SG, muchas publicaciones abordan los cambios fisicoquímicos y nutricionales resultantes de la DO en la matriz alimentaria y en la solución osmótica, dichos cambios deben manejarse para mejorar la calidad del producto (Rezende y Gomes, 2021).
Pese a ello, una de las desventajas de esta tecnología es el tiempo considerablemente prolongado bajo el cual se desarrolla, lo que en términos de productividad resulta ineficiente (Kowalska et al., 2020), por lo que el empleo de ultrasonido y agitación favorece en gran medida el proceso de OD. La aplicación de ondas sonoras de alta frecuencia (ultrasonido) en la industria alimentaria presenta ventajas importantes frente a los tradicionales métodos de procesamiento de alimentos (Li et al., 2021): el hecho de operar a frecuencias produce continuamente que dentro del alimento se originen regiones de compresión y descompresión rápida con la consecuente formación de microcanales que favorecen los procesos difusivos tanto de agua como se sólidos (Pantelidou et al., 2021). Por su gran potencial, se ha empleado ondas ultrasónicas en la OD de tallos de Pakchoi (Wu et al., 2020), ciruela (Rahaman et al., 2019), Syzygium cumini (Sharma y Dash, 2019), ñame chino (Li et al., 2020), durazno (Chu et al., 2021) y caqui (Bozkir et al., 2019). Asimismo, niveles adecuados de agitación minimizan la resistencia que ofrece el alimento hacia la transferencia de masa en el mismo mediante la disminución de la capa límite de agua que se crea entre el alimento y la solución osmótica, lo que produce una fuerza impulsora que permanece casi constante (Rastogi et al., 2002). Se ha reportado que su aplicación en la OD favorece la eliminación de agua al mismo tiempo que limita la absorción de sólidos en el material alimenticio (Azuara et al., 1996), no obstante, al igual que el ultrasonido reduce el tiempo de proceso de OD.
Ante ello, este trabajo tuvo por objetivo evaluar el efecto de la temperatura y concentración de soluciones de panela en la cinética y coeficiente de difusividad de la transferencia de masa en la osmodeshidratación de aguaymanto (Physalis peruviana) por ultrasonido y por agitación.
METODOLOGÍA
Materia prima
Los frutos de aguaymanto (Physalis peruviana) fueron adquiridos en su madurez fisiológica desde el caserío El Olivo, ubicado al norte de la ciudad de Huamachuco (La Libertad, Perú), a una altitud de 2365 m.s.n.m. con coordenadas 17M - 7,736209 N - 78,081233 E. La zona se caracteriza por mantener un clima relativamente templado con temperaturas que varían desde 17 hasta 22 °C durante el año, con una humedad relativa del 69 %. La panela necesaria para la elaboración de las soluciones hipertónicas tuvo como procedencia el Valle de Condebamba, ubicado al norte de la ciudad de Cajabamba (Cajamarca, Perú), a una altitud de 2807 m.s.n.m. con coordenadas 17M - 7,573604 N - 78,069593 E. La temperatura de esta zona varía entre 15 y 20 °C a lo largo del año con una humedad relativa de 67 %. Con la panela adquirida se prepararon soluciones con concentraciones de 30, 45 y 60 °Brix, las cuales se acondicionaron a temperaturas de 30, 45 y 60 °C cada una antes de ser empleadas para la OD del aguaymanto.
Caracterización fisicoquímica
Los frutos de aguaymanto fueron caracterizados fisicoquímicamente antes del proceso de OD, evaluando humedad (AOAC.23.003), cenizas (AOAC 923.03), fibra (AOAC 991.43), proteína (AOAC 976.05), acidez titulable (AOAC 942.15), pH (AOAC 981.12), sólidos solubles (AOAC 932.12), Azúcares reductores (Método de Lane-Eynon). En tanto que en el aguaymanto fresco y deshidratado osmóticamente se determinó Vitamina C (AOAC 967.21), calcio (AOAC 968.31) y capacidad antioxidante por el método DPPH (Brand-Willams et al., 1995)
Deshidratación osmótica
Los aguaymantos obtenidos en su madurez fisiológica pasaron por un proceso de descerado en NaOH al 0,05 % a 80 °C por 90 s, para ser luego enjuagados en acido crítico a 0,05 % en agua destilada (Encina y Ureña 2007). La proporción entre la fruta y la solución osmótica fue de 1:10. Durante el periodo de OD (7 h) se realizó un control de pesos que sirvieron para determinar los valores de De,w y De,s.
Cinética de osmodeshidratación
La cinética de la OD de aguaymanto se realizó a través del agua pérdida y sólidos ganados (WL y SG respectivamente), para lo cual se emplearon las ecuaciones 1 y 2:
En las que w 0 y 𝑤 𝑓 representan el peso de la muestra antes y después del proceso de OD respectivamente;X0 y Xf representan respectivamente la fracción de agua antes y después del proceso de OD y se expresan en base seca; S0 y Sf representan la fracción de sólidos presentes en las muestras antes y después del proceso de OD.
Cálculo del coeficiente de difusividad promedio
La determinación de De,w y De,s se realizó empleando el modelo matemático que propone Azuara et al., (1992) y que está desarrollado para una geometría esférica de acuerdo con las ecuaciones 3 y 4. Este modelo es un modelo empírico cuya ventaja radica en que no se hace necesario alcanzar el equilibrio para poder predecir sus parámetros, puesto que está basado en el ajuste entre la ecuación y los datos experimentales, además que no toma en consideración aspectos como la estructura del material (Giannakourou et al., 2020).
Técnicas empleadas en la osmodeshidratacións
La agitación del medio osmótico fu de 50 y 100 rpm, para lo cual fue necesario emplear un quipo agitador incubador de marca TERMO SCIENTIFIC y modelo SHKE4450-1CE. El ultrasonido empleado fue de 40 kHz (frecuencia constante) en todos los tratamientos utilizando para ello, un equipo ultrasonido marca BRANSONIC, modelo 8510E-DTH.
Análisis estadístico
La OD del aguaymanto se desarrolló con un diseño factorial 2k + pc de acuerdo con el cuadro 1. En la que k hace referencia a la cantidad de variables independientes y pc a los puntos centrales del diseño.
Para este análisis, se empleó el software estadístico STATISTICA en su versión 12.0. para determinar los coeficientes de regresión con su respectivo nivel de significancia (p < 0,05) para elaborar un modelo codificado de primer orden. El modelo estadístico se validó con un análisis de varianza.
RESULTADOS
Caracterización fisicoquímica del aguaymanto
En la caracterización fisicoquímica del aguaymanto (cuadro 2) destaca su alto contenido de vitamina C (39,96 mg/100 g), azúcares reductores (28,01 mg/100 g), calcio (7,30 mg/100 g) y capacidad antioxidante (10,28 µmolTE/g).
Los valores obtenidos en la caracterización fisicoquímica son ligeramente diferentes a los reportados por otros autores (Bazalar-Pereda et al., 2019; Guiné et al., 2020), lo que se puede atribuir a factores como zona de producción, las condiciones edafológicas, la época de cosecha, la sensibilidad del método de análisis empleado y el estado de madurez de la fruta. El aguaymanto presentó una concentración de agua inicial de 82,50 %, lo que le confiere una susceptibilidad al deterioro microbiano y la acidez fue de 1,50 % (expresado como ácido cítrico) que concuerda con lo reportado en otras investigaciones (Guiné et al., 2020), variando entre 1,3 y 1,7 % (Sepúlveda y Sáenz, 1994).
La capacidad antioxidante de los frutos de aguaymanto es atribuible a diversos compuestos bioactivos presentes en su estructura celular, como la vitamina C, polifenoles, carotenoides y ácido clorogénico. En este sentido, en aguaymanto deshidratado por liofilización se ha reportado contenidos de fenoles (26,24 mg GAE/100 g de fruto fresco), flavonoides (1,48 mg QE/100 g de fruto fresco), taninos (1,74 mg ácido tánico/100 g de fruto fresco) y antocianinas (0,88 µg/100 g de fruto fresco) presentes en el extracto etanólico (Muñoz et al., 2021).
Cinética de osmodeshidratación
Las curvas de la cinética de OD se presentan en las figuras 1 y 2 para WL y SG respectivamente para los tres tratamientos. Estas curvas corresponden a los tratamientos más rigurosos del diseño experimental (panela al 60% p/p, 60 °C y velocidad de 100 rpm para agitación y panela al 60% p/p a 60 °C para ultrasonido y testigo).
La eliminación de humedad (Figura 1) fue rápida en las tres primeras horas, luego de esto la velocidad siguió una tendencia logarítmica, siendo casi constante al cabo del proceso de 420 minutos (7 horas). Esto debido a la microestructura compleja del tejido vegetal, en la que la OD debe explicarse como un proceso donde varios otros mecanismos influyen en la transferencia de masa. Es decir, inmediatamente después de sumergir la fruta en la solución de OD, la presión capilar inicial induce un flujo de solución OD en los vacíos del tejido. Entonces, durante la OD, ocurren simultáneamente otros tres mecanismos: por un lado, ocurre una deshidratación celular causada por gradientes de aw; por otro, existe tanto una difusión de sólidos solubles como una impregnación de células deformadas provocada por cambios de volumen celular. Además de la transferencia de masa, debido a las propiedades viscoelásticas de las células, también se produce simultáneamente una contracción y una relajación estructurales; sin embargo, tienen tasas diferentes (Sulistyawati et al., 2020). Este comportamiento es observado en todos los procesos de osmodeshidratación de la mayoría de las frutas, vegetales y carnes (Prithani y Dash, 2020). Por otro lado, es evidente que la porosidad del material a deshidratar influye directamente en la tasa de WL y SG, como sucede en kiwi o yacón con mayor pérdida de agua en la primera hora del proceso de OD (Brochier et al., 2019) y que la agitación mejora la eliminación de agua comparado con el tratamiento testigo. En la misma línea, el uso de ultrasonido en la OD de aguaymanto permite una máxima remoción de agua (46,62 %), lo que ya es una mejora significativa.
Al respecto, en paralelepípedos de pera, Mehta et al. (2021) indican que factores como concentración de solución osmótica, tiempo y temperatura de proceso favorecen significativamente con un efecto lineal tanto la WL y SG. Este mismo efecto fue observado en este trabajo cuando al incrementar la temperatura y concentración de panela, los valores de WL y SG se incrementaron. De manera similar, Ghellam et al. (2021) reportan valores más altos de pérdida de agua con la aplicación de un vacío pulsado en comparación con una deshidratación osmótica de agitación única.
En la ganancia de sólidos (Figura 2), el proceso de agitación ejerció un leve efecto comparado con la aplicación de ultrasonido. Barman y Badwaik (2017) señalan que en rodajas de carambola se puede conseguir a 2800 rpm una pérdida de agua máxima de 75,65 %, mientras que los sólidos se absorbieron en un máximo de 6,76 %. Por otro lado, los ultrasonidos favorecieron de manera considerable los valores de SG en el aguaymanto, de tal manera que se alcanzó una ganancia de 14,25 %, siendo evidente que la agitación incrementa, aunque no en gran medida como lo hace el ultrasonido, los valores de WL con valores de SG inferiores a aquellos sistemas no agitados.
La WL en la OD con ultrasonido es superior a los valores reportados con otras técnicas (Goula et al., 2017), pues los microcanales que se forman en el interior del material alimenticio, favorecen la difusión de las moléculas de agua (Cichowska et al., 2019). De acuerdo con Mehta et al. (2021), el efecto esponja que ocasiona la aplicación de ultrasonidos mantienen a las moléculas de agua dentro de los capilares del material alimentario de donde se crea canales microscópicos facilitando la eliminación del agua, además la eliminación de gas desde el alimento favorece que los poros se llenen con la solución osmótica incrementando la concentración de sólidos dentro del material alimenticio. Otro efecto positivo de los ultrasonidos es la creación de burbujas, las que al expandirse y colapsar generan el fenómeno llamado cavitación, con lo cual se logra la eliminación de las moléculas de agua que se encuentran adheridas fuertemente en la estructura del alimento (Cichowska et al., 2019), además, la transferencia de materia se ve favorecida por la transmisión de las ondas acústicas provocada por los movimientos oscilatorios del ultrasonido.
Coeficientes de difusividad
En el cuadro 3 se muestran los coeficientes difusivos tanto del agua como de los sólidos en los tratamientos testigo y ultrasonido respectivamente, mientras que en el cuadro 4 se presenta para el tratamiento con agitación.
Cuadro 3 Coeficientes de difusividad para los tratamientos sin movimiento (testigo) y con ultrasonido.
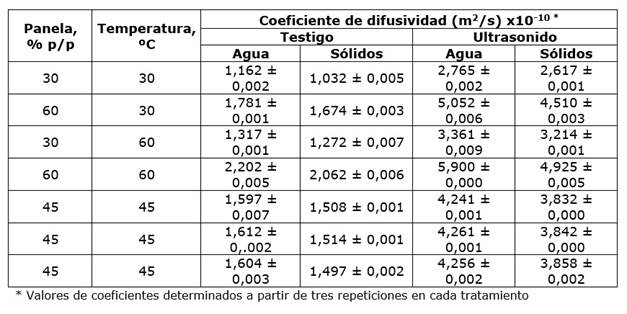
Los coeficientes de difusividad calculados con el modelo de Azuara para el agua variaron entre 1,162 y 2,202 x 10-10 m2/s, en tanto que para sólidos estuvo entre 1,032 y 2,062 x 10-10 m2/s. En el proceso de OD con agitación, los valores de De,w y De,s variaron entre 1,663 y 4,694 x 10-10 m2/s y 1,546 y 4,230 x 10-10 m2/s respectivamente. Por su parte, el ultrasonido incrementó estos valores tanto para sólidos como para agua ya que para De,w y De,s estuvieron entre 2,765 y 5,900 x 10-10 m2/s y 2,617 y 4,925 x 10-10 m2/s respectivamente. Estos valores están dentro del intervalo que indican Nahimana et al. (2011) que señalan que en la OD de cualquier producto alimenticio, los valores de De,w y De,s varían entre 1,4 y 42,2 x 10-10 m2/s y 0,4 y 36,0 x 10-10 m2/s respectivamente, al respecto, Aguirre-García et al. (2022) señalan a la temperatura como la más importante variable de influencia directa en el proceso de OD. Por lo tanto, llevar a cabo un proceso de OD a temperaturas altas, generaría un incremento en la difusión de agua y sólidos con la consecuente pérdida de peso del material, no obstante, puede ocurrir variaciones en los valores de De,w en las mismas condiciones bajo las cuales se desarrolla la OD, lo cual es atribuible a condiciones de madurez de la fruta, el lugar de procedencia y la forma estructural. En la OD de rodajas de kiwi, Prithani y Dash (2020) reportan que la difusividad efectiva del agua de las muestras pretratadas con ultrasonidos (25 kHz x 20 min) osciló entre 5,460 y7,300 x 10-10m2/s y la difusividad de soluto se varió entre 2,925 y 3,511 x 10-10m2/s dentro del intervalo de temperatura 25-60 °C; atribuyendo que la mejora en WL y SG en las rodajas de kiwi pretratadas con ultrasonido fue debida a la rotura celular y la formación de canales microscópicos.
Análisis estadístico
La Figura 3 muestra los gráficos de Pareto para De,w y De,s, donde se aprecia el efecto de las variables independientes. Se aprecia que la agitación no ejerce efecto significativo (p>0,05) de manera lineal sobre De,w y De,s y de manera interaccionada con la temperatura para De,s, lo que no ocurre para el tratamiento testigo y el con aplicación de ultrasonido.
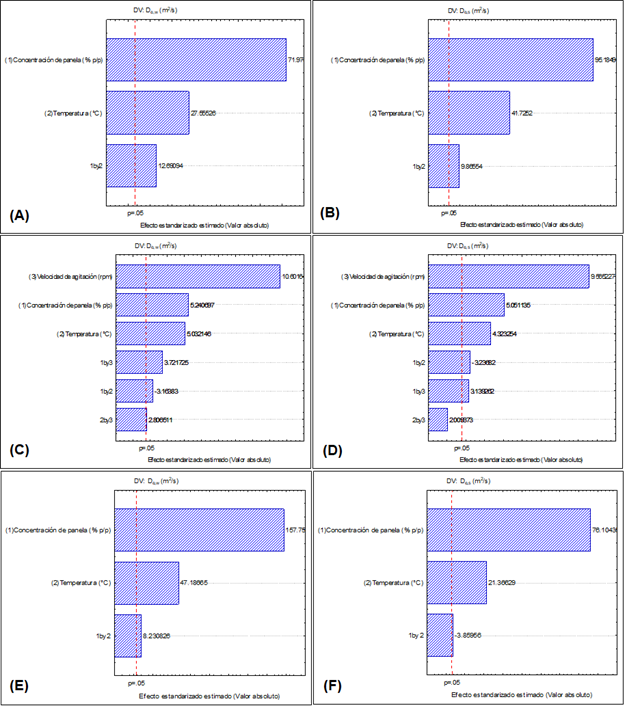
Figura 3 Gráficos de Pareto del efecto de la concentración de panera y temperatura sobre los coeficientes de difusividad para el agua (De,w) y sólidos (De,s). (A) y (B) presentan el gráfico de Pareto para el tratamiento testigo, (C) y (D) para el tratamiento en agitación y (E) y (F) para el tratamiento en ultrasonido.
Propiedades fisicoquímicas del aguaymanto sometido a OD
Los valores de vitamina C, calcio y capacidad antioxidante del aguaymanto sometido a OD en soluciones de panela se presenta en el cuadro 5, para los 3 tratamientos empleados. Los porcentajes que se presentan están calculados en base a las concentraciones del aguaymanto fresco sin deshidratar.
En este cuadro se aprecia una perdida superior de vitamina C en la OD con agitación, pues se pierde hasta el 60,23 %, ligeramente superior a lo que se pierde en el tratamiento sin agitación (58,67 %), siendo la aplicación de ultrasonido la que presentó una mayor protección de esta vitamina con solo el 25,47 %, valores similares a los reportados por Aredo et al. (2012). Al respecto, según Sakooei-Vayghan et al. (2020), existen varios estudios donde reportan que la DO asistida por ultrasonido incrementa la transferencia de compuestos fenólicos del tejido de la fruta a la solución osmótica, como el caso de la OD de manzana, donde una temperatura de 60 °C disminuyó el contenido de compuestos fenólicos y vitamina C de la manzana.
El efecto del ultrasonido sobre la absorción de calcio fue superior a los demás tratamientos, alcanzando un incremento del 11,45 % de este mineral, a lo que le siguió la agitación con 6,46 y el testigo con 0,39 %. Al respecto, en la OD de piña en soluciones de sacarosa común con lactato de calcio al 6 %, reportan un incremento en la concentración de calcio desde 24,472 a 676,317 mg/100 g (Lee y Konsue, 2021).
Por otro lado, se observó que la capacidad antioxidante se relaciona con la concentración de vitamina C, pues en el tratamiento con ultrasonido se encontró la menor pérdida (7,77 %), lo que pone en evidencia estudios realizados en jugos de cítricos donde concluyen que la aplicación de ultrasonido ejerce un efecto protector de esta vitamina (Aadil et al., 2013). De acuerdo con Wu et al. (2020), el ultrasonido favorece la eliminación de oxígeno del interior del alimento, con lo que el proceso oxidativo de la vitamina C se ve reducido y con ello, su capacidad antioxidante.
CONCLUSIONES
Se evidenció una rápida difusión con la consecuente eliminación de agua y ganancia de sólidos en el transcurso de las tres primeras horas de OD, obteniendo valores máximos de WL de 46,62 % en ultrasonido, de 34,53 % en agitación y de 23,67 % en el tratamiento testigo al cabo de 7 horas de proceso. Así mismo, se obtuvieron valores de SG de 14,25 % en ultrasonido, de 7,79 % en agitación y de 4,63 % en el tratamiento testigo. Los coeficientes de difusividad del agua y de los sólidos, fueron superiores en los tratamientos con ultrasonido, el cual también permitió una mejor conservación de vitamina C y capacidad antioxidante del aguaymanto. En consecuencia, el incremento de la concentración del agente osmótico y de la temperatura de proceso produce que los procesos difusivos sean más rápidos. De tal manera de todos los tratamientos, aquel que presentó mejores condiciones finales en el aguaymanto osmodeshidratado fue en la aplicación de ultrasonido en una concentración de panela del 60% en peso y una temperatura de 60 °C.
























