Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO  Similares em Google
Similares em Google
Compartilhar
Revista Colombiana de Química
versão impressa ISSN 0120-2804versão On-line ISSN 2357-3791
Rev.Colomb.Quim. v.35 n.1 Bogotá jun. 2006
Yazmin Yaneth Agámez Pertuz1, Luis Alfredo Oviedo Aguiar1 , Uriel Navarro Uribe2 , Miguel Angel Centeno3 y José Antonio Odriozola3
1Dpto. Química, Facultad de Ciencias, Universidad Nacional de Colombia, Bogotá, Colombia, E - mail:yazya23@yahoo.es
2ECOPETROL-Instituto Colombiano del Petróleo, Piedecuesta, Santander, Colombia
3Instituto de Ciencia de Materiales de Sevilla. Centro Mixto CSIC-Universidad de Sevilla. Avda. Americo Vespucio s/n. 41092 Sevilla. España
RESUMEN
El catalizador de FCC está constituido por partículas de composición compleja donde el componente activo es una zeolita Y. En este trabajo se presentan los resultados texturales y estructurales de una zeolita USY comercial lixiviada, de una serie de catalizadores con 7, 15, 25, 35 y 45% de material activo y los de estos materiales desactivados hidrotérmicamente. Las muestras se caracterizaron por fluorescencia de rayos X (FRX), difracción de rayos X (DRX), resonancia magnética nuclear de silicio (29Si RMN) y fisiadsorción de nitrógeno a 77 K. A partir de estos resultados se hallaron correlaciones entre el volumen de microporo y el contenido de zeolita y entre el grado de cristalinidad y el porcentaje de zeolita. Además, se encontró que un tratamiento con sólo 20% de vapor de agua a 1033 K durante 16 horas destruye los grupos estructurales Si(2Al) y Si(3Al) como reflejo de la dealuminización drástica que sufre el material.
Palabras claves:zeolita USY, tratamiento hidrotérmico, textura, volumen de microporo, estructura, cristalinidad.
ABSTRACT
FCC catalyst is made up of particles of complex composition where the main active component is a Y zeolite. This work presents the textural and structural results of a commercial USY zeolite which had been previously prepared from a set of catalysts with 7, 15, 25, 35 y 45% of active material and of the hydrothermally deactivated materials zeolite. The samples have been characterized by X-ray fluorescence (XRF), X-ray diffraction (XRD), 29Si NMR spectroscopy and nitrogen adsorption at 77K. From these results was found correlations between micropore volume and zeolite content and degree crystallinity and %zeolite. Also, it was found that an hydrothermal treatment at 1033 K with only 20% steam during 16 hours destroys the structural groups Si(2Al) and Si(3Al) as a reflection of the strongly dealumination of the zeolite component of the catalyst.
Key words:USY zeolite, hydrothermal treatment, texture, micropore volume, structure, crystallinity.
INTRODUCCION
Los catalizadores comerciales de ruptura catalítica, son partículas complejas donde una zeolita USY es dispersada en una matriz amorfa constituida por sílice, alúmina, caolín, arcilla y diferentes aditivos como promotores de combustión, reductores de emisiones de SOx, mejoradores de octano y pasivadores de Ni y V. El componente activo más importante del catalizador es la zeolita-Y que es un material cristalino de poro grande con máxima abertura de 0,74 nm, tamaño de unidad de celda aproximadamente de 2,45 nm, una relación Si/Al entre 3 y 5 y que presenta selectividad de forma por tener los sitios más activos localizados en la estructura microporosa (1,2) . Por su estructura de microporos, su gran contribución al área del catalizador, su carácter ácido y por la participación de su superficie externa en la reacción, la zeolita Y es extremadamente activa y selectiva en la conversión de hidrocarburos (3,4). La actividad intrínseca de la zeolita es una función de la densidad y de la fortaleza de los sitios ácidos localizados en los microporos y en el área externa (5), parámetros factibles de controlar en el catalizador variando el contenido de zeolita-Y en una cantidad dada de matriz o ajustando el tamaño de la unidad de celda y las dimensiones del cristal de la zeolita.
El número de sitios ácidos en una zeolita y la fortaleza de éstos son parámetros esenciales que determinan el tipo y la naturaleza de las reacciones que ocurren en un proceso de ruptura catalítica FCC (3,5), donde el catalizador está en contacto a alta temperatura, con un número grande de moléculas de hidrocarburos de alto peso molecular (C25-C100) promoviendo reacciones, donde la zeolita se desactiva por dos mecanismos: reversibles (formación de coque, neutralización de sitios ácidos por especies de carácter básico) e irreversibles (cambios en la estructura porosa, reducción de las dimensiones de la unidad de celda, alteraciones de la acidez, aumento de la relación Si/Al, pérdida de cristalinidad por dealuminización y la generación de material amorfo) que disminuyen severamente la actividad y la selectividad del catalizador (6-11).
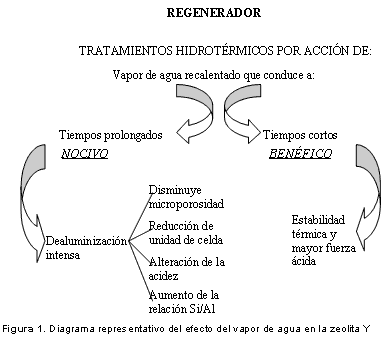
La selectividad de la zeolita varía notablemente con la naturaleza del área externa porque el craqueo de hidrocarburos de alto peso molecular ocurre fundamentalmente en la parte activa de la matriz y/o en los sitios ácidos localizados en la superficie externa de la zeolita-Y (12,13), de donde es factible decir que las zeolitas más selectivas en la ruptura de hidrocarburos pesados son las de menor área externa. A nivel del regenerador, el catalizador gastado es sometido a temperaturas entre 953 y 1063 K en una atmósfera fuertemente oxidante donde el vapor de agua generado durante la combustión del coque, desestabiliza la zeolita (11). La figura 1 muestra que el efecto del vapor de agua recalentado sobre la zeolita varía con la severidad del tratamiento, para tiempos de contacto cortos el efecto es benéfico porque aumenta la estabilidad térmica e incrementa la fortaleza del sitio ácido mientras que en condiciones drásticas, la zeolita experimenta modificaciones profundas derivadas de la dealuminización intensa.
Figura 1.Diagrama representativo del efecto del vapor de agua en la zeolita Y Las modificaciones de tipo textural, estructural y químicas del catalizador a nivel del regenerador, crean la necesidad de realizar una serie de estudios que permitan establecer la naturaleza y la magnitud de estos cambios con referencia a la zeolita en el catalizador no tratado, para evaluar con precisión la variación del volumen de microporo y del área externa, la evolución del grado de cristalinidad y de la acidez y el cambio en la relación Si/Al y en el número de átomos de aluminio por unidad de celda.
La fisiadsorción de N2 a 77 K y baja presión relativa es una técnica importante para la caracterización de sólidos microporosos (14) porque hace factible determinar cuantitativamente el volumen de microporos y el área externa a partir de la curva t obtenida usando los valores de espesor estadístico estimados con referencia a la curva universal de De Boer (15). El grado de cristalinidad entendido como el porcentaje de estructura de zeolita en la masa de muestra analizada (16) se evalua por difracción de rayos X (DRX) tomando como patrón el difractograma de una zeolita de referencia en tanto que las modificaciones de la naturaleza de los sitios ácidos se determina adecuadamente por resonancia mágnética nuclear de silicio (29Si RMN) (17). Como la microporosidad es un parámetro inherente a la naturaleza de la zeolita USY y el proceso catalítico en estos materiales está relacionado con las propiedades ácidas localizada en las microcavidades, en este trabajo se presenta un modelo empírico que simula la variación de la composición de la partícula del catalizador durante el proceso FCC, para evaluar la textura, la estructura y los cambios inducidos por el vapor de agua recalentado en la zeolita y en una serie de mezclas con "caolín clay" (matriz) y clorhidrol (ligante) antes y después del tratamiento.
Parte Experimental
Preparación de los catalizadores. La zeolita USY W.R. Grace Davidson se lixivió con ácido clorhídrico 0,01N a 303 K por 2 horas para remover parte del aluminio no estructural y preservar la estructura cristalina, el material resultante se denominó USYL y se utilizó para sintetizar los catalizadores que contienen 7, 15, 25, 35 y 45% de USYL en "caolín clay" y clorhidrol (18). Para la preparación de los catalizadores en este trabajo, se agregó a una solución con 10% de ligante la cantidad apropiada de "caolín clay" y se adicionó en cada caso, con agitación (100 rpm), el porcentaje requerido de zeolita. La suspensión se homogenizó con ultrasonido durante 15 minutos y se extendió en un recipiente de superficie amplia para someterlo a un proceso cuidadoso de eliminación del solvente a 333 K por 12 horas para evitar la formación de productos de adición con el caolín y con el ligante. El producto de adición resultante se maceró a un tamaño de partícula de 150 micras, se calentó por 1 hora a 373 K aplicando una rampa de 5 K min-1 y se calcinó a 773 K durante 12 horas usando la misma velocidad de calentamiento para prevenir posibles reacciones en estado sólido con formación de nuevas fases entre la zeolita, el caolín y el clorhidrol. Una fracción de cada uno de estos catalizadores y de la zeolita USYL se desactivó hidrotérmicamente a 1033 K en un flujo de aire saturado con 20% de vapor de agua durante 16 horas para obtener la zeolita desactivada denominada USYLV y la serie de catalizadores que contienen este material.
Caracterización de los catalizadores. El análisis químico de la zeolita USYL y USYLV se realizó por Fluorescencia de Rayos X (FRX) en un equipo Siemens SR3000 y el del "caolín clay" y del clorhidrol por absorción atómica en un espectrofotómetro Perkin Elmer Aanalist 300. La composición superficial se estimó por Espectroscopía fotoelectrónica de rayos X (XPS) en un espectrómetro V.G. Microtech MT500 FISONS INSTRUMENTS conectado a un analizador de energía de electrones VG 100 AX utilizando la radiación Ka del aluminio (hv = 1485eV), operando la fuente de rayos X a 15 kV y 20 mA, registrando los espectros con un vacío de 10-9 torr. La corrección de las energías de enlace de los espectros se hizo con referencia al valor 103,3 eV del Si2p.
La unidad de celda y la cristalinidad se determinaron por DRX usando un Difractómetro Shimadzu XRD-600 con anticátodo de cobre calibrado con un patrón de silicio de alta pureza (99,99%) y una desviación estándar de ±0,01. Los difractogramas entre 14 y 35° 2ø, se registraron a temperatura ambiente y con un grado de avance de 0,02° 2ø /s. El parámetro de red se calculó con base en las reflexiones 331, 511, 440, 533, 642, 822, 751 y 664 con ayuda del programa lapod para una red cúbica y la cristalinidad se determinó tomando como referencia en cada caso las intensidades de las reflexiones correspondientes a las de los materiales frescos.
La naturaleza de los sitios ácidos de las zeolitas USYL y USYLV se estableció por RMN de estado sólido en un espectrómetro Brucker DRX-400. Los espectros 29Si NMR se registraron a 79,5 MHz con 500 scans y L.B. de 50 Hz usando tetrametilsilano como referencia.
La evaluación de las propiedades texturales por fisiadsorción de nitrógeno a 77 K se llevó a cabo en un sortómetro Quantacrome Autosorb-1 equipado con un transductor que alcanza una presión relativa de 10-6, desgasificando las muestras por 12 h a 573K. El área total superficial, el volumen de microporo y el área externa se calcularon aplicando la teoría de la curva t con referencia a la curva universal de De Boer para sólidos no porosos (15).
RESULTADOS Y DISCUSIÓN
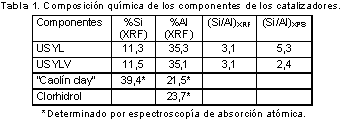
Análisis químico. La tabla 1 muestra la composición química de los componentes de las mezclas catalíticas. El valor de 3,1 encontrado para la relación atómica (Si/Al)FRX de las zeolitas es característico de este tipo de materiales y concuerda con los reportados en la literatura (11,12). El efecto del tratamiento hidrotérmico no se refleja en estos resultados porque corresponde a la relación Si/Al másica. El sólido utilizado como 'matriz' es un "caolín clay" con un contenido de silicio y de aluminio atómico de 21,5 y de 39,4% respectivamente y el clorhidrol usado como ligante tiene un contenido de aluminio de 23,7% y de 44,7% como Al2O3. El tratamiento hidrotérmico produjo una variación en la relación (Si/Al)XPS de 5,3 a 2,4 que corresponde a una disminución del 54,7% reflejo de la migración del aluminio removido hacia la superficie del sólido (19).
Propiedades texturales. En la Figura 2 se presentan las isotermas de adsorción de nitrógeno a 77 K de la zeolita USYL con las de los catalizadores frescos y en la figura 2b las correspondientes a la zeolita USYLV y los productos desactivados. Las gráficas de la figura 2a muestran que independientemente del contenido de zeolita, las isotermas son de tipo I donde el componente microporoso es quien determina la forma y es el responsable de la fuerte adsorción de nitrógeno a bajas presiones.
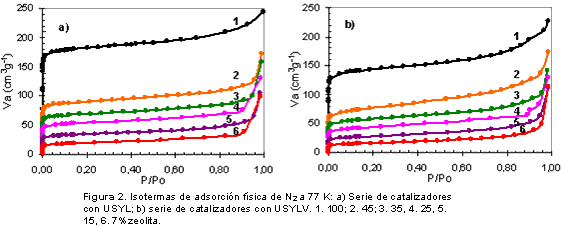
Estos resultados permiten establecer, que como la forma de las isotermas es una característica específica de los materiales microporosos dependiente únicamente del volumen de microporo e independiente del contenido de material y del tratamiento al que es sometido, la microporosidad calculada por fisiadsorción de nitrógeno se puede utilizar para cuantificar la cantidad de material microporoso en una mezcla.
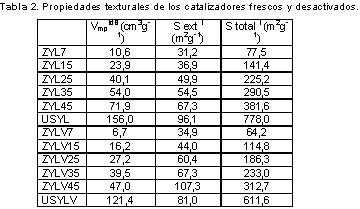
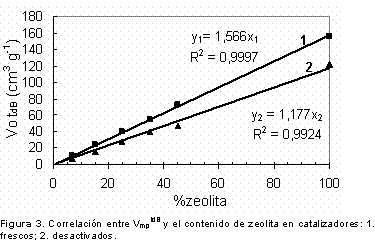
Además en la tabla 2 se establece que para los materiales no tratados, el área microporosa contribuye con más del 80% al área superficial total de los sólidos y el volumen de microporo aumenta linealmente con el contenido de zeolita como se indica en la figura 3, de donde se deduce que para los sólidos frescos y desactivados, la adsorción en los microporos es independiente del contenido de caolín y de ligante y a pesar de que el vapor de agua disminuye drásticamente el volumen de microporo de la zeolita (34,6 cm3g-1) por destrución de masa cristalina, la mesoporosidad generada por el tratamiento hidrotérmico no interfiere en la determinación de la microporosidad remanente.
Caracterización espectroscópica de los catalizadores. Las Figuras 4a y 4b presentan respectivamente, los difractogramas indexados de acuerdo a la norma ASTM D3906 de la zeolita USYL, de la serie de catalizadores frescos y los de la zeolita fresca y de estos materiales desactivados donde se observan las reflexiones características correspondientes a los planos 331, 511, 440, 533, 642, 822, 751 y 664 asignadas a la zeolita y las reflexiones localizadas en 25,3° y 26,7°,2ø del "caolín clay". Estos resultados ponen en evidencia que en la conformación de las mezclas ni durante el tratamiento térmico e hidrotérmico no se produce una nueva fase cristalina resultante de las interacciones de los componentes que afecten la composición del catalizador.
De la comparación de los patrones de difracción de los materiales frescos y desactivados tomados en las mismas condiciones, se deduce que el tratamiento hidrotérmico sólo se manifiesta en la disminución de la intensidad de las reflexiones y en el desplazamiento de éstas hacia valores de 2ø mayores y en la tabla 3 , se establece que por efecto del tratamiento con sólo 20% de vapor de agua a 1033K durante 16 horas, la zeolita USYL sufre modificaciones severas a nivel estructural donde el parámetro de red disminuye en 0,021 nm, la relación Si/Al estructural, (Si/Al)DRX aumenta de 5,8 a 20,9 (3,6 veces) y el número de átomos de aluminio por unidad de celda (NAl)DRX y el porcentaje de cristalinidad disminuye en 24 átomos y en 25,8% respectivamente como consecuencia de la dealuminización que sufre la estructura y la migración del aluminio a la superficie externa de la zeolita (20,21).

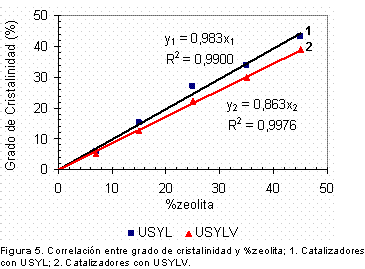
Con base en el comportamiento mostrado en los difractogramas y en el hecho de que no se detectó la formación de un compuesto de adición nuevo generado por los distintos componentes de las mezclas que afecten la composición del catalizador, se relacionó el grado de cristalinidad con el porcentaje de zeolita, como se muestra en la Figura 5 , y se encontró la existencia de una correlación lineal que demuestra que el grado de cristalinidad refleja la cantidad de zeolita remanente después del tratamiento, que esta magnitud se puede determinar bien por DRX, debido a la no interferencia del caolín y el ligante, por lo que, la correlación obtenida con los catalizadores preparados permite calcular el contenido real de zeolita de un catalizador comercial en el rango de composición comprendido entre 0 y 45%zeolita.
El espectro 29Si RMN de la Figura 6 de la zeolita USYL muestra la existencia de las señales en: -106,8; -102,1; -96,2 y -90,0 ppm asignadas respectivamente a los sitios Si(0Al), Si(1Al), Si(2Al) y Si(3Al). La señal en -111,3 ppm es atribuida a una parte amorfa, constituida por especies de silicio no estructural (22). El efecto del 20% de vapor de agua a 1033 K durante 16 horas, destruye los sitios más ricos en aluminio, Si(3Al) y Si(2Al) y reduce drásticamente los sitios Si(1Al), dejando principalmente en la estructura de la zeolita los sitios Si(0Al).
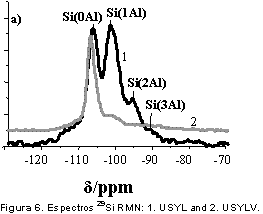
La cuantificación de los espectros 29Si RMN de la zeolita USYL y USYLV reportada en la Tabla 4 indica que el tratamiento hidrotérmico genera pequeños cambios en el desplazamiento químico de los sitios Si(0Al) y Si(1Al), produce la desaparición de los sitios Si(2Al) y Si(3Al) y ocasiona el incremento de 43,4% en la cantidad de sitios Si(0Al). Estos resultados y el aumento de 4,5 a 17 en la relación (Si/Al)29Si RMN estructural concuerda con la tendencia hallada por DRX y corrobora que el tratamiento con sólo 20% de vapor de agua en las condiciones de este trabajo genera cambios sustanciales en la composición química y en la estructura de la zeolita.

CONCLUSIONES
La adsorción de nitrógeno a 77 K y baja presión relativa se puede utilizar para calcular el volumen de microporo y la cantidad de material microporoso en mezclas de zeolita y material amorfo porque la isoterma producida es característica e independiente del contenido y del tratamiento térmico e hidrotérmico que sufre el material microporoso. Bajo condiciones de limpieza superficial adecuadas y tiempos de equilibrios apropiados se puede calcular la cantidad real de zeolita en un catalizador en función del volumen de microporo determinado por fisiadsorción de nitrógeno a 77 K de acuerdo a la ecuación VotdB = 1,566 * %zeolita para los catalizadores frescos y VotdB = 1,177 * %zeolita para los catalizadores desactivados.
El tratamiento hidrotérmico con 20% de vapor de agua a 1033 K por 16 horas es suficiente para bajar la cristalinidad de la zeolita USYL a 74,2% y reducir la microporosidad en 22,2%. Además, ocasiona modificaciones severas en la composición de la estructura cristalina remanente ya que cambia la distribución de la fuerza ácida disminuyendo el número de átomos de aluminio por unidad de celda en un 38,5% y aumentando la fortaleza de los sitios ácidos residuales destruyendo drásticamente los entornos Si(2Al) y Si(3Al).
Las correlaciones: %Cristalinidad = 0,99 * %zeolita para el catalizador fresco y %Cristalinidad = 0,86 * %zeolita para el catalizador desactivado, encontradas en este trabajo, tienen una aplicación práctica muy importante es los procesos de evaluación y selección de los catalizadores de FCC, porque permiten calcular el contenido real de zeolita en un catalizador comercial en el intervalo de composición entre 0 y 45% de este material.
Agradecimientos:Al Instituto Colombiano del Petróleo por el suministro de la zeolita USY y el "caolín clay" y a la Universidad Nacional de Colombia por el soporte financiero.
BIBLIOGRAFIA
1.Humpphries, A.; Harris, D.H.; O'Connor, P. (1993). The nature of active sites in zeolites: Influence on catalyst performance. Fluid Catalytic Cracking, Studies in Surface Science and Catalysis. J.S.Maguee an M.M. Mitchell, Jr. Editors. Elsevier, Amsterdam. 76, pp.41-81. [ Links ]
2.Stockwell, D.; Brown, S.; Ryu, J.Y. (2005). U.S. Patent 6.942.784. [ Links ]
3.Dwyer, J.; Rawlence, D. (1993). Fluid catalytic cracking: chemistry. Catalysis Today 18, 487-507. [ Links ]
4.Williams, B.A.; Miller, J.T.; Snurr, R.Q.; Kung, H.H. (2000). An explanation for the differences in catalytic hydrocarbon cracking activity between steam and chemically dealuminated Y zeolites. Microporous and Mesoporous Materials 35-36, 61-74. [ Links ]
5.Kung, H.H.; Williams, B.A.; Babitz, S.M.; Miller, J.T.; Snurr, R.Q. (1999). Towards understanding the enhanced cracking activity of steamed Y zeolites. Catalysis Today 52, 91-98. [ Links ]
6.Man, R. (1993). Fluid catalytic cracking: some recent developments in catalyst particle design and unit hardware. Catalysis Today 18, 509-528. [ Links ]
7.He, Ming-Yuan. (2002). The development of catalytic cracking catalysts: acidic property related catalytic performance. Catalysis Today 73, 49-55. [ Links ]
8.Al-Khattaf, S. (2002). The influence of Y-zeolite unit cell size on the performance of FCC catalytsts during gas oil catalytic cracking. Applied Catalysis A: General 231, 293-306. [ Links ]
9.Corma, A.; Grande, M.S.; Gonzalez-Alfaro, V.; Orchilles, A.V. (1996). Cracking activity and hydrothermal stability of MCM-41 and its comparison with amorphous silica-alumina and a USY zeolite. Journals of Catalysts 159, 375-382. [ Links ]
10.Pine, L.A.; Maher, P.J.; Wachter, W.A. (1984). Prediction of cracking catalyst behavior by a zeolite unit cell size model. Journal of Catalysis 85, 466-476. [ Links ]
11.Navarro, U.; Trujillo, C.A.; Oviedo, L.A.; Lobo, R. (2002). Impact of deactivation conditions on the acidity of Y zeolites used in the formulation of FCC catalysts, studied by FTIR of adsorbed CO. Journal of Catalysis 211 (1) 64-74. [ Links ]
12.De la Puente, G.; Falabella Sousa-Aguiar, E.; Figueiredo Costa, A.; Sedran, U. (2003). The influence on selectivity of the aluminum content in the matrix of FCC catalysts. Applied Catalysis A: General 242, 381-391. [ Links ]
13.Al-Khattaf, S.; de Lasa, H. (2002). The role of diffusion in alkyl-benzenes catalytic cracking. Applied Catalysis A: General 226, 139-153. [ Links ]
14.Falabella Sousa-Aguiar, E.; Liebsch, A.; Chaves, B.C.; Costa, A. (1998). Influence of the external surface area of small crystallite zeolites on the micropore volume determination. Microporous and Mesoporous Materials 25, 185-192. [ Links ]
15.De Boer, J.H.; Linsen, B.G.; Osinga, Th.J. (1965). Studies on pore systems in catalysts. VI. The universal t-curve. Journal of Catalysis 4, 643-648. [ Links ]
16.Carvalho, A.P.; Brotas de Carvalho, M.; Pires, J. (1997). Degree of crystallinity of dealuminated offretites determinated by X-ray diffraction and by a new method based on nitrogen adsorption. Zeolites 19, 383-386. [ Links ]
17.Shertukde, P.; Keith Hall, W.; Dereppe, J.M.; Marcelin, G. (1993). Acidity of H-Y zeolites: Role of Extralattice aluminum. Journal of Catalysis 139, 468-481. [ Links ]
18.Lutz, W.; Ruscher, C.H.; Heidemann, D. (2002). Determination of the framework and non-framework [SiO2] and [AlO2] species of steamed and leached faujasite type zeolites: calibration of IR, NMR, and XRD data by chemical methods. Microporous and Mesoporous Materials 55, 193-202. [ Links ]
19.Wang, Q.L.; Giannetto, G.; Torrealba, M.; Perot, G.; Kappenstein, C.; Guisnet, M. (1991). Dealumination of zeolites II. Kinetic study of the dealumination by hydrothermal treatment of a NH4NaY zeolite. Journal of Catalysis 130 (2) 459-470. [ Links ]
20.Scherzer, J. (1993). Correlation between catalyst formulation and catalytic properties. Fluid Catalytic Cracking, Studies in Surface Science and Catalysis. J.S.Maguee an M.M. Mitchell, Jr. Editors. Elsevier, Amsterdam. 76, pp.145-182. [ Links ]
21.Peters, A.W. (1993). Instrumental methods of FCC catalyst characterization. Fluid Catalytic Cracking, Studies in Surface Science and Catalysis. J.S.Maguee an M.M. Mitchell, Jr. Editors. Elsevier, Amsterdam. 76, pp.183-222. [ Links ]
22.Engelhardt, G. (2001). Solid state NMR spectroscopy applied to zeolites. Introduction to zeolite science and practice, Studies in Surface Science and Catalysis. H. Bekkum, E.M. Flanigen, P.A. Jacobs, J.C. Jansen Editors. Elsevier, Amsterdam. 137, pp.387-418. [ Links ]














