Pneumocystis jirovecii es un agente infeccioso oportunista que puede causar neumonía en pacientes inmunosuprimidos y que se conoce como neumonitis por Pneumocystis. Se presenta, especialmente, en pacientes con el virus de la inmunodeficiencia humana (HIV) y, en menor porcentaje, en receptores de trasplantes de órganos sólidos. Su incidencia después del trasplante renal es inferior al 5 %, pero cuando se presenta, lo hace de manera súbita y grave y con una alta incidencia de insuficiencia respiratoria hipoxémica. En 59 % de los pacientes se requiere asistencia respiratoria mecánica, lo cual se ha asociado con la posibilidad de perder el injerto y con una mortalidad de hasta 39 % 1,2. Los principales factores de riesgo de la infección son con medicamentos supresores de células T, el manejo del rechazo agudo, la infección previa por citomegalovirus, la linfopenia prolongada y el contacto con portadores hospitalizados o atendidos en hogares de cuidado.
Esta infección se presenta como consecuencia de una reinfección por exposición a portadores asintomáticos o por la reactivación de una colonización crónica 2,3. Dado que en la mayoría de los casos los síntomas son sutiles y puede no presentarse inflamación, la sospecha clínica es fundamental 1. La deshidrogenasa láctica y el beta-D-glucano son marcadores no invasivos de utilidad, pero son inespecíficos y no logran determinar la gravedad de la enfermedad ni la respuesta terapéutica 2,4,5. La reacción en cadena de la polimerasa (PCR) para detectar el microorganismo, en cambio, tiene muy buenas sensibilidad y especificidad, pero no logra diferenciar la colonización previa de la infección aguda. Sin embargo, cuando resulta positiva, a pesar de la citología negativa, y hay síntomas sugestivos de inmunosupresión, se recomienda el tratamiento 1,2. La visualización de estructuras indicativas de P. jirovecii mediante el uso de tinciones de plata metenamina o calcoflúor en la citología del lavado broncoalveolar, confirma el diagnóstico y son pocos los casos en los que se requiere la biopsia pulmonar 1, 2).
Caso 1
Se presenta el caso de un hombre de 54 años que había recibido un trasplante renal seis años antes, y en quien el injerto había tenido una buena evolución, sin episodios de rechazo. Había recibido tratamiento inmunosupresor de base con 500 mg de micofenolato de mofetilo cada 12 horas, 50 mg de ciclosporina cada 12 horas y 5 mg de prednisolona al día; la creatinina basal era de 1,1 mg/dl.
Consultó tras cinco días de fiebre, malestar general, disnea y tos; presentó hipoxemia grave y rápida progresión a insuficiencia respiratoria aguda que requirió asistencia respiratoria mecánica.
En la radiografía de tórax, se encontró un infiltrado intersticial basal derecho, por lo que se inició empíricamente la administración de piperacilinatazobactam y claritromicina, sin que el paciente presentara mejoría. En una nueva radiografía, se encontraron infiltrados generalizados de predominio parahiliar (figura 1), por lo que se practicó una fibrobroncoscopia. El lavado broncoalveolar fue negativo y no hubo aislamiento microbiológico (cuadro 1).
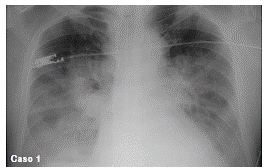
Figura 1 Radiografía de tórax del paciente del caso 1. Se observan infiltrados intersticiales de predominio parahiliar
Cuadro 1 Resultados de los exámenes de laboratorio
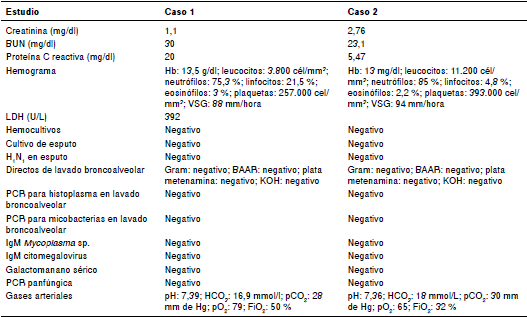
BUN: nitrógeno ureico; Hb: hemoglobina; VSG: velocidad de sedimentación globular; LDH: lactato deshidrogenasa; BAAR: bacilos ácido-alcohol resistentes; KOH: hidróxido de potasio; PCR: reacción en cadena de polimerasa; pCO2: presión parcal de dióxido de carbono
Se sospechó, entonces, la presencia de gérmenes oportunistas y se añadieron trimetoprim-sulfametoxazol, anfotericina B y esteroides al tratamiento.
En la biopsia pulmonar, se observó daño alveolar difuso y la PCR fue positiva para P. jirovecii en el tejido, pero negativa en el lavado broncoalveolar. La condición clínica del paciente se deterioró progresivamente hasta presentar falla orgánica múltiple e hipoxemia resistente al tratamiento; finalmente, el paciente falleció diez días después de ser hospitalizado.
Caso 2
Este es el caso de una paciente de 28 años que había recibido un trasplante de riñón seis años antes. El protocolo de inmunosupresión utilizado inicialmente incluyó anticalcineurínicos, que luego se sustituyeron por la proteína mTOR (mammalian Target of Rapamycin) debido a la toxicidad. La creatinina basal de la paciente era de 1,5 mg/dl.
Consultó tras 15 días de tos seca y fiebre intermitente y, en el momento del ingreso, presentaba buen estado general, sin dificultad respiratoria.
En la radiografía inicial de tórax, se observaron infiltrados mixtos bilaterales de predominio basal (figura 2). En la tomografía de tórax de alta resolución, se evidenciaron opacidades en vidrio esmerilado de localización bilateral difusa que comprometían ambos campos pulmonares (figura 2).
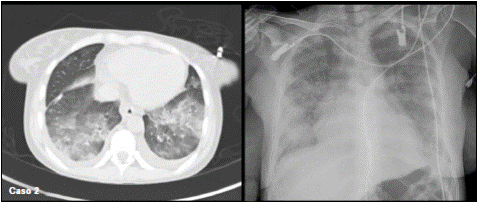
Figura 2 Tomografía axial de tórax de alta resolución de la paciente del caso 2. a. Se observan opacidades en vidrio esmerilado de localización bilateral difusa, que comprometen ambos campos pulmonares. b. Radiografía de tórax inicial con infiltrados mixtos de predominio basal.
Dado el buen estado clínico de la paciente, no se utilizaron antibióticos inicialmente, se solicitaron estudios complementarios (cuadro 1) y se suspendió el sirolimus.
Se le practicó una fibrobroncoscopia y un día después presentó deterioro clínico con rápida progresión a insuficiencia respiratoria hipoxémica, por lo que hubo necesidad de darle asistencia respiratoria mecánica no invasiva. Además, presentó deterioro de la función renal, por lo cual se inició el tratamiento antibiótico empírico con piperacilina-tazobactam y claritromicina.
Una vez se obtuvo el reporte de la citología del lavado broncoalveolar, que demostró la presencia de estructuras indicativas de P. jirovecii en la tinción de plata metenamina, se inició el tratamiento con trimetoprim-sulfametoxazol y esteroides, con el cual se resolvió la insuficiencia respiratoria y se recuperó la función renal basal.
Discusión
A pesar de que la profilaxis con trimetoprimsulfametoxazol ha disminuido el número de casos de neumonitis por P. jirovecii en pacientes después de un trasplante renal, aún no hay consenso sobre el momento de su aparición, que puede darse entre los tres y los seis meses del trasplante, tiempo en el cual las dosis de medicamentos inmunosupresores son mayores, e incluso un año después o al cabo de un período indefinido.
En reportes previos sobre la aparición de esta condición después de un periodo largo del trasplante se informa de incidencias de 33 % a los 12 meses y de hasta 18 % después de 10 años 1,6,7.
Se describen dos casos de pacientes que presentaron insuficiencia respiratoria hipoxémica por P. jirovecii seis años después del trasplante renal, con resultados diferentes.
Las experiencias previas demuestran que los resultados de la profilaxis son variables. Por ejemplo, Anand, et al. 8, informaron sobre la experiencia en un solo centro en casos en los cuales se administró trimetoprim-sulfametoxazol solo durante un mes después del trasplante renal. De 1.352 pacientes, a cuatro (0,3 %) se les diagnosticó neumonitis por P.jirovecii; en dos, el diagnóstico se hizo en el primer año del trasplante, ambos después de los primeros seis meses, y en los otros dos, 15 meses después.
Por otra parte, Borstnar, et al. 9, demostraron una disminución de la incidencia de la neumonitis por P. jirovecii al suministrar profilaxis durante más de un año, y registraron su aparición entre los seis y hasta los 148 meses después del trasplante. En los pacientes con trasplante renal se ha encontrado que una baja tasa de filtración glomerular y la linfopenia son factores de riesgo para la infección, con una mediana de 10,2 años a partir del primer año de profilaxis 1. La edad, la infección por citomegalovirus y el recuento total de linfocitos, también se consideran criterios predictores de neumonía por P. jirovecii en receptores de trasplante de órganos sólidos 1.
En nuestra institución, la profilaxis con trimetoprimsulfametoxazol se aplica durante los primeros seis meses del trasplante renal. Sin embargo, en los casos que se describen, los episodios de neumonía por P. jirovecii se presentaron años después, sin relación con un factor de riesgo específico. Ambos pacientes recibían dosis mínimas de medicamentos inmunosupresores, ninguno recibía profilaxis contra P. jirovecii y no habían presentado episodios de rechazo, lo que sugiere que el riesgo de este agente oportunista persiste en el tiempo y siempre se debe tener presente en el diagnóstico diferencial ante la presencia de síntomas respiratorios o neumonitis en los pacientes con trasplante, independientemente del tiempo de evolución.
No se recomienda la profilaxis indefinida, pues su incidencia no es tan alta, y los efectos secundarios, especialmente la disfunción renal y las tasas de resistencia en bacilos Gram negativos, limitan el beneficio, por lo que solamente se recomienda en casos de rechazo acompañado del aumento de los medicamentos inmunosupresores, así como en casos de brotes 6,10.
El trimetoprim-sulfametoxazol se considera el tratamiento de elección. Sin embargo, el tiempo de administración no se ha establecido para los pacientes con trasplante de órganos, y tampoco para el uso concomitante de esteroides. En las guías se recomienda administrar metilprednisolona en dosis de 40 a 60 mg dos veces al día durante cinco a siete días y luego suspenderla progresivamente en el curso de una a dos semanas, para un total de 14 a 21 días según la gravedad de los casos 2.
Otros tratamientos con dapsona, atuovacuona o primaquina más clindamicina o pentamidina, se recomiendan para los casos en los cuales está contraindicado el trimetoprim-sulfametoxazol, ya sea por alergia o por deterioro de la función renal 2. Solo se cuenta con un estudio prospectivo que demostró la eficacia de la atovaquona en la profilaxis de neumonía por P. jirovecii, con menores efectos secundarios que el trimetoprim-sulfametoxazol 11.
Por otro lado, el tratamiento con pentamidina se ha asociado con mayor toxicidad y se ha demostrado que con dapsona solo es útil en casos leves a moderados 1,2. Cuando existe resistencia o intolerancia al tratamiento con trimetoprim-sulfametoxazol, las opciones son escasas.
Tu, et al. 12, reportaron mejores resultados en tres casos de neumonía por P. jirovecii en pacientes con trasplante renal tratados con caspofungina y trimetoprim-sulfametoxazol, pues los efectos secundarios fueron menores, especialmente en pacientes críticos con granulocitopenia, compromiso hepático y deterioro de la función del injerto.
El uso de esteroides en los pacientes con hipoxemia se ha estudiado más en aquellos con HIV, en quienes mejora la supervivencia. En otro estudio en pacientes sin HIV, el resultado fue mejor 1. Sin embargo, en otros, las altas dosis de esteroides se asociaron con un incremento de la mortalidad 2, o no se encontró diferencia en la supervivencia en pacientes con trasplante de órganos sólidos 3.
En este contexto, es importante hacer más estudios que validen esta recomendación 2. En los dos casos que se presentan, los pacientes recibieron tratamiento con trimetoprim-sulfametoxazol y esteroides debido a la gravedad de la insuficiencia respiratoria, y los resultados difirieron, pues uno de ellos murió en tanto que la otra se recuperó completamente.














