INTRODUCCIÓN
Los tumores de glándulas salivales constituyen del 2 % al 6,5 % de todas las neoplasias de cabeza y cuello. El 80 % son de origen epitelial y el 75 % son benignos; el más frecuente es el adenoma pleomórfico1. Existen otros tipos de adenoma, entre ellos el canalicular, término acuñado en 1953 por Bauer y colaboradores2, retomado en 1983 por Gardner y colaboradores3 y finalmente incluido en la clasificación de la Organización Mundial de la Salud del año 20054.
A continuación describimos un caso de adenoma canalicular (AC) multifocal con antecedente de un tumor similar en la misma localización resecado 13 años antes.
PRESENTACIÓN DEL CASO
Mujer de 58 años que consultó en junio de 2015 por presentar un nódulo elástico de 8 mm de diámetro y 10 meses de evolución en el labio superior. Tiene el antecedente de una lesión de características similares en la misma localización resecada 13 años antes, que fue diagnosticada como compatible con AC de células basales de glándula salival menor.
Se extirpó completamente la lesión actual junto con una glándula salival accesoria adyacente. Se obtuvieron dos fragmentos de tejido: el primero de 0,8 x 0,8 x 0,6 cm, pardo con superficie externa lisa y consistencia firme; el segundo, de 0,4 x 0,3 x 0,3 cm, pardo claro de consistencia blanda. El estudio histopatológico de la lesión mostró un nódulo tumoral encapsulado constituido por células columnares dispuestas en cordones de una o dos hileras, que se interconectaban en algunas zonas para formar estructuras tubulares semejantes a ductos. Algunos de estos estaban dilatados formando pseudoquistes ocupados por material eosinófilo y ocasionales histiocitos espumosos. En medio del componente epitelial, se reconoció un estroma de tejido conectivo laxo mixoide ricamente vascularizado. No se observaron pleomorfismo, necrosis ni mitosis atípicas (Figura 1). Los estudios de inmunohistoquímica mostraron en las células tumorales positividad fuerte y difusa con los marcadores pancitoqueratina (AE1-AE3), S100, CEAp y vimentina; positividad focal con el antígeno de membrana epitelial (EMA, por su sigla en inglés) y proteína ácida glial fibrilar (GFAP, por su sigla en inglés). El índice de proliferación celular con Ki67 no superó el 2 % y los marcadores para células mioepiteliales, calponina y p63 fueron negativos (Figura 2). Con estos hallazgos se hizo el diagnóstico de AC de glándula salival menor.
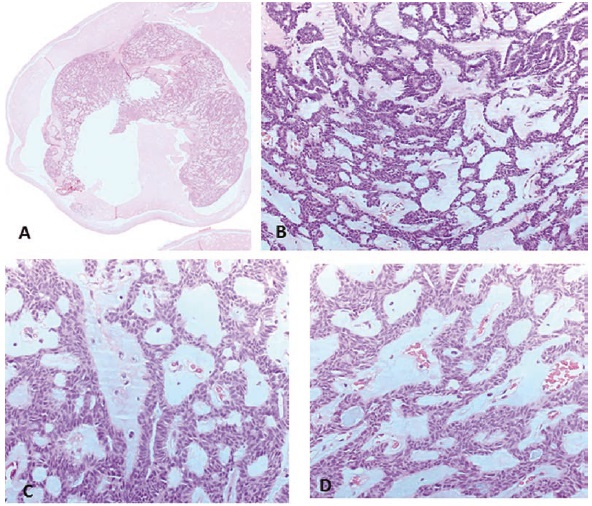
Figura 1 Adenoma canalicular. A. Nódulo circunscrito y encapsulado (HE, 2,5X). B. Se observan cordones de doble fila de células columnares o cúbicas con patrón alternante (HE, 20X). C. Los cordones que están en contacto estrecho se separan para formar estructuras similares a ductos (HE, 40X). D. Estroma laxo mixoide ricamente vascularizado, (HE, 40X)

Figura 2 Marcadores de inmunohistoquímica. A. Positividad nuclear y citoplasmática para S100 (40X). B. Positividad citoplasmática fuerte y difusa con AE1-AE3 (40X). C. Positividad citoplasmática en degradé con vimentina (40X). D. Positividad citoplasmática con CEA (40X). E. Calponina negativa (40X). F. Ki67 menor del 2 % (40X)
El segundo fragmento correspondió a una glándula salival menor constituida por lóbulos de acinos mucosos y el sistema usual de ductos. Se identificaron tres focos incipientes de una lesión tumoral nodular no encapsulada; el mayor de 1,1 mm, de características morfológicas similares a las del tumor ya descrito. Los estudios de inmunohistoquímica mostraron en los focos de células tumorales positividad fuerte y difusa con los marcadores pancitoqueratina (AE1-AE3) y S100. Fueron negativos para células mioepiteliales, los marcadores calponina y p63. Estos hallazgos se interpretaron como focos incipientes de AC que sugirieron multifocalidad de esta neoplasia (Figura 3). En el seguimiento de 5 meses no se ha observado recurrencia de la lesión.
DISCUSIÓN
El AC es una neoplasia epitelial benigna infrecuente (1 % de las neoplasias de glándulas salivales), que se origina casi exclusivamente en las glándulas salivales menores. Se localiza en la cavidad oral con predilección por el labio superior (70 % a 90 % de los casos) y rara vez en otros sitios, como el paladar y la parótida1)(3)(5)(6)(7)(8)(9. Suele presentarse en adultos mayores de 50 años con máxima incidencia en la séptima década. Es más común en mujeres que en hombres (relación 2:1)5)(7. Estos tumores se manifiestan como nódulos submucosos, indoloros, no ulcerados de crecimiento lento, que miden de 0,5 a 3 cm1)(5)(7. Rara vez son multifocales1)(3)(7)(10 y de acuerdo con Thompson y colaboradores, esto se presenta en el 9 % de los casos5.
HALLAZGOS MORFOLÓGICOS
Macroscópicamente se observan como nódulos circunscritos y usualmente encapsulados. En la histopatología, se observan cordones de doble fila de células columnares o cúbicas con patrón alternante descrito como “collar de perlas” (beading): los cordones se disponen paralelamente en contacto estrecho y posteriormente se separan formando estructuras similares a ductos que dan origen al término “canalicular” de este tumor1)(3)(4)(5)(6)(7)(8)(9)(11)(12)(13)(14. Estas estructuras similares a ductos, pueden dilatarse y llegar a conformar quistes con formaciones papilares1)(5)(11. Se pueden observar mórulas de células epiteliales intraluminales e histiocitos espumosos5.
Las células tumorales son monótonas con bordes indistinguibles, núcleos ovales o redondos y sin evidencia de mitosis1)(4)(5)(7. Un hallazgo histológico importante es la ausencia de células mioepiteliales5. El estroma es mixoide, edematoso, hipocelular y ricamente vascularizado por vénulas y capilares congestivos1)(3)(4)(5)(6)(7. Nódulos multifocales no encapsulados de características histológicas similares se localizan adyacentes a la masa principal; este hallazgo es más evidente en la microscopía que en la clínica1)(7)(15)(16.
INMUNOHISTOQUÍMICA
Este tumor es positivo para pancitoqueratinas (AE1- AE3), S100, SOX 10 y vimentina. La GFAP puede ser positiva en un patrón aislado y lineal en la interfaz del tumor con el tejido conectivo1)(5)(17)(18)(19. La expresión del EMA es variable1)(4)(5)(6)(14)(18 y el índice de proliferación celular con Ki67 es menor del 2 %18. Los marcadores utilizados para la demostración de células mioepiteliales: calponina, actina del músculo liso, miosina de cadena pesada y p63 son negativos1)(5)(18.
HISTOGÉNESIS
Para algunos autores el AC se origina de las células luminales de los ductos intercalares5, mientras que para otros, los hallazgos ultraestructurales y de inmunohistoquímica sugieren que se origina de una célula intermedia con características de ducto intercalar y estriado20.
DIAGNÓSTICO DIFERENCIAL
Los diagnósticos diferenciales más importantes son los siguientes: adenoma de células basales, carcinoma adenoide quístico y adenoma pleomórfico1. El 70 % de los adenomas de células basales se presentan en la glándula parótida y el 20 % en el labio superior1. La variante tubular, compuesta por pequeñas estructuras similares a ductos constituidos por células columnares uniformes sin evidencia de mitosis atípicas puede recordar la morfología del AC; sin embargo, los marcadores mioepiteliales son con frecuencia positivos en los adenomas basales tubulares y negativos en el AC1)(5.
El adenoma pleomórfico presenta una matriz mixocondroide y posee células mioepiteliales positivas para p63, calponina, actina del músculo liso y miosina de cadena pesada5)(18. Otra diferencia con el AC es que la GFAP no presenta patrón lineal sino positividad fuerte y difusa en las células tumorales17.
El carcinoma adenoide quístico muestra un patrón bifásico infiltrativo con invasión perineural, células mioepiteliales identificables por inmunohistoquímica, estroma pobremente vascularizado, mitosis frecuentes y Ki67 mayor del 20 %5)(13)(18.
TRATAMIENTO
El tratamiento del AC es quirúrgico con resección local. El pronóstico es excelente4)(9 y no se produce recurrencia después de la escisión completa19.
CONCLUSIÓN
Los AC de glándula salival son neoplasias benignas infrecuentes con multifocalidad menor del 10 %. En nuestro caso, la presencia de múltiples focos tumorales en la glándula salival accesoria extirpada, como se observa en la Figura 3, plantearía la posibilidad de desarrollar otros AC en la misma localización.















