Introducción
Desde el punto de vista de la supervivencia y perpetuación de las especies, la reproducción, puede ser considerado como un proceso fundamental de los organismos, por lo tanto, el control de los ciclos reproductivos de las especies ícticas sometidas a cultivo, es uno de los factores más importantes para asegurar el éxito de la acuicultura y constituye un requisito indispensable para la introducción de nuevas especies a los sistemas de producción (Cruz-Casallas et al., 2006).
Desde hace algunos años en Colombia se ha generado un interés por algunas especies de peces del orden de los bagres Siluriformes. Especies dulceacuícolas como Epseudoplatystoma magdaleniatum, anteriormente Pseudoplatystoma fasciatum (Bagre rayado), Leiarius marmoratus ((Yaque), Pimelodus grosskopffi (Capaz), Phractochphalus hemioliopterus (Cajaro), Sorubim cuspicaudus (Blanquillo), Pimelodus blochii (Nicuro), Callophysus macropterus ((Mapurito), Eremophilus mutisii (Capitán de la sabana) y Pimelodus pictus (Tigrito), han sido valoradas para su producción a nivel de laboratorio y se han evaluado algunos de sus aspectos reproductivos (Rodríguez-Pulido y Mojica-Benítez, 2005).
Ariopsis seemanni, es un bagre marino presente en la costa pacífica colombiana donde tradicionalmente los peces adultos de gran tamaño (mayor a 25 cm longitud total), han sido parte del consumo alimenticio de pobladores costeros. Sobre los peces de edad temprana de esta especie (5-10 cm de longitud total), se ha presentado en las últimas dos décadas una alta presión pesquera sobre el recurso natural silvestre, debido a que son usados en acuarios, como peces ornamentales marinos, aclimatados a un ambiente dulceacuícola, y comercializados tanto a nivel nacional como internacional (Lasso et al., 2011). Los peces son capturados en las costas del Pacífico, comercializados nacionalmente en ciudades capitales (Cali, Medellín, entre otras) y exportados principalmente por vía aérea desde Bogotá a otros países. Esta especie en Colombia ha sido priorizada como una especie en la cual hay que desarrollar investigaciones debido a la potencialidad que tiene para actividades acuícolas (MADR y IICA, 2011).
Son pocas las investigaciones encontradas sobre Ariopsis seemanni. Estas se refieren principalmente a aspectos biológicos y ecológicos (Ortega, 1996), filogenéticos (Betancur et al., 2007), nutricionales (Dallos-Rodríguez, 2007; Lamouroux-López, 2014), morfológico relacionado con el encéfalo (Londoño y Hurtado-Giraldo, 2010), el tracto digestivo (Gómez-Ramírez et al., 2010), el nervio óptico (Castañeda-Cortés et al., 2013), e histológico relacionado con el ojo (Tovar-Bohórquez et al., 2013).
Realizar experiencias encaminadas a la reproducción inducida de A. seemanni, llegan a ser herramientas hacia una alternativa para la producción de juveniles, dadas las condiciones reproductivas particulares relacionadas con esta especie. Así mismo se plantea la hipótesis, que peces tratados con HGC tendrán una mejor respuesta en el desarrollo gonadal en términos de cantidad de oocitos en maduración final y ovulación, con respecto a aquellos tratados con EPC. El presente ensayo evaluó el efecto de dos tratamientos hormonales con gonadotropina coriónica humana (HGC) y dos tratamientos hormonales con extracto pituitario de carpa (EPC), y sus efectos sobre la cantidad de oocitos en maduración final y el desove en Ariopsis seemanni.
Materiales y métodos
Área de estudio. La investigación se realizó en las instalaciones de la estación acuícola Bahía Málaga de la AUNAP ubicada en los 3o 55’ Lat. N y los 77o 21’ Long. O (Cantera et al., 2014), en el corregimiento de Juanchaco, jurisdicción del municipio de Buenaventura, caracterizada por una temperatura ambiental entre 26 y 28ºC, humedad relativa del 90% y una pluviosidad de 9.000 mm (PNNC, 2014).
Área experimental. En 140 m2, se adecuó un sistema con abastecimiento de agua marina y aireación constantes, donde se ubicaron 24 tanques plásticos de 100 L con tapa, usados como contendores en cada una de las unidades experimentales para cada una de las parejas de peces (Figura 1).
Material biológico. Para el experimento se utilizaron 24 parejas (hembra y macho), que fueron obtenidos en finales del mes de enero y capturados del medio natural en la Quebrada Valencia, al interior del caserío de La Plata (4° 02`16 Lat. N y 77º 13`47 Long. O) (Figura 2), colectados por pescadores artesanales de la región, utilizando anzuelos, chinchorro y atarraya. Estos peces fueron transportados en lancha una hora hasta la estación acuícola de la Aunap en Bahía Málaga. Al momento de la recepción de los peces, se verificaron si había presencia/ausencia de heridas en la piel, daños corporales, mutilaciones y movilidad natatoria en los peces.

Fuente: Google Maps, Google earth.
Figura 2 Zona (recuadro amarillo) de captura de peces de Ariopsis seemanni
Los procedimientos metodológicos a nivel de laboratorio que involucraron organismos vivos como peces, los cuales están relacionados con la manipulación, mantenimiento, observación, tratamiento, sacrificio y otros, tomaron en consideración el cumplimiento bioético de cuidado y bienestar animal, para el uso de organismos animales con propósitos de investigación, docencia y evaluación (CCAC, 2005; NRC. 2011).
Los peces obtenidos e identificados sexualmente, se ubicaron por sexo, en dos tanques de 2500 L cada uno (Figura 3) para facilitar su manipulación, durante 24 horas se mantuvo un flujo continuo (6,6 L/min) de agua marina y aireación moderada, con el propósito de reducir el estrés por captura y transporte. Luego de este periodo, se procedió al registro de medidas biométricas en longitud y peso de cada reproductor. Para la manipulación de los peces, se utilizó como anestésico aceite de clavo de olor (LA-TOUR®) a una concentración de 10 ppm. La longitud total de cada reproductor se registró mediante una regla (0-100 cm) y el peso con una balanza digital (Kern modelo PCB, 1.0 g sensibilidad 0.1 g). Se colocaron en proporción de 1:1 un macho y una hembra en cada unidad experimental.

Figura 3 Peces adultos de Ariopsis seemanni separados por sexos: machos (Izquierda), hembras (Derecha)
Los peces utilizados tuvieron un peso promedio de 263.6±42.2 g y 174.4±30.4 g y una longitud total promedio de 25.31±1,28 y 22.21±0.97 cm, para hembras y machos, respectivamente.
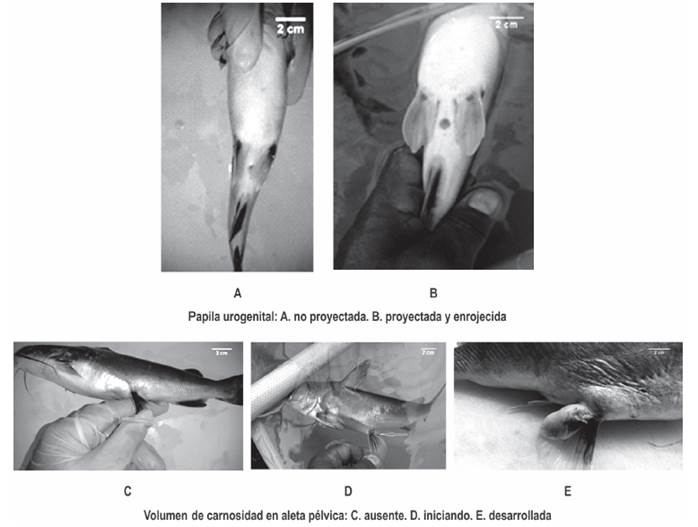
Inducción hormonal. Tomando en consideración que para esta especie, no es viable realizar biopsias ováricas para extraer oocitos y determinar el estado exacto de desarrollo en ellos; así como también que no existe el referente científico indexado, acerca del estado del desarrollo de los oocitos, asociado directamente al grado de prominencia o volumen de la carnosidad presente en la base de las aletas pélvicas en las hembras de Ariopsis seemanni; (aspecto morfológico particular reconocido por algunos investigadores de la presencia de esta carnosidad en las épocas de reproducción y estados de madurez sexual de las hembras), al inicio del experimento, el estado de madurez en las hembras, se estimó de manera indirecta considerando el tamaño de la carnosidad en la base de las aletas pélvicas (figura 4).
Se plantearon cuatro tratamientos hormonales: T1: 5 mg EPC/kg; T2: 7 mg EPC/kg; T3: 2000 UI HGC/kg y T4: 1000 UI HGC/kg. Con base en el peso de cada reproductor, se determinó la cantidad de cada hormona a aplicar. En las hembras se aplicó una dosis preparatoria y doce horas después, una dosis final; en los machos se administró la mitad de la dosis total en cada tratamiento, suministrada cuando se aplicó la dosis final en hembras. Se utilizó un método de tratamiento hormonal invasivo agudo por inyección (Alvarez-Lajonchére y Hernández Molejón, 2001). Las dosis hormonales fueron inyectadas en la base de la aleta pélvica de los peces (figura 4), utilizando jeringas plásticas para insulina (1 ml x 31 G x 8mm). Para corroborar que se presentó ovulación y/o desove en las hembras, se tomó en consideración el concepto propuesto por Woynarovich y Horváth, (Woynarovich y Horváth, 1980), en donde manifiestan que la ovulación comienza con la desaparición de la capa folicular del oocito celular, la concentración de los cromosomas y termina con la primera división meiótica. Al mismo tiempo, el folículo, que mantiene los huevos sujetos a la pared del ovario se rompe, se disuelve parcialmente y los oocitos caen a la cavidad ovárica. Y el desove, se comprende como la expulsión de los oocitos, en donde la masa de óvulos puede ya fluir libremente por el poro genital. Cada una de las hembras inducidas hormonalmente, fue sacrificada por enfriamiento (usando hielo en el agua) y les fue practicada una disección post mortem, al final del experimento. La ausencia de desove espontáneo de las hembras se verificó con base en la no presencia de huevos en cada uno de los tanques de las unidades experimentales y por la ausencia de huevos en la cavidad bucal de cada macho potencialmente incubante revisado (Segura-Berttolini y Mendoza-Carranza, 2013). La disección post mortem, permitió posteriormente identificar el estado de madurez sexual en las hembras, utilizando los criterios planteados en la escala de madurez gonadal propuesta por Nikolsky (1963).
Para estimar el grado de desarrollo de los oocitos se consideró el tamaño y coloración; determinando: oocitos pequeños (3-5 mm) de color blanco, como oocitos inmaduros y oocitos grandes (> 12 mm) color diferente a blanco, como oocitos en maduración final. Debido a que no hay referente indexado para la clasificación del tipo de oocitos en maduración final en esta especie, en este trabajo se planteó la siguiente clasificación: Oocitos tipo I. Oocitos en estado de maduración, de coloración amarillo - anaranjado y alta vascularización periférica; Oocitos tipo II. Oocitos en maduración, de coloración amarillo - verde, baja vascularización periférica; Oocitos tipo III. Oocitos, de coloración verde claro traslucido, escasa vascularización periférica. Tomando en consideración la cantidad de estos oocitos en maduración, se estimó la fecundidad promedio; se estimó el índice de ovulación, mediante el porcentaje de la relación entre la cantidad de hembras que presentaron ovulación respecto de la cantidad de hembras inducidas hormonalmente.
Monitoreo calidad del agua. En la fase de inducción hormonal fueron monitoreados parámetros fisicoquímicos en el agua: temperatura promedio, 28.43±0.36 ºC, medida un termómetro Brixco (0-50 ºC, sensibilidad 1ºC); concentración promedio de oxígeno disuelto (OD), 7.16±0.06 mg/L, y porcentaje (%) promedio de saturación, 80.2±0.006%, medidos con una sonda paramétrica YSI, modelo 550ª; salinidad promedio 28.8±0.02 UPS, medida con un salinómetro refractómetro Atago® modelo S10α, y el flujo promedio de agua, 0.97±0.046 L/min, el cual se determinó con mediciones de aforo de caudal (L/min).
Diseño experimental. Se utilizó un diseño de clasificación simple, con una distribución completamente al azar (DCA), con cuatro tratamientos y seis réplicas por tratamiento, para u n total de 24 unidades experimentales asociadas al modelo contrastadas al efecto de los tratamientos. Se utilizó el programa Statgraphics® Centurión XV versión 15.02.5, que permitió realizar análisis de varianza paramétrica de efectos fijos (ANOVA) simple, los análisis efectuados se realizaron a un nivel de confiabilidad al 95%. La aleatoriedad de los datos se verificó, mediante la comprobación de los supuestos de homocedasticidad (Levene’s) y prueba de normalidad (Kolmogorov-Smirnov).
Resultados
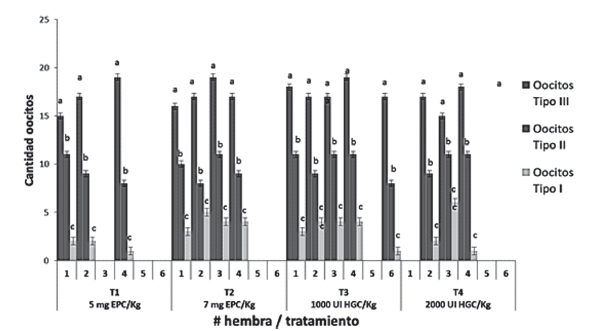
La Figura 5 presenta algunos de los rasgos externos de madurez sexual que se reconocieron en hembras de Ariopsis seemanni. La tabla 1 presenta, respuesta a ovulación y al desove en cada hembras de cada tratamiento, signo (-) denota evento no ocurrido, signo (+) evento ocurrido, cantidad y tipo de oocitos en maduración final. La Figura 6 presenta la cantidad de oocitos en maduración en cada uno de las hembras en cada tratamiento. Al final del experimento, en la Figura 7 se pueden observar los diferentes tipos de oocitos encontrados en estado de maduración.
Tabla 1 Respuesta reproductiva en hembras de Ariopsis seemanni, cantidad de oocitos en maduración en un ensayo de reproducción inducida (n= 24).
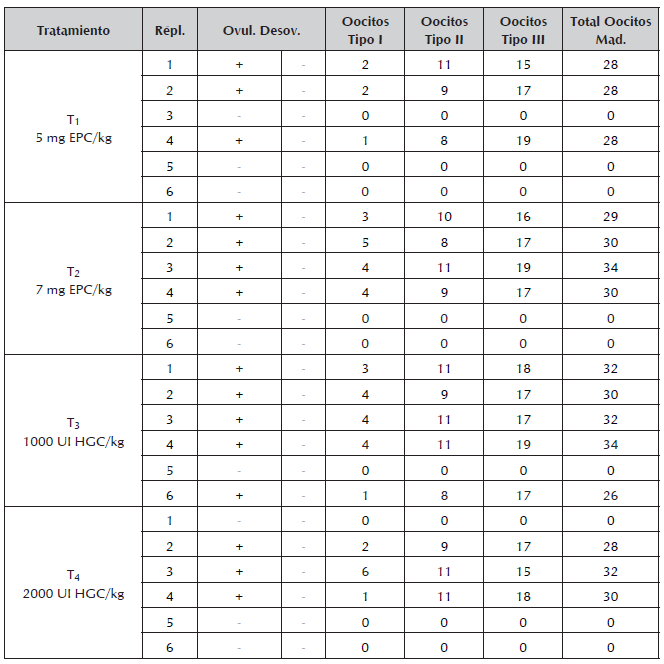
Répl.= Réplica; Ovul.= Ovulación; Desov.= Desove; Mad.= Maduros.
Discusión
Se reconocieron rasgos externos de madurez sexual en las hembras considerando proyección y enrojecimiento de la papila urogenital y presencia de carnosidad en la aleta pélvica (Woynarovich y Horváth, 1980; Acevedo y Ángel, 1999; Chaparro, 1994). La inflamación de la papila urogenital observada en las hembras de A. seemanni, es un rasgo que también ha sido reportado en hembras maduras de Bagre marinus (Caballero-Chávez, 2013); en hembras de 19 cm LT de A. bonillai, donde se reconoce este rasgo y donde se presenta una carnosidad triangular en la aleta pélvica, que se torna muy agrandada y enrojecida durante el estado de madurez sexual (Galvis-Cortes, 1983; Olaya-Nieto et al., 2007).
Aunque la condición inicial de madurez en las hembras de A. seemanni, fue asumida de manera indirecta, comprendiendo que los rasgos externos no son criterios de garantía absoluta de la determinación de un desarrollo oocitario exacto (Zanuy y Carrillo, 1987), se reconoce, la necesidad de haber determinado la posición del núcleo en los oocitos que hubiesen podido haber sido extraídos de la gónada (Acevedo y Ángel, 1999), mediante biopsia ovárica (Zanuy y Carrillo, 1987); que para el caso de A. seemanni, no es viable, o recomendable debido al gran tamaño (> 12 mm) en los oocitos, los que al tratar de ser extraídos mediante una cánula de un diámetro de 15-20 mm, causarían daño y lesiones en el oviducto en las hembras, posiblemente conllevando traumas que pueden bloquear los procesos endocrinos necesarios para maduración y el desove y en caso extremo causar la muerte en las hembras. Se logró identificar estado IV de madurez sexual en las hembras al final del experimento (Nikolsky, 1963).
En los sacos ováricos de A. seemanni, se pudieron observar oocitos en diferentes estados de desarrollo (tamaño, coloración y posición en el saco ovárico). Oocitos en maduración, hacia el extremo posterior del saco ovárico y oocitos inmaduros en la región anterior. La presencia de oocitos en diferente estado de desarrollo podría hacer considerar: 1) Un desarrollo diferencial o asincrónico de los folículos reproductivos. Esta condición asincrónica, estaría acorde al concepto planteado años atrás para la especie (Ortega, 1996). 2) Un desarrollo sincrónico por grupos de oocitos, que conllevaría a un proceso de reproducción durante varios días, teniendo desoves parciales. Este concepto podría considerarse, como estrategia reproductiva que favorece la supervivencia de los alevinos; tomando en consideración el planteamiento que refiere la capacidad bucal que tienen los machos de algunos Áridos en los procesos de incubación de huevos fecundados. Un caso contrario es lo reportado por Amezcua y Muro-Torres (2012), para Occidentarius platypogon, otra especie de bagre, donde encontraron una condición de madurez gonadal, que les permitió determinar un desarrollo sincrónico de oocitos y un proceso de desove anual.
La fecundidad media encontrada en las hembras de A. seemanni fue de 3.07±1.02 para oocitos en maduración: tipo I, de 9.80±1.86 para oocitos tipo II y de 17.20±1.26 para oocitos tipo III; la fecundidad promedio total fue de 30.07±2.34 oocitos en maduración final (considerando las 15 hembras en las que se encontraron estos tipos de oocitos). Valores cercanos son reportados por Acero, 2000 (en Olaya-Nieto et al., 2007) en A. bonillai con una fecundidad media de 36 oocitos. Para el Bagre marinus, se reportaron cantidades de 21 a 33 ovocitos hidratados y un máximo de 62; este último valor en hembras maduras de 350 a 555 mm de longitud y 351 a 1980 g de peso (Mendoza-Carranza y Hernández-Franyutt, 2005). Podría considerarse, de manera preliminar, que A. seemanni es una especie de fecundidad promedio entre las especies de áridos de este género.
Por otra parte, el diámetro promedio global de los oocitos de A. seemanni, fue de 13.2±3.6 mm. Estos tamaños son similares a los reportados para A. bonillai, por Toro y Villa (1983) entre 1-2 cm; por Chaparro et al., (2002) entre 0.9-1.6 cm; por Olaya-Nieto, et al., (2007) entre 0.8-1.6 cm y también por Olaya-Nieto et al., (2007) con un promedio de 1.2±0.13 cm
Según los resultados relacionados con fecundidad y tamaño de los oocitos, en A. seemanni, se conservan los planteamientos de Yáñez-Arancibia (Olaya-Nieto et al., 2007), acerca de los bagres marinos donde se manifiesta una aparente baja fecundidad, en un sentido estricto, con base al tamaño de sus oocitos, pero donde biológicamente existen mecanismos que aseguran una alta supervivencia de huevos y larvas, huevos grandes en tamaño y reservas de vitelo y una protección de huevos y larvas, gracias a la incubación bucal de los machos.
Las medidas en longitud y peso en las hembras de A. seemanni, muestran ejemplares entre 28 a 33 cm y entre 189 a 357 g, en estado de madurez sexual. Longitudes similares se reportan en hembras de otros bagres marinos: 25.2 cm de longitud furcal en hembras maduras de Bagre marinus (Caballero-Chávez, 2013); para Occidentarius platypogon, una longitud de madurez sexual de 35 cm (Amezcua y Muro-Torres, 2012); en A. bonillai, la talla de primera madurez sexual reportada entre 22.0 y 24.0 cm LT (Olaya-Nieto et al., 2007).
La maduración en oocitos se pudo verificar al reconocer y diferenciar oocitos en diferente color y tamaño respecto a oocitos pequeños inmaduros de color blanco (Figura 7). La ovulación se observó encontrando oocitos en maduración en el saco ovárico, que no tenían conexión con la pared del ovario. En todos los tratamientos hormonales, se tuvieron hembras que presentaron oocitos en estado de maduración final, solamente nueve hembras inducidas hormonalmente, no presentaron este tipo de oocitos en maduración final. Los resultados de los análisis estadísticos efectuados permiten inferir que no existieron diferencias estadísticamente significativas (figura 6), entre los tratamientos utilizados frente a la cantidad de cada uno de los tipos de oocitos en estado de maduración final ovulados (P Valor: p=0,60; p=0,59; p=0,34; para oocitos Tipo III, II y I respectivamente). Se realizaron análisis de varianza para analizar si pudiese existir efecto del peso o la longitud de las hembras en cada uno de los tratamientos, llegando a determinar que tampoco existieron diferencias estadísticamente significativas al respecto (Peso: P valor = 0,16; Longitud: P valor =0,49).
No se obtuvieron desoves espontáneos en las hembras inducidas; probablemente este evento se puede asociar a varios sucesos: haber utilizado peces no adaptados durante varios meses a condiciones de laboratorio, que las dosis de hormona utilizada en los tratamientos, aunque produjeron ovulación (índice de ovulación del 50% al 66,67% con EPC y del 50% al 83,33% con HGC), posiblemente pudiesen haber tenido un efecto insuficiente sobre el desove, y que el mismo proceso de desove estuviese influenciado adicionalmente por estímulos exógenos, a los que se tuvieron durante el experimento; por ejemplo haber colocado refugios artificiales en los tanques, disponer de un sustrato adicional diferente (Tucker, 1966), haber utilizado una proporción macho a hembra mayor, que produjera mayor disponibilidad de feromonas en el medio, posibilitando un desove grupal más eficiente, que en parejas de peces aisladas (Mylonas et al., 2010), una condición de baja salinidad que pudiese haber mejorado procesos fisiológicos similares a ambientes naturales. Los planteamiento expuestos, hacen necesario considerar en la reproducción inducida en A. seemanni, la inclusión de condiciones ambientales abióticas y factores externos de manejo como factores importantes, adicionales al agente hormonal (Carrillo et al., 2009). En este sentido, algunos de los valores de calidad de agua registrados durante el experimento, estuvieron dentro del rango de confort reportados para reproducción de especies tropicales (Yu et al., 2008).
Aunque existen concentraciones de la HGC con la cuales se han logrado desoves en especies como Lutjanus guttatus, Lutjanus campechanus, Morone saxitilis, Dicentrarchus labrax entre algunas, el uso de HGC se ha generalizado; sin embargo, su molécula es muy diferente a la de los peces, por lo que no ha sido efectiva o eficiente en algunas especies con las dosis sugeridas y requeridas lo que puede ocasionar utilizar altas cantidades, con márgenes de seguridad muy estrechos, por lo que se pueden provocar sobredosis que a menudo producen desoves parciales, obstrucción del poro genital, entre otros, con resultados negativos, tanto por la mala calidad de los huevos, como causar daños e incluso mortalidad en los reproductores (Alvarez-Lajonchére y Hernández, 2001). La cantidad de hormona utilizada en cada uno de los tratamientos de esta investigación, se planteó como dosis punto de partida, considerando los posibles efectos, mencionados anteriormente. Se deben implementar prácticas con nuevas dosis y otras presentaciones hormonales que puedan inducir la ovulación.
Conclusión
Las concentraciones de 5 y 7 mg de EPC/kg y de 1000 y de 2000 UI de HGC/kg, empleadas durante el experimento lograron inducir ovulación de oocitos en hembras de A. seemanni en estado de madurez sexual capturadas del medio natural, No se lograron desoves espontáneos en las hembras inducidas, evento que pudo estar influenciado por la ausencia de otros factores exógenos determinantes a los manejados durante la investigación. La presente investigación se reporta como el primer trabajo de reproducción inducida para la especie.